En la actualidad, el uso de de fármacos anti-TNF es cada vez más amplio y abarca diferentes especialidades. Tanto la enfermedad de Crohn como la psoriasis tienen indicación para estos tratamientos. A su vez existen varios tratamientos anti-TNFα aprobados para ambas enfermedades, lo que en ocasiones dificulta la elección del agente biológico.
Adalimumab es un anticuerpo monoclonal anti-TNFα completamente humano, lo que le confiere menor inmunogenicidad y posiblemente, mejor tolerancia. Adalimumab está aprobado tanto en la enfermedad de Crohn (patrón inflamatorio con brote moderado-grave y en la enfermedad fistulizante) como en la psoriasis (moderada-grave).
Existen casos publicados de tratamiento con infliximab en pacientes con enfermedad de Crohn y psoriasis1 con resultados espectaculares en ambas enfermedades, pero no hemos encontrado casos descritos tratados con adalimumab como tratamiento simultáneo para ambas enfermedades.
Presentamos un caso de una paciente diagnosticada de psoriasis cutánea generalizada, que desarrolló una enfermedad de Crohn ileal de patrón inflamatorio y que fue tratada con adalimumab como tratamiento de las 2 enfermedades.
Se presenta el caso de una mujer de 35 años, sin alergias conocidas, con antecedentes de fumadora de 10 cigarrillos/día, hipertensión arterial y esteatosis hepática. En el año 2007 se le diagnosticó una psoriasis cutánea en placas generalizada tratada con calcipotriol crema hasta el año 2010 y que siguió control regular en el servicio de dermatología. Durante el primer trimestre del año 2010, la paciente manifestó un empeoramiento de la extensión de su psoriasis, en forma de placas infiltradas con hiperqueratosis importante de predominio en extremidades inferiores y superiores con una puntuación en el Psoriasis Area and Severity Index Score (PASI) de 13. El tratamiento con ciclosporina se desestimó por los antecedentes de hipertensión arterial, de igual manera que con metotrexato y acitretina por los precedentes de esteatosis hepática. La paciente no refirió antecedentes familiares de interés.
La paciente fue derivada por el servicio de dermatología al servicio de digestivo en septiembre de 2010 por episodios de diarreas líquidas de 3 meses de evolución (hasta 10 deposiciones diarias), sin productos patológicos y dolor abdominal leve de predominio en hipogastrio, sin episodios de fiebre. La paciente no presentaba pérdida de peso, ni otras manifestaciones extraintestinales, y negó la ingesta de antiinflamatorios no esteroideos (AINE).
En la exploración física destacó una talla de 165cm, un peso de 65kg y constantes normales. Normohidratada con palidez cutánea. No se palpaban adenopatías periféricas. La exploración abdominal fue normal. El tacto rectal y la exploración perianal descartaron la presencia de fisuras y/o fístulas.
Se realizaron las siguientes exploraciones complementarias para su diagnóstico: analítica: Hb 11g/dl; volumen corpuscular medio (VCM) 75 fl; leucocitos 11.000×106/l (sin desviación a la izquierda); plaquetas 445.000×106/l; velocidad de sedimentación globular (VSG) 50mm; proteína C reactiva (PCR) 60mg/l; proteínas totales 68g/l; albúmina 42g/l; colesterol, función hepática y renal normales. Hierro 4μmol/l; ferritina 12 ng/ml; vitamina B12 y ácido fólico normales.
Las serologías de los virus de la hepatitis B (VHB) y C (VHC) y del virus de la inmunodeficiencia humana (VIH) fueron negativas. El estudio de heces con coprocultivos, parásitos y toxina de Clostridium difficile fue negativo. El estudio de tuberculosis con PPD fue negativo. La serología para Yersinia y Anisakis fue negativa. El sedimento de orina tuvo un resultado negativo. Se realizó colonoscopia total con exploración de 15cm del íleon distal, en la que se observa una válvula ileocecal y un colon con una mucosa normal pero un íleon distal con presencia de múltiples aftas sin otras lesiones. Se realizaron biopsias de íleon y de colon seriadas. Las biopsias de colon fueron normales y las de íleon evidenciaron una leve inflamación crónica inespecífica. Posteriormente, se completó el estudio con una TC abdominal que reveló un dudoso engrosamiento y un aumento de la captación en la pared del íleon terminal que podrían estar relacionados con cambios inflamatorios. No se observaron adenopatías. El resto del estudio se presentó sin alteraciones.
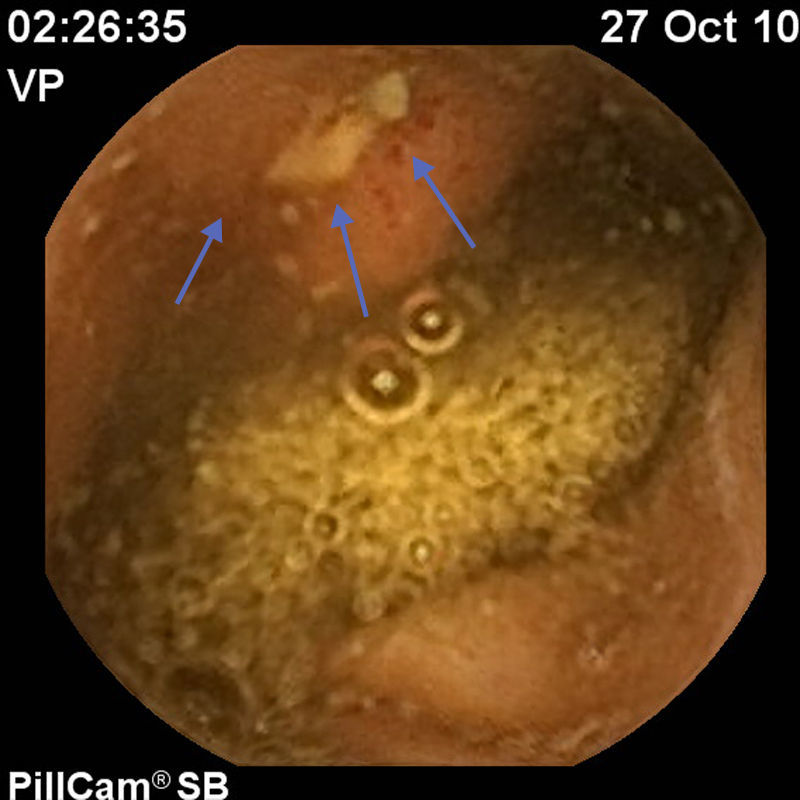
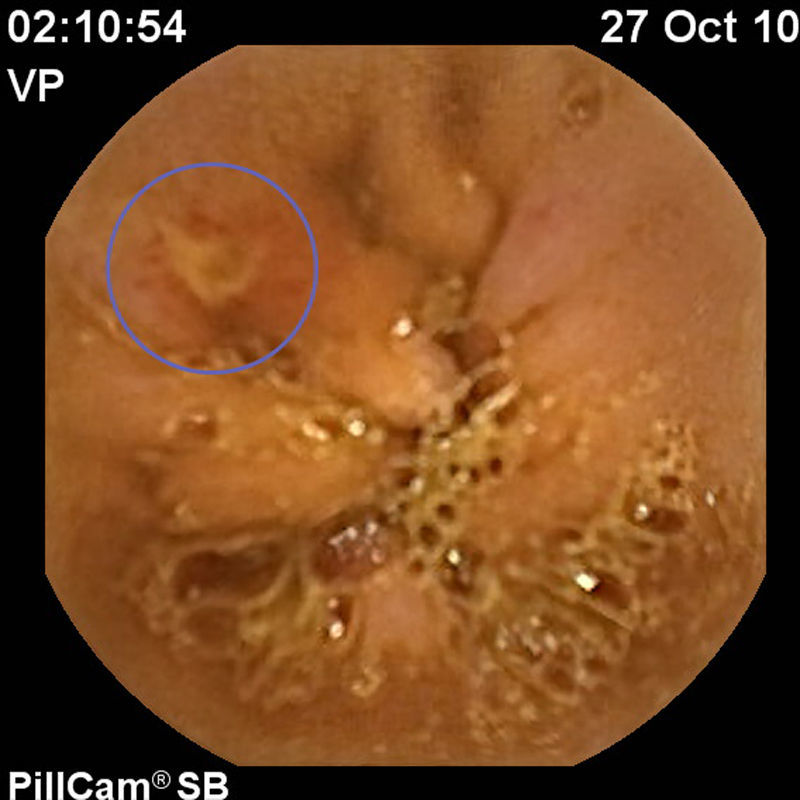
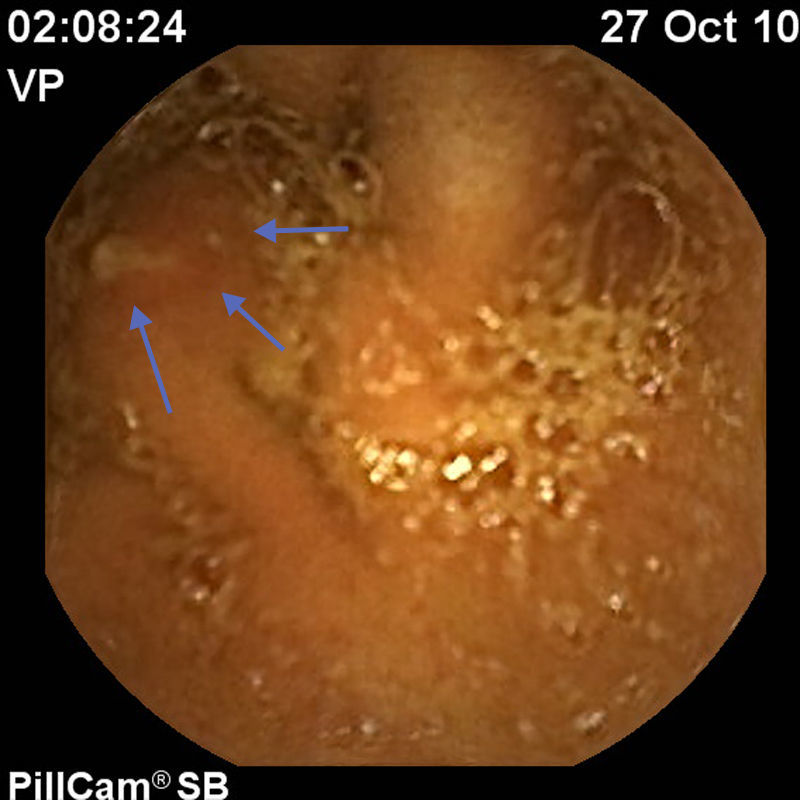
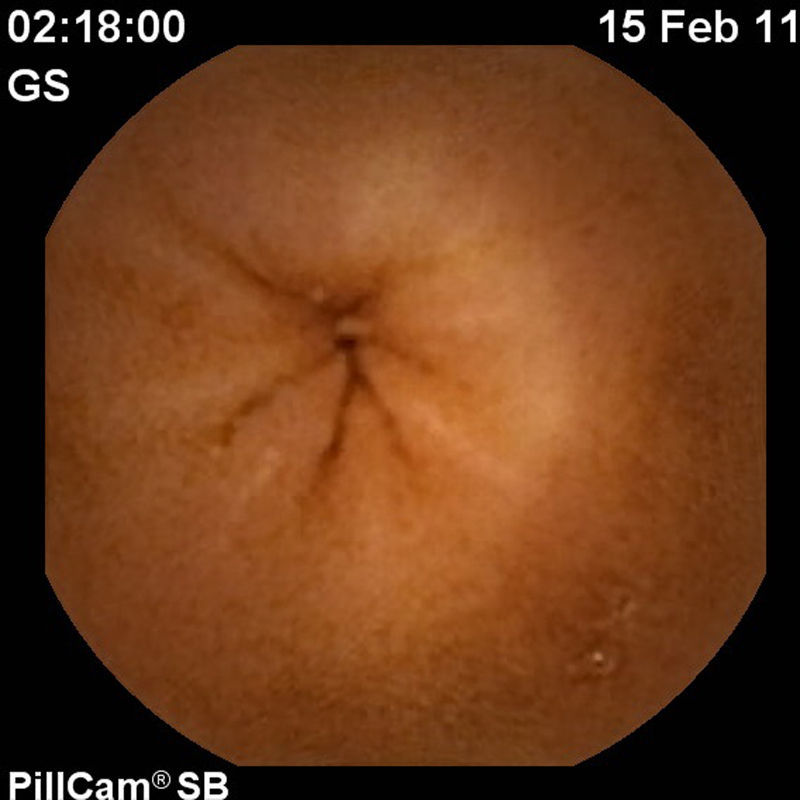
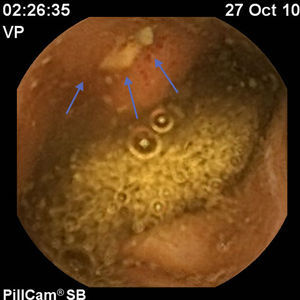
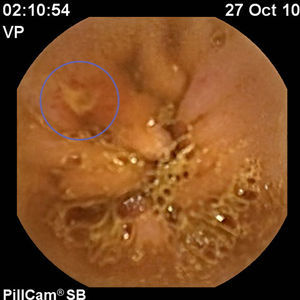
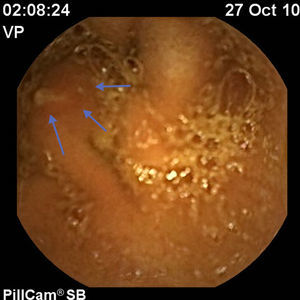
Para completar el estudio de la ileítis y ante la sospecha de enfermedad de Crohn se practicó una cápsula endoscópica en octubre del 2010 que reveló múltiples aftas en yeyuno (> 20 lesiones), así como múltiples úlceras de diversas formas y tamaños, localizadas en el íleon proximal y medio (un total de 15 lesiones), hallazgos indicativos de enfermedad de Crohn (figs. 1–3).
Se cataloga según la clasificación de Montreal como: A2 (edad entre 17-40 años), L1 (afectación del íleon distal), y B1 (comportamiento inflamatorio). Se evalúa la actividad mediante el Crohn's Disease Activity Index (CDAI), considerando una actividad leve (< 220 puntos).
En este momento se revalora el caso. Se trata de una paciente fumadora con psoriasis generalizada en placas con afectación extensa, puntuación del PASI al diagnóstico de 13, en brote actual, que se manifiesta con una enfermedad de Crohn ileal de patrón inflamatorio, de brote leve-moderado pero con afectación mucosa extensa. Tras valorar el caso con el servicio de dermatología, en noviembre de 2010, se decide iniciar un tratamiento de inducción de remisión para ambas enfermedades con adalimumab s.c. 160 y 80mg en las semanas 0 y 2, respectivamente. Antes de comenzar, se descarta la presencia de infección tuberculosa y de otras infecciones bacterianas o virales. La paciente presentó una respuesta clínica y analítica excelente con la práctica desaparición de las lesiones cutáneas psoriásicas (PASI 1) y una disminución del CDAI hasta <150 puntos después de la primera dosis de adalimumab.
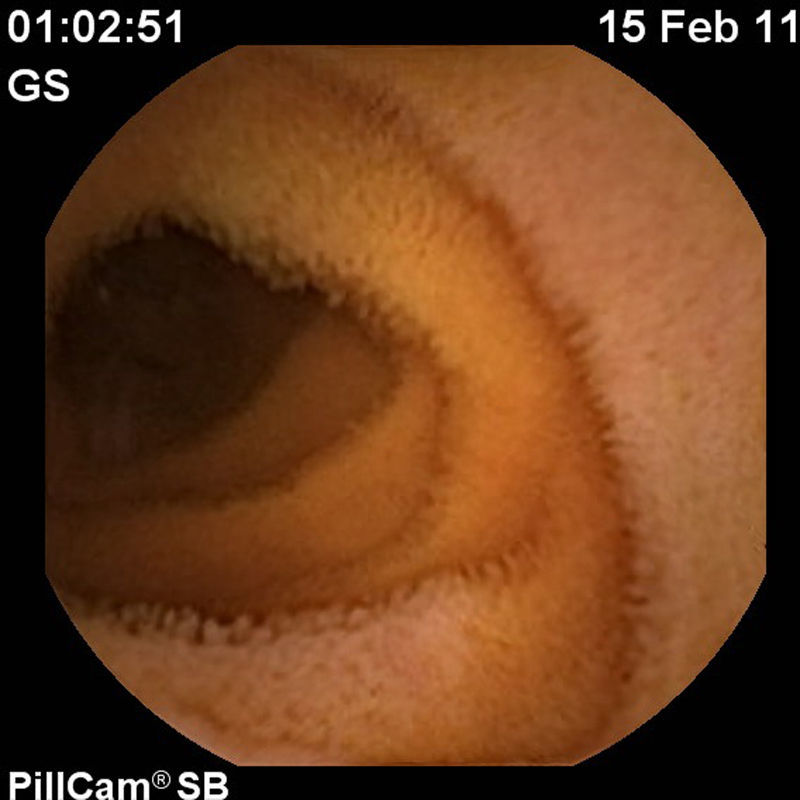
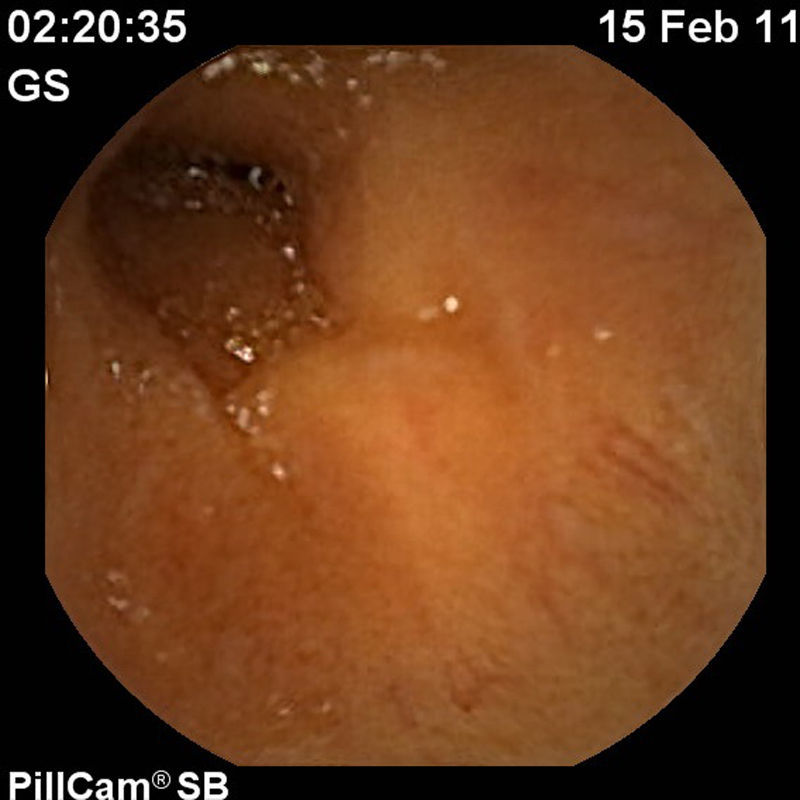
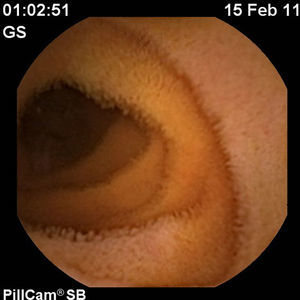
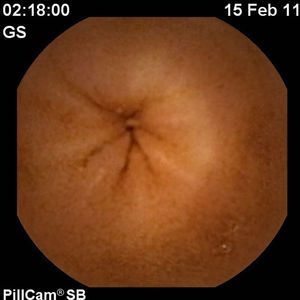
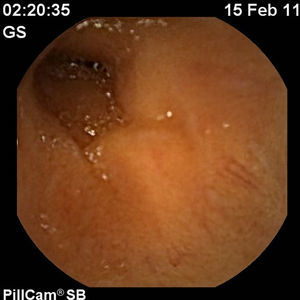
En febrero de 2011, 16 semanas después de iniciar el tratamiento, se decidió realizar una cápsula endoscópica para valorar la curación mucosa, observando una mucosa de intestino delgado totalmente normal compatible con una remisión profunda (figs. 4–6).
En la actualidad, la paciente es controlada en las consultas externas de los servicios de dermatología y de digestivo. Abandonó el hábito tabáquico. Está en tratamiento de mantenimiento con adalimumab 40 mg s.c. cada 15 días. La paciente se mantiene en remisión clínica, no ha presentado recidiva clínica de la enfermedad de Crohn ni de la psoriasis cutánea. No ha presentado efectos secundarios a la medicación y los controles analíticos son normales (hemograma, bioquímica y PCR).
El diagnóstico de la enfermedad de Crohn se basa en un conjunto de hallazgos clínicos, endoscópicos, radiológicos y/o histológicos. La afectación exclusiva del intestino delgado ocurre en un 30-40% de pacientes. Se descartaron otras causas de úlceras en intestino delgado como las infecciosas con el estudio microbiológico (Yersinia enterocolitica, Mycobacterium tuberculosis, Salmonella, Anisakis), interrogando a la paciente por posibles causas farmacológicas (AINE, anovulatorios orales, digoxina, diuréticos, cocaína, ergotamina), causas tumorales (linfomas, carcinoides, adenocarcinoma o metástasis intestinales) y otras causas inflamatorias o autoinmunes (yeyunoileítis ulcerativa, enteritis eosinofílica, enfermedad del injerto contra el huésped). En este caso, ante la sospecha de enfermedad de Crohn con biopsias no concluyentes, utilizamos la cápsula endoscópica para completar el estudio. En los casos de sospecha de enfermedad de Crohn, la cápsula endoscópica es más sensible que otras técnicas de imagen en el diagnóstico de lesiones de la mucosa en el intestino delgado. Antes de realizar la cápsula endoscópica, se recomienda efectuar una exploración radiológica (TC abdominal o enterorresonancia) o una cápsula Patency para descartar una estenosis intestinal.
En nuestro caso, una paciente joven con enfermedad de Crohn de inicio endoscópicamente grave y psoriasis cutánea generalizada extensa, el cuadro general nos decidió a iniciar de forma precoz la administración de adalimumab como tratamiento de ambas enfermedades. El hecho de presentar ambas enfermedades pensamos en primera indicación un tratamiento anti-TNF, si bien la enfermedad de Crohn sin psoriasis cutánea en este paciente hubiera tenido indicación de corticoides con valoración a posteriori de inicio de un tratamiento inmunosupresor (azatioprina). Se descarta metotrexato por la presencia de esteatosis hepática.
Adalimumab es un anticuerpo monoclonal anti-TNFα completamente humano, lo que le confiere menor inmunogenicidad y, posiblemente, mejor tolerancia. Adalimumab ha demostrado ser eficaz en el control del brote agudo y en el mantenimiento de la respuesta conseguida en la enfermedad de Crohn inflamatoria con brote moderado-grave y en la enfermedad de Crohn fistulizante. La dosis de inducción en pacientes con enfermedad de Crohn activa moderada-grave es de 160mg s.c. en la semana 0, seguidos de 80mg s.c. en la semana 2. Estudios controlados y aleatorizados demuestran que adalimumab es una alternativa válida para inducir la respuesta en pacientes que nunca han recibido anti-TNFα y en pacientes que han sido tratados con infliximab y que han perdido la respuesta o son intolerantes a este.
En el estudio CLASSIC I2, los pacientes que recibieron la dosis de 160/80mg presentaron una probabilidad 3 veces mayor de conseguir la remisión clínica y aproximadamente 2 veces más posibilidades de conseguir una respuesta clínica significativa respecto a los pacientes tratados con placebo, resultando dicha respuesta superior a la obtenida con 80/40mg. La dosis de mantenimiento recomendada es de 40 mg cada 2 semanas, si bien la dosis semanal de 40mg puede ser utilizada en caso de pérdida de eficacia.
Al final del estudio CHARM3, los pacientes que no habían recibido nunca antes anti-TNF presentaron un mayor porcentaje de remisión que los pacientes que habían recibido dicho tratamiento con anterioridad. Además, se observó que un 83% de los tratados con adalimumab estaban en remisión 3 años después de ser incluidos en el estudio. En teoría, la curación mucosa disminuye las complicaciones y la cirugía, deteniendo la progresión de la enfermedad. La evaluación de un fármaco no debe estar basada únicamente en la mejoría sintomática, pero la curación mucosa debería ser un objetivo (endpoint) fundamental. El gran inconveniente para definir la curación endoscópica radica en los múltiples índices heterogéneos y no validados existentes, así como en las diferencias interobservador. El estudio EXTEND4(EXTend the Safety and Efficacy of Adalimumab Through ENDoscopic Healing) es el primer ensayo prospectivo, doble ciego y controlado con placebo que tiene como objetivo principal el estudio de la cicatrización mucosa. En este estudio, adalimumab ha demostrado la cicatrización completa de la mucosa en la semana 12 (27% en el grupo adalimumab vs. 13% del placebo, p=0,056) y el mantenimiento de la cicatrización en la semana 52 (24% de adalimumab vs. 0% del placebo, p<0,001), lo que refuerza su uso continuado en estos pacientes. En el mismo estudio, y presentado más tarde por Sandborn et al.5, se observa que la terapia de mantenimiento con adalimumab conlleva un incremento de la cicatrización de la mucosa en los pacientes con una duración de la enfermedad de Crohn menor (< 5 años), en comparación con los pacientes con una duración mayor (≥ 5 años). Además, los pacientes tratados con adalimumab que muestran curación mucosa en la semana 12 presentan una mejor calidad de vida al cabo de un año, y Colombel et al.6 demuestran su eficacia para lograr una remisión profunda, definida como remisión clínica (Crohn's Disease Activity Index [CDAI] <150) y curación mucosa (ausencia de úlceras mucosas).
Los datos disponibles sobre adalimumab, obtenidos en 19.000 pacientes con 6 enfermedades inflamatorias mediadas por el sistema inmunitario durante 10 años, avalan su seguridad a largo plazo7.
Por otra parte, adalimumab también está indicado en caso de psoriasis cutánea. La psoriasis es una enfermedad crónica inflamatoria de la piel, potencialmente debilitante, asociada a artritis erosiva. Es interesante señalar el incremento de la prevalencia de psoriasis en la enfermedad de Crohn con cifras entre 5-9% según los estudios frente a un 1,4% en pacientes control. Es importante conocer estar asociación ya que hay artículos que hacen referencia a un tratamiento común para ambas enfermedades, que un porcentaje significativo de casos pueden aparecer en combinación7. Por otra parte, existe la posible aparición de o exacerbación de lesiones psoriásicas durante el tratamiento con anti-TNF (reacción paradójica), con una aparición estimada en un 0,6-5% según diferentes estudios8.
El tratamiento de la psoriasis moderada-grave ha cambiado espectacularmente desde la aprobación de los agentes biológicos. En concreto, existen 5 tratamientos biológicos aprobados para la psoriasis, siendo los anti-TNFα los preferidos por los dermatólogos. Con todo, en ocasiones la elección del agente biológico resulta difícil. En lo que respecta al adalimumab, un subanálisis del estudio REVEAL9,10 demuestra su eficacia en la psoriasis moderada-grave y la semejanza de sus efectos secundarios con los del placebo. El 71% de los pacientes tratados con adalimumab alcanzaron una respuesta PASI 75 (porcentaje de pacientes que alcanzan una mejoría de 75% de su psoriasis respecto a su línea de base) en la semana 16, frente al 7% de los pacientes tratados con placebo.
Recientemente, Panaccione et al.11 han publicado un estudio sobre la seguridad de adalimumab en aproximadamente 24.000 pacientes recogidos de 71 ensayos clínicos, en 6 diferentes enfermedades autoinmunes (incluyendo psoriasis y enfermedad de Crohn). En este estudio se presentan los resultados de seguridad a más largo plazo (más de 12 años) de un fármaco anti-TNF. El estudio concluye que no existen diferencias en el perfil de seguridad.
En la actualidad, la eficacia demostrada por los tratamientos anti-TNFα en la psoriasis cutánea y en la enfermedad de Crohn nos hace considerar este tratamiento como una primera opción para aquellos pacientes en que ambas enfermedades concurren con una afectación extensa.