La translocación bacteriana consiste en el paso de bacterias viables desde la propia luz intestinal, sin rotura de la integridad de la mucosa intestinal, a sitios extraintestinales, como los ganglios linfáticos mesentéricos, la sangre, el líquido ascítico o el páncreas1-5. Este fenómeno ha despertado creciente interés en los últimos años, debido a las múltiples implicaciones clínicas que, de forma progresiva, se le han ido atribuyendo1,2,5-7. En la tabla I se representan las principales situaciones que se han relacionado con la aparición de translocación bacteriana.
La consecuencia más previsible de la translocación bacteriana es su contribución al desarrollo de infecciones1,5,6. En un interesante estudio, O'Boyle et al8 incluyeron a 448 pacientes sometidos a laparotomía por diferentes motivos y analizaron la incidencia de translocación bacteriana y su relación con el desarrollo posterior de infecciones bacterianas. Estos autores observaron que la incidencia de translocación bacteriana fue del 15,4%, y fueron factores predictivos de translocación la edad superior a 70 años, la cirugía urgente y, especialmente, la obstrucción intestinal distal. El 41% de los pacientes con translocación bacteriana presentaron infecciones bacterianas en el postoperatorio, frente al 19% en los pacientes sin translocación bacteriana, apoyando así el papel de la translocación bacteriana en el desarrollo de infecciones.
Sin embargo, la translocación bacteriana no sólo se ha relacionado con el desarrollo de diferentes tipos de infecciones en diversas situaciones experimentales y clínicas, sino que se ha sugerido que estaría implicada en otros procesos de gran importancia clínica, entre los que destaca el desarrollo del fallo multiorgánico en pacientes críticos, generalmente ingresados en unidades de cuidados intensivos1,2,7. Los pacientes con quemaduras graves y aquellos con politraumatismos son dos ejemplos clásicos de esta situación. Algunos autores, sin embargo, cuestionan si la translocación bacteriana es causa o consecuencia de los fenómenos inherentes al fallo multiorgánico5,7.
Otro aspecto de la translocación bacteriana que ha despertado recientemente especial interés consiste en los efectos que puede producir en los pacientes con cirrosis. En efecto, como veremos más adelante, la cirrosis favorece la aparición de translocación bacteriana, hecho observado tanto en animales de experimentación como en humanos3-5,9. En un reciente estudio, Cirera et al9 han demostrado translocación bacteriana a ganglios linfáticos mesentéricos en el 30,8% de los pacientes cirróticos en estadio C de Child-Pugh sometidos a laparotomía, frente a menos del 10% en pacientes no cirróticos y en pacientes cirróticos en estadio A o B de Child-Pugh. Este estudio no sólo demuestra claramente que la translocación bacteriana ocurre en los pacientes cirróticos (hecho observado con anterioridad en animales de experimentación), sino que este fenómeno es más frecuente en los pacientes con un mayor deterioro de la función hepática y de la hemodinámica portal y sistémica. La translocación bacteriana representaría un paso fundamental para explicar la patogenia de las infecciones bacterianas en la cirrosis, especialmente la peritonitis bacteriana espontánea3-6,10,11. Pero no sólo es así, sino que estaría implicada en el daño celular hepático, con el consiguiente deterioro de la función hepática, en la desregulación inmunológica y en las alteraciones hemodinámicas que favorecerían la aparición de ascitis, insuficiencia renal y hemorragia digestiva en la cirrosis. Estos interesantes aspectos de la translocación bacteriana en la cirrosis han sido revisados recientemente por Albillos et al6.
PATOGENIA DE LA TRANSLOCACION BACTERIANA
La aparición de translocación bacteriana supone una pérdida de la función de barrera que la pared intestinal ejerce frente a la propia flora de la luz intestinal2. Se han implicado tres tipos de mecanismos necesarios para que se produzca la translocación bacteriana2,12 (tabla II). En primer lugar, la alteración en el normal equilibrio ecológico bacteriano de la flora intestinal, concretamente el sobrecrecimiento bacteriano por bacilos aerobios gramnegativos. En segundo lugar, la disfunción de los mecanismos de defensa inmunológica del huésped. Finalmente, la alteración en la barrera intestinal, con el consiguiente incremento en la permeabilidad intestinal a las bacterias. En general, se considera que son necesarios todos estos factores para que la translocación bacteriana llegue a producirse.
El sobrecrecimiento bacteriano intestinal desempeña un papel muy importante en la patogenia de la translocación bacteriana2,10,11,14 y estaría favorecido por diversos factores como las alteraciones en los mecanismos de defensa inmunológica locales15,16, la disminución en la motilidad intestinal13, la administración prolongada de antibióticos que determinaría el sobrecrecimiento de bacterias resistentes17,18 o la malnutrición2.
Entre los mecanismos de defensa inmunológica locales frente al desarrollo de translocación bacteriana son de especial importancia las placas de Peyer, los linfocitos y macrófagos de la pared intestinal y la producción de IgA local y excretada con la bilis1. En este sentido, se ha observado una disminución de la producción de IgA en la bilis de ratas con quemaduras16 y en el intestino de pacientes con cirrosis alcohólica15, que podría contribuir al desarrollo de translocación bacteriana en estas situaciones. A nivel sistémico, se han descrito múltiples alteraciones en los mecanismos de defensa inmunológica1,11 en las diferentes situaciones en que se produciría la translocación bacteriana, destacando la disminución en la actividad del sistema reticuloendotelial19, la disfunción en la actividad fagocítica de los neutrófilos20 y la disminución en la concentración de diversas proteínas del suero con actividad opsónica1,21.
Finalmente, las alteraciones en la pared intestinal como consecuencia de la nutrición parenteral2, la desnutrición2 o de factores hemodinámicos, como el shock22,23 o la hipertensión portal24-27, también determinarían un aumento en la permeabilidad intestinal a las bacterias o a sus productos como la endotoxina, favoreciendo así la translocación bacteriana. Además, se ha observado que la endotoxemia es otro factor que favorece, a su vez, la translocación bacteriana27, creando así un círculo vicioso.
Los mecanismos por los cuales la translocación bacteriana contribuiría al fallo multiorgánico en los pacientes críticos, así como al deterioro hepático, inmunológico y hemodinámico en la cirrosis no son bien conocidos. Sin embargo, se especula que la liberación de citocinas y la consiguiente respuesta inflamatoria como consecuencia del paso de bacterias o de sus productos, como la endotoxina, a la circulación sistémica desempeñaría un papel muy importante5-7.
PREVENCION DE LA TRANSLOCACION BACTERIANA
Se han sugerido diversos métodos para evitar la translocación bacteriana (tabla III): tratar los factores desencadenantes o favorecedores, evitar siempre que sea posible la nutrición parenteral en beneficio de la vía enteral1,2, y la administración de antibióticos10,28. La administración de antibióticos ha demostrado su utilidad en diferentes situaciones. En el campo de la gastroenterología destacan la prevención de la infección del tejido pancreático necrótico en las pancreatitis graves28 y la profilaxis de infecciones bacterianas en las enfermedades hepáticas, principalmente insuficiencia hepática fulminante29,30 y cirrosis10,23,31-34.
Sin embargo, la administración de antibióticos profilácticos presenta diversos inconvenientes, entre los que destacan los efectos secundarios, el coste económico y, especialmente, el desarrollo de resistencias bacterianas17,18,28. Por ello, se ha intentado encontrar alternativas a los antibióticos13,24,35-37. El desarrollo de resistencias bacterianas a los antibióticos es un fenómeno de importancia creciente en todo el mundo38. El uso, en ocasiones indiscriminado, de antibióticos de amplio espectro en humanos y animales, y el aumento de los pacientes inmunodeprimidos como consecuencia del sida y de tratamientos inmunodepresores, con el consiguiente incremento en la incidencia de infecciones, son dos factores que contribuyen a su expansión37. Entre las recomendaciones de la OMS para intentar controlar el problema destacan la reducción del uso de antibióticos en animales y plantas y la búsqueda de alternativas a los antibióticos, como la terapia de interferencia microbiana (TIM), es decir, el uso de probióticos36.
PROBIOTICOS Y PREBIOTICOS
Los probióticos son bacterias vivas cuya administración es beneficiosa para la salud39. Poseen diversas características que determinan su potencial efecto beneficioso en la prevención de infecciones, especialmente por patógenos de origen intestinal, y de la translocación bacteriana35,40. Existe un gran número de probióticos, especialmente lactobacilos y bifidobacterias, y entre sus características (tabla IV) destacan la supervivencia en el tracto gastrointestinal a las secreciones digestivas, la adherencia al epitelio intestinal41, la seguridad para el uso en humanos y, en especial, la modulación de la flora intestinal inhibiendo a bacterias potencialmente patógenas41,42 y diversos efectos inmunomoduladores e inmunoestimulantes, como el estímulo para la proliferación de células inmunitarias43, el aumento en la actividad de las células fagocíticas44 o el incremento en la producción de IgA43. Hay que señalar, sin embargo, que no todos los probióticos exhiben todas estas propiedades, y que el efecto de una cepa en una situación concreta puede ser muy diferente del de otra cepa, debido a sus diferentes características35.
En el campo de las infecciones se ha demostrado la eficacia de la administración de diferentes probióticos en la prevención de la recurrencia de la diarrea por Clostridium difficile45, en la profilaxis de la candidiasis vaginal35,46 y de las infecciones urinarias de repetición35,47, y en la prevención y tratamiento de la diarrea infantil por rotavirus48-51.
Otra posibilidad es administrar prebióticos, es decir, ingredientes no digeribles de la dieta cuya ingesta estimularía selectivamente el crecimiento y la actividad de determinadas bacterias intestinales que tienen el potencial de mejorar la salud del huésped37,52. Se ha observado que la administración de fibra2,53, como la etilhidroxietil celulosa54, disminuye la incidencia de translocación bacteriana en modelos experimentales. El tratamiento con oligosacáridos no digeribles, como la lactulosa55, el lactitol56, la oligofructosa y la inulina57,58, estimula el crecimiento de las bacterias intestinales «favorables», como las bifidobacterias y los lactobacilos, que podrían inhibir a las bacterias potencialmente patógenas, y así disminuiría la translocación bacteriana. Finalmente, se puede administrar la combinación de probióticos y prebióticos. Estas combinaciones se conocen como simbióticos52.
Comentaremos a continuación los dos campos dentro de la gastroenterología en los que la translocación bacteriana tiene mayor trascendencia y la posible utilidad de los probióticos y prebióticos en su prevención: la pancreatitis grave y las enfermedades hepáticas (ictericia obstructiva, insuficiencia hepática fulminante y cirrosis).
PANCREATITIS GRAVE
La pancreatitis grave, generalmente definida de acuerdo con diversas escalas, como las de Ranson, APACHE II o de Glasgow28, suele acompañarse de necrosis del tejido pancreático y presenta todavía una mortalidad del 25%, frente al 1,5% de las pancreatitis leves59. Una complicación muy importante de la pancreatitis grave es la infección de la necrosis, que ocurre en el 30-70% de los casos y que comporta un aumento de la mortalidad28. De hecho, se considera que el 80% de los fallecimientos en los pacientes con pancreatitis grave es debido a la infección de la necrosis60,61.
La infección del tejido pancreático necrótico se produce en la mayor parte de los casos como consecuencia de la translocación bacteriana de la flora intestinal28,62,63. Se ha demostrado en ratas con pancreatitis experimental el paso de bacterias desde la luz intestinal a ganglios linfáticos mesentéricos, líquido ascítico, tejido pancreático, sangre y otras localizaciones extraintestinales62,63, y se ha comprobado un aumento en la permeabilidad intestinal a Escherichia coli marcada radiactivamente64. En efecto, en la pancreatitis grave concurren las circunstancias que favorecen la aparición de translocación bacteriana: sobrecrecimiento bacteriano intestinal como consecuencia de la disminución en el peristaltismo intestinal62, y alteraciones inmunológicas y de la barrera intestinal como consecuencia de la liberación de citocinas y los trastornos hemodinámicos63-66.
Una medida de utilidad para prevenir la infección del tejido pancreático es el uso de la nutrición enteral frente a la parenteral28. Así, se ha observado en ratas con pancreatitis experimental que la nutrición enteral disminuye la translocación bacteriana y la endotoxemia67. En pacientes se ha demostrado que la nutrición enteral disminuye la incidencia de infecciones en comparación con la nutrición parenteral28,68. Otro método para evitar la infección pancreática es la administración de antibióticos profilácticos de amplio espectro por vía parenteral28. Diversos estudios han evaluado la utilidad de diferentes antibióticos en la profilaxis de la infección de la necrosis pancreática28,69. Éste es todavía un tema controvertido. Sin embargo, un reciente metaanálisis ha demostrado que la profilaxis antibiótica para evitar la infección de la necrosis pancreática mejora la supervivencia en la pancreatitis grave69.
El principal problema de la administración profiláctica de antibióticos de amplio espectro es el desarrollo de infecciones por gérmenes resistentes38, entre ellos los hongos70,71. Por ello, se ha planteado la posibilidad de utilizar probióticos en la profilaxis de la infección de la necrosis pancreática71,72. En este sentido, Li et al71 demostraron que la administración de antibióticos aumenta la translocación bacteriana por Candida albicans en ratones con pancreatitis experimental, y que una combinación de probióticos y vitaminas la disminuye. Mangiante et al72 han observado que la administración de Lactobacillus plantarum 299v a ratas con pancreatitis experimental disminuye la incidencia de translocación bacteriana. Son precisos más estudios, tanto experimentales como clínicos, para poder evaluar adecuadamente el posible papel de los probióticos en la profilaxis de la translocación bacteriana y la infección de la necrosis pancreática y la prevención del fallo multiorgánico en los pacientes con pancreatitis grave.
ENFERMEDADES HEPATICAS
La ictericia obstructiva, la insuficiencia hepática fulminante y la cirrosis representan tres situaciones que se acompañan de una elevada incidencia de infecciones bacterianas causadas por bacterias de origen intestinal. En el caso de la insuficiencia hepática fulminante, la incidencia de infecciones llega hasta el 80%29,30 y, en los pacientes cirróticos, la incidencia puede alcanzar el 40%73,74. Se considera que la translocación bacteriana, como en el caso de la pancreatitis, desempeña un papel fundamental en la patogenia de las infecciones en estos pacientes, especialmente en el desarrollo de la peritonitis bacteriana espontánea, infección frecuente y grave, característica de los pacientes cirróticos con ascitis5,10,11. Nuevamente, para explicar la translocación bacteriana concurren, en estas situaciones, el sobrecrecimiento bacteriano intestinal14,21, los trastornos en los mecanismos de defensa inmunológica15,19-21 y las alteraciones en la barrera intestinal24,25.
Diversos estudios han demostrado la eficacia de la profilaxis antibiótica en la prevención de infecciones bacterianas en los pacientes con insuficiencia hepática fulminante30,75 o con cirrosis32-34. Sin embargo, como ya se ha comentado anteriormente, el principal inconveniente de este método es la aparición de resistencias bacterianas17,18,38,76. La administración de probióticos o prebióticos puede ser una alternativa útil a los antibióticos en estos pacientes.
ICTERICIA OBSTRUCTIVA
Se ha demostrado que la ictericia obstructiva favorece la translocación bacteriana y la endotoxemia77-79, y con frecuencia estos pacientes desarrollan infecciones bacterianas, especialmente colangitis79 e insuficiencia renal79, que se han relacionado con la respuesta inflamatoria a la endotoxemia79. De nuevo, la translocación bacteriana sería debida al sobrecrecimiento bacteriano intestinal relacionado con la disminución del peristaltismo y de la concentración de bilis en la luz intestinal77,78, y a alteraciones de los mecanismos de defensa inmunológica, como el sistema reticuloendotelial81, y de la barrera intestinal26. El mejor sistema para prevenir las infecciones en estos pacientes es, evidentemente, solucionar la causa de la ictericia (extracción de cálculos coledocales, colocación de prótesis en las neoplasias). En ocasiones se administran antibióticos para evitar la colangitis, especialmente cuando se realiza una colangiopancreatografía retrógrada endoscópica79. En un modelo experimental de ictericia obstructiva en ratas se ha demostrado la utilidad de los antioxidantes (vitaminas C y E) en la prevención de la translocación bacteriana, probablemente al estabilizar la barrera intestinal26. En el campo de los prebióticos, la lactulosa disminuye la translocación bacteriana en animales de experimentación80 y la endotoxemia en pacientes con ictericia obstructiva78. No conocemos ningún estudio que haya evaluado el papel de los probióticos en la ictericia obstructiva.
INSUFICIENCIA HEPATICA FULMINANTE
Hasta la actualidad, sólo se han publicado estudios experimentales sobre el efecto de los probióticos y prebióticos en esta situación. Wang et al42 observaron, en un estudio con ratas a las que se inducía insuficiencia hepática aguda mediante hepatectomía subtotal del 90%, que la administración oral de harina de avena con Lactobacillus reuteri R2LC disminuía la incidencia de translocación bacteriana desde un 90% en las ratas con hepatectomía tratadas con salino hasta el 17% en las ratas con hepatectomía que recibieron el probiótico. Los autores demostraron que las ratas con hepatectomía tratadas con salino presentaban una alteración en la ecología de su flora intestinal. Efectivamente, se observaba en estas ratas un aumento de Escherichia coli y una disminución de lactobacilos en comparación con las ratas control. Sin embargo, en las ratas con hepatectomía tratadas con el probiótico se comprobó la corrección de este desequilibrio ecológico, aumentando los lactobacilos y, probablemente como consecuencia de ello, disminuyendo la concentración de Escherichia coli. Es decir, en este modelo experimental se observa un trastorno de la ecología intestinal normal de la rata que, probablemente, desempeña un papel importante para explicar su elevada incidencia de translocación bacteriana. Este desequilibrio es corregido por el probiótico, siendo éste al menos uno de los mecanismos por los que Lactobacillus reuteri R2LC disminuiría la incidencia de translocación bacteriana.
En otro estudio, Adawi et al82 evaluaron varios probióticos administrados por vía rectal en un modelo experimental diferente de insuficiencia hepática aguda: la administración de D-galactosamina. Nuevamente en este estudio, la incidencia de translocación bacteriana en las ratas con insuficiencia hepática que no recibieron probióticos fue muy elevada, del 100%. Las 5 especies de lactobacilos ensayadas presentaron efectos variables, obteniéndose una disminución estadísticamente significativa de la incidencia de translocación bacteriana únicamente con Lactobacillus rhamnosus.
Este estudio, además de apoyar la posible utilidad de determinados probióticos en la prevención de la translocación bacteriana en la insuficiencia hepática fulminante, es un ejemplo de un problema importante común a toda la investigación con probióticos ya comentado anteriormente: la heterogeneidad de los probióticos35,37. En efecto, existen muchos probióticos con características diferentes entre sí y, por tanto, ejercen unos efectos distintos ante una determinada situación experimental o clínica. Es decir, un probiótico concreto puede ser útil en una situación determinada, pero otro, incluso otra cepa de la misma especie, puede no producir los mismos efectos, debido a que sus propiedades son distintas. Por otra parte, un cepa puede ser útil en una situación y no serlo en otra, ya que sus propiedades así lo determinan.
En el campo de los prebióticos, Wang et al54 han observado que la administración de etilhidroxietil celulosa disminuye el sobrecrecimiento bacteriano intestinal y la translocación bacteriana en ratas con insuficiencia hepática aguda inducida mediante hepatectomía subtotal.
CIRROSIS E HIPERTENSION PORTAL
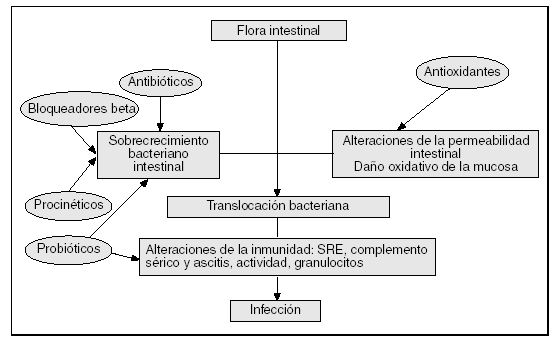
En la búsqueda de alternativas a los antibióticos en la prevención de la translocación bacteriana y las infecciones en la cirrosis se han ensayado diversas opciones que actuarían a diversos niveles de la secuencia patogénica (fig. 1).
Fig. 1. Esquema patogénico de las infecciones bacterianas en las enfermedades hepáticas y alternativas a los antibióticos en su prevención.
El sobrecrecimiento bacteriano intestinal desempeña un papel muy importante para explicar la translocación bacteriana en la cirrosis14,21. Este trastorno ecológico intestinal sería debido en gran parte al enlentecimiento en el tránsito intestinal24, consecuencia a su vez de la hipertensión portal a través del aumento en la actividad simpática, la síntesis de óxido nítrico y el daño oxidativo11,24,83. Se ha demostrado que los procinéticos13 y los bloqueadores beta24, al acelerar el enlentecido tránsito intestinal, reducen el sobrecrecimiento bacteriano intestinal y, como consecuencia, disminuyen la incidencia de translocación bacteriana en la cirrosis experimental inducida por tetracloruro de carbono (Cl4C). En pacientes cirróticos se ha observado que un procinético (cisapride) disminuye el sobrecrecimiento bacteriano intestinal al acelerar el tránsito intestinal13,84 y que los pacientes que reciben bloqueadores beta y nitratos como profilaxis secundaria de hemorragia por varices presentan una menor incidencia de peritonitis bacteriana espontánea que los pacientes en profilaxis con tratamiento endoscópico85.
Otra posibilidad es mejorar la barrera intestinal. Así, se ha observado en un modelo experimental de hipertensión portal no cirrótica (prehepática) que los antioxidantes, al mejorar el estrés oxidativo de la mucosa intestinal, probablemente consecuencia de la isquemia debida a la hipertensión portal, disminuyen la translocación bacteriana26. En la cirrosis experimental inducida por la administración de Cl4C se han obtenido resultados similares86.
La administración de probióticos podría ser, teóricamente, una alternativa muy interesante a los antibióticos en la cirrosis. En efecto, algunos probióticos poseen características que los hacen especialmente idóneos, entre las que destacan la modulación de la flora intestinal y la inmunoestimulación35,42-44,47. Ya hemos comentado la importancia del sobrecrecimiento bacteriano intestinal en la patogenia de la translocación bacteriana en la cirrosis14,21. Por tanto, cabe suponer que la administración de probióticos puede disminuir el sobrecrecimiento bacteriano, especialmente por gramnegativos, que son las bacterias más frecuentemente causantes de translocación bacteriana e infecciones en la cirrosis. Además, el efecto inmunoestimulante de los probióticos podría mejorar algunas de las alteraciones en los mecanismos de defensa inmunológica presentes en la cirrosis. Por ejemplo, se ha demostrado que Lactobacillus johnsonni La1 aumenta la actividad fagocítica de los granulocitos de sangre periférica en voluntarios sanos44. Por todo ello, los probióticos podrían ser de utilidad para la prevención de la translocación bacteriana en la cirrosis y la hipertensión portal.
Wiest et al87 han evaluado el efecto de una cepa de Lactobacillus acidophilus sobre la flora cecal y la translocación bacteriana en ratas con hipertensión portal prehepática, sin observar diferencias en la concentración de enterobacterias en el ciego ni en la incidencia de translocación bacteriana entre las ratas control y las tratadas con el probiótico. Sin embargo, la hipertensión portal prehepática experimental no reproduce adecuadamente muchas de las alteraciones presentes en la cirrosis.
Por ello, se han realizado dos estudios que han investigado el efecto de los probióticos en la cirrosis experimental inducida mediante la administración de Cl4C. En uno de ellos, Bauer et al88 han utilizado Lactobacillus GG, un probiótico que ha demostrado su eficacia en diversos campos, especialmente en el tratamiento y la prevención de la diarrea infantil48,51. En este estudio tampoco se encontraron diferencias entre las ratas tratadas y las ratas control en la concentración de enterobacterias cecales ni en la incidencia de translocación bacteriana o de peritonitis bacteriana. Sin embargo, como ya se ha comentado anteriormente, cepas diferentes de probióticos pueden tener efectos diferentes en una misma situación experimental o clínica; es decir, el hecho de que Lactobacillus GG no fuera eficaz en este modelo experimental no implica que otro probiótico sí pudiera serlo35,47,83.
En un estudio realizado en nuestro laboratorio por Chiva et al86 se ha evaluado la administración de un vehículo con antioxidantes (vitamina C y glutamato) asociado o no a un probiótico, Lactobacillus johnsonii La1 en la misma situación experimental, en ratas con cirrosis inducida por Cl4C. En este estudio pudimos comprobar que los antioxidantes, asociados o no al probiótico, disminuían la concentración de enterobacterias de la flora intestinal y reducían la incidencia de translocación bacteriana con respecto a las ratas cirróticas tratadas con agua. Probablemente este efecto fuera debido a que la disminución del daño oxidativo de la mucosa intestinal habría mejorado el peristaltismo intestinal89, disminuyendo así el sobrecrecimiento bacteriano, y habría reducido la permeabilidad intestinal al paso de bacterias27. Sin embargo, sólo las ratas tratadas con antioxidantes asociados a Lactobacillus johnsonii La1 presentaron una disminución estadísticamente significativa de la endotoxemia, probablemente como consecuencia de un efecto estimulante del probiótico sobre la actividad destoxificante del sistema reticuloendotelial, deprimida en la cirrosis y en parte responsable de la endotoxemia que ocurre en esta enfermedad90,91. Este efecto no se habría producido en las ratas tratadas sólo con antioxidantes.
Existen muy pocos datos disponibles en pacientes cirróticos y, en cualquier caso, ningún estudio ha evaluado la posible utilidad de los probióticos en la prevención de infecciones en estos pacientes. Ya hemos comentado anteriormente las consecuencias desfavorables que la translocación bacteriana (aparte de favorecer las infecciones) puede producir en la cirrosis. Efectivamente, el paso fuera de la luz intestinal de las bacterias o sus productos, como la endotoxina, constituye un estímulo fluctuante pero continuado en el tiempo para la producción de citocinas proinflamatorias, como el factor de necrosis tumoral alfa (TNF-α) o la interleucina 6 (IL-6), entre otras, de óxido nítrico y de otras sustancias con actividad vasoactiva, como la prostaciclina, que pueden empeorar el daño celular hepático, especialmente el TNF-α, y aumentar las alteraciones hemodinámicas de la cirrosis6,90,92-94.
El aumento en las concentraciones de determinadas citocinas y el estímulo antigénico mantenido pueden favorecer la desregulación del sistema inmunitario y, así, contribuir al desarrollo de infecciones6. En este sentido, se ha demostrado que la descontaminación intestinal selectiva con norfloxacina aumenta los valores del factor C3 del sistema del complemento en el líquido ascítico en pacientes cirróticos con ascitis95. Este hecho sugiere que uno de los factores predisponentes a la infección más importantes en los pacientes cirróticos, la disminución en los valores de complemento en sangre y ascitis21,96, sería debido, al menos en parte, a la llegada continuada de bacterias o sus productos (que consumirían dichos factores) a la sangre y al líquido ascítico. La administración de antibióticos disminuiría la translocación bacteriana y aumentaría las concentraciones de complemento al disminuir su consumo.
Finalmente, el incremento en la presión portal y en la vasodilatación esplácnica favorecerían la aparición de complicaciones, como la hemorragia digestiva por varices o el desarrollo de ascitis e insuficiencia renal94,97. El hecho de que la descontaminación intestinal con antibióticos disminuya la producción de óxido nítrico90 y el grado de vasodilatación en los pacientes cirróticos98, probablemente al disminuir la translocación bacteriana, apoyaría esta hipótesis. Por todo ello, podemos suponer que la administración de probióticos, si redujera la translocación bacteriana, mejoraría la hemodinámica de los pacientes cirróticos. En este sentido, De Santis et al99 han observado una disminución en la presión portal estimada por ecografía Doppler en un paciente cirrótico tratado con una combinación de probióticos (VSL#3).
En el campo de los prebióticos, la lactulosa y el lactitol son utilizados en los pacientes cirróticos para el tratamiento y la prevención de la encefalopatía hepática. Se ha observado que la administración de lactitol disminuye la concentración de enterobacterias y enterococos en la flora fecal de pacientes cirróticos56 y, por este mecanismo, podría disminuir la translocación bacteriana y la incidencia de infecciones. Teniendo en cuenta que la endotoxemia favorece la translocación bacteriana27, la capacidad de la lactulosa para disminuir la endotoxemia78 también podría contribuir a la prevención de la translocación en estos pacientes.
La administración de probióticos y prebióticos ofrece grandes posibilidades en la prevención de la translocación bacteriana y sus consecuencias en las enfermedades hepáticas. Sin embargo, los datos disponibles son aún muy escasos y es necesaria la realización de más estudios, tanto experimentales como clínicos, para determinar la posible utilidad de los probióticos y prebióticos en estas enfermedades.