Los errores de medicación son el evento adverso más frecuente de la asistencia sanitaria. La validación farmacéutica (VF) busca reducirlos. Los objetivos fueron evaluar el impacto de la implementación de una mejora de la calidad mediante una herramienta de priorización automática de la validación (HPAV) de fármacos de alta relevancia clínica (FARC) en pacientes hospitalizados en el tiempo hasta la intervención farmacéutica (IF), y en el número de errores de medicación detectados.
Material y métodosEstudio retrospectivo-observacional unicéntrico de dos fases. Fase preexposición (F-Pre): VF de camas con dispensación en dosis unitaria (octubre-2015/febrero-2016). Fase postexposición (F-Post): VF utilizando una HPAV de FARC en camas de hospitalización (octubre-2016/febrero-2017).
Se seleccionaron los FARC del listado de fármacos de alto riesgo del Institute for Safe Medication Practices. Los datos se obtuvieron del registro de IF (Access®) y de la prescripción electrónica. Las variables recogidas fueron: edad y sexo de los pacientes, características del fármaco prescrito, tiempo hasta IF. Se compararon los resultados de ambas fases (pre- y postexposición).
ResultadosSe analizaron 477 IF en 404 pacientes, con una edad media de 65,9±19,5 años (53,22% mujeres). El tiempo medio hasta IF fue de 25,6±24,72h en la F-Pre y 18,87±20,44h en la F-Post (p=0,01). En la F-Pre se realizaron 106 IF (35,85% prevención de reacciones adversas) frente a 371 IF (39,62% conciliación de la medicación) en la F-Post.
ConclusionesLa herramienta de priorización automática de la validación de fármacos permitió detectar e intervenir un mayor número de errores de medicación en los pacientes hospitalizados. Además, se pudo reducir significativamente el tiempo hasta la IF.
Medication errors are the most common adverse events in healthcare. Pharmaceutical validation (PV) seeks to reduce them. The aims of this study were to assess the impact of the introduction of an automated tool for the validation (VPAT) of the high clinical relevance drugs prescription (HCRD) over time of pharmaceutical intervention (PI), and to quantify the number of medication errors detected before and after its implementation.
Material and methodsA two phase retrospective-observational single centre study was designed. A pre-intervention phase (Pre-P): PV of beds with Unit Dose Dispensing (October 2015 - February 2016), was followed by a post-intervention phase (Post-P): PV using a VPAT of HCRD in hospital patients (October 2016 - February 2017).
HCRD were selected from the list of high-risk drugs of Institute for Safe Medication Practices. The data was obtained from the PI record (Access®) and the computerised prescription. The variables collected were: age and gender of the patients included, data of drugs prescription, and time to PI.
ResultsA total of 477 PI were analysed in 404 patients, with a mean age of 65.9±19.5 years (53.22% women). The mean time up to PI was 25.6±24.72h in the Pre-P, and 18.87±20.44h in the Post-P (P=0.01). In Pre-P, 106 PI were performed (35.85% prevention of adverse reactions) compared to 371 PI (39.62% medication reconciliation) in Post-P.
ConclusionsThe VPAT enabled a greater number of medication errors to be detected and intervened in hospitalised patients, with a significantly reduced time to PI.
Uno de los objetivos principales de los profesionales sanitarios es garantizar la seguridad del paciente. Para poder cumplir con tal objetivo, se puede actuar de forma específica en los distintos niveles asistenciales y en las transiciones entre estos niveles. Uno de los puntos críticos puede ser velar por una farmacoterapia segura a través de la revisión de las prescripciones médicas.
Los errores de medicación (EM) son el evento adverso más frecuente de la asistencia sanitaria1, pudiendo afectar al curso clínico del paciente, a su calidad de vida o incluso relacionarse con mayor mortalidad2. El estudio EMOPEM cuantificó los EM observados en distintos hospitales durante los años 2007 a 2011, observándose estos con una frecuencia de entre el 21,7 y el 35,6% en los distintos períodos estudiados3. Centrándonos en los pacientes hospitalizados, el estudio ENEAS mostró que los eventos adversos más frecuentes eran los relacionados con la medicación (37,4%), siendo más de un tercio de estos prevenibles (34,8%)4.
Estos EM son susceptibles de ocurrir en cualquier etapa del proceso farmacoterapéutico, destacando la prescripción, transcripción y administración5. La implantación de la prescripción electrónica asistida es una mejora que incrementa notablemente la seguridad del paciente, ya que permite evitar errores de interpretación de prescripciones manuales e incorporar alertas predefinidas6. Innovaciones tecnológicas más avanzadas, como la implementación de sistemas de soporte a la toma de decisiones clínicas7, ayudan más si cabe a reducir la probabilidad de EM. No obstante, se trata de una herramienta compleja, que precisa de softwares no disponibles en todos los centros y que no resuelven errores clásicos como la conciliación incorrecta de la medicación. La validación farmacéutica, como filtro de seguridad externo entre la orden médica y la administración enfermera, permite también prevenir otro tipo de errores como son las dosis o pautas incorrectas por una mala cumplimentación del formulario electrónico.
Los servicios de farmacia hospitalaria ofrecen este filtro de seguridad gracias al proceso de revisión de tratamiento de los pacientes ingresados conocido como validación farmacéutica8. Un proceso por el cual, disponiendo de la información clínica del paciente (a través de las historias clínicas, informes de atención primaria) y aplicando el conocimiento de la farmacoterapia en su conjunto característico de la profesión, el farmacéutico realiza una valoración del tratamiento del paciente y valida el tratamiento en caso de considerarlo adecuado. En caso de que no sea así, se realiza una serie de recomendaciones al prescriptor para evitar y solventar posibles errores de prescripción, o adecuar el tratamiento a las características individuales del paciente (pacientes ancianos, situación de insuficiencia renal, etc.). A este proceso se le conoce como intervención farmacéutica (IF)9.
Cabe destacar que existe una alta heterogeneidad de patologías dentro del ámbito hospitalario, el curso clínico de las mismas es cambiante, la variabilidad en las características inter- e intraindividuales, la alta complejidad terapéutica de los pacientes pluripatológicos, etc. Esto hace que no todos los pacientes se beneficien en la misma medida del proceso de revisión del tratamiento farmacológico. Un ejemplo es el estudio de Delgado Silveira et al. en el que se pudo observar como la IF en la población anciana reduce significativamente los problemas relacionados con los medicamentos10. Se hace por tanto necesaria la priorización de los pacientes en la validación farmacéutica para detectar EM en el menor tiempo posible. En vista de esto, en nuestro servicio de farmacia se diseñó una herramienta para mejorar la calidad asistencial que permitiera focalizar la actuación en pacientes en tratamiento con fármacos de alta relevancia clínica (FARC).
Los objetivos de este trabajo fueron evaluar si la utilización de esta herramienta de priorización de la validación de FARC podía reducir el tiempo hasta IF y cuantificar el número de EM detectados por el farmacéutico antes y después de su implantación. Asimismo, evaluar el grado de aceptación de las intervenciones realizadas.
Material y métodosSe diseñó un estudio retrospectivo, observacional y unicéntrico con dos fases.
Una fase preexposición (septiembre-2015 a abril-2016): en ella se utilizó un sistema de validación convencional en el que el orden de validación va determinado por la logística de distribución de medicamentos a los servicios clínicos (sistema de dispensación de medicamentos en dosis unitaria, 800 camas). La segunda fase o fase postexposición (septiembre-2016 a abril-2017): correspondió a una fase donde se implantó un filtro localizador que permite priorizar la validación de FARC, independientemente del sistema de dispensación.
Este estudio se realizó en un hospital universitario de 1.200 camas. En ambas fases, la validación farmacéutica se llevó a cabo por parte del Área de Validación Farmacoterapéutica (durante los días laborables) y del personal farmacéutico de guardia (días no laborables) de forma ininterrumpida. En la fase postexposición, la herramienta de priorización de la validación se utilizó en dos momentos del día (por la mañana y por la tarde).
Fármacos de alta relevancia clínicaLos fármacos de alta relevancia clínica o FARC incluidos en la validación prioritaria fueron consensuados por el servicio de farmacia a partir del listado de fármacos de alto riesgo del Institute for Safe Medication Practices (ISMP). Estos fármacos fueron: antineoplásicos orales, antiarrítmicos de estrecho margen terapéutico (digoxina), inmunosupresores, fármacos para el tratamiento de la hipertensión pulmonar, antirretrovirales (tratamiento del VIH), fármacos para el tratamiento de la hepatitis B y la hepatitis C.
Variables estudiadasLos datos se obtuvieron de una descarga de prescripciones realizadas durante los períodos evaluados, del registro de IF del servicio de farmacia (creado en Access®) y de la prescripción integrada en la historia clínica electrónica. Las variables recogidas fueron: edad, sexo, fármaco, grupo farmacológico, tipo de intervención realizada, tiempo hasta que se realizó la intervención y grado de aceptación de estas.
Análisis estadísticoEl análisis estadístico se realizó con el software IBM SPSS® Statistics (Nueva York, Estados Unidos). La homogeneidad entre las poblaciones se analizó mediante la prueba t de Student y el test de chi-cuadrado. El estudio de asociación entre la variable cuantitativa «tiempo hasta IF» se calculó mediante la prueba t de Student.
Los parámetros que se estudiaron fueron el tiempo medio hasta IF, las diferencias de tiempo medio entre ambas fases y el grado de aceptación, tanto globales como por grupos terapéuticos. Se incluyeron en el estudio todos los datos obtenidos, pero solo se analizaron los datos globales y los de aquellos grupos terapéuticos sobre los que se habían realizado más de 10 intervenciones en ambas fases del estudio.
ResultadosSe analizaron un total 477 intervenciones en 404 pacientes (1,18 intervenciones/paciente) con una media de edad de 65,9±19,5años, de los cuales el 53,22% fueron mujeres. Se compararon los datos de ambas fases y se comprobó que existían diferencias estadísticamente significativas en las características de los pacientes en cuanto a la edad y el sexo en las fases comparadas (p=0,002 y p<0,05, respectivamente).
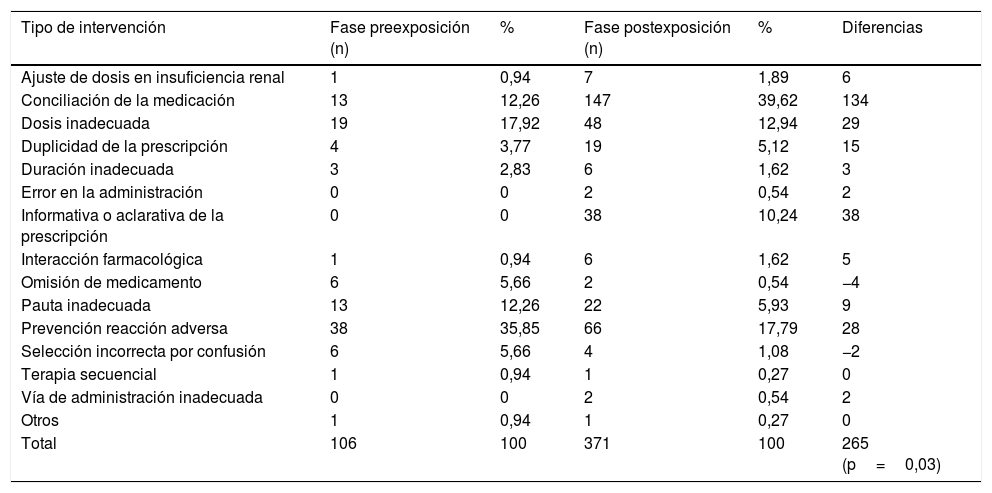
En las tablas 1 y 2 se recogen las intervenciones realizadas por tipos y por grado de aceptación, respectivamente, en ambas fases, así como las diferencias encontradas entre las mismas. En la tabla 3 se recogen los datos de intervenciones realizadas, grado de aceptación y tiempo por intervención agrupados por grupos terapéuticos. Se recogen también las diferencias halladas en cuanto al tiempo por intervención.
Intervenciones farmacéuticas realizadas, por tipo de intervención, en ambas fases
| Tipo de intervención | Fase preexposición (n) | % | Fase postexposición (n) | % | Diferencias |
|---|---|---|---|---|---|
| Ajuste de dosis en insuficiencia renal | 1 | 0,94 | 7 | 1,89 | 6 |
| Conciliación de la medicación | 13 | 12,26 | 147 | 39,62 | 134 |
| Dosis inadecuada | 19 | 17,92 | 48 | 12,94 | 29 |
| Duplicidad de la prescripción | 4 | 3,77 | 19 | 5,12 | 15 |
| Duración inadecuada | 3 | 2,83 | 6 | 1,62 | 3 |
| Error en la administración | 0 | 0 | 2 | 0,54 | 2 |
| Informativa o aclarativa de la prescripción | 0 | 0 | 38 | 10,24 | 38 |
| Interacción farmacológica | 1 | 0,94 | 6 | 1,62 | 5 |
| Omisión de medicamento | 6 | 5,66 | 2 | 0,54 | −4 |
| Pauta inadecuada | 13 | 12,26 | 22 | 5,93 | 9 |
| Prevención reacción adversa | 38 | 35,85 | 66 | 17,79 | 28 |
| Selección incorrecta por confusión | 6 | 5,66 | 4 | 1,08 | −2 |
| Terapia secuencial | 1 | 0,94 | 1 | 0,27 | 0 |
| Vía de administración inadecuada | 0 | 0 | 2 | 0,54 | 2 |
| Otros | 1 | 0,94 | 1 | 0,27 | 0 |
| Total | 106 | 100 | 371 | 100 | 265 (p=0,03) |
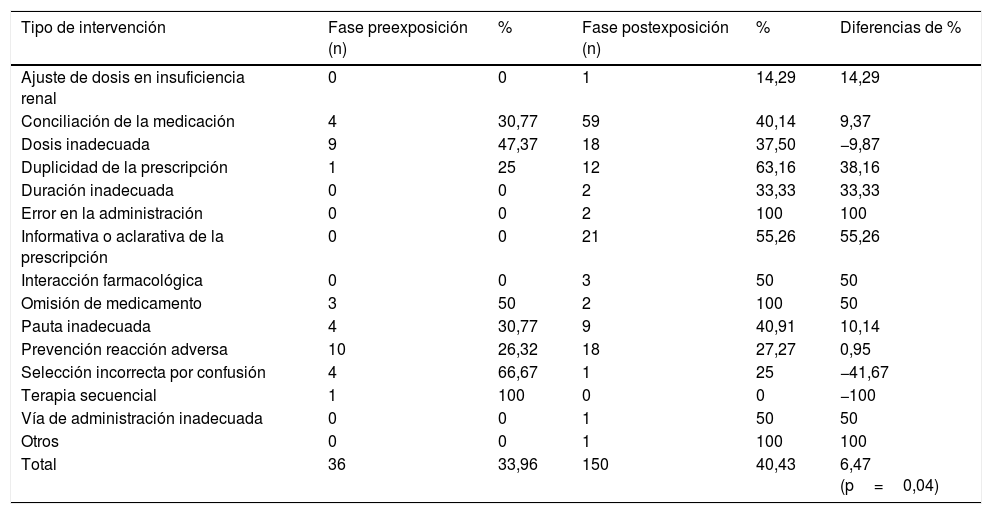
Intervenciones farmacéuticas aceptadas, por tipo de intervención, en ambas fases y diferencia de porcentaje entre ellas
| Tipo de intervención | Fase preexposición (n) | % | Fase postexposición (n) | % | Diferencias de % |
|---|---|---|---|---|---|
| Ajuste de dosis en insuficiencia renal | 0 | 0 | 1 | 14,29 | 14,29 |
| Conciliación de la medicación | 4 | 30,77 | 59 | 40,14 | 9,37 |
| Dosis inadecuada | 9 | 47,37 | 18 | 37,50 | −9,87 |
| Duplicidad de la prescripción | 1 | 25 | 12 | 63,16 | 38,16 |
| Duración inadecuada | 0 | 0 | 2 | 33,33 | 33,33 |
| Error en la administración | 0 | 0 | 2 | 100 | 100 |
| Informativa o aclarativa de la prescripción | 0 | 0 | 21 | 55,26 | 55,26 |
| Interacción farmacológica | 0 | 0 | 3 | 50 | 50 |
| Omisión de medicamento | 3 | 50 | 2 | 100 | 50 |
| Pauta inadecuada | 4 | 30,77 | 9 | 40,91 | 10,14 |
| Prevención reacción adversa | 10 | 26,32 | 18 | 27,27 | 0,95 |
| Selección incorrecta por confusión | 4 | 66,67 | 1 | 25 | −41,67 |
| Terapia secuencial | 1 | 100 | 0 | 0 | −100 |
| Vía de administración inadecuada | 0 | 0 | 1 | 50 | 50 |
| Otros | 0 | 0 | 1 | 100 | 100 |
| Total | 36 | 33,96 | 150 | 40,43 | 6,47 (p=0,04) |
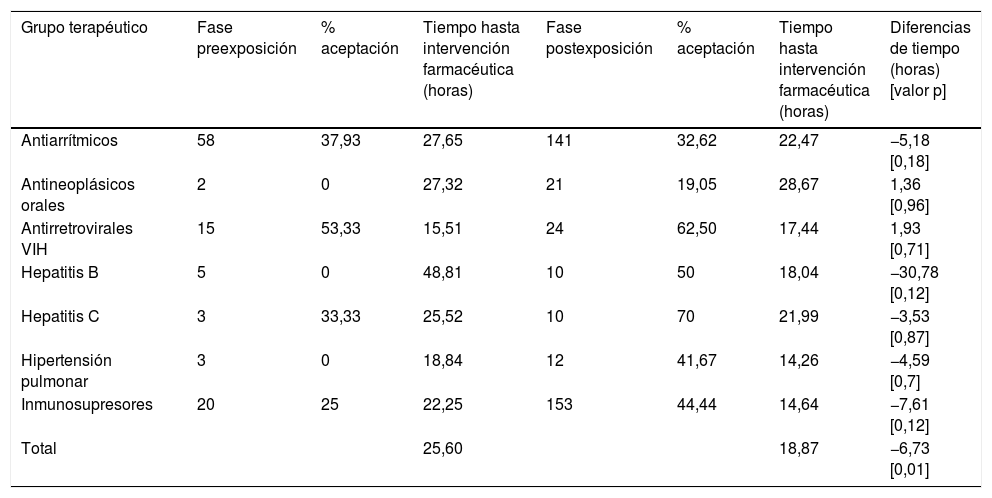
Intervenciones realizadas por grupos terapéuticos, porcentaje de aceptación, tiempo por intervención y diferencias de este entre ambas fases
| Grupo terapéutico | Fase preexposición | % aceptación | Tiempo hasta intervención farmacéutica (horas) | Fase postexposición | % aceptación | Tiempo hasta intervención farmacéutica (horas) | Diferencias de tiempo (horas) [valor p] |
|---|---|---|---|---|---|---|---|
| Antiarrítmicos | 58 | 37,93 | 27,65 | 141 | 32,62 | 22,47 | −5,18 [0,18] |
| Antineoplásicos orales | 2 | 0 | 27,32 | 21 | 19,05 | 28,67 | 1,36 [0,96] |
| Antirretrovirales VIH | 15 | 53,33 | 15,51 | 24 | 62,50 | 17,44 | 1,93 [0,71] |
| Hepatitis B | 5 | 0 | 48,81 | 10 | 50 | 18,04 | −30,78 [0,12] |
| Hepatitis C | 3 | 33,33 | 25,52 | 10 | 70 | 21,99 | −3,53 [0,87] |
| Hipertensión pulmonar | 3 | 0 | 18,84 | 12 | 41,67 | 14,26 | −4,59 [0,7] |
| Inmunosupresores | 20 | 25 | 22,25 | 153 | 44,44 | 14,64 | −7,61 [0,12] |
| Total | 25,60 | 18,87 | −6,73 [0,01] |
En la fase preexposición se realizaron un total de 106 intervenciones sobre los fármacos seleccionados, con un tiempo medio por intervención de 25,60±24,72h. En la fase postexposición se realizaron un total de 371 intervenciones sobre los fármacos seleccionados, con un tiempo medio por intervención de 18,87±20,44h. Estas diferencias fueron estadísticamente significativas (p=0,01).
DiscusiónEn términos globales, se pudo observar un descenso de 6,73h (p=0,01) en el tiempo hasta detección e intervención sobre EM de los fármacos seleccionados. Este descenso del tiempo es particularmente destacado en los dos grupos sobre los que mayor número de IF se realizaron en ambas fases: antiarrítmicos (27,65h en la fase preexposición vs. 22,47h en la fase postexposición) e inmunosupresores (22,25h vs. 14,6h, respectivamente). Por el contrario, no se observó una disminución de este tiempo hasta IF en los grupos de antineoplásicos orales y fármacos antirretrovirales para el tratamiento del VIH. En este análisis por grupos terapéuticos, los resultados no fueron estadísticamente significativos.
Atendiendo al número de IF realizadas y a su grado de aceptación, se realizaron un mayor número de intervenciones en la fase postexposición (incremento absoluto de 265 intervenciones; p=0,03), obteniendo un grado de aceptación significativamente mayor en esta fase (incremento absoluto del 6,47%; p=0,04). El hecho de que haya habido un aumento importante en el número de intervenciones realizadas puede deberse al sistema de registro de las intervenciones. En la fase preexposición las intervenciones se registraban de forma manual en la base de datos, abriendo la posibilidad de que no se registraran el total de IF realizadas por el limitado tiempo disponible para ello. Sin embargo, en la fase postexposición se desarrolló un sistema informático que permitió la automatización de este registro desde la prescripción electrónica y, por tanto, el registro del total de las IF realizadas.
En cuanto a los grupos terapéuticos, aquellos con IF más frecuentes coinciden en ambas fases: inmunosupresores y antiarrítmicos han sido los grupos con mayor número de errores detectados. En los fármacos inmunosupresores se observa un aumento importante de la proporción de intervenciones realizadas (18,86% vs. 41,24%), con un mayor grado de aceptación de estas (25% vs. 44,44%). Dentro de los antiarrítmicos, hay un descenso de la proporción de intervenciones realizadas (54,72% vs. 38,01%), pero se mantiene un similar grado de aceptación de estas (37,93% vs. 38,01%). El hecho de que se mantenga el grado de aceptación a pesar de disminuir el número de intervenciones podría atribuirse a que el cambio en la prioridad del proceso de validación (anteponer el alto impacto clínico de EM en estos grupos de fármacos a la dispensación de medicamentos a las unidades de hospitalización) hace que se revisen los tratamientos con mayor exhaustividad, interviniendo solamente en aquellos errores que realmente suponen un peligro para el paciente. De esta manera, se evitan intervenciones que no aportan valor al proceso de validación. En el caso concreto de los antiarrítmicos, otra probable explicación es que en ambas fases estos fármacos se revisaban diariamente al tratarse de medicamentos potencialmente inapropiados (MPI) en la población anciana, por lo que su proceso de validación no se vio alterado por el estudio.
Haciendo el análisis de los tipos de intervenciones, se observa nuevamente que los EM más frecuentes detectados e intervenidos mantienen un perfil similar en ambas fases. No obstante, cabe destacar el mayor peso del proceso de conciliación de la medicación para la detección de errores en los pacientes ingresados, con un aumento del porcentaje de este tipo de intervenciones (12,26% en la fase preexposición frente al 39,62% en la fase postexposición), teniendo además un grado de aceptación mayor (30,77% y 40,14%, respectivamente).
En cuento al tiempo hasta intervención, Pablos et al. realizaron un estudio en fármacos antirretrovirales VIH en el que midieron el tiempo hasta la detección de errores de conciliación11, obteniendo una mediana de 68h hasta detección e intervención. No obstante, solo se ha podido acceder al resumen del estudio en el momento de la redacción del artículo. No se han encontrado referencias a otros estudios publicados que hayan analizado el tiempo hasta IF, por lo que se puede decir que nuestro estudio es el primero que cuantifica tanto la duración de este proceso como la reducción de EM tras la implantación del sistema de validación prioritaria.
Existen trabajos que han estudiado el grado de aceptación de las intervenciones realizadas en diferentes niveles asistenciales12,13. Dentro del ámbito hospitalario, Bertoldo y Paraje obtuvieron un grado de aceptación del 94-96%14, mientras que Gaspar et al. obtuvieron un 72,6%15. En ambos casos se contabilizaron las IF realizadas sobre cualquier tipo de fármaco, siendo la comunicación de estas de forma presencial y mediante parte interconsulta, respectivamente, y mediante notas asociadas a la prescripción electrónica en el caso de nuestro estudio. Esto podría explicar la diferencia en el grado de aceptación, ya que tanto la presencia física en el equipo clínico como la rutina de lectura de partes interconsultas facilitan la aceptación de las IF realizadas.
A pesar de obtener un grado de aceptación inferior a los de la bibliografía consultada (40,43% en el período postexposición), el proceso de validación farmacéutica consta de reconocimiento en nuestro centro y cuenta con buena valoración por parte de los demás profesionales sanitarios16, lo que implica un importante papel del farmacéutico a la hora de revisar los tratamientos.
La principal limitación de nuestro estudio fue que el proceso de validación de tratamientos y, por tanto, la detección e intervención de EM, solo era posible en las unidades de hospitalización con prescripción electrónica. A pesar de que esta prescripción se encontraba instaurada en toda la hospitalización convencional, no se pudo acceder a las prescripciones de ciertas unidades que utilizan habitualmente estos fármacos, como las unidades de cuidados intensivos o el servicio de urgencias, y no fue posible llevar a cabo la revisión de tratamientos y detección de posibles EM.
En conclusión, la implantación de una herramienta de priorización en la validación permitió detectar e intervenir un mayor número de EM en FARC, reduciendo significativamente el tiempo hasta la IF. De los grupos terapéuticos analizados, inmunosupresores y antiarrítmicos de estrecho margen terapéutico fueron los grupos en los que se observaron más EM, con una relevante reducción en el tiempo hasta IF a estos errores.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.