Determinar el riesgo de presentar eventos cardiovasculares mayores en pacientes con síndrome coronario agudo e implante de stent, que suspendieron la doble terapia antiagregante antes de un año de tratamiento.
MétodosEstudio analítico de pacientes con síndrome coronario agudo e implante de stent que recibieron doble terapia antiagregante al egreso hospitalario. Se describieron las características sociodemográficas, clínicas y paraclínicas. Se determinó la prevalencia de suspensión de doble terapia antiagregante antes de un año de tratamiento y el riesgo de eventos cardiovasculares mayores mediante un modelo de riesgos proporcionales Cox.
ResultadosSe incluyeron 873 pacientes. La prevalencia de suspensión de doble terapia antiagregante fue 39,18%. El grupo que continuó la terapia por un año tuvo mayor frecuencia de enfermedad coronaria previa (19,13% p=0,03). La principal indicación del procedimiento en los pacientes que suspendieron la terapia fue infarto sin ST elevado (36,8%). La suspensión de la doble terapia antiagregante antes del año estuvo asociada con mayor incidencia de MACE a un año (HR 1,31 95% IC 0,65-2,62 p=0,45). La presencia de enfermedad arterial periférica, diabetes mellitus y más de un vaso enfermo se relacionó con eventos adversos cardiovasculares a un año.
ConclusionesLa suspensión antes de los doce meses de la doble terapia antiagregante en pacientes con implante de stent posterior a un síndrome coronario agudo, es frecuente y parece no estar asociada con mayor incidencia de desenlaces cardiovasculares mayores; sin embargo, la causa de la interrupción puede influir en los desenlaces clínicos y debe tenerse en cuenta en la práctica clínica.
To determine the risk of developing major adverse cardiovascular events (MACEs) in patients with acute coronary syndrome and stent implant who suspended dual antiplatelet therapy before one year of treatment.
MethodsAnalytical study of patients with acute coronary syndrome and stent implant who received dual antiplatelet therapy upon hospital admission. Sociodemographic, clinical and paraclinical features were described. The prevalence of dual antiplatelet therapy suspension before one year of treatment was determined, and for assessing the risk of major adverse cardiovascular events a Cox proportional hazard regression model was used.
Results873 patients were included. Prevalence of dual antiplatelet therapy suspension was 39.18%. The group who continued the therapy during a year had a higher frequency of previous coronary disease (19.13%, p=0.03). The main indication for the procedure in patients who interrupted their treatment was infarction without ST elevation (36.8%). Dual therapy suspension before one year was not related to a higher incidence of MACEs after one year (HR 1.31, CI 95% 0.65-2.62 p=0.45). The presence of peripheral arterial disease, diabetes mellitus and more than one abnormal vessel was related to adverse cardiovascular effects within one year.
ConclusionsThe suspension of dual antiplatelet therapy before twelve months in patients with a stent implant posterior to an acute coronary syndrome is frequent and does not seem to be associated to a higher incidence of major adverse cardiovascular events; nevertheless, the reason for the interruption could influence the clinical outcome and must be taken into account for clinical practice.
La doble terapia antiagregante consiste en la administración de ácido acetilsalicílico más un inhibidor del receptor plaquetario P2Y12 como clopidogrel, prasugrel o ticagrelor, posterior a la implantación de stent coronario, ya que, se ha demostrado que esta reduce la incidencia de eventos cardiovasculares mayores tales como muerte, infarto agudo de miocardio y trombosis del stent1,2.
Las guías recomiendan que la duración de la doble terapia sea de por lo menos 12 meses tanto para stent convencional como para medicado, en pacientes con síndrome coronario agudo3. Sin embargo, se reportan tasas de interrupción del 8,8 al 14% dentro de los doce meses siguientes. Las principales causas del cese prematuro son los eventos adversos de sangrado, la necesidad de cirugía y por indicación médica4,5.
A pesar de las recomendaciones de las guías de manejo de la doble terapia antiagregante (DTA), existe divergencia frente al tiempo exacto de duración del tratamiento, pues se ha demostrado que la interrupción prematura de los inhibidores del P2Y12 es un factor de riesgo para desarrollar algún tipo de evento cardiovascular mayor. Con el fin de esclarecer los hallazgos en los diferentes estudios, se han llevado a cabo revisiones sistemáticas y metaanálisis que tratan de explicar los beneficios y daños de la suspensión o continuación de la doble terapia antiagregante y su impacto en los resultados clínicos. En estos se concluye que hay evidencia considerable que apoya el riesgo elevado de eventos cardiovasculares adversos debido a la suspensión del clopidogrel, como también que la tasa de riesgo/beneficio entre suspender o continuar la doble terapia después de un periodo inicial recomendado, debe ser individualizada con base en los riesgos futuros de sangrado o infarto de miocardio que tenga cada paciente. Adicionalmente, se concluye que mucha de esta evidencia es cuestionable y el tiempo exacto permanece incierto, y por consiguiente se necesitan más estudios6–8.
Dada la incertidumbre que envuelve este tema y la disponibilidad actual de stents de segunda y tercera generación, que tienen menor incidencia de trombosis tardía del stent, se consideró determinar si la suspensión temprana (antes de los 12 meses) de la doble terapia antiagregante, aumenta la incidencia de eventos cardiovasculares mayores (MACE) en una cohorte de pacientes con síndrome coronario agudo que fueron llevados a intervención coronaria percutánea con implante de stent.
MétodosEstudio observacional analítico basado en un registro institucional de la Fundación Valle del Lili, clínica de alta complejidad ubicada en Cali, Colombia, llamado DREST (Drug Eluting Stent) el cual incluye adultos de 18 años o más a quienes se les ha hecho intervencionismo coronario percutáneo con implante de stent convencional o medicado a partir del año 1994. El registro incluye información sociodemográfica y antecedentes médicos del paciente, del procedimiento índice (angiografía coronaria), características de la lesión y de los stent implantados. Además, se obtiene información del egreso hospitalario y del seguimiento en los meses 1, 6 y 12 posteriores al procedimiento, incluyendo variables como síntomas, recurrencia de eventos cardiovasculares mayores, estado vital y medicamentos recibidos. El seguimiento se realiza de forma personal en los controles periódicos por cardiología o vía telefónica cuando no hay información de los controles médicos.
Para el estudio fueron elegibles los pacientes que se encontraran en el registro DREST desde el 01 de enero de 2008 hasta el 31 de diciembre de 2014. Participaron pacientes que tuvieran implante de stent convencional o medicado cuya indicación fuese síndrome coronario agudo incluyendo así infarto agudo de miocardio con elevación del segmento ST (IAMSTE), infarto agudo de miocardio sin elevación del segmento ST (IAMNST) y angina inestable; además, al momento del egreso hospitalario recibían terapia dual con ácido acetilsalicílico y clopidogrel. Se excluyó a los pacientes con stent de primera generación (recubiertos con paclitaxel o sirolimus), terapia antiplaquetaria dual con ticagrelor o prasugrel, o procedimientos realizados antes del 01 de enero de 2008.
Se definió IAMSTE como el cuadro clínico de dolor torácico sugestivo de isquemia asociado con elevación de biomarcadores cardíacos, troponina I como positiva cuando fue mayor del percentil 99 para el valor de referencia y nueva o presumible elevación del segmento ST–onda T, o cambios de bloqueo completo de rama izquierda nuevos, desarrollo de ondas Q patológicas en el electrocardiograma o identificación de un trombo intracoronario durante angiografía. Se definió IAMNST cuando se presentó lo anterior excepto elevación del ST, en tanto que angina inestable como la presencia de dolor torácico sugestivo de isquemia en paciente con factores de riesgo sin evidencia de hallazgos electrocardiográficos sugestivos de isquemia o troponina I positiva9.
Las características de la lesión tratada se clasificaron según las guías del Colegio americano de cardiología en lesión tipo A, B1, B2 y C10. Posterior al implante del stent se tuvo en cuenta la clasificación de Thrombolysis in Myocardial Infarction (TIMI) como marcador angiográfico de la eficacia de la reperfusión coronaria; se definió de la siguiente forma: TIMI 0, ausencia de perfusión; TIMI 1, penetración sin perfusión; TIMI 2, reperfusión parcial; TIMI 3, perfusión completa11. Los eventos cardiovasculares mayores en este estudio son el combinado de muerte por todas las causas (cardíaca o no cardíaca), IAMSTE o IAMNST y necesidad de revascularización del vaso tratado, definida como cualquier intervención percutánea repetida o derivación quirúrgica de cualquier segmento del vaso diana.
Se describieron las características demográficas, antecedentes médicos e indicación del procedimiento de los pacientes llevados a intervención coronaria percutánea e implante de stent mediante números absolutos y porcentajes de prevalencia de cada factor, lo cual se graficó en una tabla de acuerdo con el uso de la DTA durante un año comparado con el uso por menos de un año. Las pruebas de comparación se llevaron a cabo con prueba de Chi2 o test exacto de Fisher de acuerdo con el cumplimiento de supuestos. Para las variables cuantitativas como la edad se realizó la prueba de Shapiro-Wilk para determinar la distribución normal y según cumplimiento de supuestos se describieron como promedios o medianas, con medidas de dispersión, desviación estándar o rango intercuartílico. Se compararon con pruebas paramétricas (t de Student) en caso de cumplir con los supuestos de normalidad, o pruebas no paramétricas (Wilcoxon, Mann-Whitney) en caso contrario.
Se estableció como suspensión de DTA aquel individuo que luego del egreso hospitalario, durante el control del primer y sexto mes refirió no recibir la doble antiagregación, o que al final de los 12 meses ya había suspendido el medicamento. El caso contrario fue quien mantuvo la DTA durante los 12 meses de seguimiento. La proporción de pacientes se determinó por el número absoluto de participantes que no recibían la DTA al mes dividido por la cantidad de pacientes que alcanzaron seguimiento al mes, a los 6 meses y 12 meses respectivamente. Se estableció la incidencia de MACE como el combinado de muerte por todas las causas (cardíaca o no cardíaca), IAMSTE o IAMNST de acuerdo con las definiciones previamente establecidas y revascularización del vaso. Esta incidencia se estratificó de acuerdo con la presencia o ausencia de la DTA al año. Se estableció el peligro relativo de presentar un MACE con base en la presencia o ausencia de DTA al año, en un modelo de riesgos proporcionales Cox, en el que se incluyó el evento como la incidencia de MACE y el tiempo en días desde el procedimiento índice hasta el año de seguimiento. La principal variable de exposición fue la suspensión de la doble terapia antiagregante, y se ingresaron en el modelo cada una de las variables como sexo, edad, antecedentes médicos, hallazgos angiográficos, indicación del procedimiento, una a una y posteriormente se realizó una razón de verosimilitud postestimación para establecer el aporte de cada variable al modelo. Se hicieron tablas de los modelos de regresión no ajustadas y ajustadas.
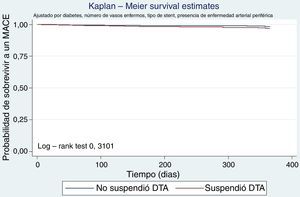
Por último, se diseñó un modelo con todas las variables estadísticamente significativas en el análisis exploratorio y se estableció una probabilidad de retiro del modelo de regresión de 0,20 con el fin de construir un modelo final. Se hicieron pruebas de validez del modelo. Se graficó una curva de Kaplan-Meier de acuerdo con la presencia o ausencia de doble terapia antiagregante al año de seguimiento y se aplicó la prueba estadística Log Rank. Se utilizó el paquete estadístico Stata 14® para el análisis de los datos. El estudio fue aprobado por el Comité de Ética en Investigación Biomédica de la Fundación Valle del Lili.
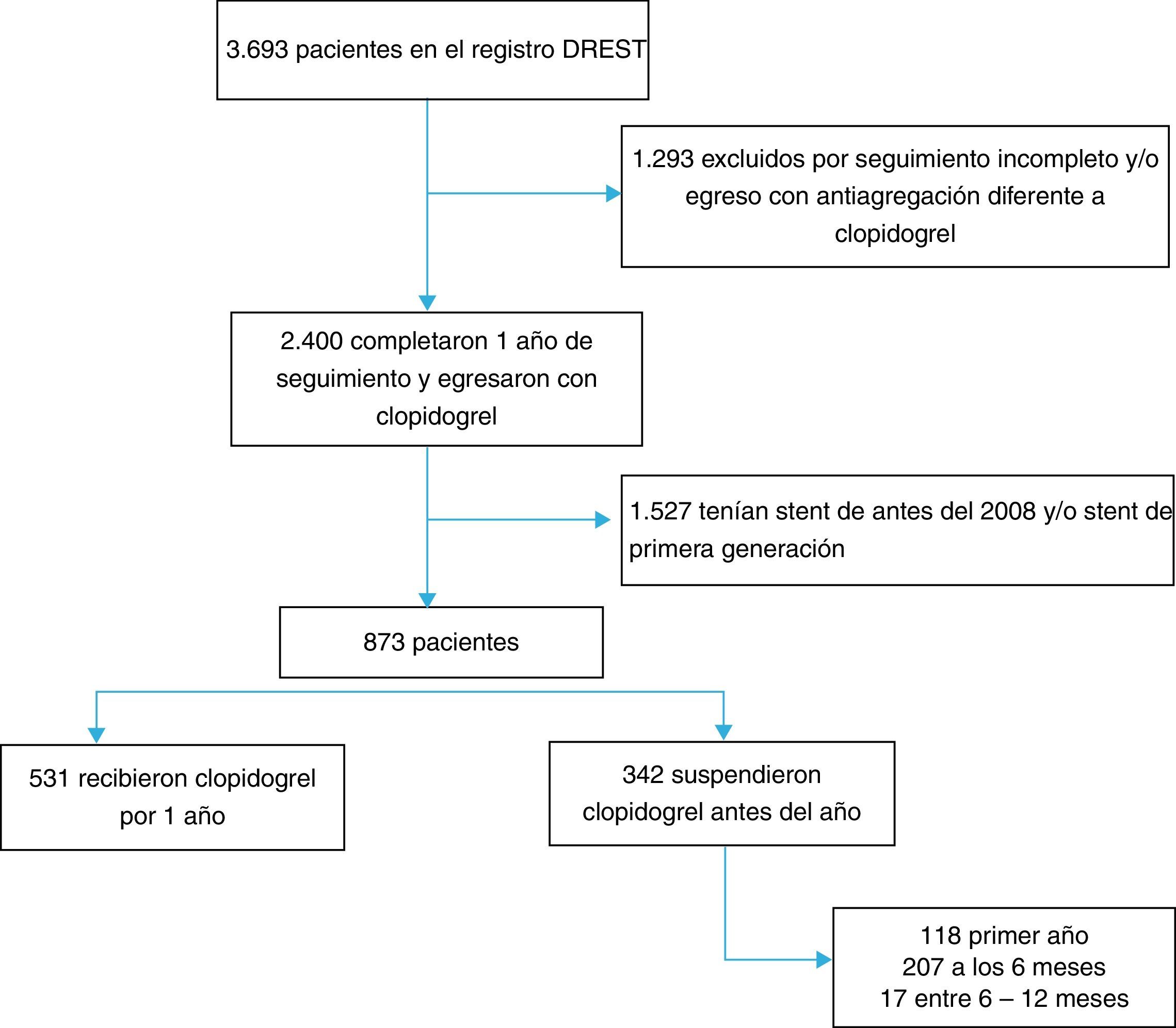
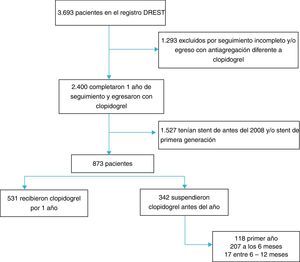
ResultadosEl registro institucional DREST tiene 3.693 pacientes incluidos a partir del año 1994, fecha en la que se hizo la primera angiografía coronaria con intervención percutánea coronaria e implante de stent convencional o medicado en la institución. Un total de 2.400 pacientes tuvieron al menos 360 días de seguimiento y recibían clopidogrel al egreso hospitalario. Se excluyeron los stents antes del 2008 y stents medicados de primera generación, para un total de 873 pacientes. De estos, 531 recibieron clopidogrel durante 12 meses (60,82%) y 342 (39,18%) suspendieron el medicamento antes del año (fig. 1). En el primer mes luego del egreso, 118 pacientes suspendieron clopidogrel (13,51%), a los 6 meses 207 pacientes habían suspendido clopidogrel y el resto (4,97%) suspendió el medicamento entre 6 meses y antes del año. La prevalencia de suspensión de la doble terapia antiagregante antes del año fue 342/873 (39,18%).
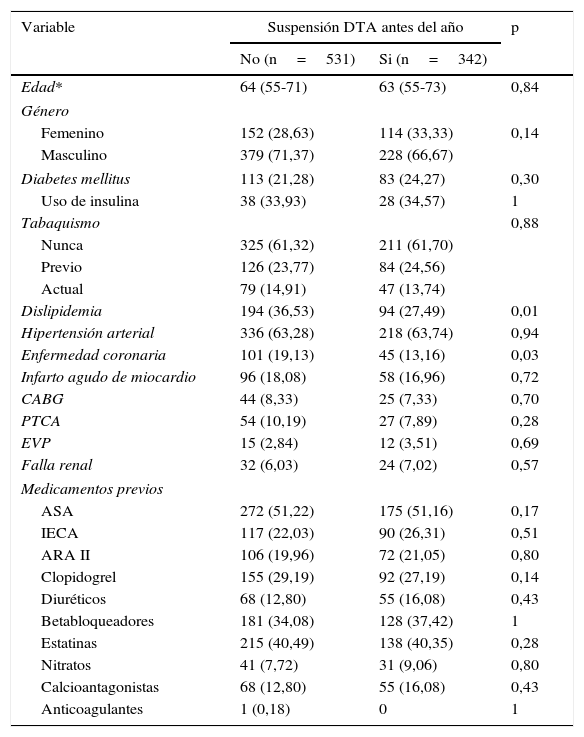
La mediana de edad fue 64 años (rango intercuartílico [RIQ] 55-72 años) sin diferencias en edad entre aquellos pacientes que suspendieron la DTA antes del año de seguimiento (p=0,84), siendo más frecuente el sexo masculino en ambos grupos (71% vs. 66% p=0,14) (tabla 1). Los antecedentes médicos más frecuentes fueron hipertensión arterial (63,28% y 63,74% respectivamente), dislipidemia (36,53% y 27,49%) y diabetes mellitus (21,28% y 24,27%) sin diferencias por uso de DTA. Hubo mayor frecuencia de enfermedad coronaria previa en quienes no suspendieron la DTA antes del año (19,13% vs. 13,16% p=0,03). Cerca de la mitad de los pacientes recibían ácido acetilsalicílico antes del evento en ambos grupos (p=0,17) y alrededor de 30% recibían clopidogrel (p=0,14). Menos de un tercio recibía inhibidores de la enzima convertidora de angiotensina (IECA) o antagonistas del receptor de angiotensina II (ARA II), y 34% vs. 37% recibían betabloqueadores (tabla 1).
Características demográficas y antecedentes médicos según la duración de la doble terapia de antiagreación
| Variable | Suspensión DTA antes del año | p | |
|---|---|---|---|
| No (n=531) | Si (n=342) | ||
| Edad* | 64 (55-71) | 63 (55-73) | 0,84 |
| Género | |||
| Femenino | 152 (28,63) | 114 (33,33) | 0,14 |
| Masculino | 379 (71,37) | 228 (66,67) | |
| Diabetes mellitus | 113 (21,28) | 83 (24,27) | 0,30 |
| Uso de insulina | 38 (33,93) | 28 (34,57) | 1 |
| Tabaquismo | 0,88 | ||
| Nunca | 325 (61,32) | 211 (61,70) | |
| Previo | 126 (23,77) | 84 (24,56) | |
| Actual | 79 (14,91) | 47 (13,74) | |
| Dislipidemia | 194 (36,53) | 94 (27,49) | 0,01 |
| Hipertensión arterial | 336 (63,28) | 218 (63,74) | 0,94 |
| Enfermedad coronaria | 101 (19,13) | 45 (13,16) | 0,03 |
| Infarto agudo de miocardio | 96 (18,08) | 58 (16,96) | 0,72 |
| CABG | 44 (8,33) | 25 (7,33) | 0,70 |
| PTCA | 54 (10,19) | 27 (7,89) | 0,28 |
| EVP | 15 (2,84) | 12 (3,51) | 0,69 |
| Falla renal | 32 (6,03) | 24 (7,02) | 0,57 |
| Medicamentos previos | |||
| ASA | 272 (51,22) | 175 (51,16) | 0,17 |
| IECA | 117 (22,03) | 90 (26,31) | 0,51 |
| ARA II | 106 (19,96) | 72 (21,05) | 0,80 |
| Clopidogrel | 155 (29,19) | 92 (27,19) | 0,14 |
| Diuréticos | 68 (12,80) | 55 (16,08) | 0,43 |
| Betabloqueadores | 181 (34,08) | 128 (37,42) | 1 |
| Estatinas | 215 (40,49) | 138 (40,35) | 0,28 |
| Nitratos | 41 (7,72) | 31 (9,06) | 0,80 |
| Calcioantagonistas | 68 (12,80) | 55 (16,08) | 0,43 |
| Anticoagulantes | 1 (0,18) | 0 | 1 |
Variables presentadas como número absoluto (porcentaje), * mediana (rango intercuartílico). CABG: cirugía de bypass coronario, PTCA: angioplastia coronaria transluminal percutánea, EVP: enfermedad vascular periférica. ASA: ácido acetil salicílico, IECA: inhibidor de la enzima convertidora de angiotensina, ARA II: antagonista de receptor de angiotensina II.
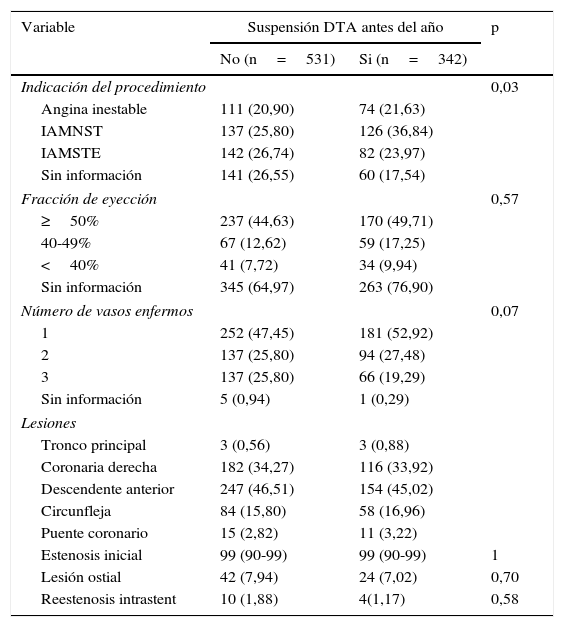
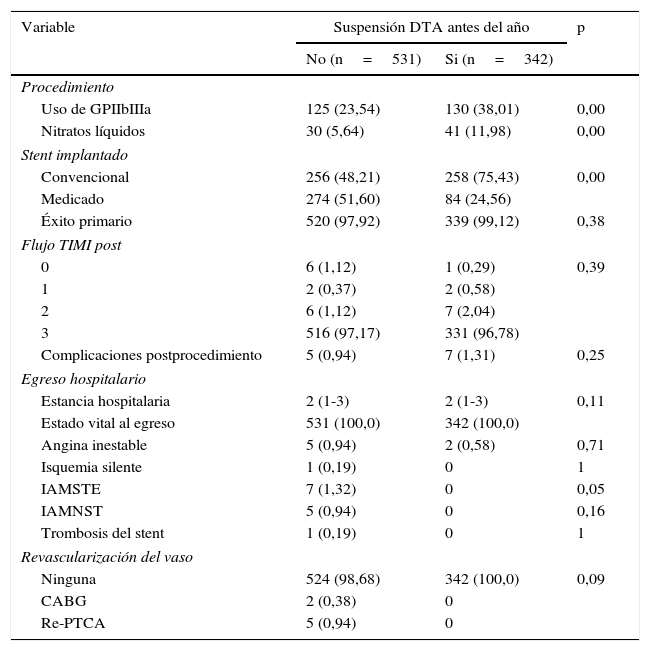
La indicación del procedimiento en los pacientes que suspendieron la DTA fue IAMNST (36,8%) seguido por IAMSTE (23,9%), mientras que para el otro grupo la principal indicación fue el IAMSTE (26,7%) (p=0,03). En la angiografía de ambos grupos se encontró que la mitad de los pacientes solo tenían un vaso enfermo, las lesiones tratadas se localizaban principalmente en la descendente anterior en su segmento proximal, en el segmento medio y en la coronaria derecha en su segmento medio. En cuanto a las características del vaso tratado se encontró que para ambos grupos la estenosis inicial fue 99% y las características relacionadas con tortuosidad y calcificación fueron similares para quienes suspendieron y aquellos que continuaron la terapia (tortuosidad severa 2,25% y 2,92%, calcificación severa 2,82% y 5,84% para los que no y si suspendieron la DTA respectivamente). En las tablas 2 y 3 se describen los hallazgos angiográficos, el tipo de stent implantado y las variables del egreso hospitalario.
Indicación de procedimiento y hallazgos angiográficos según la duración de doble terapia antiagregante
| Variable | Suspensión DTA antes del año | p | |
|---|---|---|---|
| No (n=531) | Si (n=342) | ||
| Indicación del procedimiento | 0,03 | ||
| Angina inestable | 111 (20,90) | 74 (21,63) | |
| IAMNST | 137 (25,80) | 126 (36,84) | |
| IAMSTE | 142 (26,74) | 82 (23,97) | |
| Sin información | 141 (26,55) | 60 (17,54) | |
| Fracción de eyección | 0,57 | ||
| ≥50% | 237 (44,63) | 170 (49,71) | |
| 40-49% | 67 (12,62) | 59 (17,25) | |
| <40% | 41 (7,72) | 34 (9,94) | |
| Sin información | 345 (64,97) | 263 (76,90) | |
| Número de vasos enfermos | 0,07 | ||
| 1 | 252 (47,45) | 181 (52,92) | |
| 2 | 137 (25,80) | 94 (27,48) | |
| 3 | 137 (25,80) | 66 (19,29) | |
| Sin información | 5 (0,94) | 1 (0,29) | |
| Lesiones | |||
| Tronco principal | 3 (0,56) | 3 (0,88) | |
| Coronaria derecha | 182 (34,27) | 116 (33,92) | |
| Descendente anterior | 247 (46,51) | 154 (45,02) | |
| Circunfleja | 84 (15,80) | 58 (16,96) | |
| Puente coronario | 15 (2,82) | 11 (3,22) | |
| Estenosis inicial | 99 (90-99) | 99 (90-99) | 1 |
| Lesión ostial | 42 (7,94) | 24 (7,02) | 0,70 |
| Reestenosis intrastent | 10 (1,88) | 4(1,17) | 0,58 |
DTA: doble terapia antiagregante, IAMNST: infarto agudo de miocardio sin elevación del segmento ST, IAMST: infarto agudo de miocardio con elevación del segmento ST.
Hallazgos angiográficos, complicaciones postprocedimiento e incidencia de eventos adversos según el uso de doble terapia de antiagregación
| Variable | Suspensión DTA antes del año | p | |
|---|---|---|---|
| No (n=531) | Si (n=342) | ||
| Procedimiento | |||
| Uso de GPIIbIIIa | 125 (23,54) | 130 (38,01) | 0,00 |
| Nitratos líquidos | 30 (5,64) | 41 (11,98) | 0,00 |
| Stent implantado | |||
| Convencional | 256 (48,21) | 258 (75,43) | 0,00 |
| Medicado | 274 (51,60) | 84 (24,56) | |
| Éxito primario | 520 (97,92) | 339 (99,12) | 0,38 |
| Flujo TIMI post | |||
| 0 | 6 (1,12) | 1 (0,29) | 0,39 |
| 1 | 2 (0,37) | 2 (0,58) | |
| 2 | 6 (1,12) | 7 (2,04) | |
| 3 | 516 (97,17) | 331 (96,78) | |
| Complicaciones postprocedimiento | 5 (0,94) | 7 (1,31) | 0,25 |
| Egreso hospitalario | |||
| Estancia hospitalaria | 2 (1-3) | 2 (1-3) | 0,11 |
| Estado vital al egreso | 531 (100,0) | 342 (100,0) | |
| Angina inestable | 5 (0,94) | 2 (0,58) | 0,71 |
| Isquemia silente | 1 (0,19) | 0 | 1 |
| IAMSTE | 7 (1,32) | 0 | 0,05 |
| IAMNST | 5 (0,94) | 0 | 0,16 |
| Trombosis del stent | 1 (0,19) | 0 | 1 |
| Revascularización del vaso | |||
| Ninguna | 524 (98,68) | 342 (100,0) | 0,09 |
| CABG | 2 (0,38) | 0 | |
| Re-PTCA | 5 (0,94) | 0 | |
DTA: doble terapia antiagregante, GPIIbIIIa: Glicoproteína IIb IIIa, Flujo TIMI: Thrombolysis in Miocardial Infarction en sus siglas en inglés, TIMI 0: Arteria completamente ocluida, TIMI 1: El contraste solo infiltra el trombo, no perfunde distalmente a la oclusión, TIMI 2 Arteria abierta y permeable, pero flujo retrasado en el tiempo, TIMI 3: arteria permeable con flujo normal, IAMSTE: infarto agudo de miocardio con elevación del segmento ST, IAMNST: infarto agudo de miocardio sin elevación del segmento ST, CABG: cirugía de bypass coronario, PTCA: angioplastia transluminal coronaria percutánea.
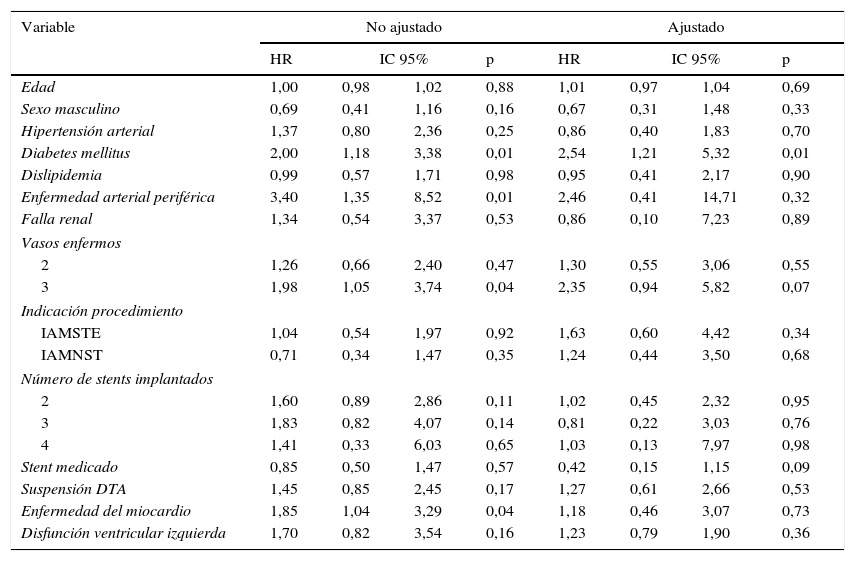
Se elaboró un modelo de riesgos proporcionales en el que se determinó el peligro relativo de presentar un evento adverso cardiovascular mayor a un año de seguimiento de acuerdo con cada uno de los factores incluidos en el análisis exploratorio. La tabla 4 corresponde al modelo univariado (no ajustado) y multivariado (ajustado). Se observó que la presencia de diabetes mellitus y enfermedad arterial periférica fueron predictores de MACE a un año en el análisis no ajustado, relación que se mantuvo en el análisis ajustado. Una vez se determinó el aporte de cada variable al modelo de regresión y ajustes por potenciales confusores, se encontró que el riesgo de presentar un MACE a un año de seguimiento fue mayor en aquellos con diabetes mellitus, enfermedad arterial periférica y más de un vaso enfermo (tabla 5). No hubo relación entre la suspensión de la doble terapia antiagregante antes del año y la incidencia de eventos cardiovasculares mayores a un año tanto para stent convencionales como medicados (HR 1,12 95% IC 0,59-2,14 p=0,73 y HR 0,93 95% IC 0,27-3,14 p=0,90 respectivamente). No hubo diferencias en las curvas de sobrevida de los pacientes que suspendieron la doble terapia antiagregante antes del año comparado con quienes la mantuvieron, luego del ajuste por variables potencialmente confusoras (fig. 2). Se presentaron 26 MACE en 337,12 personas-año de seguimiento en quienes no suspendieron la DTA (tasa de incidencia 0,07 95% IC 0,05-0,11) vs. 35 eventos en 322 personas-año en quienes suspendieron antes del año (0,10 95% IC 0,07-0,15). La presencia de stent medicado se relacionó con 63% menor probabilidad de presentar un MACE a un año de seguimiento.
Modelo de regresión de Cox para un evento cardiovascular adverso mayor a un año de seguimiento, no ajustado y ajustado
| Variable | No ajustado | Ajustado | ||||||
|---|---|---|---|---|---|---|---|---|
| HR | IC 95% | p | HR | IC 95% | p | |||
| Edad | 1,00 | 0,98 | 1,02 | 0,88 | 1,01 | 0,97 | 1,04 | 0,69 |
| Sexo masculino | 0,69 | 0,41 | 1,16 | 0,16 | 0,67 | 0,31 | 1,48 | 0,33 |
| Hipertensión arterial | 1,37 | 0,80 | 2,36 | 0,25 | 0,86 | 0,40 | 1,83 | 0,70 |
| Diabetes mellitus | 2,00 | 1,18 | 3,38 | 0,01 | 2,54 | 1,21 | 5,32 | 0,01 |
| Dislipidemia | 0,99 | 0,57 | 1,71 | 0,98 | 0,95 | 0,41 | 2,17 | 0,90 |
| Enfermedad arterial periférica | 3,40 | 1,35 | 8,52 | 0,01 | 2,46 | 0,41 | 14,71 | 0,32 |
| Falla renal | 1,34 | 0,54 | 3,37 | 0,53 | 0,86 | 0,10 | 7,23 | 0,89 |
| Vasos enfermos | ||||||||
| 2 | 1,26 | 0,66 | 2,40 | 0,47 | 1,30 | 0,55 | 3,06 | 0,55 |
| 3 | 1,98 | 1,05 | 3,74 | 0,04 | 2,35 | 0,94 | 5,82 | 0,07 |
| Indicación procedimiento | ||||||||
| IAMSTE | 1,04 | 0,54 | 1,97 | 0,92 | 1,63 | 0,60 | 4,42 | 0,34 |
| IAMNST | 0,71 | 0,34 | 1,47 | 0,35 | 1,24 | 0,44 | 3,50 | 0,68 |
| Número de stents implantados | ||||||||
| 2 | 1,60 | 0,89 | 2,86 | 0,11 | 1,02 | 0,45 | 2,32 | 0,95 |
| 3 | 1,83 | 0,82 | 4,07 | 0,14 | 0,81 | 0,22 | 3,03 | 0,76 |
| 4 | 1,41 | 0,33 | 6,03 | 0,65 | 1,03 | 0,13 | 7,97 | 0,98 |
| Stent medicado | 0,85 | 0,50 | 1,47 | 0,57 | 0,42 | 0,15 | 1,15 | 0,09 |
| Suspensión DTA | 1,45 | 0,85 | 2,45 | 0,17 | 1,27 | 0,61 | 2,66 | 0,53 |
| Enfermedad del miocardio | 1,85 | 1,04 | 3,29 | 0,04 | 1,18 | 0,46 | 3,07 | 0,73 |
| Disfunción ventricular izquierda | 1,70 | 0,82 | 3,54 | 0,16 | 1,23 | 0,79 | 1,90 | 0,36 |
Vasos enfermos: comparado con un vaso enfermo, indicación del procedimiento comparado con angina inestable. Número de stents implantados comparado con un stent. IAMSTE: infarto agudo de miocardio con elevación del segmento ST, IAMNST: infarto agudo de miocardio sin elevación del segmento ST. DTA: doble terapia antiagregante. Disfunción ventricular izquierda: fracción de eyección menor a 40%.
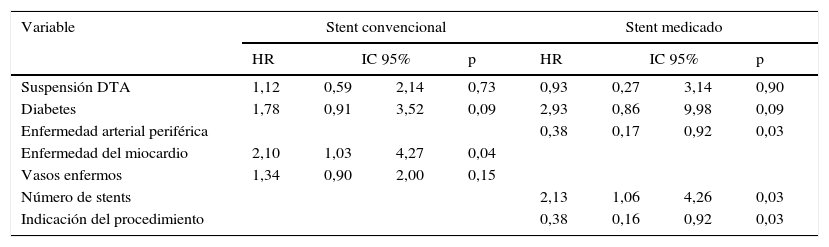
Modelo de riesgos proporcionales Cox ajustado según el tipo de stent implantado
| Variable | Stent convencional | Stent medicado | ||||||
|---|---|---|---|---|---|---|---|---|
| HR | IC 95% | p | HR | IC 95% | p | |||
| Suspensión DTA | 1,12 | 0,59 | 2,14 | 0,73 | 0,93 | 0,27 | 3,14 | 0,90 |
| Diabetes | 1,78 | 0,91 | 3,52 | 0,09 | 2,93 | 0,86 | 9,98 | 0,09 |
| Enfermedad arterial periférica | 0,38 | 0,17 | 0,92 | 0,03 | ||||
| Enfermedad del miocardio | 2,10 | 1,03 | 4,27 | 0,04 | ||||
| Vasos enfermos | 1,34 | 0,90 | 2,00 | 0,15 | ||||
| Número de stents | 2,13 | 1,06 | 4,26 | 0,03 | ||||
| Indicación del procedimiento | 0,38 | 0,16 | 0,92 | 0,03 | ||||
DTA: doble terapia antiagregante. Enfermedad del miocardio: infarto agudo de miocardio previo, más de un vaso enfermo comparado con un vaso enfermo, más de un stent comparado con un stent, indicación del cateterismo por infarto agudo del miocardio con ST elevado o sin ST elevado comparado con angina inestable.
La prevalencia de suspensión de la DTA en este estudio fue 39,18% mayor a la reportada en la literatura. Ferreira et al. describieron una prevalencia de suspensión del 14,4% y el registro PARIS una del 23,3% siendo la mayoría temporal12,13; mientras tanto Rossini et al. encontraron una tasa de 8,8% en su mayoría atribuida a sangrado, necesidad de ser llevado a cirugía o por decisión médica4.
Dentro del grupo que no suspendió la terapia antes del año fue más frecuente que los pacientes tuvieran enfermedad coronaria previa, dislipidemia, recibieran stent medicado durante el procedimiento, y presentaran antes del egreso más eventos cardiovasculares comparados con los pacientes que suspendieron la DTA. Se evidencia entonces que este grupo tenía mayor riesgo isquémico, lo cual podría asociarse a controles médicos más estrictos, con recomendación de usar la doble terapia por un periodo más largo, dado que esta disminuye el riesgo de eventos isquémicos mediante la prevención de la trombosis del stent y de eventos adversos relacionados con la ruptura de la placa ateromatosa. Esto pudo influir en la ausencia de menores eventos adversos en quienes mantuvieron la DTA comparado con quienes suspendieron antes del año.
No se observó una relación entre la incidencia de MACE y la suspensión de la doble terapia antiagregante antes del año (HR 1,31 95% IC 0,65-2,62 p=0,45). Nuestros resultados son similares a los presentados en varios estudios observacionales, en los que la interrupción temprana no se asoció con mayor incidencia de eventos cardíacos adversos, trombosis del stent y mortalidad por todas las causas12,14,15. Los resultados de los estudios observacionales llevaron a plantear la duración óptima de la doble terapia antiagregante tanto para stent convencional como para stent liberador de fármacos en varios ensayos clínicos controlados. El ensayo CREDO y el PCI-CURE demostraron que continuar el clopidogrel a largo plazo (12 meses) en pacientes con stent convencional, redujo significativamente el riesgo de presentar eventos isquémicos adversos1,2.
Sin embargo, para los stent liberadores de fármacos surge la incertidumbre respecto al riesgo de trombosis tardía del stent, el cual está asociado principalmente a los stents de primera generación (paclitaxel y sirolimus). Los stent liberadores de zotarolimus y everolimus, conocidos como de segunda generación, han demostrado mayor seguridad en comparación con los de primera generación. Por ello, el Colegio Americano de Cardiología y la Asociación Americana de Corazón (ACC/AHA, sus siglas en inglés) publicaron en su más reciente actualización la recomendación de continuar la DTA durante 12 meses en pacientes con síndrome coronario agudo independiente del tipo de stent implantado, y solo en aquellos que tienen alto riesgo de sangrado o que han presentado sangrado, considerar la suspensión de la doble terapia antiagregante antes del año16,17. Pese a ello, nuestros resultados no documentaron riesgo diferencial entre aquellos con stent convencional o stent medicado que suspendieron la DTA antes del año.
Por otra parte, se encontró que los pacientes con implante de stent medicados presentaron menor incidencia de MACE a un año independiente de la suspensión de la DTA antes del año (HR 0,37 95% IC 0,14-0,98 p=0,05), hecho que coincide con recientes estudios que intentaron establecer los predictores de MACE en diferentes tiempos después del manejo con stents liberadores de fármaco de segunda generación, y encontraron que el uso de estos fue un factor protector18. No obstante, también se observó mayor riesgo de eventos adversos a un año entre aquellos diabéticos, con más de un vaso enfermo y con infarto agudo de miocardio previo. En la evidencia se ha descrito la asociación entre diabetes y mayor riesgo de trombosis del stent, atribuida a que estos pacientes generalmente son resistentes a la aspirina y además tienen lesiones más complejas que requieren stents más largos, factor relacionado con trombosis del stent19,20.
Dentro de las limitaciones del estudio se incluyen la no caracterización del motivo por el cual se interrumpió el tratamiento, así como tampoco si este fue temporal o permanente. Se ha demostrado que el riesgo después de suspender el tratamiento antiplaquetario depende tanto del intervalo de tiempo como del contexto en el que este se interrumpe, pues las interrupciones debidas a hemorragia o incumplimiento se relacionan con un riesgo de MACE significativamente mayor13. Además, no se incluyó el contexto económico, acceso a servicios de salud, ocupación, apoyo social y trastornos de la salud mental de cada individuo, aspectos que pudieron influir en la continuidad del tratamiento farmacológico. Se desconoce también el efecto que pudiese tener la administración de clopidogrel en su denominación genérica comparado con el compuesto comercial, pues los estudios publicados en DTA se han hecho con medicamentos suministrados por laboratorios, y en nuestro medio, el medicamento en su presentación genérica es el más usado.
Dentro de las limitaciones también se encontró que nuestra población tuvo una alta tasa de consumo de aspirina y clopidogrel antes del procedimiento para ambos grupos, atribuido a un registro inadecuado de la información en la base de datos, por falta de homogenización para comprender los datos aportados por las historias clínicas, lo que llevó a fallas en la disposición de los datos, principalmente en aquellos medicamentos que el paciente estaba tomando de forma ambulatoria respecto a los que se les suministraron en el servicio de urgencias.
A pesar de que el tipo de estudio usado para este trabajo, podría tener variables no medidas en cada grupo que pudieran influir a favor o en contra de los resultados, se incluyeron pacientes con diferentes condiciones clínicas y tipos de stent, que son un reflejo de la práctica habitual en el mundo real.
ConclusionesLa suspensión de la doble terapia antiagregante en pacientes con implante de stent posterior a un síndrome coronario agudo antes de los doce meses, es frecuente y nuestros resultados sugieren que no parece estar asociada con mayor incidencia de desenlaces cardiovasculares mayores. Aquellos con stent medicado tienen menor incidencia de MACE a un año independientemente de la suspensión. Sin embargo, no se pudo determinar la causa de la suspensión de la DTA; esta en muchos casos puede influir en el desenlace de los pacientes, y es por eso que, a pesar de no ser medida en este estudio, debería tenerse en cuenta en la práctica clínica.
Se requieren estudios adicionales que evalúen la duración óptima de la doble terapia antiagregante en stents de última generación.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónFundación Valle del Lili.
Conflictos de interésLos autores declaran no tener conflictos de interés.