EL SR. R, DE 74 AÑOS, INGRESÓ en Urgencias después de sufrir una caída en casa. Un miembro de la familia lo encontró tendido en el suelo del garaje, donde permanecía desde hacía unas 8 horas. La radiografía reveló una fractura de la cadera derecha. Los resultados de las pruebas analíticasestaban, en gran parte, dentro de los límites de la normalidad, salvo la concentración de nitrógeno ureico sanguíneo (NUS), que estaba elevada (31mg/dl; valores normalesen un adulto sano mayor de 60 años: 8-23 mg/dl), así como la de la creatinina (1,1mg/dl; valores normales en un adulto sano: 0,9-1,3 mg/dl),con unaproporción entre NUS y creatinina de 28 (valores normales: de 6 a 22)1.
En Urgencias, entrelos antecedentes clínicos del Sr. R se encontraron hipertensión sistémica y artrosis de las dos rodillas. No presentaba ninguna enfermedad cardíaca o renal conocida, y nunca se le había realizado ningún procedimiento quirúrgico. Solo se le había recetado lisinopril, un inhibidor de la enzima convertidora de la angiotensina (ACE), para tratar la hipertensión. Comentó que también habíaestado tomando ibuprofeno dos o tres veces al día para el dolor que le causaba la rodilla.
La anamnesis del Sr. R y los valores iniciales de las pruebas analíticas sugerían que corría el riesgo de lesión renal aguda (LRA). Puesto que la función renal generalmente regresa a los valores iniciales si la LRA se identifica de forma temprana y se trata apropiadamente, todas las enfermeras deben permanecer alerta ante los factores de riesgo de la LRA, ser capaces de reconocer los primeros síntomas y signos, y estar preparadas para implementar intervenciones de enfermería apropiadas y administrar el tratamiento prescrito por el médico. Este artículo aborda el rol de la enfermera en la evaluación y tratamiento de este trastorno en adultos mayores.
Levantar sospechasEl Sr. R ingresa en la unidad médico-quirúrgica tras habérsele realizado una artroplastia total de cadera derecha con anestesia local. En la evaluación inicial, la enfermera observa que está consciente y orientado, y sus signos vitales permanecen estables. El nivel de dolor descrito corresponde a 1 en una escala de dolor numérica de 1 a 10. El resto de la evaluación física está dentro de los límites de la normalidad a excepción de un 3T, crepitantespulmonares bibasales y equimosis que afecta al lado derecho del cuerpo. Recibe una perfusión con una solución de cloruro de sodio al 0,9% (100 ml/h). La diuresis ha sido aproximadamente igual a la ingesta de las últimas 8 horas según el informe del turno anterior.
Al examinar atentamente el informe de la ingesta y la diuresis de las últimas 24 horas, la enfermera observa que, aunque el total de la diuresisse ha anotado correctamente, las auxiliares de enfermería han dejado constancia de que la diuresis por hora ha ido disminuyendo durante las últimas 4 horas. La enfermera observa que las pruebas analíticas se han ordenado desde el segundo día del postoperatorio.
Preocupada por estos hallazgos, la enfermera se pone en contacto inmediatamente con el cirujano, quien solicita estudios de diagnóstico adicionales. Los resultados revelan que el Sr. R tiene LRA.
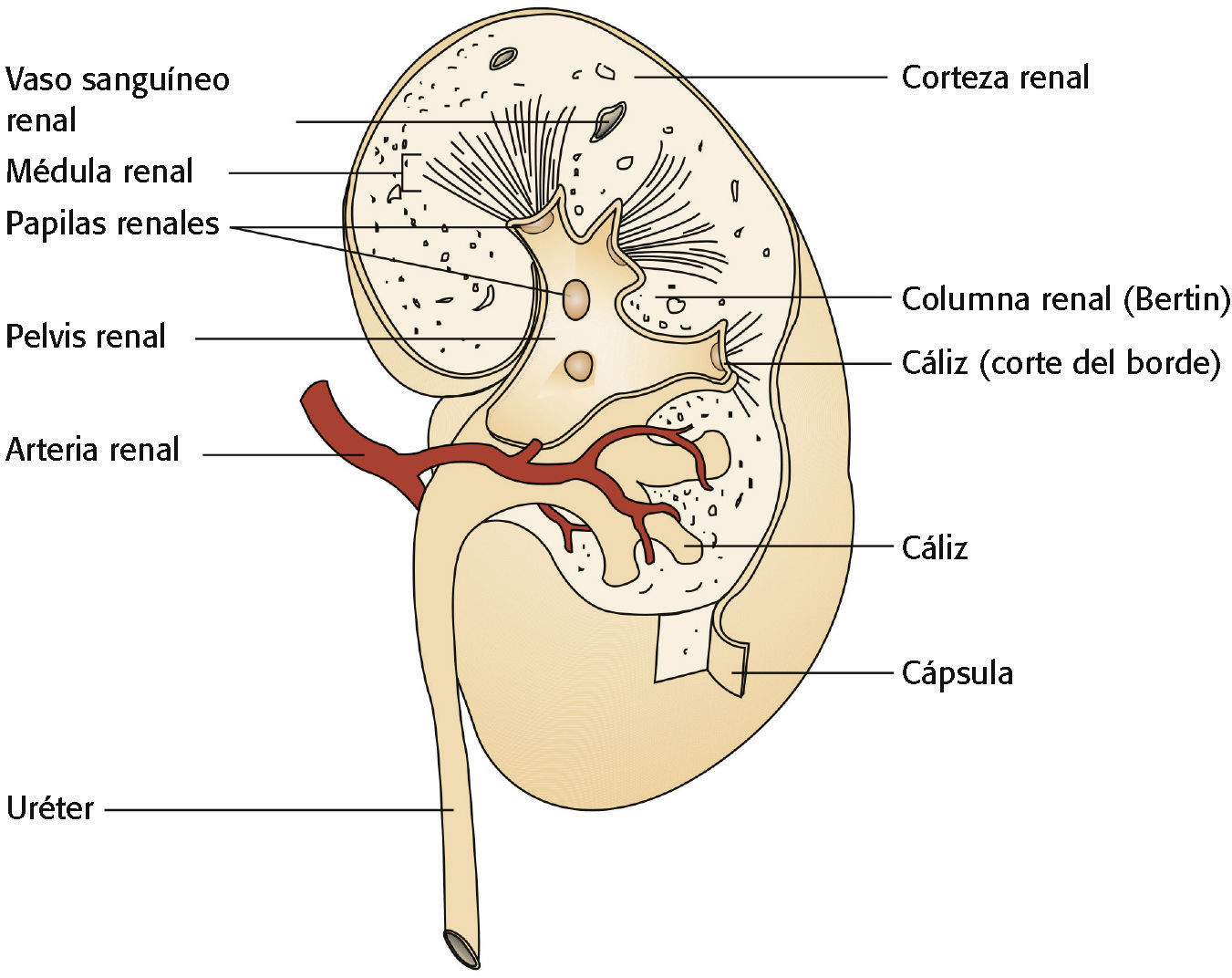
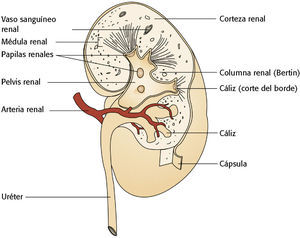
¿Qué es la LRA?Los riñones son órganos muy complejos y tienenmuchas funciones y procesos reguladores (v. Una mirada al interior del riñón y Cómo funcionan los riñones). Por definición, la LRA es una disminución repentina de la función renal que cumple cualquiera de los siguientes criterios2,3:
- •
Un aumento de 0,3mg/dlo más de la creatinina sérica (CrS) en 48 horas.
- •
Un aumento de 1,5 veces o más del valor inicialde la CrS en los últimos 7 días.
- •
Una disminución de la diuresis por debajo de 0,5 ml/kg/hora durante 6 horas.
El término LRA sustituye el término insuficiencia renal aguda (IRA), empleado anteriormente, para reflejar mejor el espectro de lesiones que van desde pequeños cambios en los marcadores de la función renal hasta la necesidad de tratamiento de reemplazo renal (TRR) que puede surgir de múltiples factores4,5. El término IRA todavía se utiliza cuando la lesión renal genera la necesidad de TRR, incluyendo hemodiálisis intermitente tradicional y tratamientos de reemplazo renal continuo (TRRC) más nuevos, como ultrafiltración continua lenta, hemofiltración venovenosa continua, hemodiálisis venovenosa continua, hemodiafiltración venovenosa continua y hemofiltración arteriovenosa continua6.
Factores de riesgoLa LRA se observa en el 15% de todos los pacientes hospitalizados y hasta en el 66% de los pacientes de la UCI7–11. Durante la última década, la incidencia de LRA ha aumentado debido a la mayor gravedad que presentan los pacientes, una población de adultos mayores en aumento y la detección de la LRA con mayor facilidad12. Entre los factores de riesgo más importantes de la LRA se pueden citar10,12–14:
- •
Tener 75 años o más.
- •
Diabetes.
- •
Hipertensión.
- •
Insuficiencia renal crónica (IRC).
- •
Insuficiencia cardíaca o hepática.
- •
Sepsis.
- •
Uso de medios de contraste radiológico intravasculares.
- •
Cirugía cardíaca después del uso de un medio de contraste radiológico.
- •
Polimedicación.
La edad avanzada es un factor importante que predispone al paciente a la LRA. A medida que una persona envejece, el riñón experimenta cambios estructurales y funcionales; por ejemplo, se reduce la masa cortical total12. Además, el flujo sanguíneo renal disminuye el 1% cada año después de los 30 años15. Por estas y otras razones, la función renal puede disminuir al 50% o más en el momento en que un paciente llega a los 70 años16.
Entre los cambios funcionales en el sistema renal se pueden citar: disminución de la capacidad de excretar una carga de sodio, disminución de la capacidad de conservar el agua cuando el paciente está deshidratado y disminución de la tasa de filtración glomerular (TFG)16,17. LaTFG disminuye un 10% cada década después de los 30 años12,18. Estos cambios renales asociados con el envejecimiento, en combinación con otros problemas fisiopatológicos, muy probablemente pueden provocar que se desarrolle una LRA15.
En muchos casos, la LRA está relacionada con trastornos médicos subyacentes. Los adultos mayores son más propensos a padecer una enfermedad crónica o más que aumentan el riesgo de LRA, como arteriopatía coronaria, insuficiencia cardíaca o diabetes mellitus. Una infección, como la sepsis, también aumenta el riesgo de LRA en adultos mayores vulnerables19–21. Otras causas son yatrogénicas, es decir, propias del tratamiento médico o quirúrgico del paciente. En pacientes de edad avanzada, la LRA por lo general tiene varias causas y puede desarrollarse incluso a partir de lesiones leves del riñón15.
Muchos medicamentos están asociados con la LRA. Algunas de los responsables más frecuentes son los fármacos antiinflamatorios no esteroideos (AINE), como el ibuprofeno; antimicrobianos, como aminoglucósidos, anfotericina B, vancomicinay aciclovir; fármacos cardiovasculares, como inhibidores de la ECA y bloqueantes de los receptores de la angiotensina (BRA); diuréticos; antidepresivos; fármacos quimioterápicos, como cisplatino y metotrexato, y medios de contraste intravascular10–12,22.
Muchos otros lesionan los riñones directamente7,10,22. El riesgo de nefrotoxicidad aumenta cuando estos medicamentos se administran durante un largo período o a dosis altas, y cuando se administra más de un medicamento nefrotóxico22. Debido a loscambios relacionados con la edad en la farmacocinética y la farmacodinámica, junto con la polimedicación (tomar más de cinco medicamentos), los pacientes mayores corren un elevado riesgo de reacciones adversas a los medicamentos y malos resultados14,23.
Los riñones ayudan a regular muchos procesos corporales, pero su función principal consiste en excretar los desechos metabólicos, mantener el equilibrio hidroelectrolítico y regular el equilibrio acidobásico. También tienen funciones endocrinas, pues secretan las hormonas renina y eritropoyetina y 25-hidroxivitamina D3-1-hidroxilasa, la enzima que convierte la vitamina D en la forma activa.
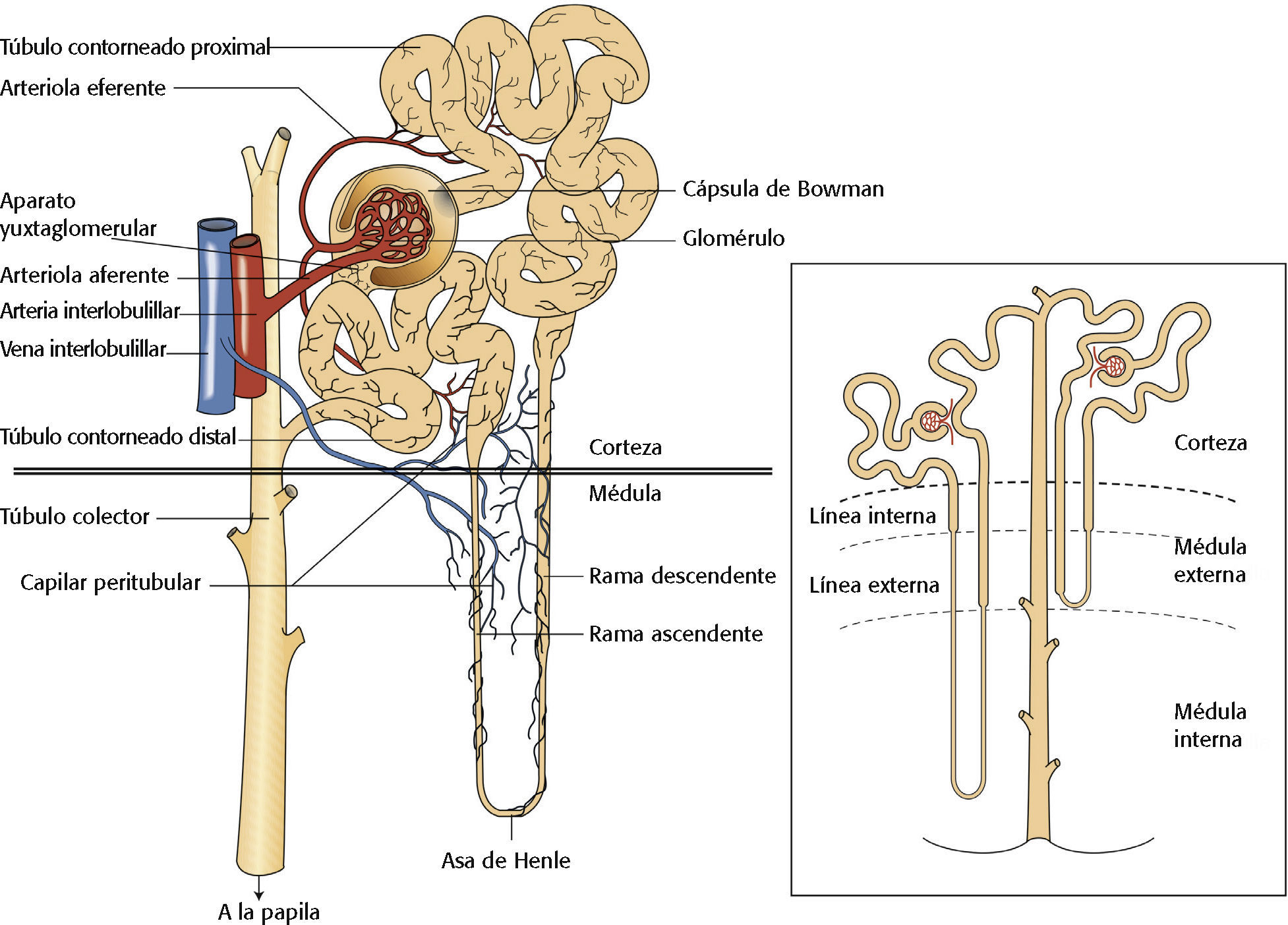
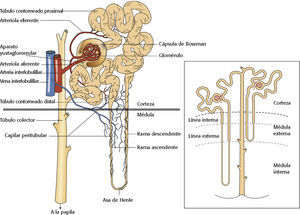
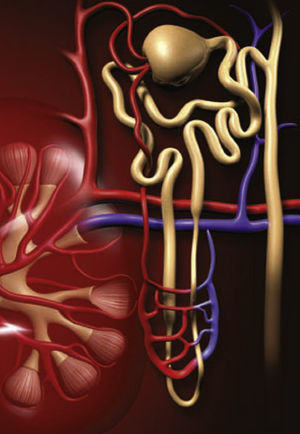
Las unidades funcionales de los riñones son las nefronas (v. la ilustración más abajo). Cada riñón contiene aproximadamente 1,2 millones de nefronas y se abastece por una arteria renal, que se divide en vasos más pequeños a la altura de la nefrona, donde una arteriola aferente suministra sangre al glomérulo. Más allá del glomérulo, los capilares se combinan para convertirse en una arteriola eferente, que luego se divide de nuevo para formar otra red capilar que rodea el sistema tubular. Finalmente, la sangre vuelve a la circulación venosa.
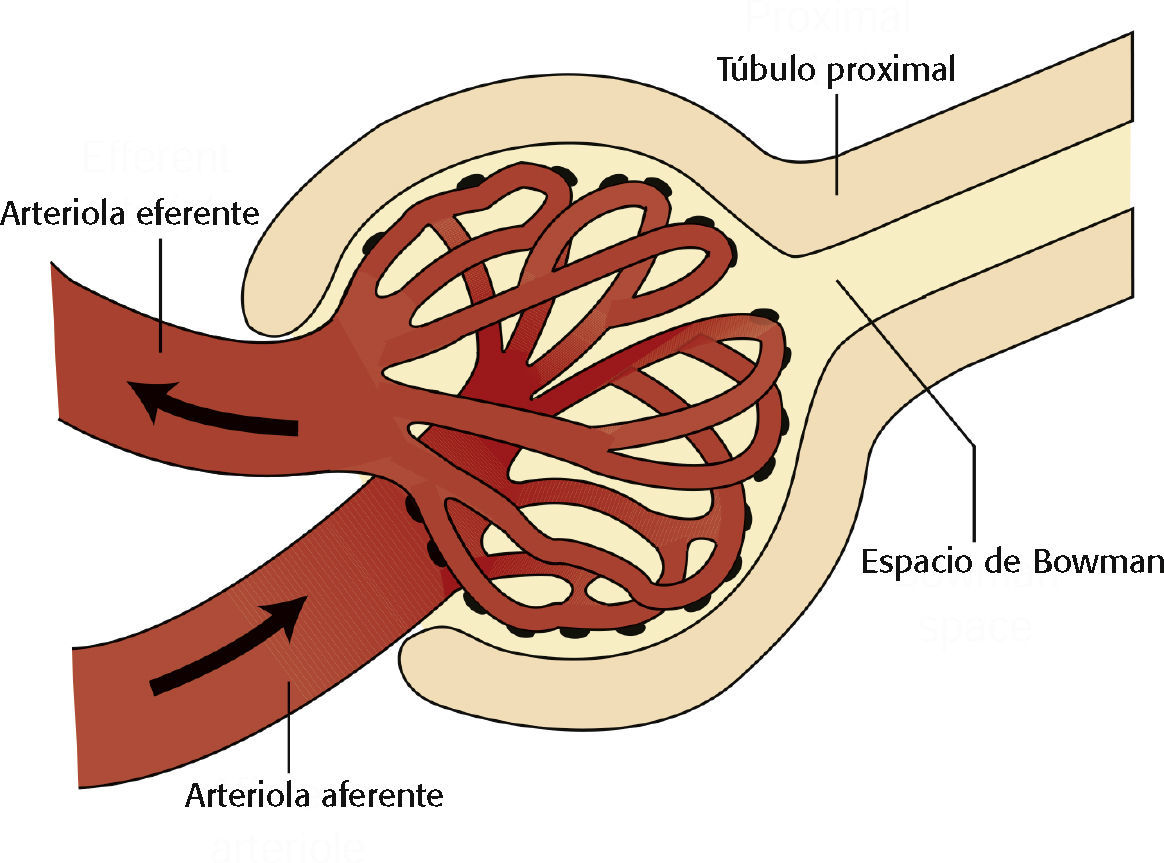
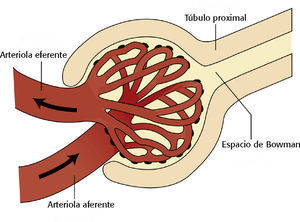
Del 20% al 25% de todo el gasto cardíaco (1.200 ml/min) llega a los riñones cada minuto. El glomérulo tiene una membrana porosa que permite que aproximadamente 125 ml/min del filtrado pasen a través de la cápsula de Bowman. La tasa de filtración glomerular (TFG) es el volumen de plasma filtrado en el glomérulo por unidad de tiempo. La TFG normal es de 90 a 120 ml/min/1,73 m2. En el sistema tubular se absorbe todo menos aproximadamente 1 ml/min, que se reabsorbe a través de la red capilar peritubular y se convierte en orina.
Aunque el glomérulo permite que se filtre todo este líquido, no permite que en condiciones normales se filtren las proteínas más grandes, como los glóbulos rojos y las plaquetas. Sin embargo, los trastornos renales pueden interrumpir este proceso, lo que permite que proteínas o células sanguíneas pasen a la orina.
El sistema tubular reabsorbe toda la glucosa, la mayoría de los aminoácidos y las proteínas pequeñas, muchos electrólitos, bicarbonato y la mayor parte de los líquidos. Esto se logra tanto por el transporte activo como por el pasivo y está regulado por la hormona paratiroidea, la aldosterona y la hormona antidiurética, así como otras hormonas. Los túbulos también secretan iones hidrógeno, iones potasio, creatinina y amoníaco.
Las recomendaciones para la estadificación de la LRA según la gravedad aparecen en la guía de práctica clínica en casos de LRA, Enfermedad renal: cómo mejorar los resultados globales (KDIGO, Kidney Disease: Improving Global Outcomes; v. Recursos para enfermeras y pacientes)2,12,14.
- •
Fase 1: CrS 1,5-1,9 veces el valor inicial o un aumento superior a/igual a 0,3 mg/dl con una diuresisinferior a 0,5 ml/kg/h durante 6-12 horas.
- •
Fase 2: CrS2,0-2,9 veces el valor inicial y una diuresis inferior a 0,5 ml/kg/h durante más de/igual a 12 horas.
- •
Fase 3: CrS 3,0 veces el valor inicial o un aumento de la creatinina sérica superior a/igual a 4,0 mg/dl; o inicio de TRR; o en pacientes <18 años, disminución de la tasa de filtración glomerular estimada (TFGe) a <35 ml/min por 1,73 m2y una diuresis inferior a 0,3 ml/kg/h durante 24 horas o más, o anuria durante 12 horas o más2,12.
Las causas de la LRA se clasifican tradicionalmente en función de la parte de la anatomía renal más afectada11,13,19:
- •
LRA prerrenal remite a los cuadros clínicos que disminuyen la perfusión renal, como hipovolemia, disminución del gasto cardíaco y hemorragia aguda11,13,24,25. Los AINE pueden causar vasoconstricción de la arteriola aferente, lo que provoca LRA aguda prerrenal (v. Arteriolas aferentes y eferentes).
- •
LRA intrarrenal (intrínseca), como resultado de una lesión directa a los riñones (vasos sanguíneos, glomérulos o túbulos intersticiales). Entre las posibles causas puede citarse la isquemia que provoca disminución prolongada de la perfusión renal, nefrotoxinas14, infecciones, enfermedad renal ateroembólica y enfermedad renal primaria.
- •
LRA posrenal (obstructiva), generadapor la obstrucción del flujo de orina por tumores, cálculos, vejiga neurógena o hiperplasia prostática10,11,13,25. Debido a la obstrucción, la orina retrocede a las estructuras del riñón y causa un aumento de la presión, una disminución de la TFG y lesión renal. Aunque la LRA posrenal es menos frecuente en la población general, el envejecimiento aumenta el riesgo.
Cuando la función renal disminuye súbitamente en la LRA, la CrS y el NUS aumentan9. Por lo general se produce oliguria (diuresis inferior a 0,5 ml/kg/h) aunque en algunos casos la diuresis es inicialmente normal o incluso está aumentada19. Además, los líquidos, los electrólitos y el equilibrio acidobásico pueden aparecer alterados9,24.
Los pacientes con LRA de leve a moderada puedenpermanecer asintomáticos a pesar de valores anómalos en las pruebas analíticas. A medida que la lesión renal progresa, aparecensíntomas y signoscomo apatía, confusión, cansancio, anorexia, náuseas, vómitos, edema periférico y aumento de peso10,13.
La LRA generalmente sigue un curso clínico previsible, aunque la gravedad de la lesión, la complejidad de la disfunción renal, el desarrollo de complicaciones y el período de tiempo de recuperación pueden variar considerablemente. El curso clínico por lo general sigue estas cuatro fases13,25:
- •
Fase inicial (inicio). Es el tiempo entre la lesión renal y la reducción de la función renal. Las enfermeras pueden ayudar a prevenir o minimizar la lesión ulterior mediante la identificación de episodios de hipotensión, sustancias nefrotóxicos y otros riesgos, y la intervención adecuada posterior.
- •
Fase oligúrica. Durante esta fase, la producción de orina disminuye por debajo de 400 ml/día13. En la LRA, esta fase se produce por lo general de 1 a 7 días después de la lesión renal y tiene una duración de 10 a 14 días. Sin embargo, en algunos casos la fase oligúrica dura semanas o meses25.
En algunos pacientes con LRA no se desarrollan oliguria (LRA no oligúrica) y mantienen la diuresis adecuada. No existe consenso en cuanto a si los pacientes con LRA no oligúrica tienen peor pronóstico que aquellos con LRA oligúrica. Aunque algunas fuentes indican que los pacientes con LRA no oligúrica presentan mejores resultados, otras lo discuten porque, en algunos casos, puede ocasionar el retraso de un tratamiento agresivo, con lo que aumenta la mortalidad7,25.
Si un paciente desarrolla oliguria, es probable que se encuentresobrecarga de volumen de líquidos, hiponatremia (alteraciones de la reabsorción renal de sodio e hiponatremia por dilución), hiperpotasemia, acidosis metabólica y elevaciones de NUS y CrS, lo que refleja la acumulación de desechos nitrogenados13,25. Si esta fase se prolonga durante un tiempo considerable, el paciente también puede desarrollar hipocalcemia, hiperfosfatemia, anemia, alteraciones de plaquetas y sangrado, disfunción del sistema inmunológico y diversos cambios neurológicos que van desde el cansancio hasta convulsiones y coma9,13,25.
La oliguria también puede estar causada por hipovolemia, que debe reconocerse y corregirse para evitar la LRA. Para determinar si la oliguria se debe a hipovolemia o a LRA, debe evaluarse la densidad de la orina y los niveles de sodio en orina. La densidad de la orina refleja la capacidad de los riñones de concentrar o diluir la orina, y normalmente está entre 1.010 y 1.025 en adultos1 (los valores de referencia pueden diferir ligeramente de un laboratorio a otro). La orina de un paciente con oliguria relacionada con hipovolemia tendrá una densidadelevada y un nivel de sodio en orina bajo (lo normal es de 40 a 220 mEq/24 h en adultos). En un paciente con oliguria a partir de una LRA, la densidad de la orinaestá fijada en 1,010 y el nivel de sodio en orina es alto1,25.
- •
Fase diurética. En esta fase, la producción de orina aumenta ya que las nefronas han recuperado la capacidad de excretar urea, que extrae el fluido a través de la membrana glomerular (diuresis osmótica). Sin embargo, los riñones no pueden concentrar ese filtrado. La diuresis durante esta fase normalmente es de 1 a 3 l/día, pero puede ser tan alta como 5 l/día25. Debido a la pérdida de líquidos, el paciente sufre hipovolemia, hipotensión, hiponatremia continua (debido a la pérdida de sodio en el filtrado) e hipopotasemia.
Si esta fase continúa, el desequilibrio acidobásico y el desequilibrio electrolítico comienzan a normalizarse y los valores de NUS y CrS mejoran. Esta fase puede durar de 1 a 2 semanas13,25.
- •
Fase de recuperación. Los riñones recuperan la capacidad de manejar los desechos metabólicos, y el NUS y la CrS vuelven a sus valores iniciales. Este proceso suele tardar varias semanas, pero en algunos casos continúa durante un máximo de 1 año13,25. Los riñones de algunos pacientesno se recuperan completamente y puede haber elevaciones leves de NUS y CrS. Otros pacientes evolucionarán a ERC y necesitarán tratamiento de por vida.
La enfermera debe obtener los antecedentes médicos detalladosde cualquier paciente que corra el riesgo de LRA para investigar si el paciente podría padecer ERC en lugar de LRA. Es más probable que un paciente con ERCpresente anemia normocítica crónica, hipocalcemia, hiperfosfatemia y un color de la piel con tono grisáceo, además de NUS y CrS elevados9.
Cada riñón contiene aproximadamente 1,2 millones de nefronas y se abastece por una arteria renal.Recomendaciones para la evaluaciónAl evaluar a un paciente que corre el riesgo de LRA, siga estas directrices:
- •
Pregúntele si ha padecido una infección últimamente ya que algunas lesiones renales se asocian con infecciones. La glomerulonefritis aguda postestreptocócica y la infección gastrointestinal por Escherichia coli son algunos ejemplos9,20,21.
- •
Valore la posibilidad de rabdomiólisis, provocada por grandes cantidades de mioglobina, que es nefrotóxica yes liberada por elmúsculo esquelético lesionado. Entre las posibles causas pueden citarse traumatismos, sobreesfuerzo muscular, sobredosis de drogas u otros tipos de lesión del músculo esquelético9. La compresión muscular, las lesiones por aplastamiento y la inmovilidad prolongada también pueden provocar la liberación de mioglobina. Por ejemplo, el Sr. R corre el riesgo de sufrir rabdomiólisis porque se ha visto obligado a permanecer en la misma posición durante horas después de caerse y fracturarse la cadera.
- •
Averigüe si el paciente tiene antecedentes de enfermedad cardiovascular, que puede aumentar la probabilidad de una alteración de la perfusión renal. Cualquier caída del gasto cardíaco afecta negativamente a la perfusión renal, por lo que es importante valorar cualquier arritmia o signos de insuficiencia cardíaca o inestabilidad hemodinámica.
- •
Evalúe también los efectos adversos durante el tiempo en que el paciente permanezca hospitalizado ya que podrían afectar a su función renal. Por ejemplo, averigüe si el paciente sufrió algún episodio de hipotensión que podría haber lesionado los riñones. Investiguecualquier posibilidad de sepsis ya que esta puede causar hipotensión profunda.
- •
Averigüe si el paciente recibió respiraciónasistida. Algunos estudios sugieren que la respiraciónasistida, incluyendo el uso de presión telespiratoria positiva, puede alterar el gasto cardíaco y contribuir al desarrollo de la LRA24.
- •
Lleve a cabo la conciliación de medicamentos en el momento del ingreso del paciente y tenga en cuenta los fármacos potencialmente nefrotóxicos. Además de los medicamentos de venta con receta, pregunte específicamente sobre el exceso de medicamentos de venta libre, así como el de hierbas medicinales y suplementos nutricionales.
- •
Reconsidere los medicamentos que se le han prescrito al paciente mientras permanezca hospitalizado. Incluya cualquier exposición a medios de contraste intravasculares, que podrían haber sido administradosen varios procedimientos radiológicos de diagnóstico o intervencionistas, incluyendo la tomografía computarizada (TC) y la coronariografía. También vuelva a revisar la dosificación de los medicamentos prescritos. En pacientes de alto riesgo, anticipe si deben supervisarse los niveles máximo y mínimo. También considere que las dosis de algunos medicamentos se prescriben en función del peso. Observe si la dosificación se basa en el peso corporal ideal o real. Algunos medicamentos se han vinculado con la LRA cuando la dosificación es incorrecta26.
- •
Evalúe y supervise atentamente el estado de hidratación del paciente. Comience con la identificación de los cambios recientes en el patrón de micción, lo que puede indicar hipo o hipervolemia. Muchos pacientes con hipovolemia presentan hipotensión ortostática27. Instruya a los pacientes con hipotensión ortostática para que cambienlentamente la postura y se sienten o se acuesten de inmediato si sienten mareo al ponerse de pie. Las medias de compresión también pueden ayudarles.
- •
Entre los síntomas y signos de hipervolemiapueden citarse hipertensión, ingurgitación yugular, aumento de peso brusco y edema periférico9,13. También puede auscultar un 3T. Valore la existencia de crepitantes pulmonares y controle también la disnea, la ortopnea y la disnea paroxística nocturna. Si continúa la hipervolemia, el paciente puede desarrollar ascitis y derrames pleurales y/o pericárdicos25. Prepare al paciente para un controlagresivo si está hemodinámicamente inestable7.
Si el estado de los líquidos cambia, también lo hace el equilibrio hidroelectrolítico del paciente. Controle NUS, CrS y los electrólitos séricos, especialmente sodio, potasio, magnesio, calcio y fosfato.
La masa muscular y la ingesta de proteínas de muchos adultos mayores han disminuido, lo cual afecta a la tasa de producción de creatina. Los niveles de CrS a menudo están dentro de los límites de la normalidad a pesar de una disminución significativa de la tasa de filtración glomerular, por lo que no se basan únicamente en la CrS para calcularla TFG en pacientes adultos mayores7,12,15.
Si la volemia o el gasto cardíaco es bajo, debe corregirse tan pronto como sea posible para evitar una lesión mayor en los riñones.- •
National Kidney Foundation(Fundación Nacional del Riñón). Es una organización muy importante en Estados Unidos que se dedica a la sensibilización, prevención y tratamiento de la enfermedad renal. www.kidney.org
- •
National Kidney Foundation. Kidney Disease: Improving Global Outcomes (KDIGO, en españolEnfermedad renal: cómo mejorar los resultados globales). Publicadas en marzo de 2012, estas fueron las primeras recomendaciones publicadas sobre la LRA. Tratan la definición, evaluación de riesgos, evaluación, tratamiento y prevención de la LRA. www.kdigo.org/clinical_practice_guidelines/pdf/KDIGO%20AKI%20Guideline.pdf
- •
National Institute of Diabetes and Digestive and Kidney Diseases(Instituto Nacional de Diabetes y Enfermedades Digestivas y Renales). Este Instituto Nacional lleva a cabo, apoya y coordina la investigación sobre la enfermedad renal, así como sobre la diabetes y las enfermedades del aparato digestivo. Ofrece recursos al paciente y referencias e información de los ensayos clínicos. www.niddk.nih.gov
- •
National Institute for Health and Care Excellence (NICE, en español Instituto Nacional para la Salud y la Excelencia Clínica). Acute Kidney Injury: Prevention, Detection and Management. NICE guidelines (La lesión renal aguda: prevención, detección y manejo; recomendaciones NICE [CG169]; Reino Unido) se publicó en agosto de 2013. Está diseñado para especialistas no nefrólogos para ayudarles en la identificación de pacientes con LRA. Hacen hincapié en la atención y los deseos del paciente.Estas recomendaciones hacen referencia a factores de riesgo, prevención, causas, manejo de la enfermedad y apoyo para pacientes y cuidadores. www.nice.org.uk/guidance/cg169/chapter/1-recommendations#assessing-riskof-acute-kidney-injury
Supervisar la diuresis a cada hora junto con la medición de la CrS puede ser un biomarcador sensible y temprano de una LRA13. Los niveles séricos de sodio serán bajos si los túbulos dañados impiden la reabsorción de sodio a partir del filtrado glomerular25.
La hiperpotasemia se produce porque la excreción normal de potasio se deteriora. Además, los niveles de potasio aumentarán tras el traumatismo del tejido, sangrado o transfusiones de sangre porque el potasio es liberado desde las células dañadas. Si el paciente presenta acidosis metabólica, los niveles de potasio sérico aumentarán a medida que los iones de hidrógeno entren en las células y fuercen al potasio a abandonar las células25.
La hiperpotasemia es muy preocupante porque puede causar arritmias cardíacas, por lo que los pacientes deben ser controlados mediante un monitor cardíaco para detectar anomalías comoondas T altas y puntiagudas, prolongación del intervalo PR, ensanchamiento delos complejos QRS y contracciones ventriculares prematuras9,25. La hiperpotasemia no tratada puede provocar taquicardia ventricular, fibrilación ventricular y paro cardíaco.
La acidosis metabólica es otro signo frecuente de la LRA. Se desarrolla porque la secreción de iones de hidrógeno se deteriora. La gasometría arterial muestra un pH bajo y un nivel bajo de bicarbonato. El bicarbonato es bajo porque se usa para amortiguar los iones de hidrógeno elevados25.
El paciente también puede presentar respiración de Kussmaul (respiraciones rápidas y profundas), que es un intento del cuerpo de restablecer el equilibrio acidobásico mediante la eliminación de más dióxido de carbono del sistema9,25. Otros síntomas y signos de la acidosis metabólica incluyen piel enrojecida, dolor de cabeza, taquicardia, náuseas y vómitos. A medida que la acidosis se agrava, el paciente puede desarrollar hipotensión, bradicardia y alteración del nivel de conciencia9.
Evalúe cuidadosamente el estado nutricional actual y prehospitalario del paciente. La desnutrición proteicocalórica participa en el aumento de la mortalidad de los pacientes con LRA9. Los estudios muestran que el 20% de los pacientes hospitalizados está desnutrido y los adultos mayores corren un riesgo aumentado7,28. La acumulación de productos metabólicos de desecho en la LRA está asociada con anorexia, náuseas, vómitos y cansancio, que también perjudica la ingesta dietética de su paciente. Preste mucha atención a la albúmina sérica, proteínas totales, glucemia, hemoglobina, colesterol, prealbúmina, transferrina, creatinina y los niveles de NUS. Mientras que la albúmina sérica es la mejor medida de la desnutrición a largo plazo debido a su semivida más larga, todas estas pruebas analíticas pueden proporcionar información importante sobre el estado nutricional del paciente.
Estudios de diagnósticoEstos estudios de diagnóstico pueden ayudar a determinar la causa subyacente de la LRA:
- •
Análisis de orina.Se controlará la densidad, la osmolalidad y los niveles de sodio de la orina. Las proteínas o células en la orina pueden indicar lesión intrarrenal, como glomerulonefritis, infección renal o síndrome de Goodpasture. Hematuria, piuria o cristales urinarios pueden ser causa de LRA posrenal, como hiperplasia prostática benigna, vejiga neurógena o cálculos renales25.
- •
Urocultivo y antibiograma si el médico sospecha que existe una causa infecciosa.
- •
Ecografía renal, que puede mostrar la lesión en los tejidos renales u obstrucción de las vías urinarias.
- •
Gammagrafía renal para evaluar el flujo sanguíneo renal.
- •
Tomografía computarizada o resonancia magnética para identificar masas u obstrucciones.
De vez en cuando se realiza una biopsia renal para investigar posibles trastornos intrarrenales, como glomerulonefritis y nefritis intersticial.
Enfermería y cuidados colaborativosDado que no existe un tratamiento curativo para la LRA, el objetivo de los cuidados es prevenir una lesión mayor y facilitar la recuperación12,29. Los cuidados al paciente incluyen la identificación inmediata y el tratamiento adecuado de la causa subyacente de la LRA. Otras prioridades sonla corrección de los desequilibrios hidroelectrolíticos, el mantenimiento del equilibrio acidobásico, la dispensación de una nutrición óptima y la prevención de complicaciones7,9,11. Vuelva a evaluar al paciente con frecuencia para detectar cambios sutiles que pueden indicar la progresión de la LRA, el desarrollo de complicaciones o la necesidad de TRR. Para ofrecerunos cuidados integrales, atienda también a las necesidades espirituales, emocionales y educativas del paciente y su familia.
Las recomendaciones KDIGO sugieren que no se utilicen diuréticos para prevenir o tratar la LRA, excepto en el tratamiento de la sobrecarga de volumen.El control de los desequilibrios de los líquidos del paciente es fundamental. Anote con precisión la ingesta y la diuresis, así como el peso diario. Si la volemia o el gasto cardíaco es bajo, debe corregirse tan pronto como sea posible para evitar una lesión mayor en los riñones. Si no se produce shock hemorrágico, las recomendaciones KDIGO sugieren administrar cristaloides isotónicos en lugar de coloides (albúmina o almidones) como tratamiento inicial para la expansión del volumen intravascular en pacientes con LRA o en riesgo de LRA2. La reposición de líquidos por lo general comienza con cloruro de sodio al 0,9%9. Las recomendaciones KDIGO sugieren que no se utilicen diuréticos para prevenir o tratar la LRA, excepto en el tratamiento de la sobrecarga de volumen2.
Si el gasto cardíaco continúacorriendo peligro, el paciente necesitará fármacos inotrópicos positivos. Sin embargo, ya no se recomienda la administración de dosis bajas de dopamina, una estrategia que se creía que beneficiaba a los pacientes con LRA mediante la mejora de la perfusión renal2. La investigación ha demostrado que su uso no supone ninguna diferencia en los resultados clínicos. Además, la dopamina puede originar complicaciones cardíacas e incluso disminuir la perfusión renal en pacientes mayores de 55 años. Por estas razones, los medicamentos inotrópicos solo están indicados en pacientes con gasto cardíaco insuficiente7.
Si el paciente es hipervolémico, se le debe recetar restricción de líquidos. En general, los pacientes solo deben recibir de 500 a 600 ml por encima de cualquier pérdida de líquidos durante las últimas 24 horas7,25. En otras palabras, si un paciente tuvo ayer una diuresis de 400 ml y ninguna otra pérdida de líquidos (por vómitos, diarrea, sangrado o por otras causas), la ingesta diaria total de líquidos debe estar restringida a un total de 900 a 1.000 ml.
Controle atentamente la hipervolemia del paciente para detectar síntomas y signos de agravamiento de la insuficiencia cardíaca y edema pulmonar. El deterioro respiratorio puede ocurrir rápidamente, por lo que evalúe con frecuencia el aumento del trabajo respiratorio y la disminución de la oxigenación. El paciente posiblemente necesiteoxigenoterapia o respiración asistida7.
Como se ha comentadopreviamente, los pacientes con LRA corren un riesgo elevado de desarrollar hiperpotasemia. Si el potasio sérico es superior a 6,5 mEq/l, se puede recetar insulina i.v. para impulsar el nivel de potasio en las células. Además, se puede recetar dextrosa i.v. para prevenir la hipoglucemia, dependiendo del nivel de glucosa sérica del paciente. El bicarbonato de sodio también impulsará el nivel de potasio en las células y ayudará a corregir la acidosis metabólica7,25.
Los efectos de estas dos terapias (insulina/glucosa y bicarbonato de sodio) solo son temporales porque el potasio finalmente saldrá de nuevo fuera de las células. Es importante vigilar atentamente los valores de las pruebas analíticas según lo prescrito para evaluar la respuesta del paciente al tratamiento7,25.
Se puede recetar gluconato de calcio o cloruro de calcio para contrarrestar los efectos tóxicos de la hiperpotasemia en la membrana celular miocárdica y prevenir arritmias7,25. Lostratamientos de urgencia adicionales de la hiperpotasemia incluyen albuterol nebulizado y resina de intercambio catiónico (sulfonato de poliestireno sódico).
Si estos tratamientos no resuelven la hiperpotasemia, el paciente puede necesitar TRR7. Además de en la hiperpotasemia en curso, la TRR está indicada en la sobrecarga de volumen, problemas de oxigenación, acidosis metabólica, arritmias cardíacas, pericarditis, derrame pericárdico y alteración del estado neurológico25.
Una evaluación minuciosa por parte de enfermería ayuda a identificar las posibles sustancias nefrotóxicos; trabaje con el equipo de atención médica para eliminarlas del plan de cuidados del paciente. Si el paciente ha recibido medios de contraste intravasculares, esté atenta a cualquier profilaxis de LRA inducida por el uso de contraste. Las recomendaciones actuales incluyen hidratación de líquidosi.v. con solución de cloruro de sodio al 0,9%, que ha demostrado ser más beneficiosa cuando se administra antes y después del procedimiento30. Las estrategias de prevención adicionales incluyen el uso de medios de contraste de baja osmolalidad o isoosmolalidad, y el uso de la dosis de estos más baja posible2.
Permanezca alerta a los medicamentos recetados o a los metabolitos de medicamentos que se excretan por los riñones. Puede ser necesario controlar los niveles de fármacos terapéuticos (máximo y mínimo) para decidir la dosis apropiada. Esté al tanto delmomento concreto de recogida de muestras con valores máximo y mínimo, comunique los resultados al equipo de atención médica, administre los medicamentos siguiendo un horario estricto y ajuste las dosis con frecuencia según lo prescrito.
Continúe vigilando los síntomas y signos de la infección, la principal causa de muerte en los pacientes con LRA. Puesto que su paciente tiene un trastorno funcional del sistema inmunológico, ponga en práctica medidas de control de infecciones, sea especialmente meticulosa con la higiene de las manos y asegúrese de que todos en la unidad también lo sean. Instruya al paciente y su familia sobre esto, especialmente sobre la higiene de manos9,25.
Proteínas o células en la orina pueden indicar lesión intrarrenal, como glomerulonefritis, infección renal o síndrome de Goodpasture.Enseñe al paciente en riesgo de atelectasia cómo utilizar un espirómetro de incentivo y cómo hacer ejercicios para toser y de respiración profunda. Si la movilidad está reducida, gire y cambie depostura al paciente al menos cada 2 horas para prevenir la acumulación de secreciones pulmonares y las úlceras de decúbito. Si el paciente puede estar fuera de la cama, explíquele la importancia de la deambulación precoz yactiva. Examine la piel del paciente cada día y aplique estrategias adicionales de prevención de úlceras de decúbito según lo indicado.
Prevenga las infecciones de las vías urinarias mediante el uso de una sonda vesical permanente solo si se cumplen las indicaciones apropiadas para ello y retírela lo más pronto posible. Si el paciente necesita una sonda urinaria, mantenga un sistema de drenaje cerrado y el flujo de la orina desobstruido. Limpie el meato con agua y jabón31.
Maneje los dispositivos de acceso venoso periférico y central, y los catéteres para diálisis con una técnica estéril rigurosa, de acuerdo con las políticas del centro. Recojalas muestras de orina, heces, sangre o esputo para cultivo y antibiograma según lo indicado. Administre los antibióticos prescritos de manera rigurosaa tiempo para evitar cualquier descenso de los niveles de fármacos terapéuticos.
El paciente con LRA necesita una ingesta de calorías adecuada para evitar el catabolismo de las proteínas corporales. Las recomendaciones KDIGO sugieren un consumo total de energía de 20-30 kcal/kg/día en pacientes con LRA2. Administre medicamentos antieméticos según la receta si el paciente presenta náuseas o vómitos. El paciente también puede necesitar potasio, sodio y la restricción de líquidos. Consulte con el dietista para organizar la ingesta nutricional adecuada y controleel consumo proteico del paciente9. Un paciente que necesita nutrición enteral y/o parenteral puede necesitar controlglucémico y TRR para eliminar el exceso de líquido25. Se ha demostrado que la nutrición enteral es segura y eficaz en pacientes con LRA, y es preferiblea la nutrición parenteral2.
La identificación temprana y la prevención de la deshidratación, sobre todo en pacientes de edad avanzada, tiene gran importancia. En los adultos mayores, muchos síntomas y signos típicos de deshidratación pueden ser imprecisos o no mostrarse. La hipotensión ortostática y la taquicardia son los hallazgos más llamativos clínicamente. A menos que la ingesta de líquidos esté restringida, los adultos mayores deben consumir 30 ml diarios de líquidos por kilogramo de peso corporal. Por ejemplo, un paciente que pesa 75 kg debe consumir 2.250 ml/día de líquidos32. Una proporción entreNUS y creatinina mayor o igual a 25 sugiere deshidratación en el adulto mayor16.
Los pacientes con LRA pueden presentar xerostomía (boca seca), sabor metálico y un aliento con un olor poco frecuente por la interacción bacteriana con la urea en la saliva9,25. También pueden desarrollar lesiones orales. Ayúdelos con una higiene oral frecuente e hidrate la mucosa oral y los labios cada 2-4 horas para evitar la degradación y mejorar la comodidad.
La disminución de la movilidad y el edema pueden poner en peligro la perfusión tisular y aumentar el riesgo de úlceras de decúbito9. Evalúe el estado de la piel del paciente en cada turno e incluya estrategias para la prevención de úlceras de decúbito en el plan de cuidados, incluyendo la deambulación en función de la situación clínica del paciente.
Consideraciones psicosocialesLos pacientes y sus familias sienten muchas emociones de diversa índole asociadas con un diagnóstico de LRA. Por ejemplo, un paciente puede temer el desarrollo de ERC, que le obligue a necesitar diálisis de por vida, con todos los cambios de estilo de vida que ello comporta. La información que le dé acerca de la LRA y el curso de la recuperación serán importantes para que el paciente mantenga una actitud positiva.
Los pacientes hospitalizados a menudo se sienten abrumados por la cantidad de información compleja, la sobrecarga sensorial del entorno, los cuidadores no familiares y la interrupción de las rutinas normales. La sensación de perder el control y la posibilidad de una larga enfermedad pueden causar frustración. La alteración de los roles familiares y laborales es otra fuente de estrés. Haga rondas con los otros miembros del equipo de atención para estar al tanto del plan de atención interdisciplinaria para que pueda abogar por las necesidades del paciente. Esta estrategia también facilita que la enfermera pueda responder a las preguntas del paciente cuando este pide más explicaciones acerca de lo que explica el dietista o el médico.
Historia de éxitoEl Sr. R fue dado de alta 2 semanas después de que se le hubiera realizado una artroplastia total de cadera derecha. Al realizar la evaluación inicial, la enfermera había reconocido muchos factores de riesgo de LRA, entre los cuales pueden citarse la edad avanzada, la inmovilidad prolongada y el uso de ibuprofeno y un inhibidor de la ECA. Con la identificación temprana de la disminución de la diuresis se lograron prevenir muchas complicaciones de la LRA y recobró la función renal sin necesidad de diálisis. El médico y la enfermera que lo visita a domicilio realizarán un atento seguimiento de los niveles de NUS y CrSa medida que se vaya recuperando.
El daño renal asociado con la LRA a menudo es reversible con unos cuidados rápidos, por lo que nunca hay que subestimar la importancia del rol de la enfermera en la evaluación y el cuidado de un paciente con LRA. ■
Ese artículo es la actualización de otro artículo que apareció originalmente en el número de marzo de Nursing2011.
Los autores y los editores declaran notener ningún conflicto de intereses económicos ni de otro tipo relacionado con este artículo.