El patrón de uso de fármacos antiepilépticos (FAE) durante el embarazo difiere entre países y está cambiando. Se desconoce en qué medida ello afecta a la población española. La eficacia de los nuevos fármacos en el control de las crisis es motivo de preocupación y puede haber cambiado a lo largo de los años debido a un mejor conocimiento de su uso durante el embarazo. Con el objetivo de analizar estos 2aspectos reportamos los resultados del registro EURAP España durante un periodo de 12 años.
Material y métodosTras el consentimiento informado, las pacientes son incluidas en el registro y evaluadas al inicio del embarazo, al final del segundo y tercer trimestres, después del parto y al año del nacimiento. Para los objetivos de este estudio hemos analizado: FAE, tipo de epilepsia, frecuencia de crisis por trimestres y a lo largo del embarazo, porcentaje de pacientes libres de crisis, y frecuencia de malformaciones congénitas mayores. Hemos comparado estas variables en 2periodos (junio de 2001-octubre de 2007) y (enero de 2008-mayo de 2015).
ResultadosUn total de 304 monoterapias del periodo antiguo se comparan con 127 del periodo nuevo. Observamos un ascenso del uso de levetiracetam (LEV) y un descenso del uso de carbamacepina (CBZ), fenitoína y fenobarbital; un leve descenso del uso de valproato (VPA), y un leve aumento de lamotrigina (LTG) y oxacarbamacepina (OXC). El tipo de epilepsia se mantiene estable para CBZ y VPA, pero cambia para LTG, con menos epilepsias generalizadas tratadas con este fármaco en el periodo nuevo. Ello no se asocia con un cambio significativo de la frecuencia de crisis, pero sí con un mejor control de las crisis de novo en el tercer trimestre. LEV se asocia a niveles de control de crisis similares a los de CBZ y VPA y mejor que con LTG. De las pacientes tratadas con LEV, un 64% tenían una epilepsia generalizada.
ConclusionesEl patrón de uso de los diferentes FAE durante el embarazo está cambiando en España, con menos uso de CBZ, fenitoína y fenobarbital y un aumento del uso de LEV. El tipo de epilepsia también cambia, con un porcentaje inferior de pacientes tratadas con LTG para epilepsias generalizadas. LEV controla las crisis de manera similar a los fármacos clásicos y mejor que la LTG.
The prescription pattern of antiepileptic drugs (AEDs) during pregnancy is changing but to what extent this is occurring in Spain remains unknown. The efficacy of newer drugs for controlling seizures is a key issue and may have changed over the years as doctors gained familiarity with these drugs during pregnancy. To assess these 2 topics, we report the results from the Spanish EURAP register gathered over a 12-year period.
Material and methodsAfter signing informed consent forms, patients were included in the register and evaluated at onset of pregnancy, at the end of the second and third trimesters, after delivery, and one year after delivery. For the purposes of this study, we analysed AEDs, type of epilepsy, seizure frequency per trimester and throughout pregnancy, percentage of seizure-free pregnancies, and frequency of congenital malformations. We then compared data from 2 periods (June 2001-October 2007) and (January 2008-May 2015)
ResultsWe compared 304 monotherapies from the older period to 127 from the more recent one. There was a clear increase in the use of levetiracetam (LEV) with declining use of carbamazepine (CBZ), phenytoin, and phenobarbital; a slight decline in use of valproate (VPA), and a slight increase in the use of lamotrigine (LTG) and oxcarbazepine (OXC). Epilepsy types treated with CBZ and VPA remained unchanged, whereas fewer cases of generalised epilepsy were treated with LTG in the new period. This trend was not associated with significant changes in seizure frequency, but rather linked to better control over de novo seizures in the third trimester. LEV was similar to CBZ and VPA with regard to levels of seizure control, and more effective than LTG. Generalised epilepsy accounted for 64% of the cases treated with LEV.
ConclusionsThe prescription pattern of AEDs during pregnancy has changed in Spain, with diminishing use of CBZ, phenytoin, and phenobarbital. Changes also reflect the type of epilepsy, since there is less use of LTG for generalised epilepsy. LEV provides similar seizure control to that of the older AEDs, and it is more effective and better than LTG.
La mayoría de las pacientes con epilepsia tiene un embarazo, parto y descendencia normales. No obstante, es bien conocido que las mujeres con epilepsia tratadas con fármacos antiepilépticos (FAE) pueden tener una descompensación de las crisis durante el embarazo, más complicaciones obstétricas (abortos, parto prematuro, bajo peso y muerte materna o fetal), y que sus hijos tienen más malformaciones congénitas y retraso en el desarrollo. El riesgo es mayor en las pacientes tratadas con dosis altas de FAE1–3.
El manejo de la epilepsia durante el embarazo requiere considerar y balancear los posibles efectos adversos de los FAE sobre el feto y los efectos de la crisis sobre la madre y el feto. Es un reto para el neurólogo el mantener el equilibrio entre el buen control de las crisis durante el embarazo y el riesgo teratogénico de los diferentes FAE.
El patrón de tratamiento con FAE difiere entre países4 y está cambiando a lo largo de los años por varios motivos5. Los nuevos FAE en general tienen una mejor tolerancia, menos efectos adversos graves, menos interacciones con otras medicaciones y una efectividad similar a los FAE clásicos en los estudios «pivotales».
El tratamiento con FAE durante el embarazo también está cambiando, aunque no sabemos hasta qué punto esto ocurre en nuestra población.
Además, la eficacia de los FAE puede haber cambiado a lo largo de los años, tras un mejor conocimiento de su farmacocinética durante el embarazo y de su eficacia en los diferentes tipos de crisis.
El presente trabajo pretende analizar si el patrón de utilización de los diferentes FAE durante el embarazo está cambiando en España y si existen diferencias en el control de las crisis durante el embarazo a lo largo de los años.
Material y métodosEl Registro Europeo e Internacional de Fármacos Antiepilépticos y Embarazo (EURAP) es un estudio observacional y prospectivo, colaborativo entre diferentes centros y países, que pretende obtener información sobre el riesgo de malformaciones fetales asociado al empleo de FAE durante el embarazo. Incluye a mujeres que estén tomando FAE en el momento de la concepción por cualquier motivo, aunque en la mayoría de los casos es por epilepsia.
Tras obtener el consentimiento informado, los datos de las pacientes se registran de forma prospectiva en 5 formularios: al inicio del embarazo, después del primer trimestre, después del segundo trimestre, después del parto y al año del nacimiento, este último puede ser por entrevista telefónica. En cada formulario se incluyen, aparte del tipo de FAE y dosis, información demográfica (edad, paridad, nivel educacional del padre y la madre), tipo de epilepsia y síndrome epiléptico, historia familiar de malformaciones o epilepsia y otros factores que podrían influir en el riesgo de malformaciones como uso de tabaco, alcohol, exposición a radiaciones, otras drogas, enfermedades intercurrentes, número de crisis convulsivas y no convulsivas por trimestres, complicaciones obstétricas, uso de ácido fólico y dosis y, por último, datos del niño como el resultado de la ecografía del 3.er trimestre, anmiocentesis o biopsia de corion —si practicada—, tets de Apgar, peso, perímetro cefálico y longitud.
España se unió a EURAP en junio del 2001. En el 2009 publicamos los resultados tras los primeros 6 años (junio de 2001-octubre de 2007) de colaboración con este registro. En este estudio concluimos que el valproato (VPA) tanto en monoterapia como en politerapia era el fármaco con mayor riesgo teratogénico, aunque no fuimos capaces de demostrar un efecto dosis/riesgo2. También observamos que las pacientes con VPA presentaban un mejor control de las crisis que las pacientes con lamotrigina (LTG).
El presente estudio analiza en primer lugar las pacientes registradas en EURAP España de junio del 2001 a octubre del 2007 y las compara con las pacientes registradas de enero del 2008 a mayo del 2015.
Posteriormente hemos analizado el número total de pacientes registradas con los fármacos nuevos LTG, oxacarbamacepina (OXC) y levetiracetam (LEV) y los hemos comparado entre sí y con los FAE clásicos: carbamacepina (CBZ) y VPA.
Para el análisis estadístico hemos utilizado el test de Fisher.
Resultados del estudio comparativoDe enero del 2008 a mayo del 2015 se incluyeron en el registro un total de 240 pacientes, de las cuales disponemos de todas las variables a analizar (incluido el año de seguimiento del recién nacido) en 154 parejas madre/niño. De ellas, 127 (82%) estaban en monoterapia.
En el estudio previo para un mismo intervalo de tiempo (6 años, de junio de 2001 a noviembre de 2007) se incluyeron un total de 304 parejas madre/niño con el mismo porcentaje de pacientes (83%) en monoterapia2.
El resultado obstétrico en el estudio actual fue de 141 nacidos vivos, 8 abortos espontáneos (5%), 2 abortos inducidos (uno por cromosomopatía, ninguno por malformación congénita) y 3 nacidos muertos.
En cuanto al tipo de epilepsia, 57 (37%) pacientes presentaron epilepsias generalizadas primarias, 90 (58%) epilepsias focales y 7 (4,5%) indeterminadas. Sin diferencias respecto a la serie previa2.
Los fármacos más utilizados en monoterapia en esta serie más reciente fueron LTG (37 casos; 29%), LEV (25 casos; 20%), CBZ (24 casos; 19%), VPA (26 casos; 20,5%), oxacarbamacepina (OXC; 6 casos; 5%), topiramato (TPM; 5 casos; 4%) y un caso con primidona.
Con relación a la serie previa (junio del 2001-noviembre del 2007)2 observamos un claro descenso del uso de CBZ del 38 al 19%, un leve descenso del uso de VPA (del 25% en la serie antigua a un 20% en la actual) y un leve aumento del uso de LTG (21% en la antigua y 29% en la actual). Aumenta de forma importante el uso de LEV con 4 casos (1,3%) en la serie antigua y 20% en la actual y descienden el fenobarbital y la fenitoína que tenían 12 casos (4%) y 10 casos (3%), respectivamente y no tienen ninguno en la serie actual.
De los niños, 8 tuvieron una o más de una malformación congénita mayor (MCM), lo que representa un 5,5% (8/144; del denominador se han excluidos los abortos, salvo por MCM), porcentaje similar al de la serie del 2001-20072. Sí observamos diferencias en el porcentaje de MCM en politerapia 7,6% (2/26) en la serie nueva respecto a un 12% en la serie antigua, probablemente porque esta nueva serie incluye menos politerapias con VPA (6 casos de 26 [23%] en la nueva y 15 de 51 [29%] en la antigua). El tipo de MCM fue en monoterapia: un labio y paladar hendido con VPA, una estenosis aórtica también con VPA; un defecto ventricular septal con CBZ, una transposición de grandes vasos con LTG, un pie equino varo con LEV y un defecto ventricular septal también con LEV. En politerapia, las MCM fueron un hipospadias (VPA y TPM) y una agenesia renal (etosuximida y TPM). No tuvimos ningún caso de espina bífida en la serie nueva y fueron 7 los de la serie antigua (3 en monoterapia con VPA, 2 en politerapia con VPA, uno en monoterapia con CBZ y un caso con VPA asociado a una cromosomopatía, [síndrome de Patau]).
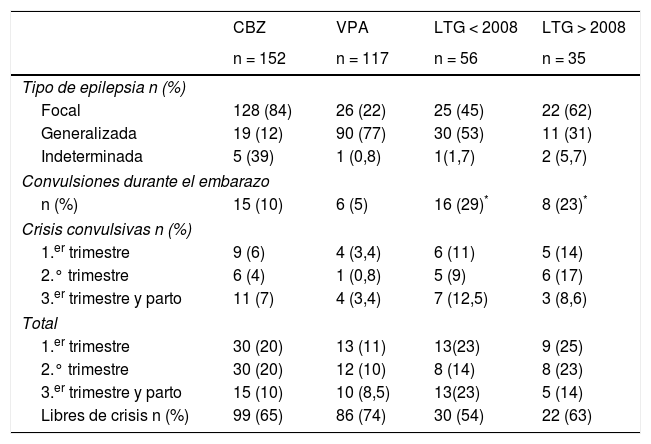
Resultados de los fármacos nuevosUn total de 56 pacientes (21%) recibieron LTG en monoterapia en la serie antigua (junio de 2001-noviembre de 2007) y 35 (24%) en la serie nueva (enero del 2008-mayo del 2015) excluidos los abortos espontáneos y las cromosomopatías. La tabla 1 muestra los resultados sobre el tipo de crisis, el número de pacientes libres de crisis, el número de pacientes con convulsiones y el reparto de las crisis por trimestres.
Tipo de epilepsia y frecuencia de crisis para carbamacepina, valproato y con lamotrigina antes y después del 2008
| CBZ | VPA | LTG < 2008 | LTG > 2008 | |
|---|---|---|---|---|
| n = 152 | n = 117 | n = 56 | n = 35 | |
| Tipo de epilepsia n (%) | ||||
| Focal | 128 (84) | 26 (22) | 25 (45) | 22 (62) |
| Generalizada | 19 (12) | 90 (77) | 30 (53) | 11 (31) |
| Indeterminada | 5 (39) | 1 (0,8) | 1(1,7) | 2 (5,7) |
| Convulsiones durante el embarazo | ||||
| n (%) | 15 (10) | 6 (5) | 16 (29)* | 8 (23)* |
| Crisis convulsivas n (%) | ||||
| 1.er trimestre | 9 (6) | 4 (3,4) | 6 (11) | 5 (14) |
| 2.° trimestre | 6 (4) | 1 (0,8) | 5 (9) | 6 (17) |
| 3.er trimestre y parto | 11 (7) | 4 (3,4) | 7 (12,5) | 3 (8,6) |
| Total | ||||
| 1.er trimestre | 30 (20) | 13 (11) | 13(23) | 9 (25) |
| 2.° trimestre | 30 (20) | 12 (10) | 8 (14) | 8 (23) |
| 3.er trimestre y parto | 15 (10) | 10 (8,5) | 13(23) | 5 (14) |
| Libres de crisis n (%) | 99 (65) | 86 (74) | 30 (54) | 22 (63) |
Se han excluido del total de pacientes los abortos, salvo por malformaciones congénitas y las cromosomopatías. Focal incluye las epilepsias de origen localizado ya sean crisis parciales o secundariamente generalizadas. Generalizada incluye todas las epilepsias generalizadas (ausencias, mioclónias, tónicas, tónico-clónicas) idiopáticas, sintomáticas o criptogénicas.
CBZ: carbamacepina; LTG: lamotrigina; VPA: valproato.
Se observaron diferencias en el tipo de crisis: en el periodo antiguo, un 53% en tratamiento con LTG tenían una epilepsia generalizada y en el nuevo solo un 31%; un 45% de las pacientes tenían una epilepsia focal en el periodo antiguo y un 62% en el más reciente (este dato no se ha analizado en otros estudios). No obstante, el cambio en el tipo de crisis tratadas no representó una reducción del número de crisis convulsivas (29% en el antiguo y 23% en el nuevo) y solo una tendencia a un mejor control de las crisis en general, 54% libres de crisis en el periodo antiguo versus 63% en el más reciente. Respecto a las crisis por trimestres se observa un mejor control de las crisis en el tercer trimestre en el periodo nuevo respecto al antiguo (14 versus 23%; p=0,29) y sin diferencias respecto al primer y segundo trimestres entre los 2periodos, con una predominancia de crisis en el primer trimestre de 23 y 25%, respectivamente. Presentaron crisis convulsivas de novo en el 2.° trimestre con relación al 1.°, 3 (5%) pacientes en la serie antigua y 2 (6%) en la nueva. Presentaron crisis convulsivas de novo en el 3.er trimestre, 5/56 (9%) pacientes en la serie antigua y 1/35 (3%) en la nueva (p=0,39). Si lo comparamos con CBZ: 3 (2%) pacientes en el 2.° trimestre y 3 (2%) en el 3.° presentaron crisis convulsivas de novo; con VPA: 1 (0,8%) en el segundo y 1 (0,8%) en el tercer trimestre.
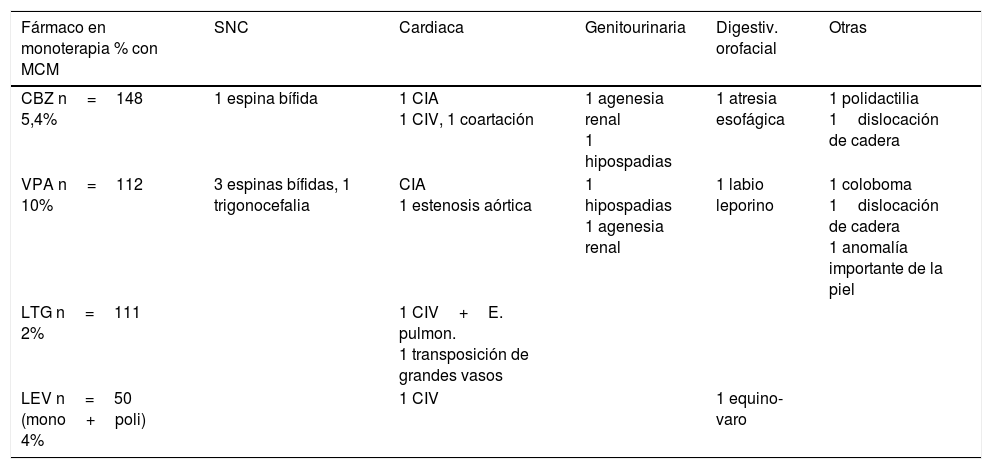
Del total de pacientes tratadas con LTG en monoterapia (111 casos, excluidos los abortos salvo por MCM y las cromosomopatías), 2 presentaron malformaciones congénitas mayores (2%). La tabla 2 muestra el tipo de malformaciones observado: un caso con transposición de grandes vasos y epilepsia focal (dosis 300mg/día) y un caso de estenosis pulmonar y defecto ventricular septal (dosis de 250mg/día) también con epilepsia focal.
Malformaciones congénitas mayores y tipo (algunas son múltiples) para los diferentes fármacos en monoterapia CBZ, VPA, LTG, y LEV (mono- y politerapia)
| Fármaco en monoterapia % con MCM | SNC | Cardiaca | Genitourinaria | Digestiv. orofacial | Otras |
|---|---|---|---|---|---|
| CBZ n=148 5,4% | 1 espina bífida | 1 CIA 1 CIV, 1 coartación | 1 agenesia renal 1 hipospadias | 1 atresia esofágica | 1 polidactilia 1dislocación de cadera |
| VPA n=112 10% | 3 espinas bífidas, 1 trigonocefalia | CIA 1 estenosis aórtica | 1 hipospadias 1 agenesia renal | 1 labio leporino | 1 coloboma 1dislocación de cadera 1 anomalía importante de la piel |
| LTG n=111 2% | 1 CIV+E. pulmon. 1 transposición de grandes vasos | ||||
| LEV n=50 (mono+poli) 4% | 1 CIV | 1 equino-varo |
Se han excluido del total de pacientes los abortos salvo por malformaciones congénitas y las cromosomopatías.
CBZ: carbamacepina; CIA: comunicación interauricular; CIV: comunicación interventricular; E. pulmon.: estenosis pumonar; LTG: lamotrigina; LEV: levetirazetam; MCM: malformación congénita mayor; SNC: sistema nervioso central; VPA: valproato.
El LEV se utilizó en monoterapia en solo 4 pacientes en el primer periodo (2001-2007) y la OXC en 13 pacientes, por lo que estos fármacos los analizaremos en su totalidad sin dividirlos entre periodo antiguo y nuevo.
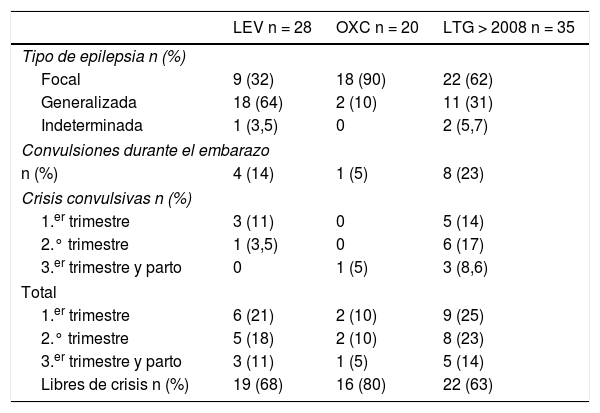
De un total de 630 pacientes con seguimiento de un año tras el parto registradas hasta mayo del 2015, 57 recibieron tratamiento con LEV. De ellas, 31 pacientes estaban en monoterapia y 26 en politerapia. El resultado del embarazo en monoterapia fue 27 nacidos vivos, 2 abortos espontáneos, un aborto inducido por cromosomopatía y un nacido muerto. El resultado del embarazo en politerapia fue de 4 abortos y 22 nacidos vivos. Presentaron MCM 2 pacientes en monoterapia y ninguna en politerapia. El tipo de malformación fue una comunicación interventricular (dosis de 1.000mg/día) y unos pies equino-varos (dosis de 1.500mg/día). La asociación más frecuente en politerapia fue con LTG (9 pacientes) seguida de la OXC (6 casos), VPA y TPM (2 casos), CBZ (3 casos), clobazam (2 casos) y 3 FAE en 3 casos. La tabla 3 muestra los resultados sobre el tipo de crisis, el número de pacientes libres de crisis, el número de pacientes con convulsiones y el reparto de las crisis por trimestres en las pacientes en monoterapia. De los 28 nacidos, 18 (64%) tenían una epilepsia generalizada y 6 (32%) tenían una epilepsia focal; en un caso la epilepsia fue indeterminada. Presentaron crisis convulsivas 4 (14%) pacientes y 19 (68%) permanecieron completamente libres de crisis durante todo el embarazo. El reparto de las crisis por trimestres mostró un predominio en el primer trimestre en las crisis convulsivas 3 (10%) y discreta mejoría en el tercer trimestre.
Tipo de epilepsia y frecuencia de crisis para levetiracetam, oxacarbamacepina y lamotrigina después del 2008
| LEV n = 28 | OXC n = 20 | LTG > 2008 n = 35 | |
|---|---|---|---|
| Tipo de epilepsia n (%) | |||
| Focal | 9 (32) | 18 (90) | 22 (62) |
| Generalizada | 18 (64) | 2 (10) | 11 (31) |
| Indeterminada | 1 (3,5) | 0 | 2 (5,7) |
| Convulsiones durante el embarazo | |||
| n (%) | 4 (14) | 1 (5) | 8 (23) |
| Crisis convulsivas n (%) | |||
| 1.er trimestre | 3 (11) | 0 | 5 (14) |
| 2.° trimestre | 1 (3,5) | 0 | 6 (17) |
| 3.er trimestre y parto | 0 | 1 (5) | 3 (8,6) |
| Total | |||
| 1.er trimestre | 6 (21) | 2 (10) | 9 (25) |
| 2.° trimestre | 5 (18) | 2 (10) | 8 (23) |
| 3.er trimestre y parto | 3 (11) | 1 (5) | 5 (14) |
| Libres de crisis n (%) | 19 (68) | 16 (80) | 22 (63) |
Se han excluido del total de pacientes los abortos salvo por malformación congénita y las cromosomopatías. Focal incluye las epilepsias de origen localizado ya sean crisis parciales o secundariamente generalizadas. Generalizada incluye todas las epilepsias generalizadas (ausencias, mioclónias, tónicas, tónico-clónicas) idiopáticas, sintomáticas o criptogénicas.
LEV: levetiracetam; LTG: lamotrigina; OXC: oxacarbamacepina.
Un total de 40 pacientes recibieron tratamiento con OXC, 22 en monoterapia y 18 en politerapia. El resultado del embarazo fue 20 nacidos vivos y 2 abortos espontáneos en monoterapia, y 17 niños normales y un aborto inducido por MCM (espina bífida OXC+VPA) en politerapia. De los 20 nacidos en monoterapia 18 (90%) tenían una epilepsia focal; presentó crisis convulsivas solo una paciente (5%) y fue en el último trimestre. Permanecieron completamente libres de crisis durante todo el embarazo 16 pacientes (80%). No hubo diferencias de las crisis por trimestres.
El estudio comparativo de las pacientes tratadas con LTG y LEV revela que las pacientes con LVT tienen con más frecuencia epilepsias generalizadas y que presentan un mejor control de las crisis convulsivas que con LTG: 14 versus 29% del periodo antiguo y 23% del periodo nuevo, con diferencias significativas de LTG respecto a VPA y sin diferencias entre VPA y LEV. El reparto por trimestres de las crisis muestra una crisis convulsiva de novo 1/28 (3,5%) con relación al primer trimestre con LEV, versus 8/56 (14%) con LTG en el periodo antiguo y 3/35 (8,6%) en el periodo nuevo.
DiscusiónEl porcentaje de epilepsias generalizadas idiopáticas y de epilepsias focales en nuestro estudio es similar en los 2periodos temporales analizados, y también similar a los observados en el registro de EURAP internacional6. En otros estudios esta variable no se ha podido analizar (registro del Reino Unido, registro de Estados Unidos)7,8 o difiere respecto al nuestro (48% epilepsias focales en el registro australiano versus 58% en el presente estudio)9. Las diferencias observadas son probablemente metodológicas, por la manera en la que se registran los datos de las pacientes: por neurólogos en el registro EURAP y por las propias pacientes en una web en el resto de los registros10. Reportar este dato es importante, ya que sabemos11–14 que las pacientes que presentan epilepsias generalizadas idiopáticas tienen más posibilidades de permanecer libres de crisis durante el embarazo que las que presentan epilepsias focales.
En nuestro estudio se observa un cambio en el patrón de tratamiento con LTG: menos pacientes con epilepsias generalizadas en el periodo nuevo (31%) respecto al antiguo (53%), probablemente porque este fármaco se sabe que no es tan eficaz en las epilepsias generalizadas mioclónicas (SANAD 2007)15. Sin embargo, y en contra de lo esperado, no se aprecia un cambio significativo en el control de las crisis durante el embarazo. Solo hemos podido mostrar una tendencia a un mejor control de las crisis en general (63 versus 53%) y en las crisis convulsivas de novo en el tercer trimestre (3 versus 9%), aunque sin significación estadística.
El registro australiano9 muestra que los fármacos clásicos en las embarazadas son más eficaces que los nuevos (LTG, LEV y TPM) en el grupo de pacientes en general y también en el grupo de pacientes tratadas después del 2008. También muestra que los fármacos clásicos son más eficaces en las epilepsias focales o generalizadas que los fármacos nuevos. El análisis de la situación de las crisis el año previo al embarazo en el registro autraliano9 muestra que en las pacientes con una epilepsia activa no existen diferencias significativas entre FAE antiguos y nuevos. Sin embargo, en el grupo de pacientes con epilepsia inactiva en el año previo al embarazo es donde los FAE nuevos muestran un significativo peor control de las crisis. Tanto el registro australiano9 como EURAP internacional13 muestran que la causa de estas diferencias es la LTG, con un peor control de las crisis durante el embarazo. En nuestro estudio no encontramos diferencias significativas en el porcentaje de crisis con LTG entre los años 2001 y 2007 y después del 2008. Reisinger et al.14 mostraron que cuando los niveles de LTG descienden por debajo del 35% de su nivel basal, se producen crisis en el segundo trimestre. Sabers et al.16 observaron que con un seguimiento exhaustivo de los niveles plasmáticos de LTG y con un ajuste de las dosis para mantener niveles adecuados se conseguía un control de las crisis similar a la de los otros FAE. En nuestro estudio no se determinaron los niveles de LTG ni los incrementos de dosis en los sucesivos trimestres para analizar si existió ajuste de dosis. No obstante, es de suponer que, tras el conocimiento de la farmacocinética de este FAE, a partir del 2008 se realizaban ajustes de dosis trimestrales. Serán necesarios estudios con una población más numerosa que realicen control de dosis y niveles y un análisis pormenorizado de la situación de las crisis previa al embarazo, para poder valorar si existe una mejoría en el control de las crisis con este fármaco, ya que su perfil de seguridad en la capacidad de producir MCM o trastornos cognitivos conductuales en el neonato es buena6,17.
En nuestro estudio se observa un descenso del uso de CBZ en el periodo nuevo y, en menor grado, de VPA. LEV aumenta de forma importante y, lo que es más interesante, se utiliza en un 64% en epilepsias generalizadas. El estudio comparativo con VPA, en el que se utiliza en epilepsias generalizadas en un 77%, no muestra diferencias significativas en favor de un FAE u otro. Sí existen diferencias entre VPA y LTG (p = 0,001) tanto en el periodo antiguo como en el nuevo, aunque este fármaco se utiliza menos, en general, en epilepsias generalizadas. Se necesitarán más estudios para corroborar estos resultados, ya que el número de pacientes con LEV en nuestra serie todavía es bajo.
Vajda et al.9 comparan LEV con VPA y no encuentran diferencias significativas entre estos FAE respecto al control de las crisis; sin embargo, se desconoce en este estudio el porcentaje de epilepsias generalizadas tratadas con LEV o VPA o la situación de las crisis en estas pacientes el año previo al embarazo. Otros estudios que analizan directa o indirectamente la frecuencia de crisis en general con LEV8,9,18 muestran porcentajes de crisis no superiores a los de los FAE clásicos.
El porcentaje de MCM se mantiene en los 2periodos analizados sin diferencias significativas2. Se observa un menor número de MCM en politerapia (7,6 en el periodo nuevo vs. 12% en el antiguo), posiblemente por una leve reducción del número de pacientes tratadas con VPA o por emplear dosis inferiores19,20. Dos de las 28 pacientes tratadas con LEV en monoterapia presentaron MCM. Este dato es sorprendente y lo atribuimos al azar, ya que la revisión de la literatura realizada por Chaudhry et al.21 aporta un porcentaje de MCM para este FAE de solo un 2,2% (27/1.213).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al grupo de estudio de epilepsia de la SEN por la difusión de EURAP y patrocinio. Al Dr. A. Cobos y al Dr. S. Quintana por su ayuda en la realización del estudio estadístico.
Colaboradores de EURAP (no reflejados en los autores) por orden de número de pacientes incluidos: E. Pastor Millán, Virgen de las Nieves, Granada; M. D. Castro Vilanova, Severo Ochoa, Madrid; I. Gracia Morales, Ruber Internacional y Hospital Clínico Universitario, Madrid; M. Codina, J. L. Becerra, Trias i Pujol, Badalona; I. Garamendi Ruiz H. Cruces, Baracaldo; E. López Gomariz, Xativa, Valencia; M. L. Galiano, Moratalaz, Madrid; J. Galán, Valme, Sevilla; P. Fossas, Mataró, Barcelona; T. García, N. Muelas, La Fe, Valencia; G. Sansa, Parc Taulí, Sabadell; D. Sopelana, Hospital Universitario de Albacete, Albacete; C. Cabeza, Salud, Toledo; J. Macarrón, Yagüe, Burgos; R. Ribacoba, Mieres, Asturias; A. Molins, Trueta, Gerona; M. Veciana, Sant Boi, Barcelona; E. Comas, Sagrat Cor, Barcelona; L. Morlas, Getafe, Madrid; A. Arribas, Vilafranca; M. Amorin, Noreste, Murcia; J. Poza, Aranzazu, San Sebastián; M. J. Imaz, L. García-Esteve, Clinic, Barcelona.