La amiodarona es un fármaco antiarrítmico de clase III ampliamente utilizado en nuestro medio para el tratamiento de arritmias cardiacas. Es un derivado benzofuránico con alto contenido en yodo que puede influir sobre la función tiroidea a diferentes niveles (hipófisis, tiroides y receptores periféricos). Puede modificar en muchos casos las concentraciones circulantes de las hormonas tiroideas y acompañarse tanto de hipo como de hipertiroidismo, si bien la mayor parte de los pacientes permanecen eutiroideos1,2.
El tratamiento de primera línea del hipertiroidismo inducido por amiodarona es fundamentalmente médico con antitiroideos de síntesis en el caso de la tirotoxicosis tipo 1 (inducida por yodo) o con glucocorticoides en la tipo 2 (por destrucción glandular). Otros fármacos menos convencionales son el perclorato potásico y la colestiramina3,4. La plasmaféresis se ha utilizado ocasionalmente en casos de intolerancia a antitiroideos, hipertiroidismo refractario y para conseguir el eutiroidismo antes de la tiroidectomía, si bien la experiencia clínica es escasa5.
Presentamos el caso de un paciente con cardiopatía estructural con hipertiroidismo severo por amiodarona refractario a tratamiento médico que precisó un elevado número de ciclos de plasmaféresis previo al tratamiento definitivo con tiroidectomía.
Varón de 53 años con hipertensión arterial, dislipidemia, obesidad, síndrome de apnea del sueño y fibrilación auricular persistente anticoagulada, por la que había recibido tratamiento con amiodarona (200mg/día) durante 3 años, con su suspensión en los 2meses previos al ingreso, momento en el que fue sustituido por bisoprolol.
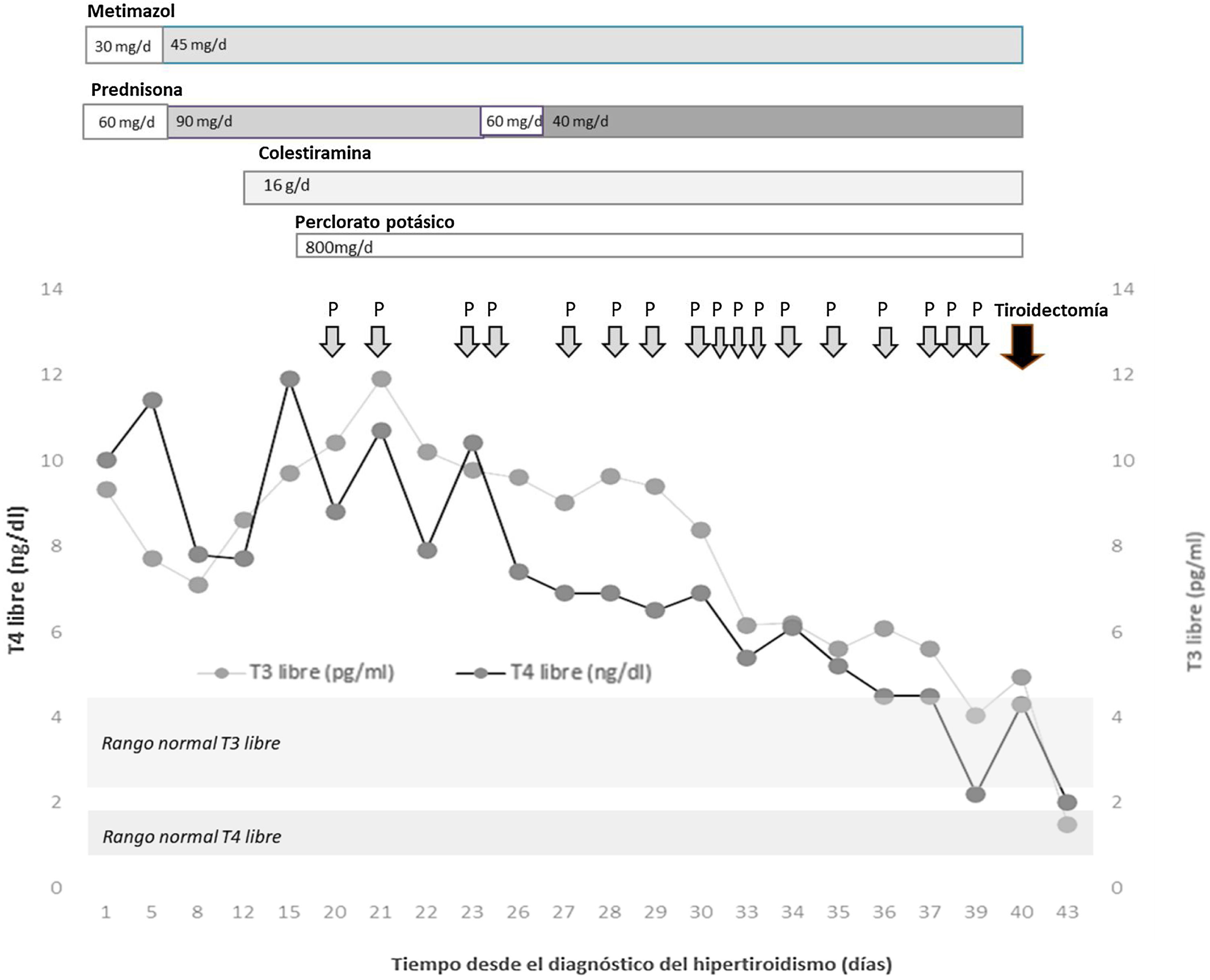
El paciente ingresó para realización de coronariografía preferente por dolor torácico con elevación de marcadores de daño cardiaco, resultando ser normal. Se completó estudio con ecocardiograma transtorácico que mostró un ventrículo derecho severamente dilatado y datos de hipertensión pulmonar severa, así como la existencia de una comunicación interauricular (CIA) tipo seno venoso superior, con indicación de cierre quirúrgico no urgente. Durante el ingreso se descubrió un hipertiroidismo franco severo (TSH<0,01μIU/ml, rango normal [RN]: 0,35-5,0; T4 libre [T4L] 10,03 ng/dl, RN: 0,7-1,98, y T3 libre [T3L] 9,3 pg/ml, RN: 2,3-4,2) una semana previa a la realización del cateterismo, sin haber presentado anteriormente exposición a contrastes yodados. Clínicamente no refería palpitaciones, temblor, nerviosismo, ni otra sintomatología de hiperfunción tiroidea. Presentaba buen control tensional y de frecuencia cardiaca con betabloqueantes. Se palpaba bocio de grado 2, sin nódulos. En la ecografía tiroidea, se objetivó una glándula de tamaño normal con vascularización disminuida. El estudio de autoinmunidad tiroidea fue negativo y la interleucina-6, normal (< 2,7 pg/ml, RN: 0,0-4,4). Ante estos hallazgos y la sospecha de hipertiroidismo inducido por amiodarona, se inició tratamiento con metimazol (30mg/día) y prednisona (60mg/día). Durante el ingreso, el paciente presentó niveles séricos crecientes de hormonas tiroideas, lo que obligó a aumentar la dosis de metimazol (45mg/día) y prednisona (90mg/día) (fig. 1). Asimismo, se asoció colestiramina (16g/día) y perclorato potásico (800mg/día). A pesar de ello y, tras supervisar la adecuada adherencia al tratamiento, a la tercera semana persistía el hipertiroidismo grave (TSH <0,01μIU/ml, T4L 11,92 ng/dl y T3L 9,76 pg/ml) estableciéndose el diagnóstico de un hipertiroidismo inducido por amiodarona severo y refractario a altas dosis de metimazol, corticoides, colestiramina y perclorato potásico, por lo que se planteó la tiroidectomía total como tratamiento definitivo. Tras comentar el caso en sesión multidisciplinar con Cirugía Cardiaca, Cardiología, Anestesia, Cirugía General y Endocrinología, se decidió realizar primero una tiroidectomía total y, en un segundo lugar, el cierre de la CIA. Con la finalidad de reducir el riesgo cardiovascular perioperatorio se inició tratamiento con plasmaféresis con el objetivo de conseguir el estado eutiroideo.
Las sesiones de plasmaféresis consistieron en recambios plasmáticos mixtos de albúmina/plasma de 1,5 volemias en cada sesión realizados por el servicio de Hematología mediante una máquina de aféresis. Como complicaciones, el paciente presentó varios episodios de rash cutáneo que precisaron tratamiento antihistamínico profiláctico con cada recambio. Durante el procedimiento, se observó una leve tendencia a la anemización (nadir de hemoglobina 11,2g/dl, RN: 12,0-17,0g/dl; tras la 11.ª sesión de plasmaféresis, 13 días tras su inicio) que no precisó tratamiento. Asimismo, se observó una hipocalcemia asintomática a pesar de suplementación intravenosa con gluconato cálcico (nadir de 7,6mg/dl; RN: 8,7-10,3mg/dl). Todas estas complicaciones resolvieron tras finalizar la plasmaféresis.
Dada la dificultad para conseguir un descenso de las hormonas tiroideas circulantes, se realizaron un total de 17 sesiones previas a la cirugía. En ningún momento se suspendió el tratamiento médico adicional, aunque sí que se realizó un descenso progresivo de dosis de prednisona hasta 40mg/día. También se determinaron en 5 ocasiones los niveles séricos de hormonas tiroideas antes y después de la sesión de plasmaféresis, consiguiéndose una reducción de sus niveles en la muestra de la extracción inmediata posplasmaféresis (T4L pre vs. posplasmaféresis 7,89±2,48 vs. 4,58±1,35 ng/dl, p=0,009; reducción del 41,9% y T3L pre vs. posplasmaféresis 8,60±2,46 vs. 8,24±2,17 pg/ml, p=0,157; reducción del 4,1%), con un nuevo incremento en el día posterior a la plasmaféresis (T4L día siguiente 6,73±1,07 ng/dl, p=0,001; incremento del 46,94% y T3L día siguiente 8,25±2,15 pg/ml, p=0,950; incremento del 0,1%).
Finalmente se realizó tiroidectomía total a los 40 días del diagnóstico inicial del hipertiroidismo, sin incidencias. El perfil tiroideo previo a la cirugía fue TSH 0,01μIU/ml, T4L 4,33 ng/dl y T3L 4,95 pg/ml. En el día inmediatamente posterior, se objetivó un descenso de la T4L hasta 3,88 ng/dl, disminuyendo a valores de 1,98 ng/dl a los 3 días de la intervención. Dada la ausencia de complicaciones posquirúrgicas y la rápida normalización de las hormonas tiroideas, el paciente fue dado de alta con tratamiento hormonal sustitutivo con levotiroxina 150 μg al día.
El recambio plasmático terapéutico (RPT) es un tratamiento raramente utilizado para el control del hipertiroidismo. El Banco de Sangre (Servicio de Hematología y Hemoterapia) se encarga de su realización, requiriendo para el procedimiento unas vías aferente y eferente que conectan con la máquina de aféresis. Su utilidad se basa en la unión de T3 y T4 a proteínas plasmáticas que son eliminadas. Al disminuir su concentración plasmática se reduce la hormonal (principalmente T4, con menor fracción libre). Además, al utilizar plasma fresco como fluido de reposición, se aportan estas proteínas que permiten la fijación de hormona libre6.
Su indicación en el hipertiroidismo no está claramente establecida. Algunos autores consideran que el RPT podría ser útil en la tormenta tirotóxica, en casos de intolerancia o refractariedad a tratamientos convencionales y como preparación prequirúrgica7, siendo su indicación más frecuente la enfermedad de Graves seguida del hipertiroidismo inducido por amiodarona8. Entre sus complicaciones se incluyen sangrado, infección, hipotensión arterial, hipocalcemia y reacciones cutáneas. Las más graves corresponden a la coagulación intravascular diseminada o tromboembolia pulmonar, con una mortalidad <1%9,10. En nuestro paciente, todas las complicaciones fueron leves y autolimitadas.
Aunque existen estudios donde fueron necesarias 4-6 sesiones de RPT para la normalización de hormonas tiroideas5,11, en nuestro caso este se incrementó a 17. Si bien es cierto que la alteración analítica fue claramente más marcada a la de otras series pudiendo, además, dificultar su control la exposición a contrastes yodados del cateterismo. Tras revisar la literatura, el presente caso sería el que mayor número de sesiones de plasmaféresis ha recibido antes del tratamiento definitivo. Así mismo, cada sesión redujo significativamente la T4L sin afectar prácticamente a la T3L; sin embargo, esta reducción fue transitoria con un incremento significativo a las 24 h, lo que justifica la repetición de sesiones. Durante la evolución, es difícil discernir el efecto neto del tratamiento farmacológico y la plasmaféresis en el control del hipertiroidismo. Si bien no se produjo descenso de las hormonas tiroideas hasta que se inició el RPT, lo que puede traducir la eficacia de esta técnica.
En conclusión, la plasmaféresis parece ser una alternativa eficaz en aquellos casos de hipertiroidismo severo inducido por amiodarona y refractario al tratamiento médico convencional en dosis máximas como preparación para un tratamiento definitivo con cirugía.
FinanciaciónLos autores declaran que no se ha recibido ningún tipo de financiación para esta investigación.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de interés relacionado con este artículo.