Dulaglutida y semaglutida son agonistas del receptor de GLP-1 (AR-GLP-1), de administración semanal, utilizados en el tratamiento de la hiperglucemia en diabetes mellitus tipo2 (DM2) y obesidad (IMC ≥30kg/m2).
ObjetivoEvaluar la eficacia y la seguridad del cambio de dulaglutida subcutánea (SC) a semaglutida SC en condiciones de vida real.
Material y métodosSe incluyeron 123 personas con DM2 en tratamiento con dulaglutida SC, en monoterapia o en combinación con otros fármacos antihiperglucemiantes, que cambiaron a semaglutida SC debido a una reducción insuficiente de la hemoglobina glucosilada (HbA1c), necesidad de mayor pérdida de peso, o intolerancia gastrointestinal a dulaglutida. Se analizaron los cambios en HbA1c y peso a los 6, 12, 18 y 24meses, y la variación de los efectos adversos asociados. Los datos se expresan como media ±desviación estándar.
ResultadosEl tratamiento previo con dulaglutida (duración 16,9±13,8 meses) se asoció con una reducción media del 0,38% en HbA1c (p=0,003 vs. basal) y una pérdida de 1,3kg (p=0,003 vs. basal). Tras el cambio a semaglutida, se observó una reducción adicional en HbA1c a los 6, 12, 18 y 24meses (−0,43%, p=0,000; −0,54%, p=0,000; −0,38%, p=0,021; −0,12%, p=0,622, respectivamente) y en peso (−2,7kg, p=0,000; −3,7kg, p=0,000; −5,4kg, p=0,001; −4,2kg, p=0,000, respectivamente). No hubo diferencias significativas en la frecuencia de efectos adversos.
ConclusionesEn condiciones de vida real, la transferencia de dulaglutida a semaglutida en pacientes con DM2 y obesidad se asocia con una reducción adicional de HbA1c y peso, sin cambios notables en la frecuencia de efectos adversos.
Dulaglutide and semaglutide are once-weekly administered GLP-1 receptor agonists (GLP-1 RAs) indicated for the treatment of hyperglycemia in individuals with type2 diabetes mellitus (T2DM) and obesity (BMI ≥30kg/m2).
ObjectiveTo evaluate the efficacy and safety of switching from subcutaneous (SC) dulaglutide to SC semaglutide, in real-world conditions.
Materials and methodsA total of 123 individuals with T2DM on SC dulaglutide, either as monotherapy or with other antihyperglycemic drugs, who switched to SC semaglutide were included. This switch was motivated by insufficient reduction in glycated hemoglobin (HbA1c), the need for greater weight loss, or gastrointestinal intolerance associated with dulaglutide. Changes with semaglutide in HbA1c and weight at 6, 12, 18, and 24months, as well as any changes in associated adverse effects. Data are expressed as mean ±standard deviation.
ResultsPrevious treatment with dulaglutide (duration 16.9±13.8 months) reduced HbA1c by 0.38% (P=.003 vs. baseline) and weight by −1.3kg (P=.003 vs. baseline). After switching to semaglutide, an additional reduction in HbA1c levels was observed at 6, 12, 18, and 24months (−0.43%, P=.000; −0.54%, P=.000; −0.38%, P=.021; −0.12%, P=.622, respectively) and in weight at 6, 12, 18, and 24months (−2.7kg, P=.000; −3.7kg, P=.000; −5.4kg, P=.001; −4.2kg, P=.000, respectively) With no significant differences in the frequency of adverse effects after switching to semaglutide.
ConclusionsIn real-world conditions, switching dulaglutide to semaglutide in obese patients with T2DM is associated with an additional reduction in HbA1c and weight, without notable changes in the frequency of adverse effects.
El péptido similar al glucagón tipo1 (GLP-1) es una hormona incretina de 30 aminoácidos producida en el intestino con efectos beneficiosos en el metabolismo de la glucosa y la regulación del apetito. Su acción deriva de la estimulación de la secreción de insulina, la supresión de la secreción de glucagón y el enlentecimiento del vaciamiento gástrico. Las opciones terapéuticas actuales para potenciar los efectos de las incretinas son el uso de inhibidores de la enzima dipeptidil peptidasa-4 (iDPP4) y los agonistas del receptor GLP-1 (AR-GLP-1). Estos últimos son una opción terapéutica establecida en el tratamiento de la hiperglucemia en personas con diabetes mellitus tipo2 (DM2) y obesidad. Actúan mimetizando el efecto del GLP-1 para estimular la secreción de insulina de forma glucosa-dependiente, disminuir la secreción posprandial de glucagón y enlentecer el vaciamiento gástrico. Todo ello produce un efecto anti-hiperglucemiante, con un riesgo intrínseco muy bajo de hipoglucemia1-3. También actúan sobre el sistema nervioso central (SNC) promoviendo la saciedad y reduciendo la ingesta calórica, y con ello contribuyen a la pérdida de peso4-7. Además, algunos AR-GLP-1 han demostrado en pacientes con DM2 una reducción de la morbimortalidad cardiovascular, tanto en prevención primaria como en prevención secundaria, convirtiéndose así en la base del tratamiento junto con inhibidores del cotransportador sodio-glucosa tipo2 (iSGLT2)8-10. Recientemente contamos con más evidencia sobre el efecto beneficioso de los AR-GLP-1 en la enfermedad hepática grasa no alcohólica (NAFLD) a través de un mecanismo de acción multifactorial que aún no es completamente comprendido pero que parece mejorar el daño hepático al promover una reducción en la esteatosis y la inflamación. Esta nueva línea de actuación es significativa, pues hasta el 70% de los pacientes con DM2 padecen NAFLD, y no disponemos de tratamientos específicos para combatirlo11.
En los pacientes con DM2 y obesidad, los AR-GLP-1 de administración semanal (exenatida LAR, dulaglutida y semaglutida) consiguen un mayor descenso de HbA1c y más pérdida ponderal cuando se comparan con los AR-GLP-1 de administración diaria y menor vida media (exenatida, liraglutida, lixisenatida). En los ensayos clínicos comparativos y aleatorizados, semaglutida ha demostrado ser más eficaz que el resto de AR-GLP-1 en la reducción de la HbA1c, siendo dulaglutida el segundo en potencia anti-hiperglucemiante12-15.
La mayor eficacia de semaglutida con respecto al resto de AR-GLP-1 podría estar relacionada con las características estructurales de la molécula16. Se trata de un AR-GLP-1 con una homología del 94% en la secuencia de aminoácidos con el GLP-1 endógeno, con tres modificaciones en su estructura que permiten una unión más prolongada a los receptores de GLP-1 y prolongan la vida media hasta aproximadamente una semana17. Además, al ser una molécula de pequeño tamaño puede llegar a regiones del SNC implicadas en el control de la ingesta. A esta característica se atribuye el hecho de que la pérdida ponderal con semaglutida sea superior a la de otros AR-GLP-1 de más tamaño como la dulaglutida, cuya entrada al SNC es más limitada18.
Aunque los estudios aleatorizados son los que aportan la mayor evidencia científica, están limitados con respecto a su validez externa, dado que estos estudios suelen incluir poblaciones de pacientes seleccionadas que pueden no reflejar las condiciones de prescripción en vida real19, en particular con respecto a los cambios entre diferentes AR-GLP-1. Existe escasa evidencia en condiciones en vida real sobre la efectividad y los posibles efectos adversos después del cambio de un AR-GLP-1 a otro. Los trabajos publicados compararon la transferencia de AR-GLP-1 de administración diaria o semanal con AR-GLP-1 de administración semanal20-22. En ellos se demuestra superioridad tanto en reducción de HbA1c como en pérdida ponderal, tras el cambio de un AR-GLP-1 diario o semanal a semaglutida subcutánea (SC)20-23. Sin embargo, en los estudios encontrados se incluyeron un número reducido de pacientes en tratamiento previo con dulaglutida, el segundo AR-GLP-1 en potencia anti-hiperglucemiante entre los de administración semanal.
Por todo lo expuesto anteriormente, el estudio SEMA-SWITCH fue diseñado para evaluar la eficacia y la seguridad, en iones de vida real, de la transferencia de dulaglutida SC semanal a semaglutida SC semanal. Al realizar la recogida y el análisis de datos, semaglutida oral no estaba comercializada en nuestro país, y por ello no fue incluida para hacer comparaciones en el estudio.
Material y métodosDiseño del estudioSe trata de un estudio retrospectivo y observacional realizado en el Hospital Clínico Universitario de Valencia (HCUV).
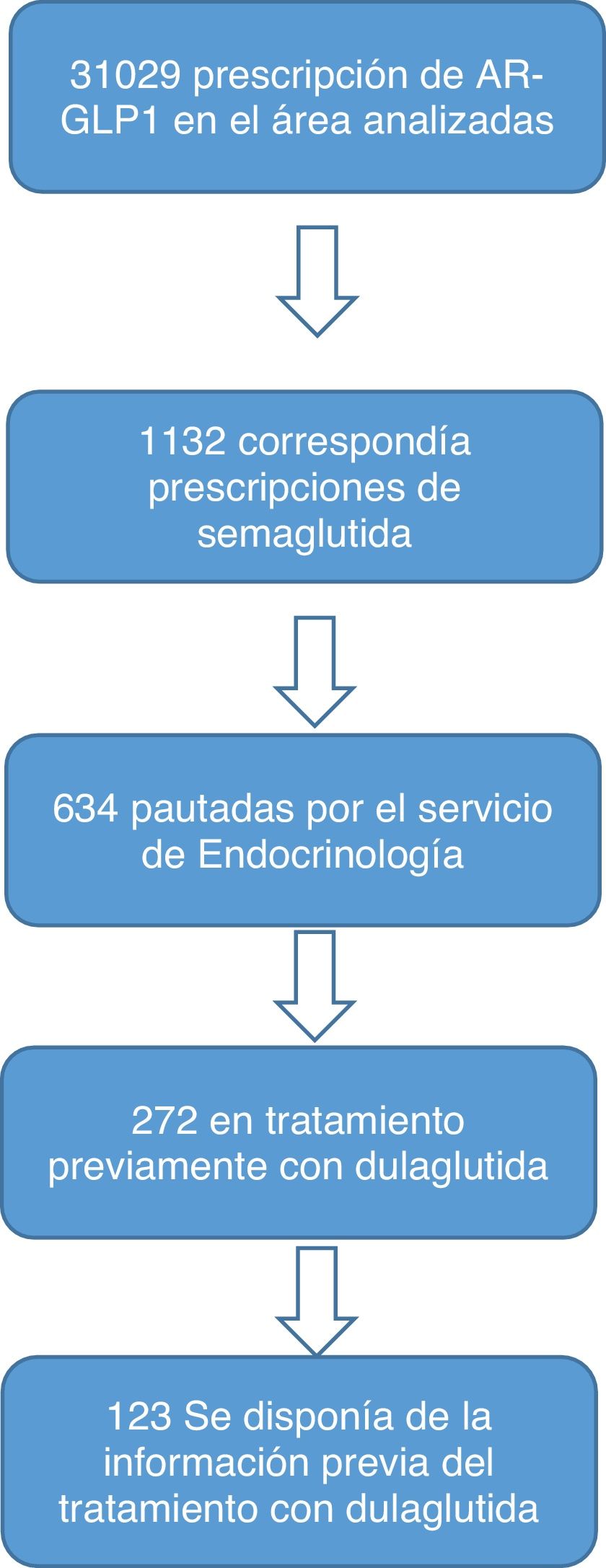
Selección de pacientesSe analizaron todas las prescripciones de semaglutida SC semanal en el área del HCUV desde mayo de 2019 (fecha de lanzamiento en España) hasta enero de 2021, encontrando un total de 482 pacientes. De estos, se seleccionó una muestra de 123 pacientes que cumplían los criterios de inclusión.
Los criterios de inclusión fueron: pacientes adultos (≥18años) con diagnóstico de DM2 e índice de masa corporal (IMC) ≥30kg/m2 que, antes de iniciar el tratamiento con semaglutida SC semanal, estaban o habían recibido previamente dulaglutida SC semanal.
Los pacientes seleccionados fueron aquellos en los que el cambio de tratamiento fue realizado por los facultativos especialistas en Endocrinología, asegurando así la adecuada recogida y seguimiento de la información. Los datos fueron recopilados retrospectivamente de las historias clínicas, complementados con información adicional obtenida telefónicamente cuando fue necesario. Se excluyeron del análisis aquellos pacientes con datos incompletos o que no tuvieran un seguimiento mínimo de 6meses después del cambio terapéutico (fig. 1).
Variables analizadas y seguimientoSe recopilaron datos demográficos y clínicos de los pacientes, incluyendo edad, sexo, duración de la diabetes, tratamiento concomitante (metformina, iSGLT2) e insulina), IMC, nivel inicial de HbA1c, peso inicial y duración del tratamiento previo con dulaglutida.
El cambio de tratamiento de dulaglutida a semaglutida fue realizado por razones clínicas. Los motivos del cambio fueron por una reducción insuficiente de la HbA1c, (considerándose insuficiente cuando esta era igual o menor al 1% tras 6meses de tratamiento) por necesidad de una mayor pérdida de peso (considerándose insuficiente cuando tras 6meses de tratamiento esta había sido inferior al 3% del peso) o por intolerancia gastrointestinal con dulaglutida. Se establecieron tres grupos de pacientes en función de dicho motivo para analizar si había diferencias entre ellos: el grupo1 (G1), en el que el motivo del cambio era una eficacia insuficiente en reducción de HbA1c; el grupo2 (G2), por una necesidad de mayor pérdida ponderal, y el grupo3 (G3), por intolerancia al fármaco previo.
Se llevó a cabo un análisis comparativo de los cambios en la HbA1c y en el peso con respecto al inicio del tratamiento, que fueron evaluados a los 6, 12, 18 y 24meses después del cambio terapéutico. Asimismo, se registraron los efectoos adversos durante el período de seguimiento.
Análisis estadísticoEl análisis estadístico se realizó utilizando SPSS-24 para datos apareados y medidas repetidas. Los resultados se expresaron como media ±desviación estándar (DE), considerando significación estadística cuando p<0,05.
Consideraciones éticasEste estudio se llevó a cabo de acuerdo con los principios éticos de la Declaración de Helsinki. Se obtuvo la aprobación de los pacientes en el momento del cambio y se mantuvo la confidencialidad de los datos durante la recogida y el análisis de los datos del estudio.
ResultadosCaracterísticas basales de los pacientes.Se incluyeron en el análisis un total de 123 pacientes con DM2 y obesidad (66 hombres y 57 mujeres), a los que se cambió su tratamiento de dulaglutida SC semanal a semaglutida SC semanal. La mayoría de estos cambios (82,4%) se debieron a una eficacia insuficiente en la reducción de HbA1c. La intolerancia gastrointestinal (10,4%) o la necesidad de una mayor pérdida de peso (7,2%) fueron, por este orden de frecuencia, otros motivos de cambio de tratamiento.
En el grupo de pacientes analizados, la edad media fue de 62años, con un promedio de IMC de 37kg/m2 y una duración media de la diabetes de 11,5años (tabla 1). Respecto al tratamiento concomitante, el 77,2% estaban en tratamiento con metformina, el 42,3% con iSGLT2 y el 50,4% con insulina.
Eficacia del tratamientoCambios en HbA1c mediaPrevio al inicio del tratamiento con dulaglutida, la muestra presentaba un valor basal de HbA1c de 8,43±1,54%. El tratamiento con dulaglutida mostró una reducción media de HbA1c de −0,38% (p=0,003) durante un período medio de tratamiento de 16,9±13,8 meses (tabla 2).
En relación con el tratamiento con semaglutida, el valor de HbA1c basal fue de 7,99±1,32%, Tras el cambio a semaglutida, se observó una reducción adicional en los niveles de HbA1c a los 6, 12, 18 y 24meses: −0,43% (p=0,000), −0,54% (p=0,000), −0,38% (p=0,021) y −0,12% (p=0,622), respectivamente (tabla 3 y fig. 2).
Antes del inicio del tratamiento con dulaglutida el peso basal era de 101,59±17,72kg. Con dulaglutida, se registró una pérdida de peso media de −1,3kg (p=0,003) durante el período medio de tratamiento de 16,9±13,8 meses (tabla 2).
Previo al cambio a semaglutida, el peso inicial era de 100,59±17,68kg. Tras el cambio a semaglutida, se evidenció una reducción de peso adicional y de mayor magnitud a los 6, 12, 18 y 24meses: −2,7kg (p=0,000), −3,7kg (p=0,000), −5,4kg (p=0,001) y −4,2kg (p=0,000), respectivamente (tabla 3 y fig. 2).
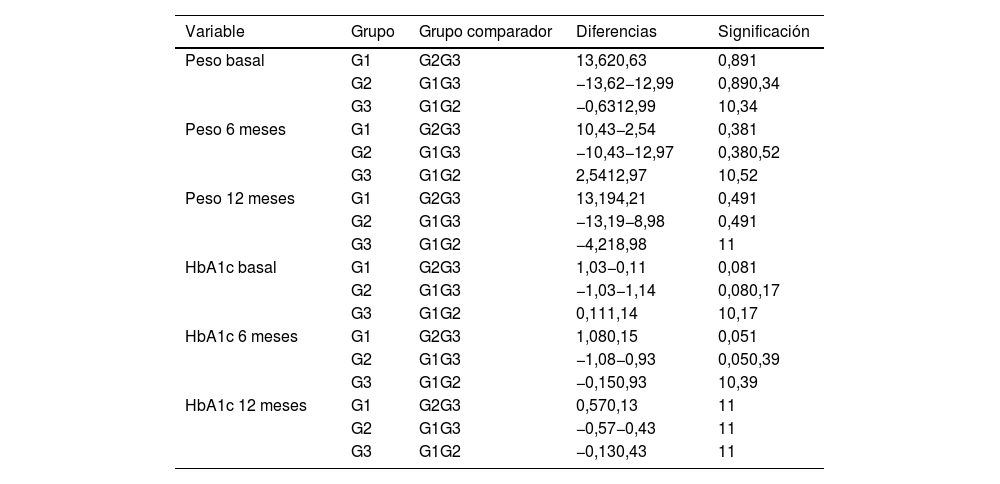
Evaluación según motivo del cambioDel total de 123 pacientes seleccionados para el estudio, se disponía información del motivo del cambio de 113 de ellos. El cambio a semaglutida fue en un 82,31% por eficacia insuficiente (G1), en un 7,96% por necesidad de mayor pérdida de peso (G2), y en un 9,73% por intolerancia (G3). Se realizó un análisis comparativo de los cambios en la HbA1c y en el peso con respecto al inicio del tratamiento, que fueron evaluados a los 6 y 12meses. Al realizar el análisis por subgrupos no se encontraron diferencias significativas en función del motivo del cambio de tratamiento en la reducción de HbA1c y la pérdida ponderal (tabla 4).
Cambios en el peso y en la HbA1c según el motivo del cambio
| Variable | Grupo | Grupo comparador | Diferencias | Significación |
|---|---|---|---|---|
| Peso basal | G1 | G2G3 | 13,620,63 | 0,891 |
| G2 | G1G3 | −13,62−12,99 | 0,890,34 | |
| G3 | G1G2 | −0,6312,99 | 10,34 | |
| Peso 6 meses | G1 | G2G3 | 10,43−2,54 | 0,381 |
| G2 | G1G3 | −10,43−12,97 | 0,380,52 | |
| G3 | G1G2 | 2,5412,97 | 10,52 | |
| Peso 12 meses | G1 | G2G3 | 13,194,21 | 0,491 |
| G2 | G1G3 | −13,19−8,98 | 0,491 | |
| G3 | G1G2 | −4,218,98 | 11 | |
| HbA1c basal | G1 | G2G3 | 1,03−0,11 | 0,081 |
| G2 | G1G3 | −1,03−1,14 | 0,080,17 | |
| G3 | G1G2 | 0,111,14 | 10,17 | |
| HbA1c 6 meses | G1 | G2G3 | 1,080,15 | 0,051 |
| G2 | G1G3 | −1,08−0,93 | 0,050,39 | |
| G3 | G1G2 | −0,150,93 | 10,39 | |
| HbA1c 12 meses | G1 | G2G3 | 0,570,13 | 11 |
| G2 | G1G3 | −0,57−0,43 | 11 | |
| G3 | G1G2 | −0,130,43 | 11 |
G1: grupo 1; G2: grupo 2; G3: grupo 3; HbA1c: hemoglobina glucosilada.
Durante el tratamiento con dulaglutida se registraron 20 efectos adversos, predominantemente leves, siendo 19 eventos gastrointestinales y una reacción cutánea leve. Tras el cambio a semaglutida se observaron 12 efectos adversos, mayormente gastrointestinales leves, y una reacción cutánea leve, además de un caso de cólico biliar. En 9 pacientes se suspendió el tratamiento con semaglutida, principalmente debido a preferencia por el dispositivo previo, eventos gastrointestinales leves o falta de respuesta (tabla 5).
DiscusiónEl objetivo principal del estudio fue analizar, en condiciones de vida real, la efectividad (medida como reducción adicional en HbA1c y peso) y seguridad (aparición de eventos adversos) del cambio de semaglutida a dulaglutida. Partiendo de los resultados obtenidos en el REWIND15, en el que dulaglutida SC semanal se asoció a una reducción media de HbA1c de −0,6% y una pérdida ponderal de −1,46kg en comparación con placebo, se tomó la decisión de no incluir a pacientes que habían hecho el cambio desde otros AR-GLP-1 diferentes a dulaglutida, por ser este el segundo análogo más potente en la fecha en la que se realizó la recogida de datos. No existen estudios previos de cambio de dulaglutida a semaglutida en condiciones de vida real, pero sí con otros AR-GLP-1. Este es un aspecto diferencial de este estudio observacional frente a otros publicados. Nuestros resultados previos con dulaglutida (tabla 2) fueron ligeramente inferiores a los observados en el REWIND15, especialmente en descenso de HbA1c. Esto podría estar justificado por el sesgo de inclusión al analizar únicamente pacientes en los que se realizó un cambio de GLP-1 por mala respuesta previa. En la mayoría de pacientes el cambio se realizó por una eficacia insuficiente en cuanto a reducción de HbA1c (82,31%).
En nuestro país, varios estudios previos han evaluado la efectividad de los AR-GLP-1 en vida real24-27. El estudio observacional de Gorgojo-Martínez et al.25 en pacientes con DM2 en condiciones de vida real evaluó la efectividad de exenatida SC 2veces al día (n=116) frente a liraglutida SC una vez al día (n=162) en un período de 52semanas. Hubo una reducción significativa tanto de la HbA1c (aproximadamente 0,5%) como del peso (pérdida en torno a 6-8kg) en cada uno de los grupos.
En otro estudio observacional posterior se evaluaron las diferencias en condiciones de vida real de efectividad de diferentes AR-GLP-1 (exenatida SC diario, lixisenatida SC diario, liraglutida SC diario, dulaglutida SC semanal)26. En dicho estudio se analizaron todas las prescripciones realizadas entre 2009 y 2016 de AR-GLP-1 con una muestra total de 735 y un seguimiento de 39meses. Durante dicho estudio se produjo un número muy pequeño de cambios de tratamiento entre AR-GLP-1 (n=47, 6,39%), siendo la mayoría de estos cambios de exenatida a liraglutida (n=24, 22% del total de cambios).
En otro estudio retrospectivo, realizado en nuestro medio con una población más grande (n=4.242), a partir de una muestra de pacientes con DM2 de centros de salud de Cataluña que iniciaron tratamiento con AR-GPL-1 (lisixenatida, exenatida y liraglutida), entre 2007 y 2014, se analizaron los cambios en peso y HbA1c tras 6 y 12meses de tratamiento. Se registró un descenso medio de HbA1c de −1% y una pérdida media ponderal de 3,6kg, resultados similares a los observados en ensayos clínicos aleatorizados27.
En 2021 se inició el estudio SWITCH-SEMA1, publicándose los resultados en 2023. Se trata de un estudio multicéntrico, prospectivo, aleatorizado y ciego, en el que el objetivo principal es comparar los efectos de semaglutida con los de liraglutida y dulaglutida. Se seleccionaron 100 pacientes con DM2 que estaban en tratamiento con liraglutida (grupoA) de 0,9 a 1,8mg/día o dulaglutida (grupoB) 0,75mg/semanal más de 12semanas y que tenían una HbA1c de entre el 6 y el 9,9% y un IMC ≥ 22kg/m2. Se asignaron al azar a continuar con su AR-GLP-1 o cambiar a semaglutida subcutánea semanal durante 24semanas.
Los niveles de HbA1c se redujeron de forma significativa en ambos grupos. En el grupoA: 7,8%±1,0% a 7,8%±0,7% (liraglutida) vs. 7,9%±0,7% a 7,3%±0,7% (semaglutida). En el grupoB: 7,8%±1,0% a 7,9%±1,2% (dulaglutida) vs. 7,8%±0,8% a 7,1%±0,6% (semaglutida).
Por lo tanto, si bien difiere en muchos puntos en cuanto al diseño con respecto a nuestro estudio, apoya los resultados28.
Por lo tanto, revisando los estudios publicados hasta la fecha, hay un número limitado de estudios comparativos entre AR-GLP-1, y son aún menos aquellos que analizan los efectos del cambio entre ellos. Además, entre los estudios que han evaluado los efectos del cambio entre AR-GLP-1, la mayoría partían de un tratamiento inicial con AR-GLP-1 de administración diaria. En este sentido, nuestro estudio es el único que aporta datos en vida real comparando los dos AR-GLP-1 de mayor eficacia y administración semanal.
Los estudios en vida real son necesarios para confirmar que los resultados obtenidos en los ensayos clínicos, que se realizan con criterios de inclusión muy estrictos, a menudo no incluyen la variedad de pacientes con DM2 y obesidad seguidos en la práctica clínica diaria. Si se comparan nuestros datos con los del SUSTAIN-7, los resultados son muy similares. En el SUSTAIN-7 se observó una reducción adicional de HbA1c de un −0,41% (IC95%: −0,57% a −0,25%; p<0,0001) y ponderal de −3,55kg (IC95%: −4,32kg a −2,78kg; p<0,0001) en comparación con dulaglutida 1,5mg13. En nuestro estudio se observó una reducción adicional en los niveles de HbA1c a los 6, 12, 18 y 24meses: −0,43% (p=0,000), −0,54% (p=0,000), −0,38% (p=0,021) y −0,12% (p=0,622), respectivamente, y una reducción de peso adicional y de mayor magnitud a los 6, 12, 18 y 24meses: −2,7kg (p=0,000), −3,7kg (p=0,000), −5,4kg (p=0,001) y −4,2kg (p=0,000), respectivamente. Cabe destacar que en el SUSTAIN-7 los datos son a un seguimiento de 9meses, y en nuestro estudio se realizó el análisis a los 6, 12, 18 y 24meses (contando con una muestra más reducida en los últimos meses de seguimiento, lo que pudo haber afectado a la significación estadística de dichos resultados).
En nuestro trabajo, tras el análisis del objetivo principal, se realizó un análisis por subgrupos con el fin de determinar si había diferencias en función del motivo del cambio en disminución de HbA1c y en la pérdida ponderal entre los diferentes grupos. Se establecieron dichos grupos en función de cuál había sido la razón que había motivado el cambio de dulaglutida a semaglutida: en el grupo1, aquellos en los que se buscaba una reducción adicional de HbA1c (G1, 82,31%); en el grupo2, aquellos cuyo objetivo era una mayor pérdida de peso (G2, 7,96%), y en el grupo3, los pacientes que no habían tolerado bien el tratamiento previo con dulaglutida (G3, 9,73%).
Al realizar el análisis por subgrupos en función del motivo del cambio observamos un descenso superior de HbA1c y mayor pérdida ponderal, al menos numéricamente, cuando el cambio se había realizado buscando mayor pérdida ponderal (G2). Sin embargo, estas diferencias no alcanzaron significación estadística (p=0,38 y p=0,52 a los 6meses y p=0,49 y p=1 a los 12meses), probablemente debido al número de pacientes incluidos en la muestra (tabla 4).
Respecto a los efectos adversos, en contraposición a lo observado en el SUSTAIN-7, en nuestro estudio el cambio de dulaglutida a semaglutida no se asoció con un incremento significativo en la incidencia de efectos adversos gastrointestinales, observándose incluso más eventos con el tratamiento previo con dulaglutida. Este hecho podría explicarse porque uno de los motivos por los que se realizaba el cambio de AR-GLP-1 fue la intolerancia previa o la baja adherencia al tratamiento con dulaglutida.
Este estudio presenta algunas limitaciones, que se comentan a continuación. Se trata de un estudio retrospectivo y fue realizado en un único centro. Otra limitación adicional fue el reducido número de pacientes incluidos, al analizarse únicamente aquellos que realizaron el cambio de dulaglutida a semaglutida. Esta circunstancia, a priori, tuvo un impacto en el número pacientes que potencialmente podrían haber sido incluidos en el estudio. Por otra parte, muchos de los pacientes que iniciaron tratamiento con semaglutida SC no se pudieron incluir en nuestro estudio al estar tratados previamente con otro AR-GLP-1 (diario o semanal) o por iniciar el tratamiento con AR-GLP-1 por primera vez.
En resumen, los resultados de este estudio sugieren que el cambio de dulaglutida SC semanal a semaglutida SC semanal puede ser recomendable, con independencia del motivo del cambio. Estos resultados confirman una mayor reducción de la HbA1c y del peso, algo deseable en las personas con DM2 y obesidad. Sin embargo, se precisan más estudios, con mayor número de pacientes, que confirmen y refuercen los resultados de este estudio. Los estudios en condiciones de vida real son relevantes y deben confirmar la eficacia y la seguridad de los nuevos fármacos de los estudios clínicos en faseII-III en el contexto de la práctica clínica habitual.
ConclusionesEl estudio SEMA-SWITCH demostró que la transición de dulaglutida SC semanal a semaglutida SC semanal se asocia con una reducción adicional tanto en los niveles de HbA1c como del peso corporal, sin cambios significativos en la incidencia de efectos adversos. Además, estos beneficios ocurrieron con independencia del motivo del cambio por eficacia insuficiente, necesidad de mayor reducción de peso o previa intolerancia previa a dulaglutida SC semanal. Estos hallazgos confirman el cambio entre AR-GLP-1 como una buena opción terapéutica cuando el tratamiento previo tenga una eficacia menor de la esperada o existan efectos adversos que condicionen su uso.
FinanciaciónPara este trabajo no se ha contado con financiación externa.
Conflicto de interesesLos autores Felipe Pardo Lozano, Arantxa Rubio Marcos, Rosa Casañ Fernandez, Amparo Bartual Rodrigo y Francisco Javier Ampudia-Blasco han participado en ponencias sobre fármacos para el tratamiento de la diabetes y para la pérdida ponderal en la obesidad. El doctor Sergio Martinez-Hervas no ha colaborado con ningún laboratorio que tenga productos para el tratamiento de la obesidad.