En el año 2010 el Grupo de Trabajo de Consensos y Guías Clínicas de la Sociedad Española de Diabetes (SED) publicó un consenso sobre tratamiento farmacológico en la diabetes tipo 2, que fue aprobado por diferentes sociedades científicas1. El grupo de trabajo ha considerado que sería de utilidad publicar un documento de consenso que abordara específicamente la insulinoterapia en la diabetes tipo 2.
Este documento es el resumen ejecutivo de un documento más amplio aprobado por las juntas directivas de la SED y la Sociedad Española de Endocrinología y Nutrición. La versión completa puede encontrase en la web de ambas sociedades (http://www.seen.es; http://www.sediabetes.org), así como en el de las restantes sociedades que se han adherido al mismo.
Criterios de insulinización y de retirada de la insulinaCuándo y cómo insulinizarInicio del tratamiento con insulinaLa insulinización puede hacerse en el momento del diagnóstico o en el seguimiento2.
- –
Al inicio de la enfermedad, si aparece pérdida de peso, cetonuria intensa o síntomas cardinales de diabetes, especialmente con HbA1c>9%.
- –
Durante el seguimiento puede ser necesaria la insulinización transitoria o permanente.
Existen varias opciones de inicio de insulinización:
- –
Insulina basal. Una o 2 dosis de insulina NPH, o una dosis de análogo basal: glargina, detemir y degludec.
- –
Insulina prandial. Se realiza con 3 dosis de insulina rápida o análogo ultrarrápido antes de las comidas.
- –
Mezclas de insulinas. Dos o más dosis de mezclas fijas de insulina rápida o ultrarrápida con insulina intermedia.
La primera opción es en la actualidad la de elección3–5. En pacientes asintomáticos se puede optar por una dosis de insulina basal antes de acostarse de 10U o 0,2U/kg en obesos (tabla 1). El ajuste de dosis se realiza en función de las glucemias basales cada 3 días (tabla 1). La titulación puede ser realizada también por el paciente, debidamente instruido.
Insulinización basal
| Ajuste fármacos no insulínicos: |
|---|
| Continuar con la misma dosis: metformina iDPP4, AR-GLP1 y/o iSGLT2 |
| Valorar suspender o reducir sulfonilureas, glinidas y pioglitazona |
| Comenzar con 10U o 0,2U/kg |
| NPH o detemir antes de acostarse |
| Glargina a cualquier hora |
| Degludec a cualquier hora |
| Ajustar la dosis de insulina según la GB |
| Aumentar la dosis de insulina cada 3 días (siempre que no haya hipoglucemias): |
| En 2U cuando durante 3 días seguidos se superen las cifras objetivo |
| En 4U cuando glucemias basales >180mg/dl |
| Disminuir la dosis de insulina cada 3-5 días |
| En 2U cuando 2-3 días consecutivos la GB es menor de un límite establecido preestablecido (en general 70-90mg/dl) |
| En hipoglucemias disminuir dosis 4U o 10% de la dosis de insulina basal |
GB: glucemia basal.
Si en 3-4 meses no se consiguen los objetivos glucémicos con insulinas basales a una dosis mayor de 0,5U/kg, habría que plantearse la intensificación terapéutica.
En pacientes muy sintomáticos, con marcada hiperglucemia basal (>280-300mg/dl) o cetonuria, puede requerir 2 dosis de insulina basal, una pauta bifásica o un tratamiento basal-bolo.
Suspension del tratamiento con insulina en pacientes con diabetes tipo 2En algunos pacientes es posible suspenderla y/o sustituirla por otros antidiabéticos. Algunas variables pueden predecir la eficacia de la sustitución de la insulina por otros antidiabéticos: a) Insulinización durante un ingreso hospitalario o proceso intercurrente con control glucémico previo adecuado con antidiabéticos no insulínicos; b) Insulinización desde el inicio con buen control mantenido desde entonces; c) Control adecuado con dosis no demasiado elevadas (<0,5U/kg/día) y duración de la diabetes <10 años, y d) Pacientes sometidos a cirugía bariátrica.
Las reducción será progresiva, por ejemplo 4U por semana. Finalmente, la decisión debe tomarse de acuerdo con el paciente. Si se produce una descompensación hiperglucémica, debemos reinstaurar la insulina. En caso de enfermedad intercurrente puede volver a necesitarla.
Pautas de insulinizaciónInsulina basalLa tabla 2 muestra las insulinas disponibles. Las basales intentan simular el patrón basal, para mantener al paciente cerca de la normoglucemia en ayunas.
Clasificación y presentación de las insulinas en España (diciembre 2017)
| Producto | Nombre comercial | Presentación |
|---|---|---|
| Acción ultrarrápida (inicio de acción: <15min; duración habitual: 3-5h) | ||
| Lispro | Humalog® KwikPen® | 5 plumas precargadas de 3ml |
| Humalog® vial | Vial de 10ml | |
| Humalog® 200 KwikPen® | 5 plumas precargada de 3ml | |
| Aspart | NovoRapid® FlexPen | 5 plumas precargadas de 3ml |
| NovoRapid® vial | Vial de 10ml | |
| NovoRapid® Penfill® | 5 cartuchos de 3ml | |
| NovoRapid® PumpCart® | 5 cartuchos de 1,6ml | |
| Glulisina | Apidra® SoloStar® | 5 plumas precargadas de 3ml |
| Apidra cartucho JuniorStar® | 5 cartuchos de 3ml | |
| Apidra® solución inyectable | Vial de 10ml | |
| Acción rápida (inicio de acción: 30min; duración habitual: 6-8h) | ||
| Regular | Actrapid® InnoLet® | 5 plumas precargadas de 3ml |
| Actrapid® vial | Vial de 10ml | |
| Humulina regular® | Vial de 10ml | |
| Acción intermedia (inicio de acción: 1h; duración habitual 12-18h) | ||
| NPH | Insulatard® FlexPen® | 5 plumas precargadas de 3ml |
| Insulatard® vial | Vial de 10ml | |
| Humulina® NPH KwikPen® | 6 plumas precargadas de 3ml | |
| Humulina® NPH vial | Vial de 10ml | |
| Insulina detemir | Levemir® FlexPen® | 5 plumas precargadas de 3ml |
| Levemir® InnoLet® | 5 plumas precargadas de 3ml | |
| Acción prolongada/lenta (inicio de acción: 1h; duración habitual ≥22-26h) | ||
| Glargina | Lantus® SoloStar® | 5 plumas precargadas de 3ml |
| Lantus® cartuchos JuniorStar® | 5 plumas precargadas de 3ml | |
| Lantus® vial | Vial de 10ml | |
| Glargina U-300 | Toujeo® SoloStar® | 3 plumas precargadas de 1,5ml |
| Glargina (biosimilar) | Abasaglar® KwikPen | 5 plumas precargadas de 3ml |
| Degludec | Tresiba® Flex Touch® | 5 plumas precargadas de 3ml |
| Todas las insulinas se presentan en concentraciones de 100U/ml excepto Humalog KiwkPen 200U que se presenta en una concentración de 200U/ml y Toujeo Solostar que se presenta en concentración de 300U/ml. Las jeringas habituales de insulina están preparadas para concentraciones de 100U/ml por lo que la extracción de insulina de estas plumas aumentaría la dosis por 3 o por 2 con riesgo de hipoglucemia. | ||
| La insulina Lantus de 100U/ml y Abasaglar (biosimilar) no son intercambiables. Deben prescribirse por marca. | ||
| Combinaciones premezcladas | ||
| Regular 30%+NPH 70% | Humulina® 30:70 KwikPen® | 6 plumas precargadas de 3ml |
| Mixtard® 30 InnoLet® | 5 plumas precargadas de 3ml | |
| Humulina® 30:70 vial | Vial de 10ml | |
| Mixtard® 30 vial | Vial de 10ml | |
| Lispro 25%+ | ||
| lisproprotamina 75% | Humalog® Mix 25™ KiwkPen® | 5 plumas de 3ml |
| Lispro 50%+ | ||
| lisproprotamina 50% | Humalog® Mix 50™ KwikPen® | 5 plumas precargadas de 3ml |
| Aspart 30%+ | ||
| aspart-protamina 70% | NovoMix® 30 FlexPen® | 5 plumas precargadas de 3ml |
| Aspart 50%+ | ||
| aspart-protamina 50% | NovoMix® 50 FlexPen® | 5 plumas precargadas de 3ml |
| Aspart 70%+ | ||
| aspart-protamina 30% | NovoMix® 70 FlexPen® | 5 plumas precargadas de 3ml |
- –
Insulina NPH. Presenta un pico de acción máxima entre las 4 y 6h y su duración efectiva es de 12h. Se puede administrar en una o 2 dosis, en combinación con fármacos orales. Puede usarse en el embarazo.
- –
Insulina detemir es un análogo soluble de insulina. La duración de acción depende de la dosis: 12h para dosis de 0,2U/kg y 20h para dosis de 0,4U/kg. En un tercio de los pacientes será preciso administrar 2 dosis para cubrir las 24h.
- –
Insulina glargina U-100 es un análogo con inicio de acción más lento que la NPH, con un perfil de acción más suave, sin picos y presenta una duración de acción de hasta 18-24h. Debe administrarse una vez al día, todos los días a la misma hora.
- –
Insulina glargina biosimilar. Las fichas técnicas de glargina U-100 y glargina biosimilar 100U/ml son casi superponibles.
- –
Insulina glargina U-300. Formulación de glargina con concentración de 300U/ml. Tiene un perfil farmacodinámico y farmacocinético más plano y prolongado que glargina U-100, menor riesgo de hipoglucemias6–8 y similar reducción de HbA1c en los pacientes con diabetes tipo 29. En los ensayos clínicos se necesitó de media una dosis basal 10-18% más alta con glargina U-300.
- –
Insulina degludec es un análogo con una duración de acción mayor de 42h con una variabilidad intrapaciente 4 veces menor que glargina U-100, con la misma eficacia pero menos hipoglucemias nocturnas. Se aconseja su administración diaria, y permite una alta flexibilidad en su administración, con períodos entre dosis de 8 a 40h. Como insulina de inicio no está financiada en España.
Todas las basales presentan la misma eficacia10,11, pero hay diferencias en el riesgo de hipoglucemias, especialmente nocturnas. La elección se basará en el perfil del paciente, en términos de seguridad y coste del tratamiento.
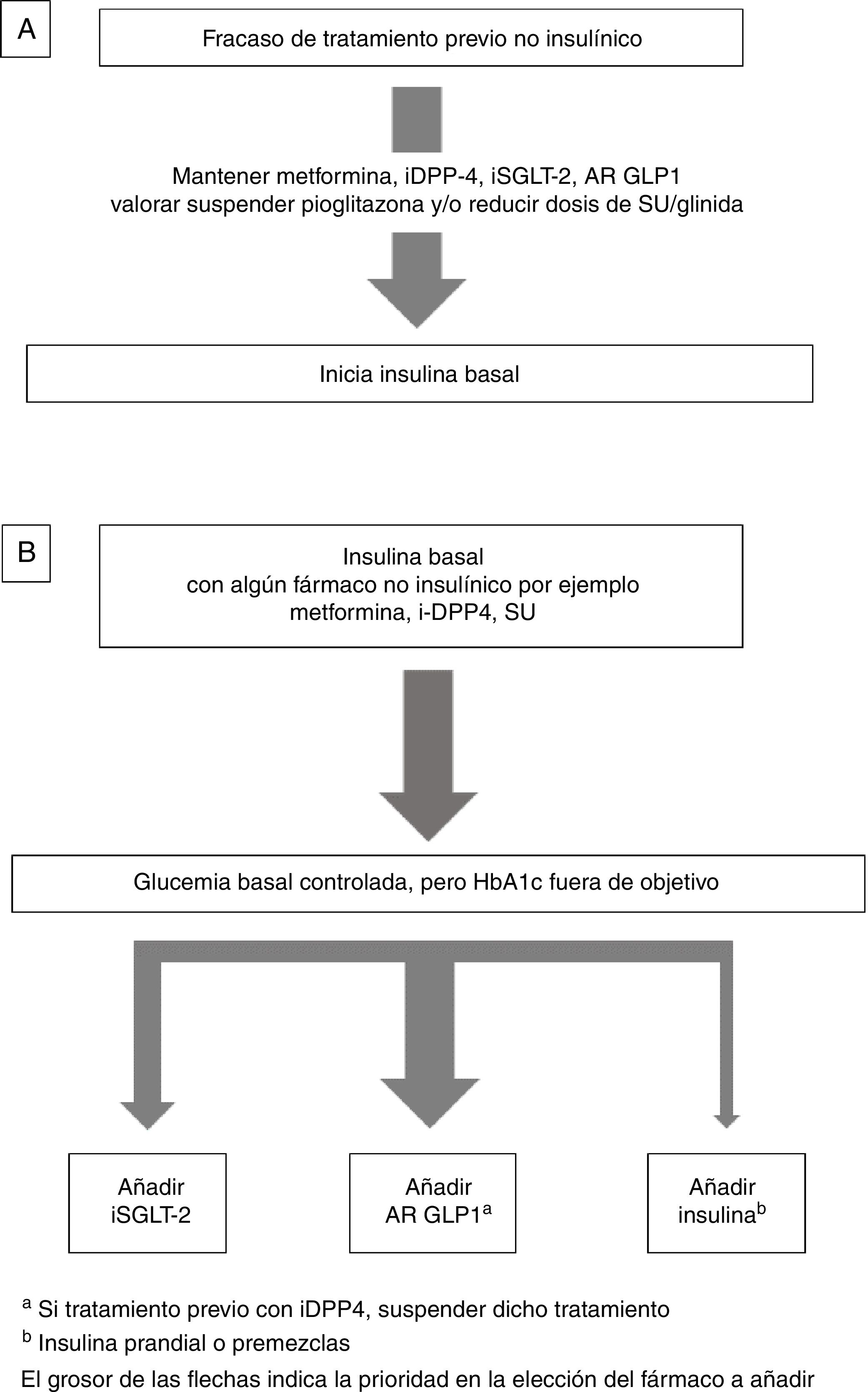
Insulina combinada con fármacos no insulínicosEn general, la insulinización basal es la de elección tras el fracaso de los fármacos no insulínicos4,12. Respecto a qué fármacos pueden usarse en combinación con la insulina basal, consideraremos 2 posibilidades (fig. 1):
Se recomienda mantener metformina, inhibidores de DPP4 (iDPP-4), agonistas del receptor de GLP1 (AR-GLP1) y/o inhibidores de SGLT-2 (iSGLT-2) si ya los estaba recibiendo, y valorar suspender pioglitazona. En el caso de suspender las sulfonilureas (SU) puede haber un empeoramiento inicial de la glucemia. En caso de mantenerlas se aconseja reducir su dosis por el riesgo de hipoglucemia12 (fig. 1A).
Intensificación de la insulina basal ¿Qué fármacos no insulínicos usar?Los pacientes suelen llevar ya algún antidiabético oral, en general metformina con o sin SU o iDPP-4, En las últimas guías4,12 se aconseja añadir un AR-GLP1 o un iSGLT-2 como alternativa a la adición de nuevas inyecciones de insulina.
Basal plusConsiste en la adición progresiva de dosis de insulina (o análogo) prandial, comenzando con aquella ingesta que mayor repercusión tenga en la glucemia posprandial, manteniendo la insulina basal. Se pueden mantener los fármacos no insulínicos, aunque es preferible suspender las SU por el incremento del riesgo de hipoglucemia13–15.
Antes de iniciar la insulina prandial, debe haberse conseguido una glucemia basal dentro del objetivo. Posteriormente, si la HbA1c está elevada se añadirá la insulina (o análogo) rápida.
En cuanto a la dosis de inicio, la tabla 3 (material suplementario) muestra 4 opciones13–15. Posteriormente habrá que ajustar las dosis (en general cada 1 o 2 semanas), hasta conseguir un objetivo glucémico posprandial personalizado. La tabla 4 (material suplementario) muestra varias posibilidades.
Una vez conseguido el objetivo posprandial, si la HbA1c no está en el objetivo, habrá que añadir otra dosis de insulina prandial en otra ingesta.
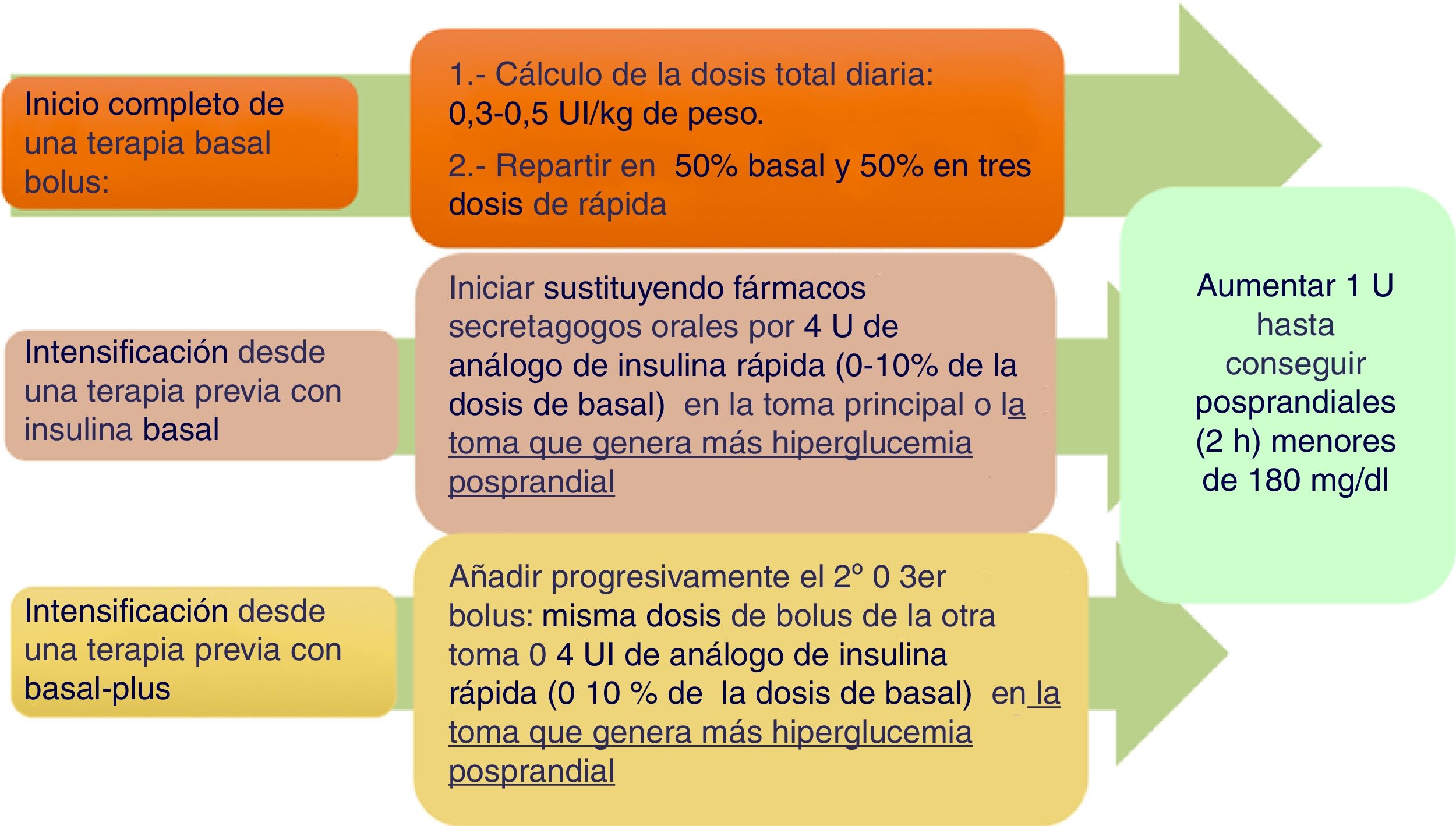
Basal boloCuando en la diabetes tipo 2 el tratamiento con insulina basal o con insulinas premezcladas no se alcanza el objetivo de control, las guías de práctica clínica recomiendan añadir insulina rápida antes de las comidas4. Los metaanálisis no han confirmado una mayor potencia hipoglucemiante, pero sí menor tasa de hipoglucemias que otras pautas16–18. Un algoritmo práctico de inicio y ajuste se describe en la figura 2.
Recomendaciones prácticas:
Cálculo de la dosis de los bolos. Se han propuesto distintos sistemas (tabla 3 del material suplementario). Nuestro grupo de trabajo considera más prudentes las 2 primeras16.
Inicio en paciente que usa insulina basal/NPH. Conviene cambiar a un análogo basal, y reducir un 20% la dosis de insulina lenta previa si el control estaba cercano al objetivo o hay alto riesgo para hipoglucemia19.
Inicio en paciente que usa insulina premezclada. Administrar el 50% como insulina lenta y el otro 50% en 3 inyecciones de insulina rápida antes de las comidas principales. Dependiendo del control previo, puede ser recomendable reducir un 20% la dosis total19.
Recomendaciones para el ajuste de la insulina. Comenzar por intentar controlar las glucemias preprandiales con la insulina basal/lenta y, posteriormente, las posprandiales con la rápida. Se han propuesto distintos sistemas (tabla 4 del material suplementario)15.
Plan nutricional al inicio de insulina. En el caso de basal-plus o basal-bolus la dieta puede ser más flexible en cuanto a horarios. Puede adaptarse el momento de la inyección de los bolos a la hora real de inicio de las tomas y, también, pueden ajustarse las dosis de la insulina rápida a la composición de cada toma16.
Insulinas premezcladasIntroducciónLas insulinas premezcladas consisten en una combinación fija de una insulina intermedia con insulina regular o con un análogo rápido20,21. Tradicionalmente se administran 2 veces al día, antes de desayuno y cena, si bien pueden administrarse en las 3 comidas principales. Puede plantearse en pacientes que parten de niveles elevados de HbA1c (≥9%) previos o en los que ya se ha optimizado la dosis de basal y se requiere control prandial22,23. Las características de las insulinas premezcladas frente a la insulina basal sola y al régimen bolo-basal se presentan en la tabla 5.
Características de la insulinización con premezclas frente a insulina basal sola y al régimen basal-bolo
| Basal (NPH/análogo basal glargina o detemir) | Basal-bolo | Premezclas | |
|---|---|---|---|
| HbA1c | ↓↓ (30-50% HbA1c≤7%) | ↓↓↓↓ | ↓↓↓a |
| Control de la glucosa en ayunas | Mejor | Mejor | Peor |
| Control de la glucosa posprandial | Peor | Mejor | Mejor |
| Complejidad | Bajaa | Alta | Moderada |
| Dosis de insulina (kg) | + | +++ | ++ |
| Hipoglucemia | + | ++ | ++ |
| Aumento de peso | + | ++ | ++ |
| Complicaciones diabetes | ¿? | ↓¿? | ¿? |
Para iniciar la insulinización con insulina premezclada una de las estrategias más utilizadas es el uso de la premezcla al 25 o 30% administrada antes del desayuno y cena. Puede comenzarse con 10U antes de dichas comidas o bien calcular la dosis a partir del peso (0,3U/kg/día) y repartirla un 50-60% antes del desayuno y 40-50% antes de la cena.
Se recomienda la realización de al menos 3 glucemias capilares diarias. Incluirán tanto pre como posprandiales. Además, se recomiendan perfiles de 6 puntos ocasionales. La tabla 6 (material suplementario) muestra un modo de ajuste de dosis22.
Transferencia de una pauta a otra de insulinaCambios de dosis entre insulinas basalesDe NPH a glargina (original o biosimilar)
Si reciben una inyección diaria, sustituir el 100% de la dosis de NPH y luego ajustar.
Si pasamos de 2 inyecciones de NPH a una dosis de glargina, reducir un 20-30%24–26.
De NPH a detemir
Mantener la misma dosis.
Insulinas o análogos basales a degludec
Cuando la basal se administre una vez al día, puede hacerse unidad a unidad. Cuando se cambie de una insulina basal administrado 2 veces al día se debe reducir la dosis un 20%27.
Insulina glargina 100U/ml (original o biosimilar) a glargina 300U/ml, y viceversa
Es aconsejable hacerlo unidad a unidad, aunque posteriormente pueden ser necesarias dosis de glargina 300U/ml un 10-18% más altas26. Cuando se cambia de glargina 300U/ml a glargina 100U/ml, la dosis debe reducirse aproximadamente un 20%.
Cambio de otras insulinas basales a glargina 300U/ml
Será unidad a unidad si la basal que se va a sustituir por glargina 300U/ml se estaba administrando en una dosis diaria. Si se estaba administrando en 2 o más dosis, la dosis inicial de glargina 300U/ml será del 80% de la dosis de la basal previa.
Cambio de una dosis de insulina basal a 2 dosis de insulina premezcladaEn general se mantendrá la dosis total, repartiendo 2/3 en el momento que ya se la estaba inyectando el paciente y 1/3 a las 12h y ajustar las dosis subiéndolas progresivamente en función de los resultados del autoanálisis. Si se sospecha hipoglucemia, reducir la dosis total un 10-20% de la dosis total de insulina.
Cambio de 2 dosis de premezcla a bolo-basal con glargina, detemir o degludecDisminuir la dosis total previa de la fracción NPH de la mezcla en el 20-30%, que se administrará como análogo lento. Repartir la dosis de insulina rápida o ultrarrápida en las 3 comidas y ajustar posteriormente.
Cambio de insulina basal a bolo-basalHabitualmente se suele comenzar por la pauta basal plus, o bien añadir insulina prandial en las 3 ingestas principales26,27.
Situaciones clínicas específicasInsulinización en el paciente con diabetes tipo 2 y enfermedad renal crónicaEn la enfermedad renal crónica el riesgo de hipoglucemia grave es el doble28–32. En general se recomienda un control glucémico menos intensivo salvo que se usen fármacos sin riesgo de hipoglucemia23.
El régimen de insulinoterapia se adaptará a los objetivos de control. En general se recomienda el uso de análogos basales y rápidos.
Terapia insulínica en la hiperglucemia inducida por glucocorticoidesEl perfil glucémico característico es un predominio de glucemias posprandiales sobre las preprandiales y de vespertina sobre la matutina (especialmente con esteroides de vida media intermedia en dosis única en el desayuno)33–36.
La insulina suele ser el tratamiento de elección por razones de eficacia y seguridad. En los pacientes con glucocorticoides de acción intermedia en monodosis matutina y sin tratamiento previo con insulina se puede iniciar insulina NPH o bifásica antes del desayuno, manteniendo los ADNIs (tabla 7 del material suplementario)33.
En general se recomiendan reducciones de la insulina proporcionales a la reducción de la dosis de corticoides. La tabla 8 del material suplementario resume las recomendaciones en caso de pacientes ya tratados con insulina previamente.
Diabetes en el paciente oncolo¿gico en situacio¿n terminalUno de los objetivos prioritarios en estos pacientes es evitar la hipoglucemia. En caso de optar por tratamiento insulínico es recomendable el empleo de dosis única de una insulina basal, preferiblemente un análogo de acción prolongada. Si se usan corticoides, la insulina basal puede no ser suficiente.
Barreras a la insulinización en diabetes tipo 2El origen de las barreras puede estar en el paciente o sus familiares, en los profesionales sanitarios o en el sistema sanitario37. Las actuaciones para resolver esas barreras actuarán sobre estos factores.
Educación terapéutica asociada a la insulinizaciónLos objetivos de la educación terapéutica (ETD) son4:
- a.
Conocer los miedos sobre la terapia.
- b.
Plantear el momento adecuado para comenzar el aprendizaje.
- c.
Conocer el tipo de insulina que se va a administrar.
- d.
Consensuar los objetivos de control glucémicos.
- e.
Aprender la técnica de inyección, zona de administración y absorción, rotación, material para inyección, conservación de la insulina, etc.
- f.
Educar en la prevención y el tratamiento de la hipoglucemia leve y grave.
- g.
Manejar la relación de la insulina con hidratos de carbono, actividad física, perfiles, días especiales y enfermedades intercurrentes.
Podemos considerar varios niveles educativos: supervivencia, básico y avanzado. La educación se individualizará:
- •
Si únicamente lleva insulina basal o insulina premezclada 2 veces al día, podrá ser suficiente con un programa educativo de supervivencia y si sus expectativas son de mayor demanda, ETD básica.
- •
Si lleva una pauta basal plus, deberá realizar un programa de supervivencia y valorar el beneficio de que realice ETD básica
- •
Si lleva insulina basal más insulina rápida, deberá realizar un programa educativo de supervivencia, valorar el beneficio de que realice ETD básica y si sus expectativas son de mayor demanda, ETD avanzada.
El Documento de Consenso completo está disponible en: http://www.seen.es y http://www.sediabetes.org, y como material adicional en la página web de la revista.