Editado por: Dr. Calos Cerdán
Cirugía General y Aparato Digestivo. Unidad de Cirugía Digestiva. Hospital Universitario de la Princesa. Madrid
Dr. Matteo Frasson
Cirugía general. Hospital Universitario y Politécnico La Fe. Valencia
Última actualización: Septiembre 2025
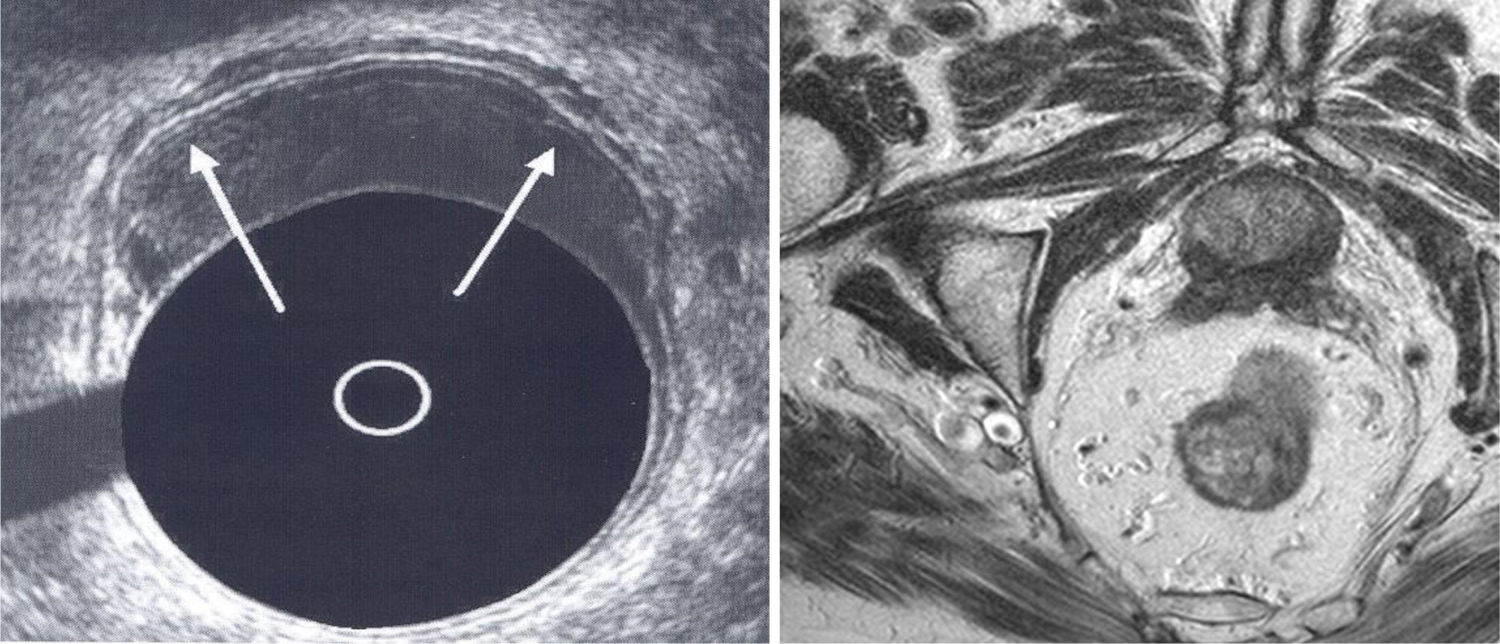
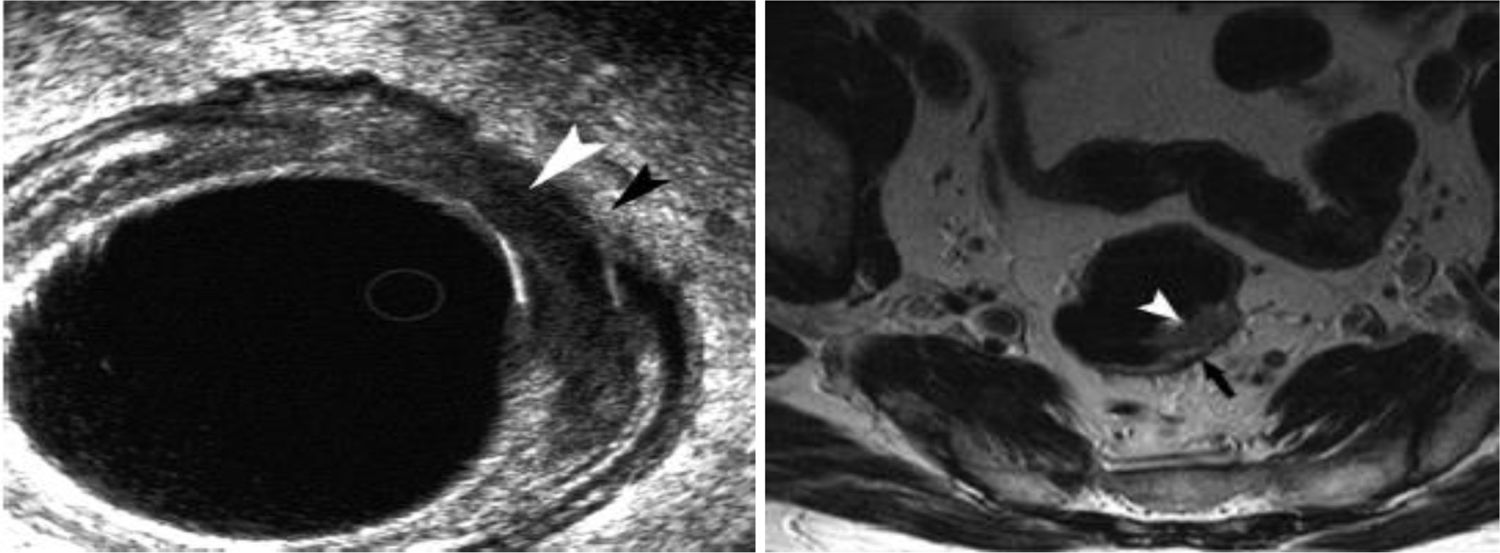
Más datosLa resección local (RL) en el cáncer de recto está indicada en el estadio T1N0M0 sin factores de riesgo anatomopatológicos, que con técnicas de cirugía endoscópica transanal obtiene resultados oncológicamente satisfactorios. Sin embargo, el primer paso es una correcta estadificación y selección de estos tumores mediante pruebas específicas realizadas en las unidades especializadas en colorrectales.
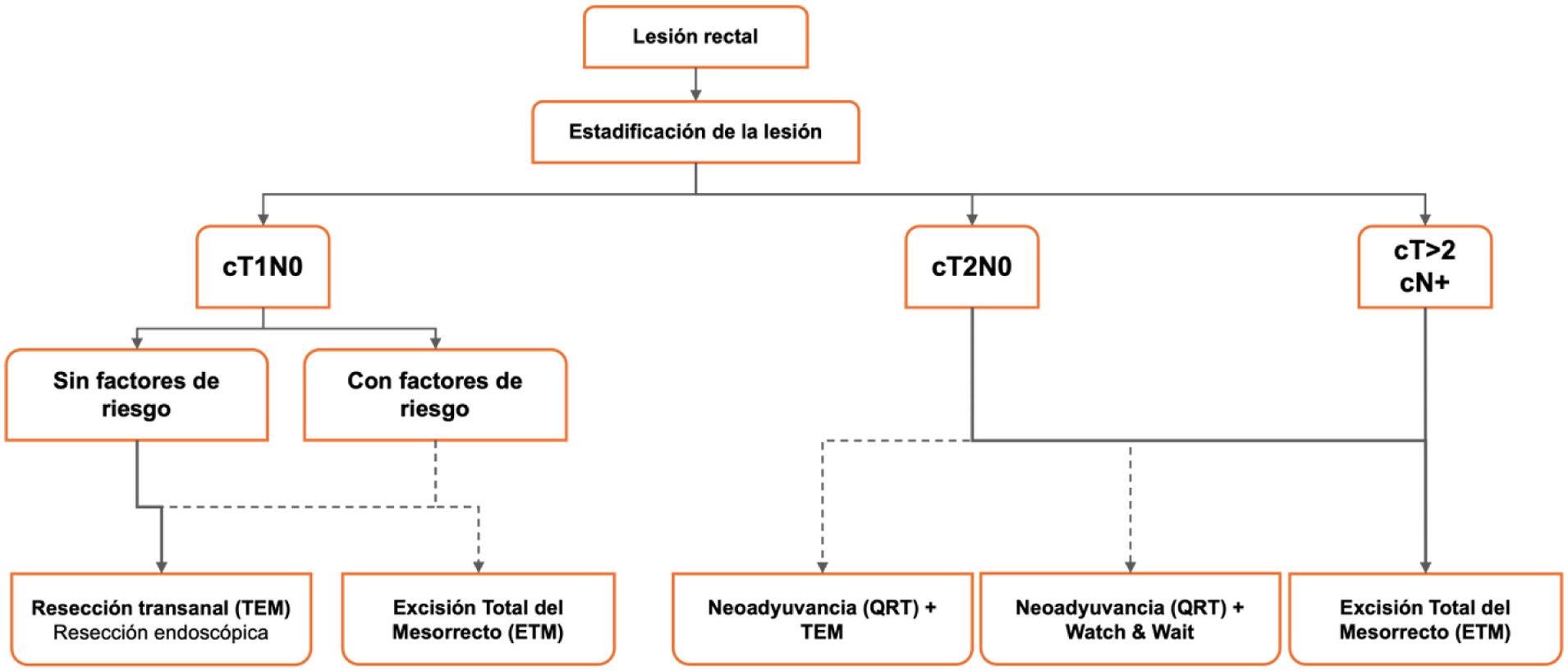
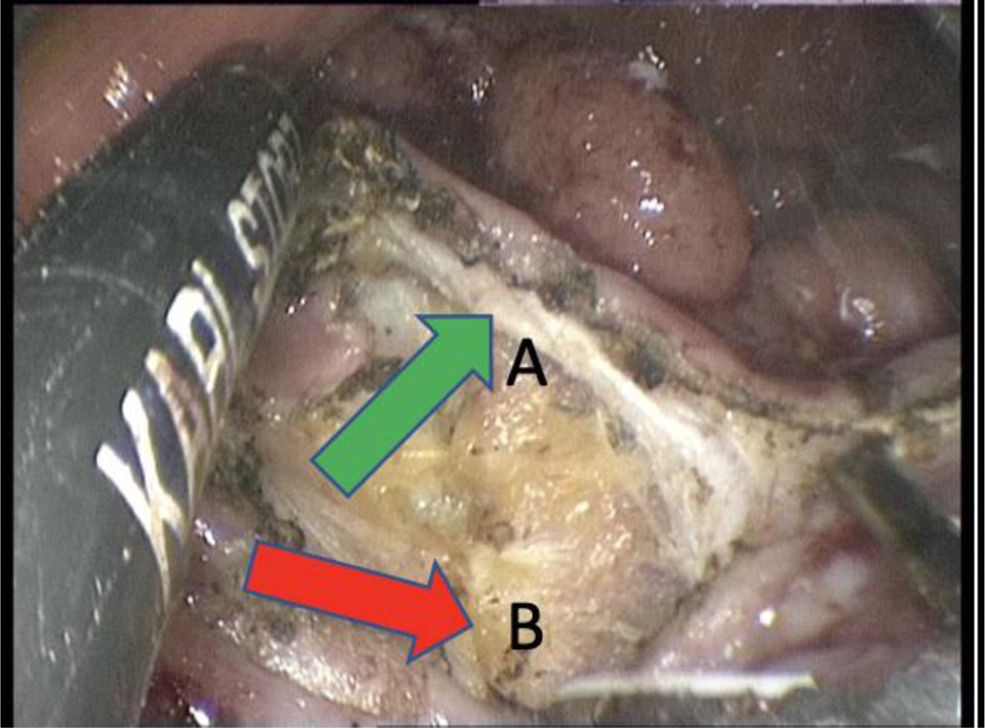
En los tumores T2N0M0 y T1 con factores de mal pronóstico, el tratamiento estándar es la escisión total del mesorrecto (ETM), procedimiento que se asocia a una elevada morbimortalidad postoperatoria, alteraciones funcionales y de calidad de vida. Por ello, nuevas estrategias de preservación de recto se encuentran actualmente como alternativa a la ETM. Entre ellas se incluyen la neoadyuvancia asociada a la RL con resultados esperanzadores y la neoadyuvancia seguida de la selección de los pacientes con respuesta clínica completa y seguimiento estricto, denominada «Watch and Wait», como tratamiento futuro idóneo, pero con cuestiones actuales a resolver.
Local resection (LR) in rectal cancer is indicated in stage T1N0M0 without unfavorable pathological factors, achieving oncologically satisfactory outcomes through transanal endoscopic surgery techniques. However, the initial step involves accurate staging and selection of these tumors through specific tests conducted in specialized colorectal units.
For T2N0M0 tumors and T1 tumors with poor prognostic factors, the standard treatment is total mesorectal excision (TME), a procedure associated with high postoperative morbidity and mortality, functional impairments, and reduced quality of life. Therefore, new organ-preservation strategies are being explored as alternatives to TME. These include neoadjuvant therapy combined with LR, which has shown promising results, and neoadjuvant therapy followed by a “Watch and Wait” approach —where patients with complete clinical response are selected for strict surveillance— as an ideal future treatment, although there are still current challenges to be addressed.