La nefropatía C1q, se describió por primera vez en 1985, como un proceso de glomerulonefritis con depósito mesangial de C1q, histológicamente similar a la nefritis lúpica, siendo inicialmente descrita como lupus renal seronegativo, sin embargo, estas dos entidades se consideran actualmente como procesos patológicos diferentes. Su asociación con artritis reumatoide es inusual y la literatura no reporta casos con presentación similar. A continuación, presentamos el caso de un hombre que desarrolla estas dos entidades.
C1q nephropathy was first described in 1985 as a process of glomerulonephritis with mesangial C1q deposit. The histology is similar to lupus nephritis, and was initially described as being seronegative renal lupus. However, these two entities are now considered different pathological processes. Its association with rheumatoid arthritis is unusual, and there are no cases with a similar presentation reported in the literature. In this article, the the case is presented of a man who developed both these conditions.
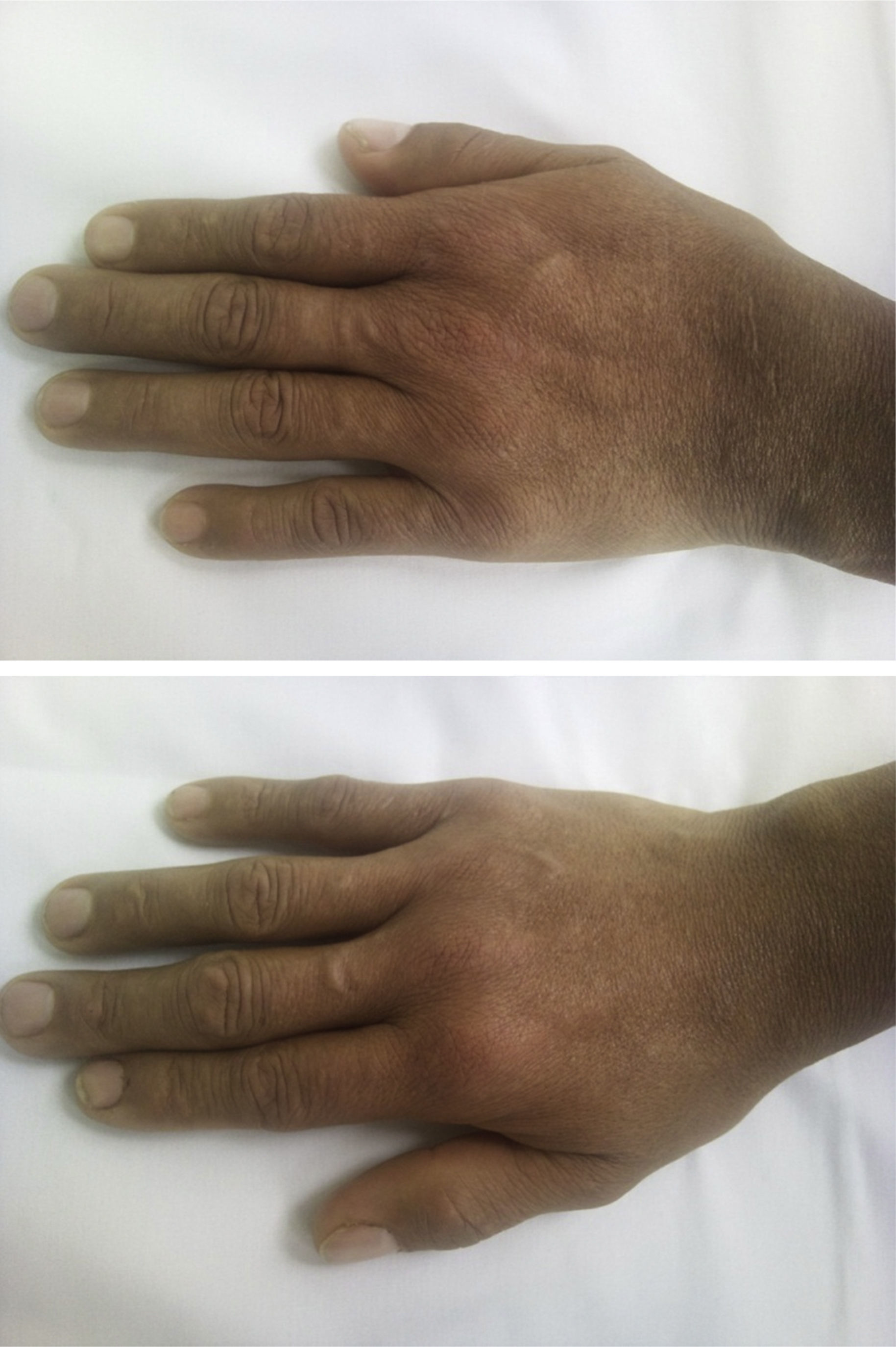
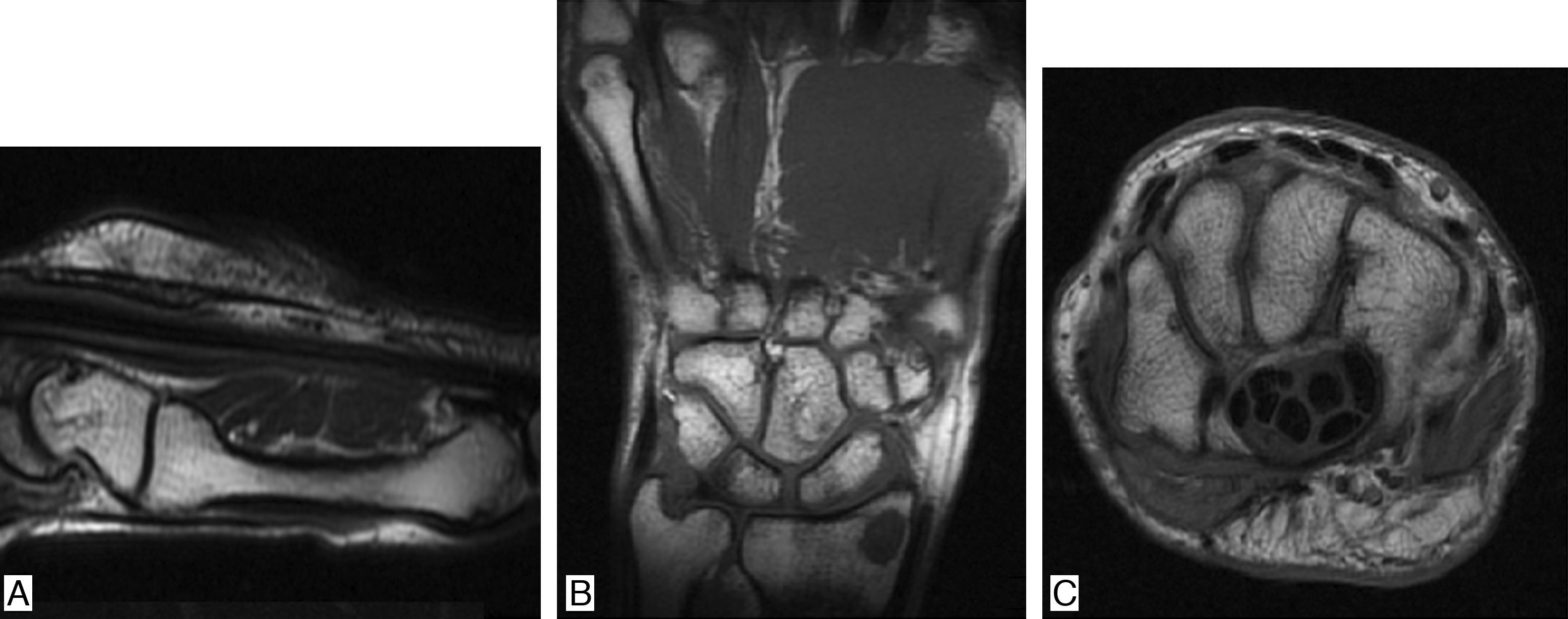
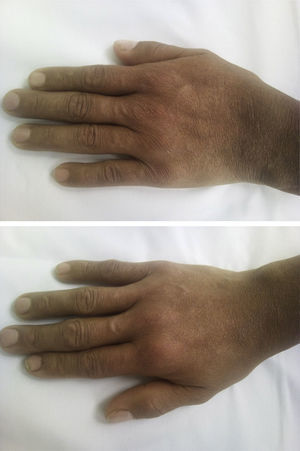
Se trata de un hombre de 38 años quien en el año 2011 cursó con síndrome nefrótico e hipertensión arterial, siendo llevado a biopsia renal, documentándose nefropatía C1q. Recibió tratamiento con 6 bolos mensuales de ciclofosfamida y posteriormente se pasó a azatioprina, presentando intolerancia gastrointestinal a este último medicamento por lo que se cambió a micofenolato, con adecuado control de nefropatía. Se descartó lupus eritematoso sistémico (LES), pues el paciente no presentaba estigmas clínicos de esta enfermedad y los estudios inmunológicos eran normales (ANAS, ENAS y anti-DNA negativos, complemento normal, anticoagulante lúpico, anticardiolipinas y B2 glicoproteína negativos). Tres años después del inicio de la nefropatía, presenta artralgias de manos de características inflamatorias, asociando episodios de sinovitis y rigidez matinal de 40 min. Al examen físico presenta sinovitis y dolor en 10 articulaciones (IFP 2 a 5 bilateral y muñecas) (fig. 1). Se toman datos de laboratorios encontrando: VSG 67mm/h, PCR 25,7mg/dl (normal entre 0-1mg/d), antipéptido cíclico citrulinado (anti-CCP) positivo en título alto (98,9mg/dl, valor normal hasta 20mg/d), factor reumatoide positivo alto (89,7mg/dl, valor normal hasta 14) mg/d. Dado el antecedente de la nefropatía y la instauración de un cuadro de artropatía inflamatoria se ampliaron estudios para descartar LES. Se tomaron muestras para ANAS, ENAS, anti-DNA, anticuerpos anticardiolipinas IgG e IgG, anticuerpos antibeta 2 glicoproteína IgG e IgM y VDRL, todos con resultados negativos, así como con complemento normal. La resonancia magnética nuclear mostró en la mano derecha erosiones corticales en todos los huesos del carpo y radio distal así como de cabeza de 2.do, 3.er y 5.o metacarpianos, con incipiente sinovitis en articulaciones metacarpofalángicas del 1.er, 2.o, 3.er y 4.o dedos. En mano izquierda con cambios inflamatorios leves sinoviales periarticulares del carpo con leve engrosamiento de la sinovial periarticular tanto dorsal como ventral, con sinovitis incipiente en metacarpofalángica generalizada (fig. 2). Dado que no había ningún hallazgo clínico o paraclínico que sugiriera la presencia de LES y ante la presencia de reactantes de fase aguda, anti-CCP y factor reumatoide positivos altos, se hizo diagnóstico de artritis reumatoide (AR), decidiéndose optimizar su manejo inmunomodulador con metotrexate 15mg cada semana, con lo que el paciente presenta adecuado control de su sintomatología articular y entra en remisión clínica de AR.
La nefropatía C1q es una enfermedad glomerular de baja frecuencia de presentación, que se caracteriza por presentar proteinuria (desde proteinuria leve hasta proteinuria en rango nefrótico) con mala respuesta a la administración de glucocorticoides, con etiología desconocida y hallazgos histopatológicos determinados por el gran componente inmune que la caracteriza. Fue descrita por primera vez por Jennette y Hipp en 1985, quienes publicaron una revisión detallada del patrón de tinción de inmunofluorescencia en 800 biopsias renales consecutivas, encontrándose C1q en 36% de las biopsias, con una intensidad de fluorescencia media de 1,6+en una escala de 6 puntos (0,0 - 4+). La intensidad y el patrón de tinción C1q en combinación con microscopia de inmunofluorescencia estándar y el análisis ultraestructural detallado, identificaron un subconjunto de pacientes que se denominó nefropatía C1q. Por definición el cien por cien de estos pacientes tenía tinción C1q con una intensidad de fluorescencia media de 3,6+ en un patrón predominantemente mesangial, con tinción granular dispersa en algunas asas capilares1.
Este tipo de nefropatía cursa con un patrón de glomerulonefritis caracterizado por depósitos predominantes de C1q mesangial, pero con un patrón histológico que recuerda la nefritis lúpica. La característica inmunopatológica distintiva es la inmunotinción dominante o codominante para C1q con depósitos electrodensos mesangiales, sin evidencia clínica o paraclínica de LES2. La literatura reporta una prevalencia muy variable con valores que oscilan entre 0,2–16%3.
Los primeros reportes de la nefropatía C1q se dieron en biopsias renales de pacientes con diagnóstico de LES, en quienes la única manifestación de compromiso lúpico era renal, pero con la característica de ser serológicamente negativos y, por ende, sin cumplir con los criterios de clasificación para LES, denominándose, en ese entonces, «lupus seronegativo». Los hallazgos en las biopsias renales en estos primeros casos demostraron la presencia de depósitos de C1q dominantes o codominantes, en especial, en mesangio, en el contexto clínico de pacientes sin otra manifestación de LES4. Posteriores estudios de correlación clínico–patológica evidenciaron en niños y adultos jóvenes con este tipo de daño renal, la presencia de proteinuria severa en rango nefrótico, con muy pobre respuesta al manejo con glucocorticoides y alta tasa de recurrencia5,6.
C1q es una proteína crítica para la función de la vía clásica de activación del sistema del complemento. En los seres humanos las concentraciones séricas normales de C1q oscilan entre 100 a 180mg/l. Es una molécula biológicamente compleja con un peso molecular de aproximadamente 459kD y está integrada por 18 cadenas de polipéptidos: 6 cadenas A, 6 cadenas B y 6 cadenas C. Cada cadena es codificada por un gen separado localizado en el cromosoma 1 entre p36,3 y p34,17.
El espectro clínico de la enfermedad es amplio, con patrones histopatológicos que varían desde enfermedad de cambios mínimos, glomerulonefritis membrano-proliferativa, hasta glomeruloesclerosis focal y segmentaria, con presentaciones clínicas variadas, que comprenden hematuria asociada a proteinuria que puede ser leve hasta rango nefrótico8.
El compromiso renal de la AR es relativamente frecuente, con una prevalencia entre 5 a 50% en las diferentes series9. Los trastornos más comunes son: nefropatía membranosa, amiloidosis secundaria, glomerulonefritis focal proliferativa mesangial, vasculitis reumatoide y nefropatía por analgésicos10. En el estudio histopatológico de nuestro caso predomina el patrón de compromiso membranoso sin presencia de amiloidosis y sin ninguna otra comorbilidad asociada. La nefropatía membranosa se asocia a tratamiento con D-penicilamina o sales de oro. La incidencia descrita es del 1% con D-penicilamina y del 1 al 3% con oro parenteral con desarrollo de proteinuria, generalmente, en los primeros 6 a 12 meses de tratamiento11. La suspensión del tratamiento genera lenta resolución de la proteinuria en aproximadamente 9 a 12 meses, debido a la ubicación subepitelial de los depósitos inmunes que limita el acceso de las células fagocíticas11,12.
La inflamación crónica en AR determina un aumento de producción de fase aguda de proteína amiloide A sérica. Un fragmento de proteína de amiloide sérica se deposita generando síndrome nefrótico. En la actualidad, es poco frecuente por la efectividad terapéutica en el control de la inflamación que determina, además, resolución de los depósitos y la proteinuria en los pacientes que la presentan13. Helin et al., describen glomerulonefritis proliferativa mensangial como hallazgo en 40 de 110 pacientes con AR, que fueron sometidos a biopsia, los cuales suelen presentarse con hematuria con o sin proteinuria10, pero estos casos, a diferencia del que presentamos, son de pacientes que tienen antecedente de AR y posteriormente presentan el compromiso renal. Dentro de los hallazgos que pueden documentarse en pacientes con AR que sugieren compromiso renal se destaca la proteinuria con o sin hematuria, por lo tanto, la detección de la enfermedad renal no debe solo incluir la medición de creatinina sino métodos sensibles para detectar proteinuria glomerular y tubular14. La microalbuminuria se puede utilizar como una simple y sensible prueba para detectar la disfunción renal subclínica en pacientes con daño renal inducido por AR15. Estas correlaciones entre clínica y laboratorios no son absolutas y no excluyen la necesidad de la biopsia renal, en algunos casos seleccionados, para establecer un diagnóstico.
Nuestro paciente presenta cuadro de artralgia inflamatoria simétrica en manos, asociado a rigidez matutina con elevación de reactantes de fase aguda, anti-CCP y factor reumatoide, todos positivos en títulos altos y con presencia de erosiones en manos, por lo que se considera cursa con AR en el contexto de un paciente con antecedente de nefropatía C1q. Al revisar la literatura no encontramos, a la fecha, el reporte de casos clínicos similares.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.