Determinar la presencia de fracturas vertebrales morfométricas y su relación con 25 OH vitamina D, índice de masa corporal y edad en mujeres seniles.
Materiales y métodosEstudio transversal. Se analizaron 319 mujeres seniles, provenientes del estudio «Salud osteomuscular del anciano». La determinación de fracturas vertebrales morfométricas se realizó de manera radiográfica, en tanto que los niveles de 25 OH vitamina D se midieron por inmunoanálisis por quimioluminiscencia (CLIA) Liaison® 25 OH vitamina D Total Assay Ref 310600, utilizando el equipo Diasorin Liaison® Analyzer. El índice de masa corporal se obtuvo, según las recomendaciones de la Organización Mundial de la Salud, como el peso en kilogramos sobre la talla en metros al cuadrado; la edad fue verificada con el documento de identidad y el ingreso del mismo a las bases de datos nacionales (SISPRO-FOSYGA).
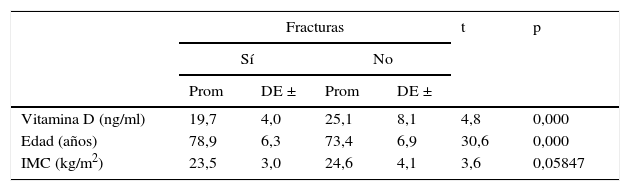
ResultadosEl promedio de edad fue de 74,3 años (DE ±7,2). La prevalencia global de fracturas fue de 17,9%; así mismo, el 54,9% de las participantes tenía valores entre 20 y 29ng/ml de 25 OH vitamina D y el 58,9% tenía valores de índice de masa corporal inferior a 25kg/m2. El promedio de 25 OH vitamina D fue inferior en las participantes fracturadas (19,7 vs. 25,1) (p<0,05); el índice de masa corporal también fue menor en las fracturadas (23,5 vs. 24,6) (p>0,05), pero la edad fue mayor: 78,9 vs. 73,4 (p<0,05). Al comparar los promedios de 25 OH vitamina D en participantes fracturadas y no fracturadas, se encontraron niveles significativamente menores de 25 OH vitamina D en las participantes con fractura mayores de 69 años, y al considerar el índice de masa corporal, los valores de 25 OH vitamina D fueron significativamente inferiores en cada una de las categorías de las participantes con fractura.
ConclusiónSe encontró una relación estadísticamente significativa entre poseer fracturas vertebrales morfométricas y tener: 1) niveles bajos de 25 OH vitamina D, 2) mayor edad, y 3) menor índice de masa corporal.
To determine the presence of morphometric vertebral fractures, as well as their relationship with 25 OH vitamin D, body mass index, and age in elderly women.
Materials and methodsA cross-sectional study was conducted on 319 elderly women from the study ‘Musculoskeletal Health in the Elderly’. The morphometric determination of vertebral fractures was performed with radiography, while the levels of 25 OH vitamin D were determined by the chemiluminescent immunoassay (CLIA) method using the Liaison® 25 OH Vitamin D Total Assay 25 (Ref 310 600), using the Liaison® Analyser. The body mass index was obtained as recommended by the World Health Organisation; weight in kilograms over height in metres squared. The age of the participants was verified by their identity card, and their income details from the national data bases (SISPRO-FOSYGA).
ResultsThe mean age was 74.3 years (SD ±7.2). The overall prevalence of fractures was 17.9%; 54.9% of participants had values between 20 and 29ng/ml 25 OH vitamin D, and 58.9% had body mass index values less than 25kg/m2. The mean 25 OH vitamin D was lower in participants with fractures (19.7 vs. 25.1) (P<.05). Body mass index was also lower in those with fractures (23.5 vs. 24.6) (P<.05), but age was higher: 78.9 vs. 73.4 (P<.05). When comparing the mean levels of 25 OH vitamin D in fractured and non-fractured participants, significantly lower levels of 25 OH vitamin D were found in participants with fractures over 69 years-old, and on comparing the body mass index, the values of 25 OH vitamin D were significantly lower in each of the categories of participants with a fracture.
ConclusionA statistically significant relationship was found between morphometric vertebral fractures and: 1) low levels of 25 OH vitamin D, 2) being older and, and 3) a lower body mass index.
Las fracturas vertebrales (FV) son una consecuencia grave de la osteoporosis y, a menudo, suelen ser subdiagnosticadas debido a la presentación clínica variable y a la ausencia de una prueba reina para su definición1. Según Pasco et al.2, alrededor del 75% de las FV no son diagnosticadas clínicamente debido a la ausencia de síntomas específicos. Una de las grandes preocupaciones es que las FV son predictoras de futuras fracturas osteoporóticas3 y se asocian con detrimentos en la calidad de vida4 y aumento de la mortalidad5.
Los niveles de vitamina D disminuidos se han relacionado con aumentos en la incidencia de fracturas, principalmente de cadera6. Se sabe que el 80% de la vitamina D circulante en sangre es obtenida a partir de la exposición al sol7, por lo que, una baja exposición al sol, sea cual sea la razón, es factor de riesgo para padecer hipovitaminosis D. Estudios en Europa determinaron que un 75% de las personas en instituciones geriátricas tienen niveles séricos de vitamina D menores de 10ng/ml8. Esto quiere decir que esta población, al ser privada del sol por sus limitaciones físicas y en el caso de las mujeres, haber pasado por la menopausia, tiene mayor riesgo de sufrir fracturas a causa de la fragilidad de sus huesos.
El otro 20% de la vitamina es debida a la nutrición. Una nutrición rica en vitamina D (huevo, leche, pescados, algunos aceites) es un factor protector. Esto ha quedado demostrado en diferentes estudios realizados en países con un alto consumo de pescado, como Japón, Noruega y Holanda, los cuales mostraron índices menores de hipovitaminosis D en comparación con países vecinos9-11. En Estados Unidos, una evaluación llevada a cabo en 20.289 personas en el National Health And Nutrition Evaluation Survey (NHANES III) mostró que, a medida que avanzaba la edad, la prevalencia de hipovitaminosis D era más marcada, y el 77% de las mujeres mayores de 70 años tenía valores menores de 30ng/ml12. Este resultado es alarmante pues la población geriátrica tiene índices más altos de morbimortalidad a causa de la osteoporosis. Al año, un 30% de las personas mayores de 65 años sufren caídas desde su propia altura, y esta proporción aumenta al 40-50% en personas mayores de 80 años13.
En un estudio realizado en Chile, en 2007, en una población de mujeres menopáusicas, se encontró osteoporosis densitométrica (scoreT más bajo que –2,5) en un 35%. El 31,9% de las pacientes tenía osteoporosis en la columna lumbar, el 14,1% en el cuello femoral y el 10,7% tenía osteoporosis en ambos sitios14, mientras que otro estudio demostró que el 47,5% de las pacientes (entre 55 y 84 años) tenía hipovitaminosis D, mediante el uso de un nivel límite de 17ng/ml15.
En Brasil, en el distrito de Oporto16, el valor promedio de 25 OH vitamina D3 fue de 25,6ng/ml; el 26,2% de los individuos tenía niveles >30ng/ml, el 45,2% presentó insuficiencia (con valores de 20 a 29ng/ml), en el 23,8% de los casos hubo déficit (25 OH vitamina D3 entre 8-20ng/ml), y déficit grave (25 OH vitamina D3 <8ng/ml) en el 4,8% de los casos.
Por su parte, el estudio Lavos demostró una prevalencia general para FV, en mujeres mayores de 50 años, del 14,2%17. Sin embargo, una investigación hecha en Argentina demostró que la latitud influye en los niveles de vitamina D en sangre, encontrando que en el norte del país había niveles más altos de vitamina D que en el sur18, dando fuerza al hecho que, en las latitudes más cercanas al Ecuador, existe mayor radiación UV que, como ya se había mencionado, es necesaria para la absorción cutánea de la vitamina D.
La insuficiencia/deficiencia de vitamina D tiene un efecto negativo a nivel del hueso y músculo, observándose un mayor número de caídas con posteriores fracturas osteoporóticas. Esto ha quedado demostrado en estudios que indican que el uso de vitamina D disminuye en un 22% el riesgo de caídas19.
Se ha considerado que una dosis de vitamina D de 700-800UI disminuye el riesgo de sufrir fractura de cadera en un 26% y fracturas no vertebrales en un 23%19. En las mujeres posmenopáusicas esto es más grave20, ya que ellas pierden el efecto protector del estrógeno, lo cual es consecuente con que aproximadamente el 33% de las mujeres entre los 60-70 años de edad y el 66% de las mujeres mayores de 80 años tienen osteoporosis21,22.
Tradicionalmente, se mide solamente la masa mineral ósea en la cadera, pero esto puede no ser suficiente para identificar todos los pacientes con osteoporosis, ya que la pérdida ósea puede producirse principalmente en la columna vertebral23. En 2009, el estudio Lavos17 reveló una prevalencia general del 10,7% de FV en mujeres de 50 a 79 años, y en Colombia se encontró el índice más alto para mujeres de 70 a 79 años: el 22% de los participantes de este rango etario mostró evidencias radiológicas de FV.
Esto llama la atención ya que, si bien no ha sido declarado por las autoridades como un «problema de salud pública», se cree que un 47% de las mujeres mayores de 50 años van a sufrir una fractura osteoporótica en lo que les queda de vida24 y, en este orden de ideas, las fracturas osteoporóticas vertebrales cobran protagonismo, ya que por lo general 2/3 de ellas son silenciosas25,26.
Por lo tanto, teniendo en cuenta que no se han encontrado estudios a escala local, regional o nacional, que den cuenta de los niveles de vitamina D como marcador importante para estimar y evaluar la aparición de FV, surgió la necesidad de llevar a cabo el presente estudio.
Materiales y métodosSe llevó a cabo un estudio descriptivo y transversal. Se estudiaron 319 mujeres posmenopáusicas que acudieron al Centro de Reumatología y Ortopedia de la ciudad de Barranquilla, durante el período 2011-2014, participantes en el estudio «Salud osteomuscular del anciano».
Las edades fueron verificadas con el documento de identidad (fecha de nacimiento vs. fecha actual) y su ingreso en las bases de datos estatales abiertas al público: Fosyga y Sispro.
La muestra se obtuvo por conveniencia, teniendo en cuenta el total de potenciales participantes que cumplieran los criterios de selección. Al ingresar en el estudio, se les practicó a las participantes estudio radiográfico morfométrico, para la detección de fracturas, y muestra de sangre para determinar niveles de vitamina D.
Criterios de inclusión- -
Paciente orientado en tiempo, persona y lugar (examen físico).
- -
Edad ≥60 años
- -
Tener habilidad para desplazarse en bipedestación de forma independiente.
- -
Aprobación de participar en el estudio mediante firma del consentimiento informado.
- -
Enfermedad que impida seguir participando en la investigación: de tipo osteomuscular o mental.
- -
Afección metabólica conocida o antecedente de cáncer.
- -
Uso de medicamentos que pueden alterar la masa ósea: heparinas, anticoagulantes orales (warfarina), agentes inmunosupresores (ciclosporina y azatioprina), acetato de medroxiprogesterona, agonistas de la hormona liberadora de hormona luteinizante, tratamientos sustitutivos con hormona tiroidea, vitamina A y retinoides sintéticos y diuréticos y antirresortivos.
- -
Uso de medicamentos que pueden alterar los niveles de vitamina D: anticonvulsivos (fenobarbital, fenitoína, primidona y ácido valproico), colestiramina y colestipol, rifampicina, y corticosteroides.
Las variables estudiadas fueron:
- -
Edad: años cumplidos en el momento del estudio, verificados con la fecha de nacimiento del documento de identidad.
- -
Índice de masa corporal (IMC): peso en kg tomado con báscula electrónica calibrada, sobre talla en m2, medida con tallímetro calibrado.
- -
Presencia de FV: la valoración se realizó mediante estudio radiográfico morfométrico, analizada por un solo radiólogo, utilizando el método de Genant para la clasificación de las fracturas8.
- -
Valores de 25 OH vitamina D: a partir de una muestra de sangre, se midieron los niveles de vitamina D: metabolito 25 OH vitamina D total, mediante el método inmunoanálisis por quimioluminiscencia (CLIA) Liaison 25 OH vitamina D Total Assay Ref 310600, utilizando el equipo Diasorin Liaison® Analyzer. No se trabajaron puntos de corte (deficiente/insuficiente/adecuado) para vitamina D, sino que se tomaron los valores a nivel razón y a nivel intervalo en grupos decenales.
Las variables fueron analizadas a nivel univariado, mediante porcentajes y promedios en las variables cuantitativas: edad, IMC y vitamina D. Posteriormente, se determinó la existencia de diferencias estadísticamente significativas (p<0,05) en cuanto a las prevalencias de fracturas respecto a las categorías de edad, IMC y vitamina D, y los promedios de estas 3 variables según el tener o no FV (prueba t y valor de p). Finalmente, se compararon los promedios de vitamina D, según la edad y el IMC, de acuerdo con tener o no FV (prueba t y valor de p).
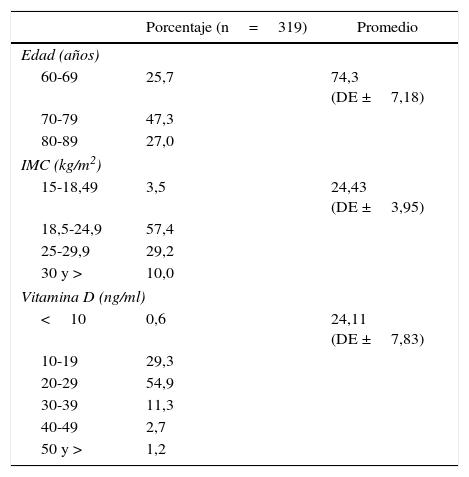
ResultadosEl promedio de edad fue de 74,3 años (DE ±7,18); la mayor proporción de participantes tenía entre 70 y 79 (47,3%). Alrededor del 39% tenía IMC >24,9kg/m2, es decir, tenía sobrepeso u obesidad.
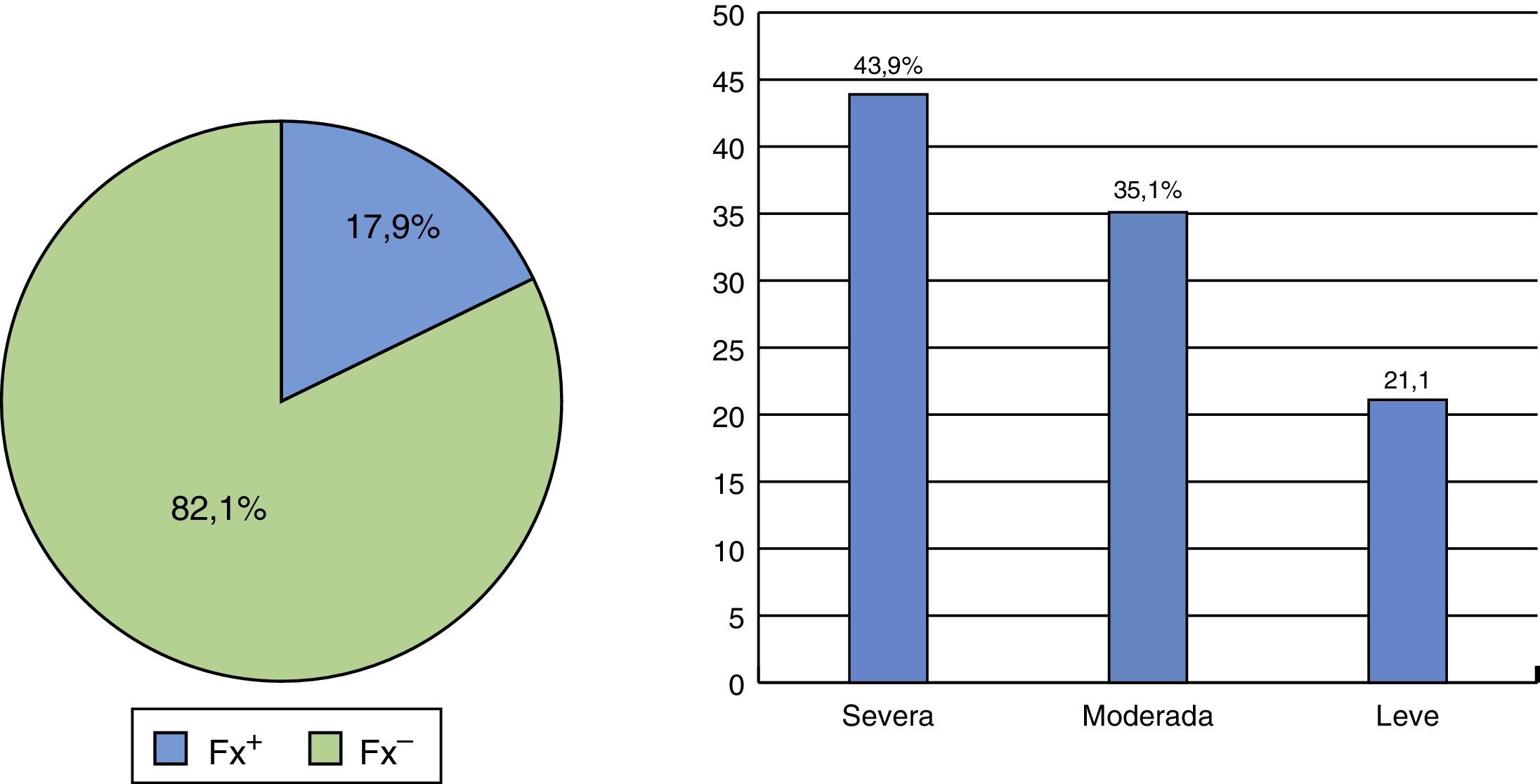
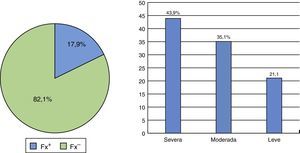
Con respecto a la vitamina D, el 54,9% de las participantes tenía valores entre 20 y 29ng/ml, con un promedio de 24,11 (DE ±7,83) (tabla 1), y la prevalencia global de fracturas en el grupo de estudio fue de 17,9% (43,9% de ellas eran severas, 35,1% moderadas y 21% leves) (fig. 1).
Distribución de frecuencia de participantes, según la edad y los valores del índice de masa corporal
| Porcentaje (n=319) | Promedio | |
|---|---|---|
| Edad (años) | ||
| 60-69 | 25,7 | 74,3 (DE ±7,18) |
| 70-79 | 47,3 | |
| 80-89 | 27,0 | |
| IMC (kg/m2) | ||
| 15-18,49 | 3,5 | 24,43 (DE ±3,95) |
| 18,5-24,9 | 57,4 | |
| 25-29,9 | 29,2 | |
| 30 y > | 10,0 | |
| Vitamina D (ng/ml) | ||
| <10 | 0,6 | 24,11 (DE ±7,83) |
| 10-19 | 29,3 | |
| 20-29 | 54,9 | |
| 30-39 | 11,3 | |
| 40-49 | 2,7 | |
| 50 y > | 1,2 | |
Fuente: elaboración propia.
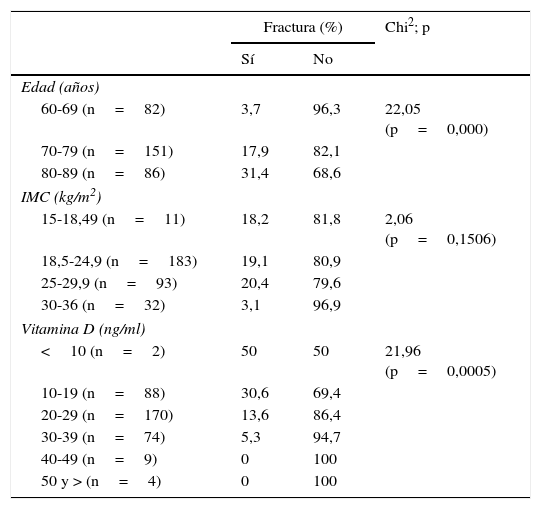
La prevalencia de fracturas fue mayor conforme se incrementó la edad, pasando de 3,7% en el grupo de 60 a 69 años, a 17,9% en el de 70 a 79, y a 31,4% en el de 80 a 89; al comparar el grupo de participantes con fracturas, con aquellos sin fractura, las diferencias en las proporciones fueron estadísticamente significativas (p<0,05) (tabla 2).
Prevalencia de fracturas según la edad, el IMC y los valores de vitamina D
| Fractura (%) | Chi2; p | ||
|---|---|---|---|
| Sí | No | ||
| Edad (años) | |||
| 60-69 (n=82) | 3,7 | 96,3 | 22,05 (p=0,000) |
| 70-79 (n=151) | 17,9 | 82,1 | |
| 80-89 (n=86) | 31,4 | 68,6 | |
| IMC (kg/m2) | |||
| 15-18,49 (n=11) | 18,2 | 81,8 | 2,06 (p=0,1506) |
| 18,5-24,9 (n=183) | 19,1 | 80,9 | |
| 25-29,9 (n=93) | 20,4 | 79,6 | |
| 30-36 (n=32) | 3,1 | 96,9 | |
| Vitamina D (ng/ml) | |||
| <10 (n=2) | 50 | 50 | 21,96 (p=0,0005) |
| 10-19 (n=88) | 30,6 | 69,4 | |
| 20-29 (n=170) | 13,6 | 86,4 | |
| 30-39 (n=74) | 5,3 | 94,7 | |
| 40-49 (n=9) | 0 | 100 | |
| 50 y > (n=4) | 0 | 100 | |
Fuente: elaboración propia.
En cuanto a los valores de IMC, las prevalencias de FV fueron similares: 18,1% en mujeres con IMC de 15 a 18,49kg/m2, 19,1% en el grupo de 18,5 a 24,9kg/m2, y 20,4% en las participantes con sobrepeso, mientras que en las mujeres con obesidad (IMC >29,9kg/m2), la prevalencia de FV fue mucho menor: 3,1%. Al comparar las 4 categorías de IMC según el tener o no FV, las diferencias no fueron estadísticamente significativas (p>0,05).
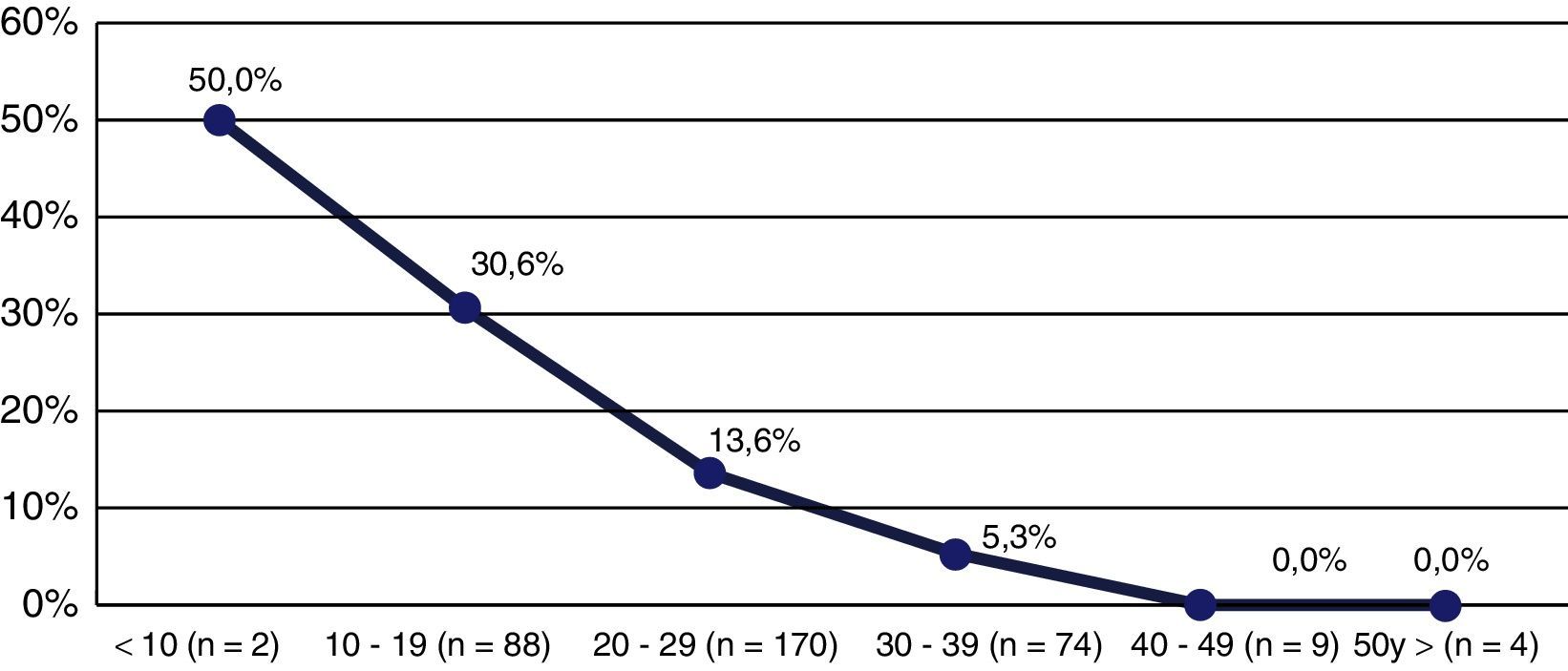
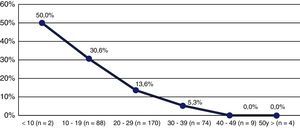
Al agrupar las participantes según los valores de vitamina D (en grupos decenales), en la categoría de <10ng/ml la prevalencia de FV fue del 50%, y en el grupo de 10 a 19ng/ml alrededor de 3 de cada 10 participantes tenían FV, mientras que en los demás grupos el porcentaje de participantes con FV fue decreciendo, hasta llegar al 0% en las mujeres con vitamina D >39ng/ml (fig. 2). De la misma forma, al comparar las categorías de vitamina D, según el tener o no fracturas, las diferencias resultaron estadísticamente significativas (p>0,05) (tabla 2).
Al comparar los promedios de vitamina D, según el hecho de tener o no FV, se encontraron diferencias estadísticamente significativas (p<0,05), con un promedio menor en las participantes con fractura: 19,7ng/ml, frente a aquellas sin fractura: 25,1ng/ml (tabla 3).
De la misma forma, el promedio de edad fue mayor en las participantes con fractura que en aquellas sin fractura, de manera significativa (p<0,05): 78,9 vs. 73,4 años (tabla 3), y el promedio de IMC fue similar entre las participantes con y sin fractura: 23,5kg/m2 y 24,6kg/m2, respectivamente (p>0,05) (tabla 3).
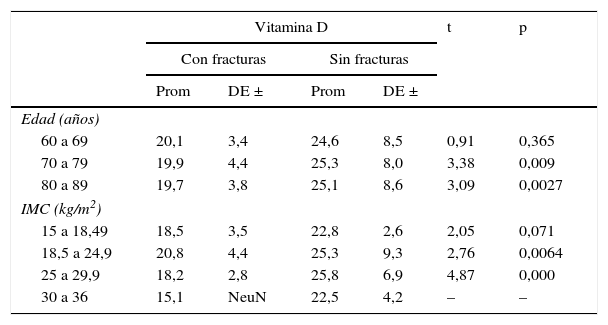
Al comparar los promedios de vitamina D en participantes fracturadas y no fracturadas, según cada uno de los grupos de edad, se encontró que en las mujeres de 60 a 69 años las diferencias no fueron significativas (p>0,05), pero sí fueron significativas en las mujeres de 70 a 79 y en las de 80 a 89 años (tabla 4).
Promedios de vitamina D, según la edad y el IMC, de acuerdo con tener o no fracturas vertebrales
| Vitamina D | t | p | ||||
|---|---|---|---|---|---|---|
| Con fracturas | Sin fracturas | |||||
| Prom | DE ± | Prom | DE ± | |||
| Edad (años) | ||||||
| 60 a 69 | 20,1 | 3,4 | 24,6 | 8,5 | 0,91 | 0,365 |
| 70 a 79 | 19,9 | 4,4 | 25,3 | 8,0 | 3,38 | 0,009 |
| 80 a 89 | 19,7 | 3,8 | 25,1 | 8,6 | 3,09 | 0,0027 |
| IMC (kg/m2) | ||||||
| 15 a 18,49 | 18,5 | 3,5 | 22,8 | 2,6 | 2,05 | 0,071 |
| 18,5 a 24,9 | 20,8 | 4,4 | 25,3 | 9,3 | 2,76 | 0,0064 |
| 25 a 29,9 | 18,2 | 2,8 | 25,8 | 6,9 | 4,87 | 0,000 |
| 30 a 36 | 15,1 | NeuN | 22,5 | 4,2 | – | – |
Fuente: elaboración propia.
En cuanto al IMC, el promedio de vitamina D fue significativamente menor (p<0,05) en las participantes con fractura frente a las no fracturadas, en los grupos de 18,5 a 24,9kg/m2 y de 25 a 29,9kg/m2 (tabla 4).
DiscusiónLa osteoporosis es una enfermedad metabólica que afecta a millones de personas en todo el mundo, y es el principal factor de riesgo para el desarrollo de fractura27. En Colombia, la prevalencia promedio de osteoporosis es del 57% en mayores de 40 años28, mientras que en la región Caribe colombiana, se ha documentado una prevalencia del 32,6% a partir de los 50 años29.
Dentro de las múltiples causas secundarias de osteoporosis, se encuentra la deficiencia de vitamina D, ya que esta interviene en el metabolismo óseo y puede contribuir a la patogénesis de la baja masa ósea y predisponer a fracturas por fragilidad, y en Colombia se han documentado altas tasas de insuficiencia o deficiencia de este componente: 71,7% en Medellín30 y 69,5% en Bogotá31. Así mismo, se ha encontrado de manera global que el 64% de las mujeres posmenopáusicas tiene hipovitaminosis D32,33.
En el presente estudio, más que indagar por la prevalencia de hipovitaminosis, se encontró que bajos niveles de vitamina D se encuentran relacionados con un aumento en la probabilidad de desarrollar FV, las cuales son un resultado grave y en muchos casos irreversible de la osteoporosis en adultos mayores y, una vez que se presentan, el riesgo de reaparición suele incrementarse34, demostrando la urgencia de identificación e intervención para este segmento de la población35. Por lo tanto, sería necesario hacer un seguimiento anual a la población de estudio, teniendo en cuenta el tiempo de aparición de la fractura.
Los resultados encontrados son similares a lo documentado por Molina et al.30, en cuyo estudio, luego de comparar los pacientes con niveles deficientes e insuficientes, se encontró que los pacientes con niveles de vitamina D deficientes constituían un factor de riesgo para la presencia de FV (RR: 1,02; IC 95%: 0,96-1,06); sin embargo, a diferencia del citado estudio, en el presente, los resultados sí fueron estadísticamente significativos (p<0,05).
Por otro lado, existen algunas limitaciones en el presente estudio, ya que no se conoce el tiempo exacto de aparición de las FV observadas. No obstante, por su aparición asintomática, en muchos casos es difícil determinar el tiempo de aparición de dicha fractura, sobre todo en los casos leves. Algunas podrían ser recientes y, en ese caso, la relación con los valores de vitamina D necesitaría ajustarse en función del tiempo. Sin embargo, se tiene a favor que otros estudios han demostrado que los efectos de las fracturas prevalentes son independientes de la masa ósea (relacionada directamente con los valores de vitamina D)36,37.
De la misma forma, es necesario llevar a cabo una valoración del IMC, teniendo en cuenta los parámetros de la Organización Mundial de la Salud para adultos mayores, pues, como es sabido, la depleción de la masa muscular en ellos puede inducir falsos positivos o falsos negativos, y esta variable podría estar correlacionada con la presencia de FV en la población de estudio, en función de la edad e interactuando con los niveles de vitamina D.
ConclusionesSe encontró una relación significativa entre los niveles de vitamina D bajos y la presencia de fracturas a nivel vertebral. Esta relación puede estar influenciada por la edad, no así con el IMC. Sin embargo, se requiere llevar a cabo estudios longitudinales para confirmar esta asociación. A pesar de ello, este es el paso preliminar que sienta un precedente importante a escala nacional.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónUniversidad Metropolitana de Barranquilla; Centro de Reumatología y Ortopedia.
Conflicto de interesesLos autores manifiestan expresamente, que no existe conflicto de intereses.