La epidermodisplasia verruciforme (EV) es una enfermedad de la piel autosómica recesiva, relacionada con la mutación EVER1 y EVER2, caracterizada por alta susceptibilidad a infecciones asociadas a ciertos tipos de papillomavirus humano llamadas EV-PVH. Los pacientes presentan lesiones verrucosas en la piel de características variadas y muchas veces asociadas a cáncer de piel no melanocítico, encontrándose una fuerte asociación con la mutación del gen EVER1 y EVER2. El caso que se presenta a continuación documenta linfopenia absoluta de CD4+ por lo que se plantea la hipótesis de una posible mutación del gen RHOH como etiología.
Epidermodysplasia verruciformis (EV) is an autosomal recessive disease of the skin commonly associated with EVER1 and EVER 2 mutations, and is characterised by high susceptibility to infections associated with certain types of human papillomavirus called EV-PVH. Patients have warty lesions on the skin of varying characteristics and are often associated with skin cancer, with a strong association being found with EVER1 and EVER2 mutation gene. The case presented below concerns an absolute CD4 + lymphopenia, and establishes the hypothesis of a possible mutation of the RHOH gene as its origin.
La epidermodisplasia verruciforme (EV) es una enfermedad autosómica recesiva de la piel con una prevalencia menor de uno por cada millón de habitantes, fue descrita inicialmente por Lewandowsky y Lutz en 1922. Se caracteriza por una alta susceptibilidad a infecciones asociadas a ciertos tipos de papillomavirus humano (PVH) llamadas EV-PVH, las cuales pueden no presentarse en la población general, dado que no se integran al genoma por ausencia del gen E51,2.
Aunque su patogénesis no está completamente definida, se sabe que la combinación de factores genéticos que llevan a una inmunodeficiencia selectiva, principalmente celular, son los causantes de la enfermedad3,4.
Los grupos de individuos donde más frecuentemente se describe esta condición son pacientes con infección por virus de inmunodeficiencia humana (VIH) o pacientes receptores de trasplante5,6. También están las formas primarias familiares por mutaciones autosómicas recesivas, mucho menos frecuentes3,7,8.
Los pacientes con EV-PVH tienen un riesgo aumentado para desarrollar cáncer de piel tipo no melanoma, especialmente en las áreas expuestas al sol, durante la segunda y tercera décadas de la vida, en especial los asociados a los serotipos 5 y 8 del PVH9,10.
En el grupo de pacientes con EV-PVH en su forma primaria, se describe la mutación de genes TMC (EVER 1 y 2) y más recientemente con mutaciones homocigotas del gen RHOH, que condicionan alteraciones en la señalización de los receptores de células T, lo que predispone a otras enfermedades infecciosas oportunistas como micobacterias, criptococos, Pneumocystis jirovecii (P. jirovecii), citomegalovirus, entre otros. Su presentación varía de acuerdo con los recuentos de CD47,8,11.
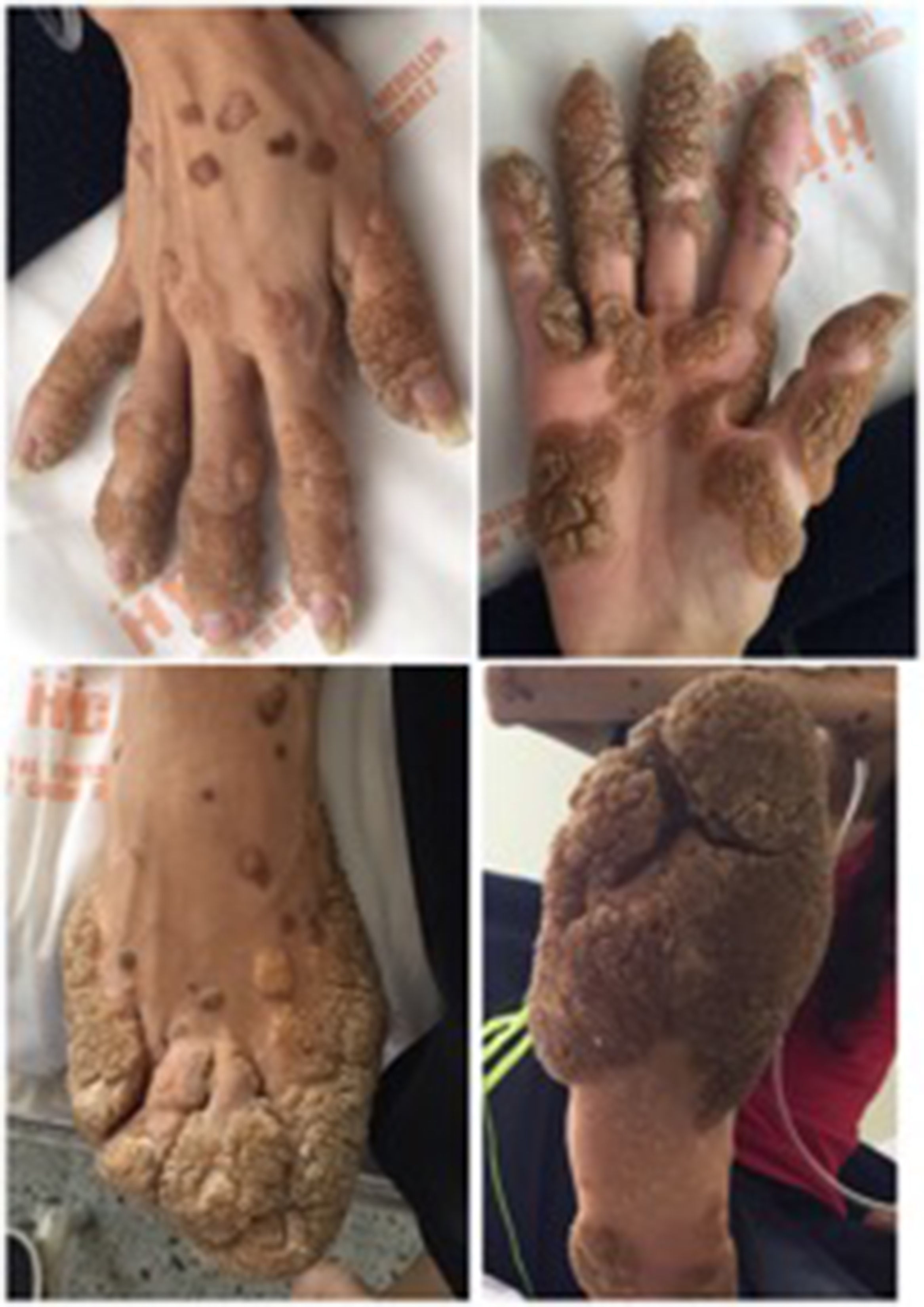
Caso clínicoMujer de 27 años, con antecedente de verrugas vulgares en dedos de manos y pies, enfermedad pulmonar definida como asma en la infancia, quien presentaba consultas a urgencias desde los 12 años por cuadros respiratorios infecciosos recurrentes (fig. 1). Como antecedente familiar importante, se registra la muerte de su hermano mayor por enfermedad pulmonar no diagnosticada a los 20 años.
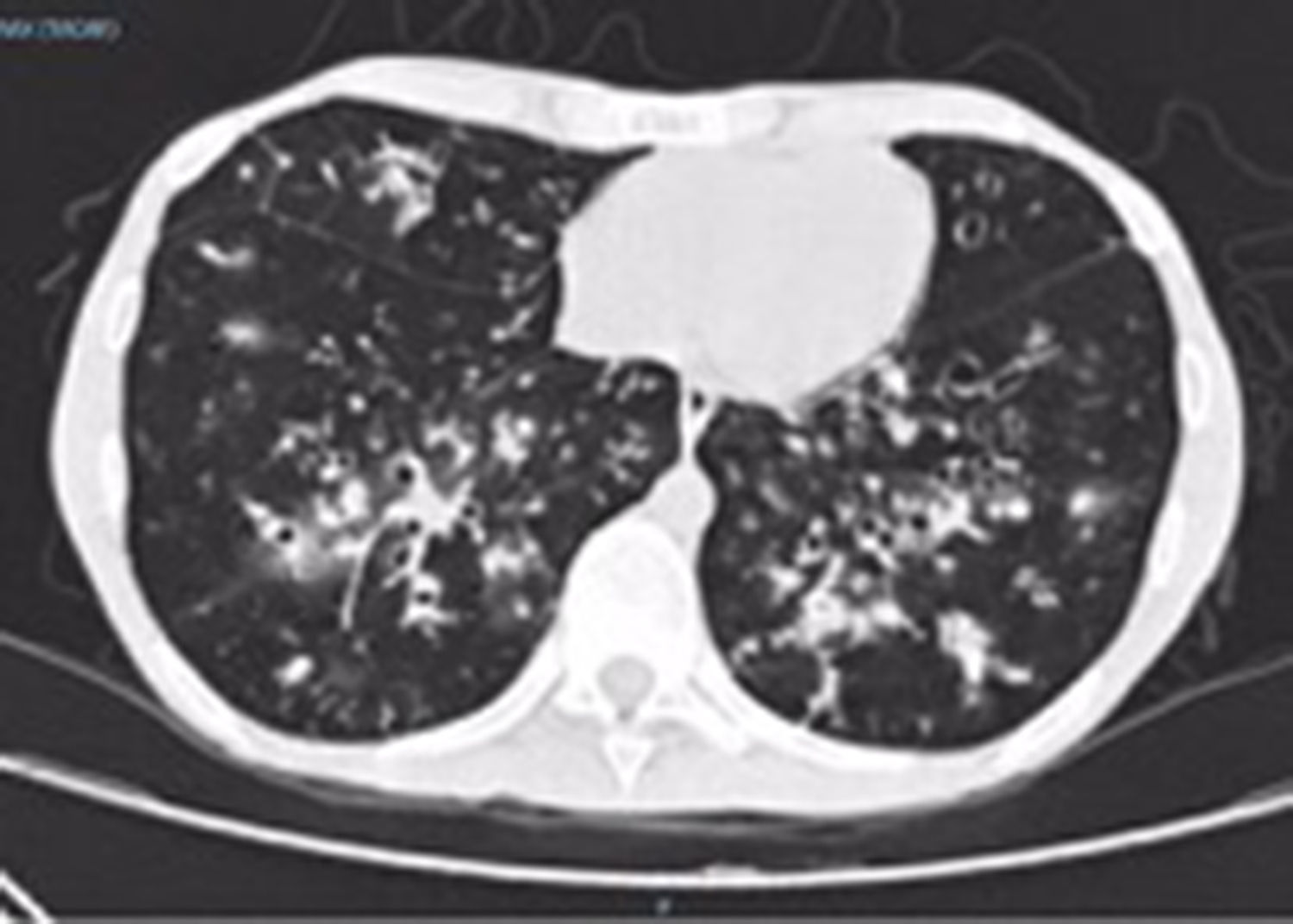
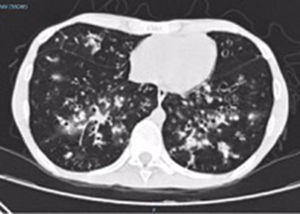
En la última hospitalización, la paciente ingresa en el hospital general de Medellín nuevamente por un cuadro sugestivo de neumonía adquirida en la comunidad, con imagen tomográfica de alta resolución (fig. 2) donde se evidencian infiltrados de predominio retículo-nodulares.
Se realiza manejo antibiótico con cefepime y fibrobroncoscopia con lavado broncoalveolar, pero sin aislamiento microbiológico. La paciente evoluciona satisfactoriamente después de 7 días de antibiótico, sin embargo, con hipoxemia persistente por lo que se ordena oxígeno suplementario y estudios ambulatorios de función pulmonar. Se documenta una espirometría con un patrón obstructivo severo, volúmenes pulmonares que descartan alteraciones restrictivas, con un daño alveolar severo por una prueba de difusión de monóxido de carbono. Pero con una clase funcional aceptable, con una caminata de 6min mayor a 300 metros.
En junta de dermatología se confirma diagnóstico de epidermodisplasia verruciforme al encontrar en biopsia de piel hiperqueratosis de tejido de cesta, acantosis leve y células vacuoladas en la epidermis superior, se indica manejo con retinoides tópicos dado lo avanzado de su enfermedad y lo mórbido que podrían causar otras terapias tales como crioterapia.
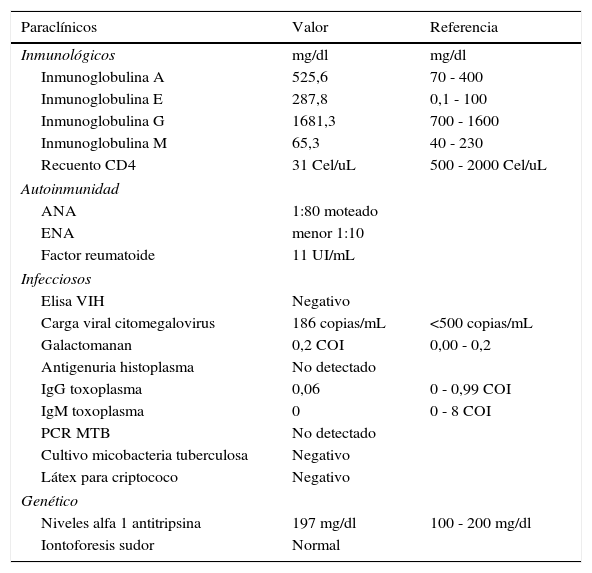
Se realizan estudios de autoinmunidad que explicaran el daño pulmonar, siendo todos negativos. Con prueba de Elisa para VIH negativa. Niveles de alfa 1 antitripsina e iontoforesis en sudor, normales (tabla 1).
Resumen de exámenes de laboratorio
| Paraclínicos | Valor | Referencia |
|---|---|---|
| Inmunológicos | mg/dl | mg/dl |
| Inmunoglobulina A | 525,6 | 70 - 400 |
| Inmunoglobulina E | 287,8 | 0,1 - 100 |
| Inmunoglobulina G | 1681,3 | 700 - 1600 |
| Inmunoglobulina M | 65,3 | 40 - 230 |
| Recuento CD4 | 31 Cel/uL | 500 - 2000 Cel/uL |
| Autoinmunidad | ||
| ANA | 1:80 moteado | |
| ENA | menor 1:10 | |
| Factor reumatoide | 11 UI/mL | |
| Infecciosos | ||
| Elisa VIH | Negativo | |
| Carga viral citomegalovirus | 186 copias/mL | <500 copias/mL |
| Galactomanan | 0,2 COI | 0,00 - 0,2 |
| Antigenuria histoplasma | No detectado | |
| IgG toxoplasma | 0,06 | 0 - 0,99 COI |
| IgM toxoplasma | 0 | 0 - 8 COI |
| PCR MTB | No detectado | |
| Cultivo micobacteria tuberculosa | Negativo | |
| Látex para criptococo | Negativo | |
| Genético | ||
| Niveles alfa 1 antitripsina | 197 mg/dl | 100 - 200 mg/dl |
| Iontoforesis sudor | Normal | |
ANA: anticuerpos antinucleares; ENA: anticuerpos extractables del núcleo; MTB: Mycobacterium tuberculosis; VIH: virus de inmunodeficiencia humana.
Dos meses después del alta reingresa por el mismo cuadro clínico. Se inicia manejo empírico antibiótico, nueva tomografía de tórax con contraste, evidenciando los cambios descritos anteriormente. Nuevo lavado broncoalveolar sin aislamiento microbiológico. El cultivo de micobacterias de la hospitalización previa es reportado negativo. Esta vez con biopsia transbronquial de pulmón que muestra cambios de inflamación moderada crónica y zonas con exudados espumosos y antracosis sin mención de cambios citopáticos o cuerpos de inclusión compatibles con citomegalovirus.
Se realiza nueva Elisa para VIH que es negativo, por lo que se hacen exámenes inmunológicos, como niveles de inmunoglobulinas que fueron normales y recuento de CD4 reportado como 31 cel/uL. Con nuevo recuento de CD4, una vez se estabilizó, de 171 cel/uL. Hallazgo que nos permite definir una inmunodeficiencia primaria. Se realizan exámenes complementarios para infecciones oportunistas los cuales fueron reportados como negativos.
Ante los hallazgos clínicos y radiológicos, asociados a hipoxemia y CD4 bajos, se inicia tratamiento empírico con trimetoprim sulfametoxasol con mejoría clínica. Se da alta con profilaxis para P. jirovecii hasta tener recuentos de CD4 mayores a 200.
DiscusiónLa EV es una condición clínica rara, donde su principal manifestación es el compromiso de piel por verrugas vulgares asociadas a PVH3. Sin embargo, en esta paciente documentamos una disminución cuantitativa de los recuentos de células CD4+ asociada a infecciones pulmonares recurrentes, que han llevado al desarrollo de un daño estructural pulmonar severo con enfisema y bronquiectasias cilíndricas asociadas con signos indirectos de infección por P. jirovecii, con buena respuesta al tratamiento empírico.
Las mutaciones más frecuentes en EV se presentan en los genes EVER1 y EVER2, también llamados TMC6 y TMC8 en la región 17q25, hasta en un 75% de los casos12,13, las cuales están estrechamente ligadas a las manifestaciones cutáneas por PVH, como lo tiene nuestra paciente, además de la mayor incidencia de cáncer no melanoma14,15. Sin embargo, en este caso reportado, la patología pulmonar infecciosa es la que ha determinado la evolución clínica y más importante aún es el hallazgo de la disminución absoluta de CD4+ en un contexto no asociado al VIH, encontrando en este grupo de pacientes con manifestaciones cutáneas e infecciones recurrentes, una mayor frecuencia de mutaciones en los genes RHOH, los cuales codifican una proteína G con un defecto en la actividad GTPasa que se expresa en las células hematopoyéticas, lo que implica la alteración en la activación de integrinas, diferenciación y activación de células T, favoreciendo la deficiencia cuantitativa de células T, en este caso de CD4+7,16.
Habiéndose descartado otras posibles causas de deficiencia de linfocitos CD4+ como infección por CMV por puntos de corte menores a 2.600 copias/ml17, infección por VIH o infección crónica por virus hepatotropos. De igual forma, se descartaron posibles etiologías autoinmunes o hematológicas primarias como explicación a la deficiencia absoluta de células T.
Es así como finalmente consideramos que la manifestación de la EV-PVH en esta paciente, podría ser secundaria a una alteración celular cuantitativa de los CD4, posiblemente asociada a mutaciones del gen RHOH, y no a una predisposición al crecimiento del PVH ligado a mutaciones del gen EVER1-2, en presencia de competencia inmunológica celular como se describe clásicamente en la fisiopatología de la EV, aunque no fue posible su caracterización genética, se plantea esta hipótesis. Desde la base fisiopatológica se propone como tema de investigación el posible efecto benéfico del trasplante alogénico de médula ósea en inmunodeficiencias primarias de CD4 sintomáticas18–20 y como tratamiento de base la profilaxis para principales gérmenes oportunistas como es el caso de P. jirovecii, entre otros.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.