Evaluar la aplicación clínica de los métodos no invasivos en el manejo de la isoinmunización, durante el período de 2006-2010.
Sujetos y métodosSe estudiaron 70 gestaciones con riesgo de anemia fetal en las que se realizó el estudio Doppler de la velocidad sistólica de la arteria cerebral media (VS-ACM). Se comparó la eficacia de la VS-ACM después de una, 2 o 3 transfusiones intrauterinas. El genotipado fetal RHD en sangre materna se realizó en las gestaciones seguidas en nuestro centro.
ResultadosSe practicó cordocentesis en 22 de gestaciones y en 20 se practicó transfusión intrauterina. Las tasas de detección y de falsos positivos de la VS-ACM en la predicción de anemia fetal moderada o severa fueron del 89 y el 15% en gestaciones sin transfusión previa, del 100 y el 41% en los casos con una transfusión previa y del 40 y el 24% cuando se practicaron más de una transfusión.
ConclusionesLa VS-ACM mantiene una sensibilidad alta en una transfusión previa aunque su especificidad disminuye.
To assess the clinical application of non-invasive methods in the management of alloimmunization from 2006 to 2010.
Subjects and methodsSeventy pregnancies with risk of fetal anemia were studied by fetal middle cerebral artery peak systolic velocity (MCA-PSV). The efficacy of MCA-PSV was compared between the first, second and third transfusions. Prenatal testing of fetal RHD blood group using maternal blood was performed in pregnancies followed-up in our center.
ResultsFetal blood sampling was performed in 22 pregnancies; of these, fetal transfusion was carried out in 20. Detection rates and the false-positive rate of MCA-PSV in the prediction of severe or moderate fetal anemia were 89% and 15% in pregnancies with no previous transfusions, 100% and 41% in patients with one previous transfusion, and 40% and 24% when more than one transfusion was performed.
ConclusionMCA-PSV has high sensitivity when there is one previous fetal transfusion but its specificity is lower.
La isoinmunización Rh, conocida también como enfermedad hemolítica perinatal, es el resultado de la sensibilización materna frente a un antígeno eritrocitario de origen paterno presente en el feto y ausente en la madre. Origina la destrucción de los hematíes que presentan el complejo antígeno-anticuerpo en el sistema reticuloendotelial fetal, principalmente en el bazo. Dejada a su evolución natural, la isoinmunización resulta en una anemia fetal leve de escasas consecuencias en un 50% de los casos, en anemia moderada que se mostrará como hiperbilirrubinemia y en kernicterus neonatal en un 25-30%, y en anemia severa que comporta la aparición de hidropesía fetal y muerte fetal intraútero en un 20-25%.
La introducción por Liley et al.1 de la valoración de la bilirrubina en el líquido amniótico mediante espectrofotometría permitió la identificación indirecta de la anemia fetal in útero, tras amniocentesis. En 1981, Rodeck et al.2 describieron la punción del cordón umbilical mediante fetoscopia. Posteriormente, la introducción de la técnica de la cordocentesis ecoguiada simplificó de manera importante la técnica de transfusión fetal in útero3. En la actualidad, técnicas diagnósticas no invasivas, como el estudio Doppler de la arteria cerebral media (ACM) propuesta por Mari et al.4, y el genotipado RHD fetal en sangre materna5,6 han sustituido la amniocentesis y parcialmente la cordocentesis en la detección de la anemia y tipado RHD fetal.
Presentamos a continuación nuestra experiencia en el manejo prenatal de la isoinmunización durante el período 2006-2010, comparándola con la del período 1990-2003, previamente publicada7, durante el cual no se aplicaba el estudio Doppler de la ACM ni el genotipado RHD no invasivo. Asimismo valoraremos el valor del estudio Doppler en la predicción de la anemia fetal después de la primera transfusión intraútero, cuando su valor está en entredicho8–10.
Sujetos y métodosDurante el período 2006-2010, y de acuerdo con nuestro protocolo asistencial, se derivaron a la Unidad de Hematología Fetal a todas aquellas gestantes afectadas de isoimmunización anti-D o anti-c con una titulación a partir de 1/16, isoinmunización anti-Kell o con antecedentes de isoinmunización en gestación previa. En las isoinmunizaciones controladas en nuestro centro (no derivadas exclusivamente para transfusión), se realizó la titulación seriada de anticuerpos irregulares a lo largo de la gestación y en la isoinmunización anti-D se realizó el genotipado RHD fetal en sangre materna en muestra remitida al Banc de Sang i Teixits de Catalunya. A partir del 2009, se introdujo el genotipado Kell no invasivo, que se realizó en el Blood National Bank Service de Reino Unido11. Cuando el resultado del genotipado fetal fue negativo para el gen RHD o Kell, la gestación se consideró de bajo riesgo de anemia fetal.
En las isoinmunizaciones anti-D, anti-Kell y anti-c, se realizó una ecografía semanal a partir de las 18 semanas, para la detección precoz de cualquier signo de hidropesía fetal, conjuntamente con el estudio Doppler de la ACM, determinándose la velocidad sistólica (VS-ACM). Cuando la VS-ACM sobrepasó 1,5 MoM para la edad gestacional4 o se hallaron signos de hidropesía fetal, se propuso la realización de una cordocentesis, por alta probabilidad de anemia moderada o grave y eventual transfusión intrauterina.
La cordocentesis se realizó según técnica convencional, previa localización ecográfica de la zona de inserción placentaria del cordón umbilical, electivamente en placentas anteriores o, alternativamente, del trayecto intrahepático de la vena umbilical. En todos los casos se contaba con concentrado de hematíes (CH) homólogo preparado en el momento de la cordocentesis para realizar una eventual transfusión. El CH se seleccionó siempre del grupo O RHD negativo, compatible con cualquier anticuerpo presente en el suero de la madre, preparado a un hematocrito conocido entre el 75-85%, con un período de conservación inferior a 7 días, irradiado, desleucocitado y procedente de donantes seronegativos para el citomegalovirus. La transfusión intrauterina está claramente indicada cuando la Hb fetal se encuentra por debajo de 0,65 MoM o –4 DE por la edad gestacional, aunque se transfundieron todos los casos con hematocritos inferiores al 30%. La transfusión se realizó mediante venoclisis con llave de 3 pasos conectada a una jeringa de 10ml, que infundía sangre hasta la aguja de punción. Durante todo el procedimiento se observó el paso de burbujas dentro del cordón, alternativamente con el control de la frecuencia cardíaca fetal. La infusión se realizó a velocidad lenta y el volumen de sangre necesaria a transfundir se calculó a partir de la volemia fetal esperada en función de la edad gestacional multiplicada por un factor determinado por los hematocritos del feto y de la unidad de sangre que se debe transfundir12. Se comprobó el hematocrito final una vez finalizada la transfusión. En casos de hidropesía fetal, se transfundió en 2 tiempos, con un máximo del 70% del volumen durante el primer tiempo, para evitar una descompensación hemodinámica por hipervolemia. Se realizó profilaxis antibiótica intravenosa, con cefoxitina 2g antes de las 26 semanas o ceftriaxona 1g im a partir de las 26 semanas. A partir de las 26 semanas, se realizó maduración pulmonar con betametasona 12mg im/24 horas antes del procedimiento, tocólisis vía oral con nifedipino 20mg en el mismo del procedimiento y NST después de su realización.
Después de una transfusión intrauterina, la gestación fue controlada semanalmente mediante ecografía y Doppler en la Unidad de Hematología Fetal siempre que fue posible. Se indicó nueva cordocentesis en función de la VS-ACM, utilizando el mismo valor crítico de 1,5 MoM después de una transfusión intrauterina. Después de 2 o 3 transfusiones, se utilizaron 2 criterios indistintamente para la indicación de nueva transfusión: la VS-ACM o una caída del hematocrito fetal fijada en un 0,9 o 0,6% diario, respectivamente.
Se indicó la finalización de la gestación entre las 36-38 semanas en aquellos fetos transfundidos, en función del intervalo de las transfusiones y las pruebas de bienestar fetal. En fetos no transfundidos, se indicó la finalización a las 38 semanas si no existían signos de anemia moderada o grave, o a partir de las 36 en los casos que sí presentaban dichos signos. Se registraron los hematocritos al nacimiento y la evolución neonatal de los fetos nacidos en nuestro centro o se solicitaron dichos datos al centro de origen o a la misma paciente.
ResultadosNuestra serie incluye 70 gestaciones, una de ellas gemelar, afectadas de isoinmunización referidas a nuestra unidad a una edad gestacional media de 25,6 semanas. El motivo más frecuente de derivación fue la presencia de anticuerpos irregulares (test de Coombs indirecto) positivos (77%), seguido de una VS-ACM alterada (13%) e hidropesía fetal (7,2%) (tabla 1). El tipo de isoinmunización más frecuente fue el anti-D (39%), seguido de anti-D+anti-c (17%), anti-Kell (11%) y anti-E (10%) (tabla 2). El origen de la isoinmunización se atribuyó a la no administración de gammaglobulina anti-D cuando estaba indicada en gestaciones anteriores en un 25% de los casos y fue desconocido en otro 25% (tabla 3).
Motivo de referencia de las 70 pacientes isoinmunizadas
| Motivo | Frecuencia (%) |
| Anticuerpos irregulares positivos | 54 (77%) |
| VS-ACM alterada | 9 (13%) |
| Hidropesía fetal | 5 (7,2%) |
| Anticuerpos irregulares post-administración de gammaglobulina | 1 (1,4%) |
| Realización de cordocentesis/eventual transfusión | 1 (1,4%) |
| Total | 70 (100%) |
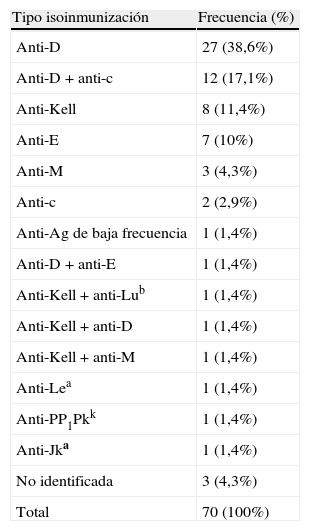
Tipo de isoinmunización
| Tipo isoinmunización | Frecuencia (%) |
| Anti-D | 27 (38,6%) |
| Anti-D+anti-c | 12 (17,1%) |
| Anti-Kell | 8 (11,4%) |
| Anti-E | 7 (10%) |
| Anti-M | 3 (4,3%) |
| Anti-c | 2 (2,9%) |
| Anti-Ag de baja frecuencia | 1 (1,4%) |
| Anti-D+anti-E | 1 (1,4%) |
| Anti-Kell+anti-Lub | 1 (1,4%) |
| Anti-Kell+anti-D | 1 (1,4%) |
| Anti-Kell+anti-M | 1 (1,4%) |
| Anti-Lea | 1 (1,4%) |
| Anti-PP1Pkk | 1 (1,4%) |
| Anti-Jka | 1 (1,4%) |
| No identificada | 3 (4,3%) |
| Total | 70 (100%) |
Origen atribuido de la isoinmunización
| Origen | Frecuencia (%) |
| No administración de gammaglobulina anti-D en gestación anterior | 18 (25%) |
| Desconocido | 18 (25%) |
| Otros (tatuajes,...) | 11 (16%) |
| Transfusión materna | 8 (12%) |
| Antecedente muerte intraútero | 6 (9%) |
| Abortos anteriores | 6 (9%) |
| Isoinmunización anterior | 3 (4%) |
| Total | 70 (100%) |
El genotipado fetal no invasivo en sangre materna se realizó en 19 casos, con resultado positivo para el gen RHD en 14 de los casos, negativo para el gen Kell en 2 casos o el RHD en un caso, presencia de un seudogén RHD vs. DAR en un caso y en un caso resultó inconclusivo.
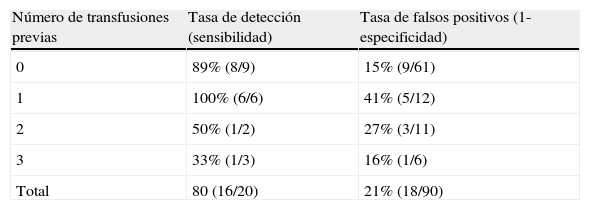
Se realizó cordocentesis en 22 (31%) isoinmunizaciones, 20 de las cuales precisaron como mínimo una transfusión intrauterina. En 14 gestaciones fue necesaria más de una transfusión: 2 transfusiones en 6, 3 transfusiones en 5 y 4 transfusiones en 3 gestaciones. La edad gestacional en que se realizaron las transfusiones varió entre 18 y 35 semanas, con una media de 29 semanas. Las tasas de detección y de falsos positivos halladas de la VS-ACM en la predicción de anemia fetal moderada o severa, en función del número de transfusiones previas, se indican en la tabla 4. La tasa de detección fue del 89% en isoinmunizaciones sin transfusión intrauterina previa y del 100% en una transfusión previa. La tasa de falsos positivos en ausencia de una transfusión previa fue del 15%, aumentó al 41% en una transfusión previa y al 27% en 2 previas. En 3 transfusiones previas disminuyó al 16%, aunque solo se trata de 3 casos.
Sensibilidad y especificidad de la VS-ACM (≥ 1,5 MoM para la edad gestacional) en la predicción de anemia fetal moderada y severa (hemoglobina<0,55 MoM para la edad gestacional), en función del número de transfusiones intrauterinas previas
| Número de transfusiones previas | Tasa de detección (sensibilidad) | Tasa de falsos positivos (1-especificidad) |
| 0 | 89% (8/9) | 15% (9/61) |
| 1 | 100% (6/6) | 41% (5/12) |
| 2 | 50% (1/2) | 27% (3/11) |
| 3 | 33% (1/3) | 16% (1/6) |
| Total | 80 (16/20) | 21% (18/90) |
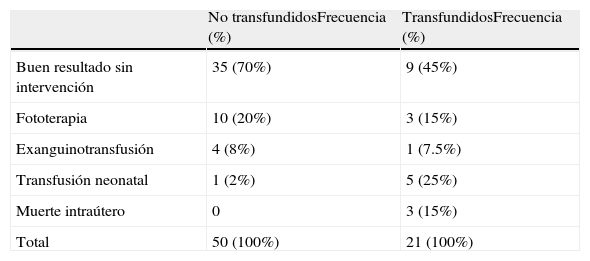
En los 53 partos atendidos en nuestro centro, el hematocrito medio de la sangre del cordón umbilical fue del 51%, con un rango entre el 30 y el 77%. Entre los 50 casos en que no se realizó ninguna transfusión intrauterina, 35 tuvieron una correcta evolución posnatal, sin precisar ninguna medida terapéutica. En 10 casos fue necesaria fototerapia (con administración de gammaglobulina en 2), en 4 casos fue necesaria alguna exsanguinotransfusión y en 2 casos transfusión neonatal (tabla 5).
Resultados perinatales en fetos no transfundidos (n=50) y en los transfundidos (n=21 en 20 gestaciones)
| No transfundidosFrecuencia (%) | TransfundidosFrecuencia (%) | |
| Buen resultado sin intervención | 35 (70%) | 9 (45%) |
| Fototerapia | 10 (20%) | 3 (15%) |
| Exanguinotransfusión | 4 (8%) | 1 (7.5%) |
| Transfusión neonatal | 1 (2%) | 5 (25%) |
| Muerte intraútero | 0 | 3 (15%) |
| Total | 50 (100%) | 21 (100%) |
En relación con los resultados neonatales de los 20 fetos en que se realizó alguna transfusión intrauterina, ocurrieron 3 muertes intraútero en fetos hidrópicos, resultando una supervivencia del 86% (18/21). En los 3 casos la defunción ocurrió en el período postransfusional en fetos afectados de hidropesía severa referidos a nuestro centro por dicho motivo, como última opción para intentar mejorar su pronóstico. En uno de ellos la muerte fue postransfusión intraperitoneal a las 17,6 semanas; en el segundo, fue a las 33,5 semanas y en el último afectó uno de los 2 gemelos dicoriales hidrópicos a las 22,6 semanas. Adicionalmente, hubo una muerte neonatal por sepsis por estreptococo β-hemolítico en otro centro, en un feto transfundido sin complicaciones posteriores. En 9 casos no fue necesaria ninguna actuación terapéutica neonatal específica, en 5 casos fue necesaria la transfusión de concentrados de hematíes, en 3 casos se precisó fototerapia y en un caso exsanguinotransfusión (tabla 5).
DiscusiónEl análisis retrospectivo de nuestra serie reciente de isoinmunizaciones (2006-2010) muestra cómo la VS-ACM es un buen predictor de anemia fetal moderada y severa, y que su tasa de detección se mantiene a medida que aumenta el número de transfusiones intrauterinas previas, aunque la tasa de falsos positivos aumenta del 15% cuando no se ha realizado ninguna transfusión intrauterina al 31% cuando hay alguna transfusión previa. Si lo comparamos con la primera serie de isoinmunizaciones publicada, podemos concluir que las técnicas diagnósticas no invasivas permiten disminuir el número de cordocentesis innecesarias.
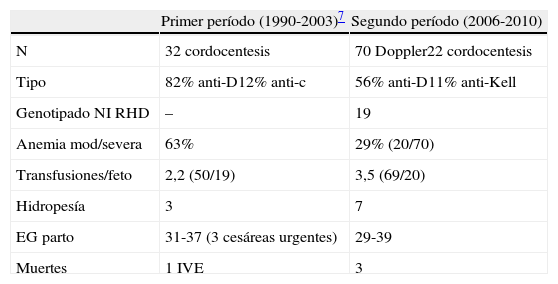
La isoinmunización RHD, que fue la primera patología fetal que dispuso de una terapia invasiva efectiva in útero mediante la transfusión intraperitoneal fetal, ha sido también el paradigma de la substitución de técnicas invasivas por las no invasivas. En primer lugar, la amniocentesis que se realizaba para detectar la bilirrubina en líquido amniótico mediante análisis espectofotométrico y la cordocentesis de entrada han sido sustituidos satisfactoriamente por el estudio de la VS-ACM. En comparación con nuestra primera serie publicada (1990-2003), se detectó el mismo número de anemias fetales (19-20) pero se disminuyó de 32 cordocentesis por sospecha de anemia fetal a 22, en ausencia de transfusión intrauterina previa, aumentando así el valor predictivo positivo del 63% al 91% (tabla 6). Nuestra tasa de falsos positivos en los casos de isoinmunización en ausencia de transfusión previa (en la gestación estudiada) fue del 15%. Esta tasa es similar a la descrita en el estudio inicial de Mari et al., que fue del 12%4 al 9,1% hallada por Deren y Onderoglu9 y a la del 14% reportado por Scheier et al.10.
Comparación de casos estudiados en nuestro centro en 2 períodos separados de tiempo
| Primer período (1990-2003)7 | Segundo período (2006-2010) | |
| N | 32 cordocentesis | 70 Doppler22 cordocentesis |
| Tipo | 82% anti-D12% anti-c | 56% anti-D11% anti-Kell |
| Genotipado NI RHD | – | 19 |
| Anemia mod/severa | 63% | 29% (20/70) |
| Transfusiones/feto | 2,2 (50/19) | 3,5 (69/20) |
| Hidropesía | 3 | 7 |
| EG parto | 31-37 (3 cesáreas urgentes) | 29-39 |
| Muertes | 1 IVE | 3 |
En caso de transfusiones previas, se observa un aumento en la tasa de falsos positivos. En nuestra serie, tras una transfusión se observa un aumento en la tasa de falsos positivos hasta el 41%, similar a la tasa del 37% hallada en la serie de Scheier et al.10 y al 45% que muestra un metanálisis reciente13. Después de 2 transfusiones previas, la tasa de falsos positivos es más discordante, ya que en nuestra serie es del 27% y en la serie de Scheier es del 90%. De la serie de Molina et al. se desprende la existencia de uno o 2 falsos positivos en isoinmunizaciones sin transfusión previa. Con tasas muy bajas de falsos positivos, las tasas de detección fueron del 73, el 85 y el 72% después de ninguna, una o 2 transfusiones14.
Los resultados de nuestro estudio sugieren que la ACM-PSV no pierde sensibilidad si se utiliza para indicar una segunda transfusión, pero sí que pierde especificidad. Así, Detti et al. propusieron aumentar el cutoff a 1,7 a partir de la segunda transfusión, para disminuir el número de cordocentesis innecesarias8. En referencia a la tasa de detección, detectaron todos los casos de anemia severa con los cutoff de 1,5 MoM en pacientes sin ninguna transfusión y con el cutoff de 1,69 MoM en los casos con una transfusión previa.
En relación con los resultados perinatales de la isoinmunización, en nuestra serie se halla una supervivencia perinatal del 86% (18/21), considerando tanto los fetos hidrópicos como los no hidrópicos. Las 3 pérdidas intrauterinas de nuestra serie ocurrieron todas ellas en el período postransfusional de una primera transfusión realizada en fetos referidos el día anterior por hidropesía severa. En un caso ocurrió después de una transfusión intraperitoneal a las 17,6 semanas y en otro en un gemelo dicorial de 22 semanas derivada por doble hidropesía severa. La muerte neonatal debido a una sepsis fulminante por estreptococo beta-hemolítico no lo hemos incluido como pérdida secundaria a la isoinmunización. En una de las series más importantes de transfusiones intrauterinas, Van Kamp et al.15 muestran una tasa de supervivencia del 92% en fetos sin hidropesía y del 78% para los hidrópicos. En la serie publicada recientemente por Molina et al.14 la tasa de supervivencia fue del 87%.
Una limitación de nuestro estudio es que un número importante de las isoinmunizaciones incluidas fueron controladas en otros centros y se nos remitieron únicamente para transfusión intrauterina, lo que dificulta un seguimiento homogéneo de nuestros protocolos y la obtención de datos perinatales. Por otro lado, aunque en este estudio se haya definido la anemia fetal con criterios muy estrictos (hemoglobina inferior a 0,55 MoMs), en la práctica clínica se transfundieron los casos en que la cordocentesis mostró un valor a un hematocrito inferior al 30%.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.