A continuación se exponen 2 estudios farmacoeconómicos que comparan el comprimido oral de fentanilo con aplicador para administración bucofaríngea (Actiq®), el comprimido de fentanilo sublingual (Abstral®), el comprimido bucal efervescente de fentanilo (Effentora®) y el fentanilo por vía nasal, con 2 tecnologías: una formulación en gel con pectina (fentanilo intranasal con pectina, PecFent®) y otra en solución acuosa sin pectina (Instanyl®). El estudio de López et al buscaba analizar los ahorros potenciales derivados de la introducción progresiva del fentanilo intranasal con pectina, para el tratamiento de pacientes mayores de edad con dolor irruptivo oncológico. El estudio de Blanco et al tenía como objetivo conocer la efectividad y eficiencia del fentanilo intranasal con pectina comparado con los otros tratamientos transmucosos comercializados en ese momento. El primer estudio mostró una disminución del coste sanitario con la introducción progresiva del fentanilo intranasal con pectina en el Sistema Sanitario Español para el tratamiento del dolor irruptivo. El segundo estudio demostró que la opción más eficiente (mayor efectividad y menor coste) en todos los casos analizados fue el espray intranasal de fentanilo con pectina.
This article presents two pharmacoeconomic studies comparing the compressedfentanyl lozengewith an integral oromucosalapplicator (Actiq®); fentanyl sublingual tablets(Abstral®); effervescent fentanyl buccal tablets(Effentora®) and nasal fentanyl with two technologies: a formulation that contains pectin in a gel-based nasal spray (PecFent®) and another formulation in an aqueous solution without pectin (Instanyl®). The first of these studies aimed to analyze the potential savings due to the progressive introduction of fentanyl pectin nasal spray for the treatment of adult patients with breakthrough cancer pain. The second study aimed to determine the effectiveness and efficiency of fentanyl pectin nasal spray compared with the other tansmucosal treatments currently on the market. The first study showed a reduction in healthcare costs with the progressive introduction of fentanyl pectin nasal spray for the treatment of breakthrough pain in the publicly-funded health system in Spain. The second study showed that the most efficient option (greatest effectiveness and lowest cost) in all the cases analyzed was the fentanyl-pectin nasal spray.
El dolor irruptivo (DI), oncológico (DIO) o no, tiene un impacto negativo sobre la función del paciente, produce trastornos psicológicos y tiene efectos sobre el estado de ánimo, la ansiedad, la depresión y el sueño; en definitiva, altera la calidad de vida de la persona. Los pacientes con cáncer suelen experimentar DI a pesar de tener instaurada una analgesia de base adecuada.
Cuando mejoramos la calidad de vida de estos pacientes con el control del DI se produce una mejoría clínicamente relevante que, desde la perspectiva de la gestión clínica (y de casos), no debe pasar inadvertida. El control del DI genera un aumento en su calidad de vida, al permitir a los pacientes una cierta movilidad, mejorar su capacidad para el cuidado personal, realizar labores sencillas domésticas y de ocio y, también, ha propiciado mejorar el sueño de aquellos que tardaban en conciliarlo por dolor al acostarse, recuperando el paciente en su conjunto su vida cotidiana1.
El problema surge cuando hay que valorar cuánto a cambio de qué. Es decir, cuánta mejoría conseguimos (aumento en la calidad de vida relacionada con la salud) en nuestros pacientes y cuánto gasto generamos (costes directos e indirectos). La pregunta que finalmente deberíamos poder responder en cualquier tipo de evaluación económica es si la nueva alternativa vale lo que cuesta.
Sabemos que el dolor irruptivo, y su mal control, se asocia con un mayor uso de los servicios sanitarios (es decir, aumento de las consultas externas y/u hospitalizaciones)2, lo que se traduce en aumento de costes directos médicos (p. ej., medicación, número de visitas, más ingresos, etc.) y más costes directos no médicos (p. ej., costes de transporte, adecuación de camas, etc.), tanto para el servicio de salud como para el paciente y sus cuidadores3. El DI también se asocia con un mayor uso de los servicios sociales y puede repercutir también en la capacidad del paciente y del cuidador para trabajar y ganar dinero, es decir, costes indirectos, ya que desencadena pérdida de la productividad4.
En un trabajo previo, la optimización del control sintomático y analgésico con el fentanilo intranasal con pectina [FINP] permitió un menor consumo de recursos sanitarios en la gestión del DIO: menos visitas a urgencias, menos visitas no programadas, menor número de ingresos hospitalarios, menos días ingresados, reducción significativa del número de episodios de DIO; todo esto condujo a una reducción importante en el coste por proceso controlado frente a no controlado5.
Desde el enfoque farmacoeconómico (y evaluación económica de tecnologías sanitarias) es importante que el coste de la realización de una intervención sea comparado con la opción de no llevar a cabo la intervención (en nuestro caso, el coste total de no tratar el DI). Por ejemplo, se ha reportado el uso de fentanilo oral para dar lugar a la reducción del uso de determinados servicios de salud (es decir, el ingreso hospitalario)6 y el aumento de la capacidad de trabajar/ganar dinero (en el dolor no oncológico)7.
Por último, la mejor arma de la que dispone un médico para ser eficiente es la efectividad; se consigue mayor eficiencia cuanto más efectivo se es, en nuestro caso, cuando se controla el DI y se mejora la gestión clínica del proceso.
En nuestro trabajo vamos a abordar la gestión clínica y económica del DI, oncológico o no, desde una doble perspectiva:
- •
En primer lugar, desde la faceta del impacto presupuestario, en este tipo de estudio el objetivo es estimar los ahorros o gastos potenciales derivados de la introducción progresiva de un nuevo fármaco en el tratamiento de pacientes mayores de edad con DIO, desde la perspectiva del Sistema Sanitario Español.
- •
En segundo lugar, desde la eficiencia, es decir, conocer la efectividad y los costes derivados del uso de fentanilo intranasal con pectina comparado con otros tratamientos empleados en el DIO a través de un análisis farmacoeconómico.
El objetivo de este estudio fue estimar los ahorros potenciales derivados de la introducción progresiva del FINP, para el tratamiento de pacientes mayores de edad con DIO, desde la perspectiva del Sistema Sanitario Español, mediante un análisis de impacto presupuestario.
Material y MétodosLa población se obtuvo del Instituto Nacional de Estadística (INE) aplicando valores de prevalencia. El seguimiento fue de 1 año, incluyendo los costes médicos directos derivados del manejo de la enfermedad: coste de la medicación, coste de la medicación de rescate y coste de las visitas médicas necesarias para el ajuste de la dosis.
Según los estudios publicados y las estadísticas del INE existen en España 316.271 casos prevalentes de cáncer; de ellos requerirán tratamiento para el DIO 72.724 pacientes mayores de 18 años y se tratarían con fentanilo al día en España 26.787 episodios de DIO.
Los 316.271 casos prevalentes de cáncer se obtienen de la población adulta mayor de 18 años publicada por el INE (38.853.982 personas)8 y la publicación de López-Abente et al9 de 2005, que indica una prevalencia de cáncer del 0,814%.
La mayoría de los pacientes con cáncer sufren dolor crónico, de moderado a intenso, durante la evolución de su enfermedad10.
Por otro lado hay diversos estudios que describen tasas de prevalencia del DIO, que oscilan entre un 23 y un 94%11. El número de episodios de DIO por paciente y día presenta un valor medio de 3 episodios12, con una dispersión de entre 1 y 25 episodios. En nuestro estudio se utilizó el valor mínimo (1 episodio por día) para calcular los gastos del mercado español.
Con los valores de prevalencia previamente descritos (316.271 casos prevalentes de cáncer) y tomando el 23% de prevalencia de DIO se obtienen 72.724 pacientes oncológicos mayores de 18 años, por año, que requerirán tratamiento para el DIO en España.
Por último, según los estudios publicados, un 75% de los pacientes recibe tratamiento para el DIO13 y se pauta fentanilo al 49,1% de ellos (datos de IMS)14. En consecuencia, para la población española se obtiene un total de 26.787 episodios de DIO tratados con fentanilo cada día (72.742 pacientes oncológicos × 1 episodio día × 75% episodios tratados × 49,1% episodios tratados con fentanilo = 26.787) (tabla 1).
Características demográficas y valores de prevalencia utilizados en el análisis del impacto presupuestario.
| Características demográficas y prevalencia | Fuente | |
|---|---|---|
| Población total adulta, ≥ 18 años | 38.853.982 | INE 2012 |
| Prevalencia de cáncer en España | 0,814% | Referencia 9 |
| % de pacientes oncológicos que presentan DIO | 62,7%* (23-94) | Media |
| (mínimo-máximo) | ||
| Número medio de episodios de DIO que sufre un paciente al día | 3,0* (1 a 25) | Referencia 12 |
| % de episodios de DIO que son tratados | 75% | Referencia 13 |
| % de episodios de DIO que son tratados con una formulación de fentanilo | 49,1% | Datos de IMS |
DIO: dolor irruptivo oncológico; INE: Instituto Nacional de Estadística.
La estimación de los recursos sanitarios se basa en 2 aspectos:
- •
Ajuste de dosis. El informe publicado por Scottish Medicines Consortium15, que incluía una evaluación económica, estimó, de los estudios clínicos de los distintos fentanilos, las dosis necesarias para la titulación, así como la medicación desperdiciada, obteniendo el coste asociado al ajuste de dosis (tabla 2). Con los fentanilos transmucosos orales un paciente requerirá, como media, 2,9 visitas al médico y recetas hasta alcanzar la dosis eficaz, y se desperdiciará, como media, un total de 3,8 comprimidos durante la titulación. En relación con el FINP, gracias a su mejor ajuste de dosis y al menor número de presentaciones comercializadas (solo 2 frente a las 5 o 6 de los fentanilos orales transmucosos), hay una menor necesidad de prescripciones médicas y, además, se observó que los pacientes en tratamiento con el FINP pueden ser instruidos a aumentar la dosis por sí mismos, sin necesidad de acudir al médico, lo que permitiría ahorrar más medicación, así como un menor número de visitas para el ajuste de dosis. Por tanto, los pacientes en tratamiento con FINP necesitarán solo 1,6 visitas médicas y desperdiciarán solo 1,6 nebulizadores.
Tabla 2.Medicación desperdiciada en la titulación, visitas médicas necesarias y medicación de rescate.
Titulación Actiq® Abstral® Effentora® PecFent® Medicación desperdiciada en ajustes de dosis 3,8 3,8 3,8 1,6 Número de recetas médicas requeridas (visitas al médico) 2,9 2,9 2,9 1,6 Pacientes que precisan medicación de rescate 15% 11,2% 23% 9% - •
Medicación de rescate. El porcentaje de pacientes que requieren medicación de rescate se obtiene de los estudios clínicos disponibles sobre los distintos fentanilos orales, así como del FINP16–19. Los estudios clínicos con FINP registran un menor porcentaje de pacientes con necesidad de medicación de rescate en comparación con el resto de fármacos (tabla 2).
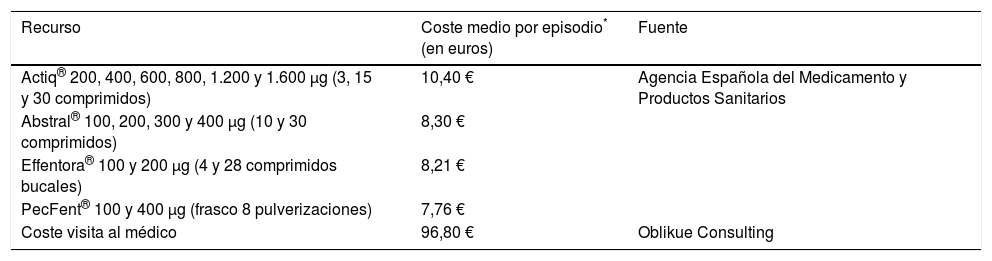
En la tabla 3 se presenta el coste medio por episodio tratado con cada uno de los fentanilos, así como el coste de cada visita al médico (obtenido este último de una base de datos de costes sanitarios españoles)20. Es importante destacar que los costes indirectos, como los gastos de transporte, así como otros debidos a la pérdida de productividad laboral darían aún datos más favorables para el FINP pero, debido a la ausencia de datos, no se han considerado en el presente estudio.
Costes unitarios.
| Recurso | Coste medio por episodio* (en euros) | Fuente |
|---|---|---|
| Actiq® 200, 400, 600, 800, 1.200 y 1.600 μg (3, 15 y 30 comprimidos) | 10,40 € | Agencia Española del Medicamento y Productos Sanitarios |
| Abstral® 100, 200, 300 y 400 μg (10 y 30 comprimidos) | 8,30 € | |
| Effentora® 100 y 200 μg (4 y 28 comprimidos bucales) | 8,21 € | |
| PecFent® 100 y 400 μg (frasco 8 pulverizaciones) | 7,76 € | |
| Coste visita al médico | 96,80 € | Oblikue Consulting |
En la tabla 4 se presentan los resultados del análisis de impacto presupuestario realizado.
Resultados del impacto presupuestario comparativo de PecFent® frente a otras formulaciones de fentanilo disponibles en España. Cálculo de costes diarios en 72.742 pacientes y con 26.787 episodios de DIO tratados cada día con fentanilo en España.
| Cálculos diarios | Antes de PecFent®* | Utilizando PecFent® en el 2,5% de los episodios de DIO en España* |
|---|---|---|
| Coste total de los episodios de DIO en 1 día (en euros) | ||
| Coste de los episodios totales tratados con Actiq® | 99.574 | 94.504 |
| Coste de los episodios totales tratados con Abstral® | 29.583 | 28.076 |
| Coste de los episodios totales tratados con Effentora® | 22.345 | 21.207 |
| Coste de los episodios totales tratados con PecFent® | – | 5.848 |
| Coste total (episodios de DIO en 1 día) | 151.502 | 149.636 |
| Ahorros diarios producidos al tratar con PecFent® el 2,5% de los episodios de DIO en España (en euros) | –1.886 | |
| Cálculos anuales | Antes de PecFent®* | Utilizando PecFent® en el 2,5% de los episodios de DIO en España* |
| Coste total de los episodios de DIO en 1 año (en euros), de los cuales: | 55.298.051 | 54.617.030 |
| Farmacológicos | 53.301.648 | 52.666.195 |
| Visitas médicas | 1.996.403 | 1.950.836 |
| Ahorros anuales producidos al tratar con PecFent® | ||
| el 2,5% de los episodios de DIO en España (en euros) | –681.020 |
DIO: dolor irruptivo oncológico.
En la tabla se muestra la información previa a la comercialización de PecFent®, es decir, cuando no era posible ofrecer este tratamiento (columna «Antes de PecFent®»). También cuando PecFent® se utiliza en el 2,5% de los episodios de DIO en España: penetración de PecFent® en su año de comercialización, año 2011 (columna «Utilizando PecFent® en el 2,5% de los episodios de DIO en España»). El incremento gradual de penetración de PecFent® permitirá ir incrementando estos ahorros año a año. En concreto, a la fecha de la elaboración de esta publicación, septiembre de 2014, la penetración de PecFent® es del 19,3%, por lo que los ahorros en el sistema sanitario serían de 5.257.474 euros = (681.020/2,5%) × 19,3%.
Se observa que, gracias a sustituir por el FINP un 2,5% de los episodios tratados con otros fentanilos se consigue un ahorro diario de 1.866 euros. Trasladado al cálculo anual, el FINP podría suponer un ahorro de 681.020 euros al año para el Sistema Nacional de Salud. El incremento gradual de penetración de PecFent® permitirá ir incrementando estos ahorros año a año (texto al pie de la tabla 4).
ConclusiónEl FINP supone una forma innovadora, eficaz y segura de administración terapéutica del citrato de fentanilo, que muestra un inicio de acción más rápido en el control del DI que se produce en los pacientes con cáncer avanzado tratados con opioides para su dolor oncológico de base.
Por sus beneficios económicos, el FINP podría plantearse como reemplazo parcial de las formulaciones de fentanilo transmucoso para el tratamiento del DIO disponibles en la actualidad, como son las formulaciones para administración por vía oral (transmucosa o sublingual).
Los ahorros observados gracias al empleo de FINP se consiguen principalmente por las siguientes características del producto:
- •
El coste medio por episodio tratado con FINP es menor que el del resto de formulaciones de fentanilo (con un ahorro de 0,6 euros por episodio).
- •
El ajuste de dosis es más sencillo que con el resto de formulaciones de fentanilo, lo que permite que se desperdicie menos medicación y que se necesite un menor número de visitas al médico para la titulación.
- •
El porcentaje de pacientes que necesitan medicación de rescate con FINP es menor.
En definitiva, el FINP presenta un perfil económico muy favorable, que permite un menor consumo de recursos sanitarios. Se estima que consiguió un ahorro de 681.020 euros en 2011 (por su uso en el 2,5% de los episodios de DIO en España). Considerando que la penetración de PecFent® en septiembre de 2014 en el Sistema Sanitario Español fue del 19,3%, permite un ahorro de 5.257.474 euros. Si dicha sustitución fuera superior en el futuro, se conseguiría aún mayor ahorro anual en el presupuesto sanitario.
Farmacoeconomía del dolor irruptivo: análisis de coste-utilidadEn este estudio5 se realizó una doble evaluación, clínica y económica, de los medicamentos con indicación en el dolor irruptivo de cáncer en nuestro país (break through cancer pain [BTCP]). De una parte se evaluaron los medicamentos desde la eficacia a partir de las fichas técnicas de cada uno de ellos y de un metaanálisis publicado21 (tabla 5).
Datos de eficacia, utilidades y costes empleados en el análisis farmacoeconómico.
| Medicamento analizado | % de episodios de dolor irruptivo controlados (IC del 95%)21,29-32 | NNT frente a placebo24,25 | AVAC (IC del 95%)32 | Coste de adquisición del medicamento (en euros) (180 días) (PVP + IVA) |
|---|---|---|---|---|
| CSF | 29 (22-38) | 3,45 (2,62-5,05) | 0,220 (0,203-0,235) | 4.160 |
| CFOT | 4.412 | |||
| CBF | 31 (25-39) | 3,23 (2,48-4,62) | 0,223 (0,209-0,237) | 4.215 |
| FINA | 55 (46-68) | 1,82 (1,54-2,22) | 0,266 (0,251-0,281) | 4.395 |
| FINP | 0,245 (0,221-0,268) | 3.824 |
AVAC: número de años ganados ajustados por calidad de vida; CBF: comprimido bucal de fentanilo (Effentora®); CFOT: citrato de fentanilo oral transmucoso (Actiq®); CSF: comprimido sublingual de fentanilo (Abstral®); FINA: espray intranasal de fentanilo acuoso (Instanyl®); FINP: espray intranasal de fentanilo con pectina (PecFent®); NNT: número de pacientes necesarios para que el tratamiento alcance el beneficio.
Costes actualizados a 2014 (base de datos del CGCOF).
Costes: costes de la medicación durante 180 días con 3 episodios de dolor irruptivo por día/paciente (actualizados a 2014).
Para apoyar al médico en la toma de decisiones se desarrolló un modelo de análisis que estima el coste-utilidad de todos los medicamentos con indicaciones para el DI utilizados en nuestro país. Este modelo analiza las reducciones previstas en la intensidad del dolor de los episodios de BTPC y cómo estas se traducen en ahorro de costes; la utilidad se midió en número de años ganados ajustados por calidad de vida (AVAC o QALY).
Los resultados analizados mostraron que la mayor eficacia, medida como ganancia en calidad de vida, se obtuvo con la opción de fentanilo intranasal con pectina frente a las otras opciones analizadas. Esta opción fue, en todos los casos, más de un 15% superior en número de años ganados con buena calidad de vida (AVAC ganados) respecto a las otras opciones orales.
Comparando uno a uno los otros tratamientos frente a FINP, los comprimidos sublinguales (CSF, comprimido sublingual de fentanilo) y los comprimidos con aplicador bucal integrado (CFOT, citrato de fentanilo oral transmucoso) proporcionaron menos años de vida ganados: –18%, y los comprimidos bucales (CBF, comprimidos bucales de fentanilo) –17%.
La opción de mayor coste (durante 180 días de tratamiento) tras el análisis farmacoeconómico fue para CFOT, con 4.412 euros, seguida de espray intranasal de fentanilo acuoso (FINA), CBF y CSF (4.395, 4.215 y 4.160 euros, respectivamente). La opción más económica fue para FINP, con 3.824 euros.
A partir de los AVAC conseguidos con 6 meses de medicación se calculó la inversión necesaria para ganar 1 año de vida con calidad con los distintos tratamientos. De todas las opciones analizadas, la opción más eficiente resultó ser FINP (mayor eficacia, es decir, más años ganados con buena calidad de vida a un menor coste). Todas las demás opciones fueron estrategias dominadas, es decir, presentaron una menor eficacia (CSF, CFOT y CBF) o similar eficacia (FINA) y todas ellas presentaron un mayor coste (fig. 1).
En la evaluación farmacoeconómica realizada, todas las opciones analizadas fueron coste-efectivas, es decir, presentaron una ratio coste/utilidad < 30.000 euros/QALY, cifra que puede considerarse como umbral en nuestro país22,23. Pero la opción más eficiente (mayor efectividad y menor coste) en todos los casos analizados es el espray intranasal de fentanilo con pectina (FINP). FINA, sin proporcionar más eficacia, ha demostrado ser significativamente más caro (+15%). CSF, CFOT y CBF demostraron una efectividad un 18% menor que FINP además de ser más caros (+9, +15% y +10%, respectivamente).
Otra forma de medir: coste por número de pacientes necesarios para que el tratamiento alcance el beneficio e impacto presupuestarioOtra forma de realizar un estudio de coste-eficacia es utilizando el número de pacientes necesarios para que el tratamiento alcance el beneficio (NNT) como una aproximación a la efectividad de los tratamientos24. En la tabla 5 de la página previa se muestra el número necesario de pacientes que tienen que utilizar un tratamiento para que uno de ellos alcance el beneficio esperado (disminución significativa y clínicamente relevante del DI) con cada uno de los fármacos objeto de estudio durante un tratamiento continuo de 180 días. El NNT se ha calculado a partir de los datos combinados de eficacia de cada fármaco estudiado (reducción absoluta del riesgo) utilizando una calculadora específica25.
El uso del NNT, como medida de eficacia que es, se ha realizado por diversas agencias evaluadoras como la CADTH (Canadian Agency for Drugs and Technologies in Health)26, el NICE (National Institute of Clinical Excellence), el CRD (Centre for Reviews and Dissemination, University of York)27 y diversa bibliografía relevante28.
En la tabla 5 se muestran los datos correspondientes a los NNT de cada uno de los fármacos analizados para el control del DIO; en la figura 2 se comparan los distintos costes por NNT de cada uno de los fármacos estudiados.
Sin embargo, en nuestra realidad sanitaria hay que tener en cuenta que partimos de un presupuesto cerrado y, por tanto, la eficiencia deberíamos calcularla también a partir de esta premisa. Supongamos que partimos de un presupuesto monetario fijo de 500.000 euros para tratar de DI a los pacientes de nuestro hospital; también sabemos que no todos los pacientes responderán de forma efectiva en la disminución del dolor, es decir, si el fármaco objeto de estudio presenta un NNT de 3, significa que de cada 3 pacientes tratados solo 1 de ellos obtendrá el beneficio del fármaco, o sea, episodios de DI evitados. En la figura 3 se muestra cómo para un mismo presupuesto el número de pacientes tratados es diferente (dependerá del coste de la medicación empleada) y cómo solo unos pocos tendrán episodios evitados (NNT).
Número de pacientes tratados y pacientes con evento evitado, con un presupuesto fijo de farmacia (500.000 euros) para 180 días de tratamiento continuo. Fentanilo intranasal con pectina consigue, con presupuesto dado, tratar más pacientes durante 180 días (131) y evita más episodios de dolor irruptivo (DI).
El FINP supone una forma innovadora que por sus beneficios económicos podría plantearse como reemplazo parcial de las formulaciones de fentanilo transmucoso por vía oral (transmucosa o sublingual). El uso del fentanilo intranasal con pectina a lo largo de 2014 en un 19,3% de los episodios consiguió un ahorro de 5.257.474 euros para el Sistema Sanitario Español33. Dicho ahorro fue debido a:
- •
Un menor coste por episodio tratado.
- •
Ajuste de dosis más sencillo (se desperdicia menos medicación y se precisan menos visitas al médico).
- •
El 91% de los pacientes no precisó medicación de rescate adicional.
El estudio de efectividad y eficiencia que comparó el FINP con los otros tratamientos transmucosos demostró que la opción más eficiente (mayor efectividad y menor coste) en todos los casos analizados fue el FINP.
Por último, en el análisis NNT el FINP permitió, a un presupuesto fijo, tratar a más pacientes y, además, ser la opción de mayor eficacia (más episodios evitados).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.