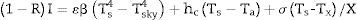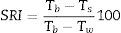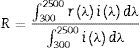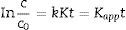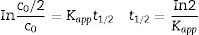Se han preparado por el método cerámico composiciones optimizadas de una cuatricromía CMYK más un pigmento verde, basados en el dopado de cobalto en celsiana (Ba0,9Co0,1)Al2Si2O8 (cian), de cromo en armalcolita (MgFe)(Cr0,2Ti2,8Fe)O10 (magenta), de níquel en geikielita (Mg0,5Ni0,5)TiO3 (amarillo), la perovskita CrNdO3 (verde) y la misma perovskita mineralizada con fluoruros alcalinotérreos (BaF2 y MgF2) (negro). Los pigmentos en polvo y los vidriados obtenidos con una frita convencional de bicocción (1.050°C) se han caracterizado respecto de su rendimiento colorimétrico mediante el modelo CIEL*a*b*; su capacidad refrigerante (como cool pigment), mediante la medida del índice de reflexión solar SRI, y su capacidad fotocatalítica, mediante el test de degradación de NaranjaII. Los resultados obtenidos se comparan con los obtenidos con pigmentos comerciales de la familia CMY del circón tomados como referencia. Los resultados indican una coloración intensa de los polvos y de las plaquetas vidriadas con valores L* inferiores a los pigmentos homólogos del circón, en cambio el chroma obtenido con los pigmentos del circón es superior (b* negativo para el cian, a* positivo para el magenta o b* positivo para el amarillo). Respecto a su capacidad refrigerante, los resultados indican valores SRI altos y superiores en el caso de la celsiana al del vanadio-circón, el verde supera ligeramente a la eskolaita Cr2O3, que se ha tomado como referencia, y en el caso de la perovskita negra sus valores SRI muy bajos (SRI=0 en el caso del polvo) y asociados a altos valores de emisividad en el infrarrojo medio la hacen interesante como pigmento para sustratos absorbentes en colectores solares. La capacidad fotocatalítica sobre NaranjaII indica valores de periodo de semivida en torno a 55-70min, inferiores a los medidos en los circones de referencia (110-190min).
Optimized compositions of a four-color CMYK plus a green pigment have been prepared by the ceramic method: cobalt doping in Celsian (Ba0,9Co0,1)Al2Si2O8 (cyan), chromium in armalcolite (MgFe)(Cr0,2Ti2,8Fe)O10 (magenta), nickel in geikielite (Mg0,5Ni0,5)TiO3 (yellow), the perovskite CrNdO3 (green) and the same perovskite mineralized with alkaline earth fluorides (BaF2 and MgF2) (black). Both pigment powder and glazed sample in a conventional double firing frit (1050°C) have been characterized with respect to its colorimetric performance by the model CIEL*a*b*, its cooling capacity (as cool pigments) by the measurement of the solar reflection index SRI and its photocatalytic capacity by means of the OrangeII degradation test. The obtained results are compared with those obtained with commercial pigments of the CMY family of the zircon. The results indicate that the coloration of the powders and the enamelled samples is more intense, with L* values lower than the zircon homologous pigments, whereas the obtained chroma with the pigments of the zircon is better (b* negative for cyan, a* positive for magenta and b* positive for yellow). Regarding its cooling capacity, the results indicate high SRI values for all samples. In the case of Celsian SRI is higher than for vanadium-zircon, the green of perovskite slightly exceeds the eskolaite Cr2O3 value that is taken as reference. In the case of the black perovskite, very low SRI values are measured (SRI=0 in the case of powder) and associated with high middle-infrared emissivity values, making it interesting as a pigment for absorbent substrates in solar collectors. The photocatalytic capacity over OrangeII indicates half-life values around 55-70minutes, lower than those measured in zircons (110-190minutes).
Los llamados pigmentos refrigerantes o refrescantes (cool pigments) son pigmentos de alta reflectividad en el infrarrojo cercano (NIR, 780-2.100nm), lo que permite un ahorro significativo en la climatización en zonas cálidas, protegiendo el edificio con una envolvente de revestimiento de alta reflectividad a los rayos infrarrojos. La utilización de recubrimientos refrescantes de alta reflectividad solar no solo afecta positivamente al propietario del edificio [1], sino que el ambiente urbano de las ciudades con techos y paredes tapizadas con colores refrescantes mejora la calidad del aire, cuya temperatura se modera por los cubrimientos refrescantes, disminuyen las emisiones de gases de efecto invernadero y se mitiga el efecto de isla de calor urbano [2]. La evolución de la intensidad de radiación solar, incluso en climas moderados y fríos, hace que las envolventes refrescantes siempre presenten un análisis de ciclo de vida positivo, por lo que estados como California o Florida ya prescriben características reflectoras mínimas para la superficie de los edificios, con planteamientos que con alta probabilidad se implementarán de forma global con el fin de mitigar el cambio climático [3].
Al incidir la radiación solar sobre el techo y las paredes de un edificio, parte de la radiación es reflejada y parte es transferida al interior del edificio. En el equilibrio térmico de una superficie insolada se cumple la ecuación 1 [4].
Donde: I=irradiación solar (W/m2); R=reflectividad solar total (también se utiliza en el texto TSR); β=constante de Stefan Boltzmann, 5,67·10−8W/m2K4.; ¿=emitancia (0,9 en materiales cerámicos); hc=coeficiente de convección (W/m2K); Ts=temperatura absoluta de la superficie insolada en el equilibrio.; Tsky=temperatura de referencia del cielo; Ta=temperatura del aire; σ=conductividad térmica (W/mK); x=espesor de la pared; Tx=temperatura en la superficie interior de la pared.
Se toman como «condiciones normales o estándar de insolación», a efectos de cálculo posterior: irradiación solar I=1.000W/m2, temperatura normal del aire Ta=310K, coeficiente convectivo hc=12W/m2K y temperatura aparente del cielo Tsky=300K.
Se define el coeficiente de reflexión solar SRI (por sus siglas en inglés) al valor:
Bajo las condiciones estándar anteriormente definidas, considerando despreciable la componente de transmisión de calor por conducción:
Tb=temperatura del cuerpo negro ideal, 355,61K (82,6°C).
Tw=temperatura del cuerpo blanco ideal 317,76K (44,7°C).
La medida del llamado índice de reflexión solar SRI puede hacerse a través de la metodología anterior, midiendo la temperatura de equilibrio térmico de la superficie Ts en las condiciones estándar de irradiación solar anteriormente descritas, o bien por el método de promediación ponderada basado en la medida de la reflectividad solar total (TSR o simplemente R) de la superficie mediante la técnica de espectrometría por reflectancia difusa UV-Vis-NIR (300-2.500nm) referida a la del espectro solar estándar (fracción total de energía solar reflejada en las condiciones atmosféricas estándar anteriormente descritas). El espectro solar utilizado es el de la American Society for Testing and Materials (ASTM G173-03, 2003). Mediante este método se calcula la reflectividad solar total de la superficie R mediante la ecuación 3.
Donde r(λ) es la medida de la reflectancia espectral a cada longitud de onda de la superficie estudiada e i(λ) es la irradiancia espectral a la longitud de onda considerada, del espectro solar estándar de American Society for Testing and Materials (ASTM G173-03, 2003) [4].
Aproximadamente el 50% del flujo solar es absorbido por la superficie terrestre. Las superficies negras absorben hasta el 90% de la radiación, y su índice de reflexión solar SRI no supera el valor 10; las blancas absorben solo hasta un 25%, con un SRI superior a 75. Las superficies blancas se mantienen más frescas que las negras. Las superficies coloreadas presentan índices de reflexión solar SRI entre el 75 y el 10%. Los pigmentos blancos de base rutilo se ha utilizado como material refrigerante en techos de residencias, al presentar reflectividades R del orden del 87%; sin embargo, muchos propietarios prefieren techos no blancos por razones estéticas. Se pueden utilizar pigmentos de diferentes colores, pero como la coloración supone cierta absorción en el visible, deberá ser compensada con una mayor reflectividad en el infrarrojo. En este sentido, en la literatura se discuten diferentes coloraciones. Thongkanluang et al. [5] describen verdes basados en la eskolaita Cr2O3, utilizada en pinturas de camuflaje militar para prevenir la detección de objetos por detectores infrarrojos, al presentar reflectividades del orden del 50-57% en el entorno NIR; asimismo se ha utilizado en recubrimientos de techos de los edificios como capa refrigerante y de buena apariencia estética, así asumida en zonas como Tailandia. Para aumentar la reflectividad NIR de la eskolaita se añaden óxidos tales como Sb2O3, SiO2, Al2O3 o TiO2, con reflectividades NIR de R=84,8, 89,4, 98,1 y 96,0%, respectivamente [5]. Thongkanluang et al. [6] obtienen pigmentos marrones utilizando composites de hematita Fe2O3 con óxidos de alta reflectividad como los descritos anteriormente (el composite en polvo más reflectivo es la mezcla 70% Fe2O3 10% Sb2O3 12% SiO2 2% Al2O3 6% TiO2 con R=46,7%). Estos marrones vidriados al 5% en esmaltes cocidos a 1.100°C sobre pasta cerámica, no definida por los autores, presenta un 41,3% de reflectancia NIR [6]. Vishnu et al. [7] obtienen una gama de pigmentos amarillos dopando con Si4+ el molibdato de itrio (Y6MoO12) y también dopando con Mo(VI) el cerato de itrio (Y2Ce2O7). En ambos casos el mecanismo de color es la modificación de la banda de transferencia de carga O2p-Mo4d que disminuye el band gap de 3,01 a 2,44eV en el primer caso y de 2,60 a 2,45eV en el segundo. Los autores prueban los pigmentos en cementos pero no en vidriados cerámicos.
El modelo CMY utiliza los colores primarios cian (C), magenta (M) y amarillo (Y): cian es el opuesto al rojo, filtrándolo, de manera que su intensidad controla la cantidad de rojo que se mostrará. De la misma manera, el magenta filtra al verde y el amarillo al azul. Teóricamente, con los CMY primarios puros es posible obtener toda la gama de colores existente; sin embargo, en la práctica se añade el negro por varias razones: a)en primer lugar, con mezcla de cian, magenta y amarillo no es posible producir un negro perfecto; por otro lado, b)el uso de negro permite utilizar menor cantidad de tintas de color, abaratando el color; por último, c)las impresiones pueden tener mucho negro con el fondo en blanco, lo que supondría mucha tinta de color para producir un negro, que además es de inferior nitidez. Una paleta de pigmentos refrescante completa debe contener al menos la cuatricromía CMYK, siendo interesante además, por razones similares al negro, por su amplia utilización, sobre todo en oriente [5] y la tradición cerámica europea (al ser un pigmento distintivo desde su introducción en Sèvres [8], un verde.
El efecto combinado de la humedad y los rayos solares estimula el desarrollo de colonias de hongos y bacterias que ensucian y modifican de forma significativa las reflectividad de los recubrimientos. Los pigmentos deben presentar, además de una alta capacidad de tinción, alta durabilidad, así como alta opacidad para cubrir de forma eficiente la superficie coloreada. En el caso de pinturas, el dióxido de titanio destaca por su alto índice de refracción (2,73 para rutilo y 2,55 para anatasa) y presentar un blanco muy puro. La anatasa se utilizó a partir de 1918 como blanqueante y opacificante en sustitución de los pigmentos tradicionales tóxicos basados en Zn, Sb o Pb, como el blanco albayalde (PbCO3)2Pb(OH)2 o el blanco litopón (un coprecipitado equimolecular de BaSO4 y ZnS). En 1940 el rutilo sustituyó a la anatasa como opacificante en pinturas por su mayor capacidad de dispersión de la luz, dado su mayor índice de refracción y sobre todo por la resistencia a la disgregación y decoloración de los polímeros de las pinturas por su baja capacidad fotocatalítica comparada con la anatasa. La fotocatálisis utiliza los radicales (p.ej., hidroxilo HO) generados por la radiación UV-Vis al activar un semiconductor en medios húmedos (agua, aire) para oxidar contaminantes orgánicos. Sin embargo, la radiación ultravioleta del sol, en el intervalo 300-350nm, en conjunción con otros factores ambientales tales como el oxígeno, el ozono y contaminantes industriales, producen la despolimerización de los plásticos por oxidación fotoquímica (fotolisis). Tanto la anatasa como el rutilo absorben la radiación ultravioleta de la luz solar protegiendo a las pinturas de su degradación fotolítica, no de la fotocatalítica asociada al carácter semiconductor de la anatasa [9,10].
Algunas corporaciones ya han desarrollado una línea de pigmentos cool [11–13]. Sin embargo, hay pigmentos clásicos que presentan interesantes características como pigmentos refrescantes y con capacidad fotocatalítica. En un trabajo anterior [14] los autores analizaron dos familias CMY de pigmentos clásicos: los basados en circón y rutilo, así como una familia no clásica basada en la geikielita o ilmenita de magnesio MgTiO3. A partir de los resultados obtenidos, los mejores pigmentos fotocatalíticos y refrigerantes en vidriados convencionales del sistema ZnO-SiO2-CaO que maduran a 1.080°C (conocido como vidriado de monococción porosa o monoporosa) resultaron ser la paleta CMY basada en el turquesa de vanadio-circón (R=48% de reflectancia total en el intervalo NIR, SRI=56, Ts=61,4°C y periodo de semivida t1/2=117min para NaranjaII), magenta de hierro-ilmenita (R=67%, SRI=82, Ts=51,5°C y t1/2=493min) o de hierro-circón (R=65%, SRI=79, Ts=52,6°C y t1/2=145min.) y amarillo de Ni,Sb-rutilo (R=66%, SRI=80, Ts=52,1°C y t1/2=431min) o de Pr-circón (R=78%, SRI=97, Ts=45,7°C y t1/2=184min), respectivamente.
El objeto del presente trabajo es la caracterización de una cuatricromía de pigmentos cerámicos CMYK más un verde, de alta capacidad colorante, con altos valores de SRI para cada gama de color, y que además presentan capacidad fotocatalítica, lo que les confiere una capacidad autolimpiante y de eliminación de contaminantes del aire, tales como compuestos orgánicos resistentes (azoderivados, por ejemplo en aguas residuales) o compuestos orgánicos volátiles (COV) y NOx en el aire.
Material y métodosSe ha preparado una cuatricromía de pigmentos cerámicos CMYK más un verde por el método cerámico de reacción en estado sólido de los óxidos o carbonatos de los cationes correspondientes. En este método, los precursores se han homogeneizado en un molino de bolas en medio acetona; una vez evaporada la acetona, el polvo resultante se calcina en crisoles de porcelana en horno eléctrico, a la temperatura correspondiente en cada caso, manteniéndola un tiempo predeterminado en cada caso. Posteriormente el horno se apaga y enfría libremente. El polvo se ha lavado con adiciones de 16ml de agua por gramo de polvo, para eliminación de sales residuales hasta que la conductividad de las aguas de lavado es inferior a los 100μS. Los 5 pigmentos estudiados son:
- 1.
Cian, basado en el dopado con cobalto de la celsiana (Ba0,9Co0,1)Al2Si2O8 (monoclínico, grupo puntual 2/m, grupo espacial I 21/c), un feldespato[15], aunque su simetría es algo diferente a la de otros feldespatos. El cobalto substituye al bario. La configuración del bario en la celsiana tiene un oxígeno muy cerca, lo que tiene un efecto importante sobre los ángulos de enlace Si-O-Si [16]. En efecto, en la celsiana, Al y Si presentan un retículo parcialmente ordenado y el Ba presenta una configuración irregular con 10 oxígenos vecinos no equidistantes del Ba. Este desorden induce una baja simetría y aumenta la barrera cinética de nucleación de los cristales. Se utilizaron como precursores BaCO3 (Panreac), Co3O4 (Aldrich), Al(OH)3 (Panreac), SiO2 (cuarzo, Sibelco). La mezcla se calcina a 1.200°C, manteniendo la temperatura 3horas.
- 2.
Magenta, basado en el dopado con cromo de la armalcolita (MgFe)(Cr0,2Ti2,8Fe) O10 (ortorrómbica, grupo puntual 2/m2/m2/m y grupo espacial Bbmm), que es la estructura de un mineral detectado por primera vez en las rocas traídas en la primera exploración lunar en 1969. Su nombre proviene de las primeras letras de los astronautas de esta primera expedición lunar [17,18]: ARMstrong, Aldrin y COLlins. Su estequiometría y estado de oxidación es variable entre los extremos (Mg0,5Fe0,5)Ti2O5 (la detectada en las rocas lunares) y la ferroarmalcolita (armalcolita ferrian) (MgFe)(FeTi3)O10 con Fe(II) en el primer caso y Fe(III) en el segundo. Se utilizaron como precursores MgCO3, Cr2O3, anatasa TiO2 y hematita Fe2O3 (todos suministrados por Panreac). La mezcla se calcina a 1.000°C, manteniendo la temperatura 3horas.
- 3.
Amarillo, basado en el dopado con níquel de la geikielita (Mg0,5Ni0,5)TiO3, que pertenece al grupo de la ilmenita (FeTiO3) (trigonal, grupo puntual 3, grupo espacial R3). En la literatura se conoce bien la estabilidad y cristalización de la fase Co-ilmenita (CoTiO3) como pigmento cerámico. Relacionados con este sistema, los compuestos Mg2TiO4 con estructura espinela y MgTi2O5 con estructura pseudobrookita se consideran en la literatura como estructuras estabilizadas por entropía: su relativamente alta entropía se asocia con la mezcla en posiciones cristalográficas específicas de diferentes cationes [19,20]. Se utilizaron como precursores MgCO3, anatasa TiO2 (Panreac) y NiO (Prolabo). La mezcla se calcina a 1.000°C, manteniendo la temperatura 3horas.
- 4.
Verde, basado en la perovskita de cromo-neodimio CrNdO3 (ortorrómbica, grupo puntual (2/m 2/m 2/m), grupo espacial Pnma). Gargori [21] ha estudiado la síntesis y caracterización de nuevos pigmentos basados en perovskitas MNdO3 con M=Fe,Cr de coloración variable, pero con interés prioritario en coloraciones marrón-rojo en el caso de la perovskita de hierro-neodimio y de coloración verde o negra en el caso de la perovskita de cromo-neodimio cuando se mineraliza con fluoruros. La relajación del campo cristalino del retículo oxigenado por la entrada de fluoruro explicaría la evolución del color verde a tonalidades grises intensas en este caso. Se utilizaron como precursores Nd2O3(Aldrich) y Cr2O3 (Panreac). La mezcla se calcina a 1.100°C, manteniendo la temperatura 3horas.
- 5.
Negro, basado en la perovskita cromo-neodimio CrNdO3, anteriormente descrita, modificada con fluoruros por adición de 2% BaF2 y un 8%MgF2 en masa. Los fluoruros fueron suministrados por Panreac S.A., y como en el caso de su homólogo verde, la mezcla se calcina a 1.100°C, manteniendo la temperatura 3horas.
Se ha estudiado su capacidad fotocatalítica mediante el test con NaranjaII, un persistente colorante sulfonato monoazo C16H11N2SO4Na, que se utiliza ampliamente como colorante modelo en los estudios de fotodegradación fotocatalítica. El mecanismo de degradación de este compuesto está bien descrito en la literatura [9]. Para realizar el seguimiento de la cinética de fotodegradación de los substratos se realizó el montaje que aparece en la figura 1 con una lámpara de mercurio de media presión de 125W de potencia, con espectro de emisión que presenta tres líneas características a 254, 313 y 365nm, empleada como fuente de irradiación UV sobre la disolución contenida en un reactor de vidrio de cuarzo (que minimiza el filtrado de la radiación UV de la fuente), refrigerado por una camisa con corriente de agua. Se utilizaron disoluciones del colorante monoazo NaranjaII de concentración 0,6·10−4M tamponadas a pH7,4 con una mezcla de NaH2PO4·4H2O y Na2HPO4·7H2O (Panreac, S.A.) a la que se añade el polvo fotocatalizador en suspensiones de 500mg/l mantenidas en agitación continua. La degradación de NaranjaII se siguió por colorimetría a 480nm. Las curvas de fotodegradación se analizan según el modelo de Langmuir-Hinshelwood [10]. Con bajas concentraciones iniciales (Co) y con baja absorción por el fotocatalizador, este modelo cinético sigue la ecuación:
donde t=tiempo de irradiación, y C=concentración actual del colorante.Al representar ln(C/Co) frente al tiempo de irradiación, la cinética que sigue el modelo Langmuir-Hinshelwood presenta una ajuste lineal, siendo la pendiente de la recta la constante aparente de velocidad de primer orden Kapp. El tiempo de semivida (t1/2) se puede calcular considerando las expresiones:
Las muestras en polvo se caracterizaron por difracción de rayosX de polvo orientado al azar en un difractómetro Siemens D5000 con radiación Cu Kα en el intervalo 10-70°2θ, velocidad de barrido 0,05°2θ/s, constante de tiempo 10s y condiciones de 40kV y 20mA. Con los polvos se obtuvieron piezas vidriadas con esmaltes al 5% en peso en una frita convencional de bicocción de composición ZnO-SiO2-CaO (1.050°C).
El color de las plaquetas vidriadas se midió mediante los parámetros de color L*a*b* siguiendo la metodología Commission International de l’Eclairage (CIE) utilizando el espectrómetro Jasco V670, con iluminante D65 y observador 10°. En este método, L* mide la claridad (100=blanco, 0=negro), a* y b* miden el chroma (−a*=verde, +a*=rojo, −b*=azul, +b*=amarillo) [22]. La caracterización microestructural de los polvos se realizó con un microscopio electrónico de Scanning Electron Microscopy (SEM) Leo-440i de LEYCA.
Para la estimación del índice de reflexión solar SRI se midió la reflectividad solar total (TSR, o simplemente R) de la superficie mediante la técnica de espectrometría por reflectancia difusa UV-Vis-NIR (300-2.500nm) referida a la del espectro solar estándar, mediante un espectrómetro Jasco V670 de las muestras en polvo y piezas vidriadas de acuerdo con el método anteriormente descrito [23]. Por último, para evaluar la reemisividad de la muestra negra en el intervalo MIR se utilizó un espectrómetro de infrarrojo por transformada de Fourier modelo Tensor 27, Bruker, con una fuente MIR y con el accesorio de ATR modelo Platinum ATR, Bruker con cristal de diamante. Con este accesorio se pueden obtener espectros en la región del infrarrojo entre 4.000cm−1 y 600cm−1 (2.500-17.000nm). La Attenuated Total Reflection (ATR) es una técnica de muestreo, utilizada en el IR, que se basa en el fenómeno que se produce cuando una radiación infrarroja entra en un cristal ATR transmisor y de alto índice de refracción. El cristal está diseñado para permitir una reflexión interna total que crea una onda evanescente sobre la superficie del cristal. Esta onda se extiende a la muestra que se mantiene en contacto íntimo con el cristal, registrándose el espectro de infrarrojo de la muestra.
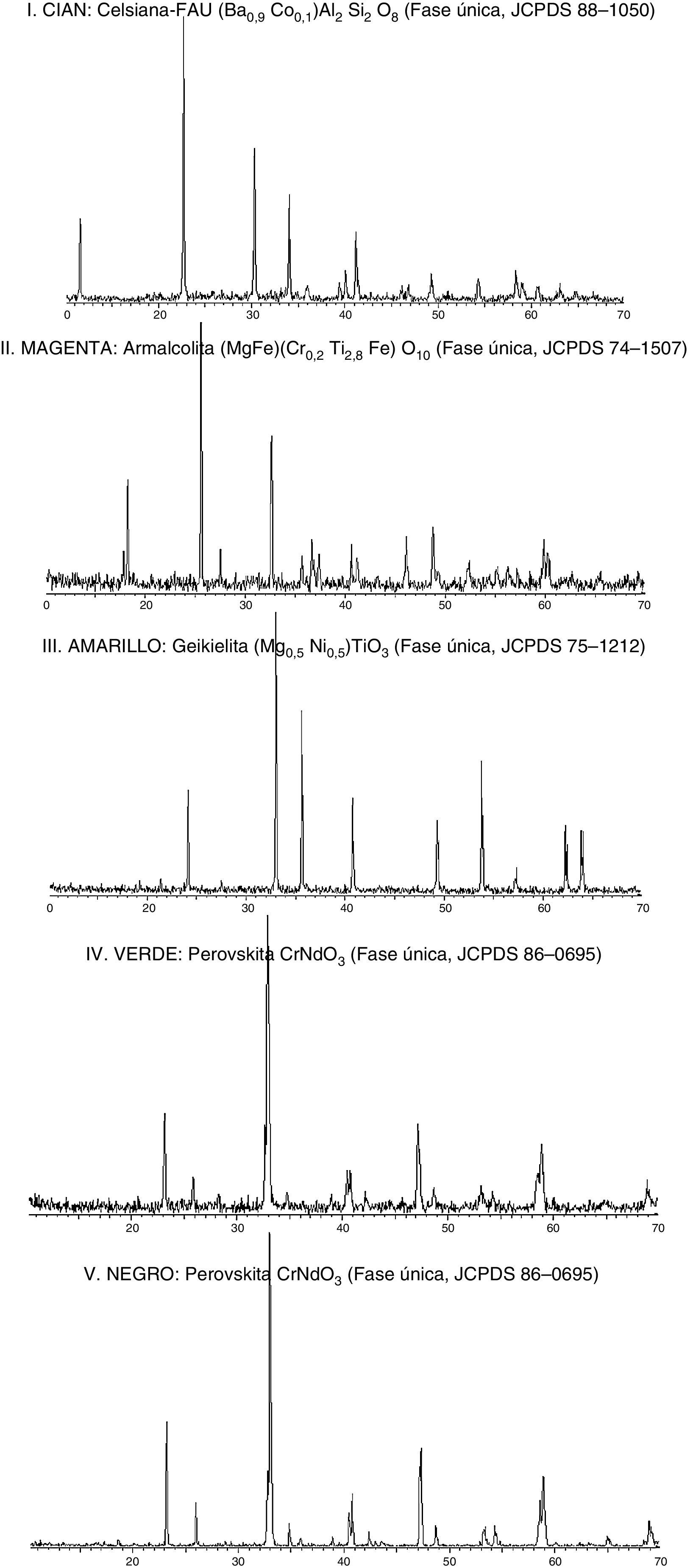
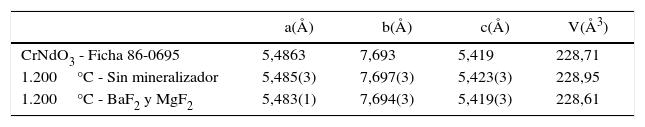
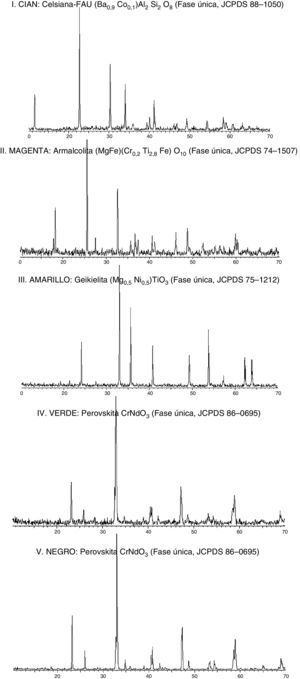
Resultados y discusiónEn la figura 2 se presenta la DRX (difracción de rayosX) de los polvos, donde se detecta en todos los casos la fase única de la disolución sólida correspondiente. En el caso de la perovskita, con el fin de diferenciar entre la coloración verde y la azul, se han medido los parámetros reticulares de la celda de la perovskita NdCrO3 verde (sin mineralizador) y la negra (con mineralizador haluro alcalinotérreo) mediante el programa DICVOL91 [24], que se presentan en la tabla 1. Se observa una ligera contracción de la celda. El tamaño de Ba2+ es mayor que Nd3+, y el Mg2+ es más pequeño que aquellos (radios de Pauling: Nd3+=98,3pm, Ba2+=135pm, Mg2+=72pm), además el F− es también ligeramente más pequeño que el O2− (F−=133pm, O2−=140pm) [25], por lo que la entrada en la red de los iones alcalinotérreos sustituyendo a Nd3+, compensada por la de flúor por oxígeno, sería consistente con los datos de la tabla 1 y explicaría el comportamiento de la muestra modificada con BaF2 y MgF2. La relajación del campo cristalino del retículo oxigenado por la entrada de fluoruro explicaría la evolución del color verde a tonalidades grises intensas en este caso.
Parámetros reticulares de los polvos de los pigmentos lavados en función del mineralizador utilizado en la síntesis de CrNdO3
| a(Å) | b(Å) | c(Å) | V(Å3) | |
|---|---|---|---|---|
| CrNdO3 - Ficha 86-0695 | 5,4863 | 7,693 | 5,419 | 228,71 |
| 1.200°C - Sin mineralizador | 5,485(3) | 7,697(3) | 5,423(3) | 228,95 |
| 1.200°C - BaF2 y MgF2 | 5,483(1) | 7,694(3) | 5,419(3) | 228,61 |
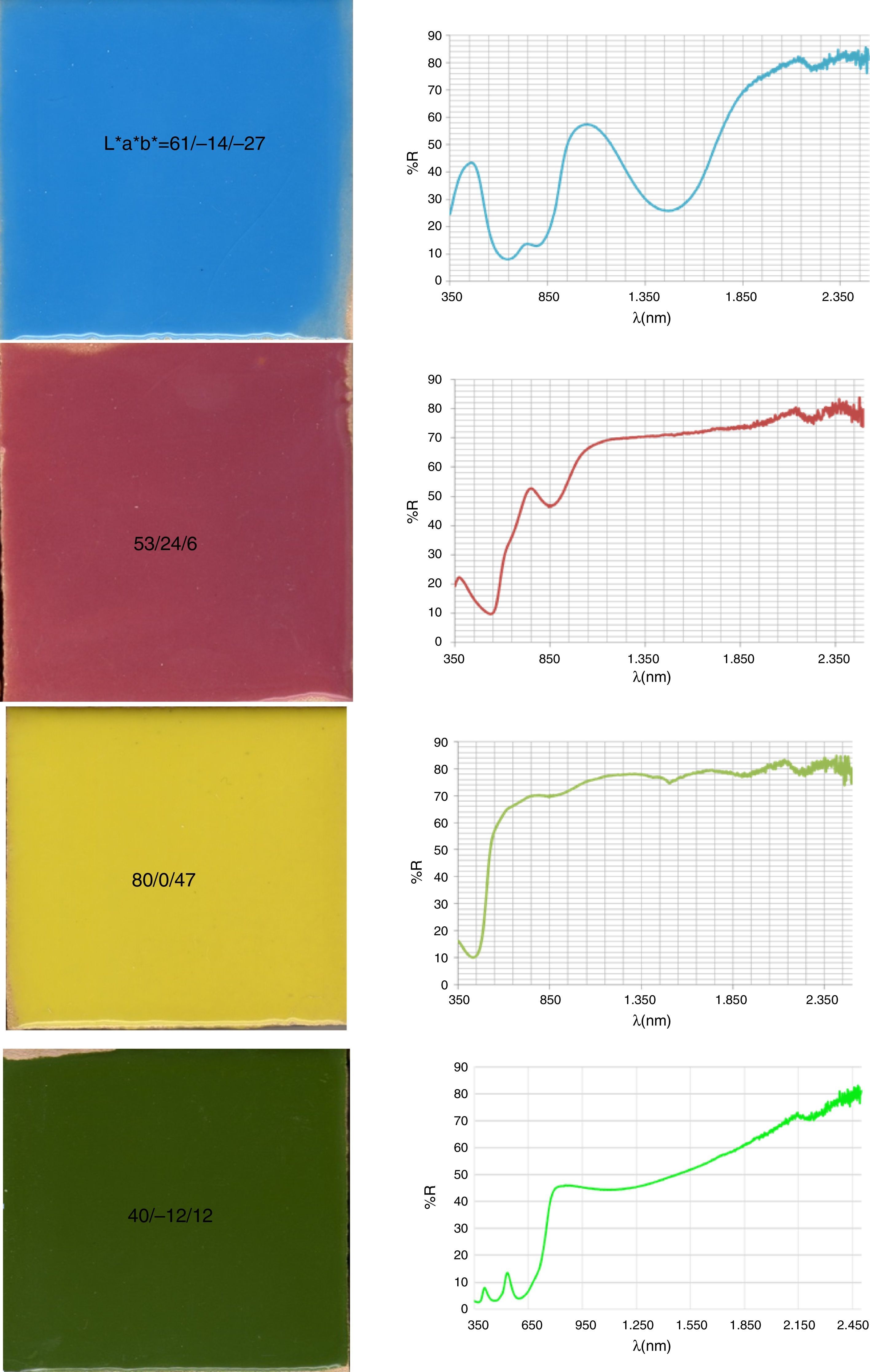
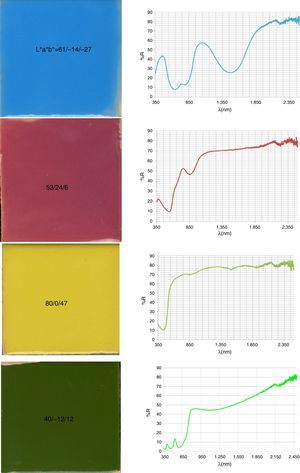
En la figura 3 se presenta la fotografía de los polvos y de las plaquetas vidriadas con esmalte al 5% en frita transparente de bicocción (1.050°C) de los cinco pigmentos analizados con sus valores CIEL*a*b*. Asimismo con fines comparativos, al final de la tabla 2 se presentan los datos de la familia CMY del circón descritos en la referencia [14] con frita de monoporosa y los obtenidos con la frita de bicocción. Al utilizar la frita de bicocción que madura a temperatura un poco más baja (1.050°C frente a los 1.080°C de la monoporosa utilizada en el estudio [14], la intensidad del color aumenta (L* baja, caso del cian) o se mantiene en valores similares, los valores del chroma aumentan en el turquesa (b* más negativo) pero disminuyen ligeramente en el coral de circón (a* disminuye) y el amarillo de praseodimio (b* disminuye).
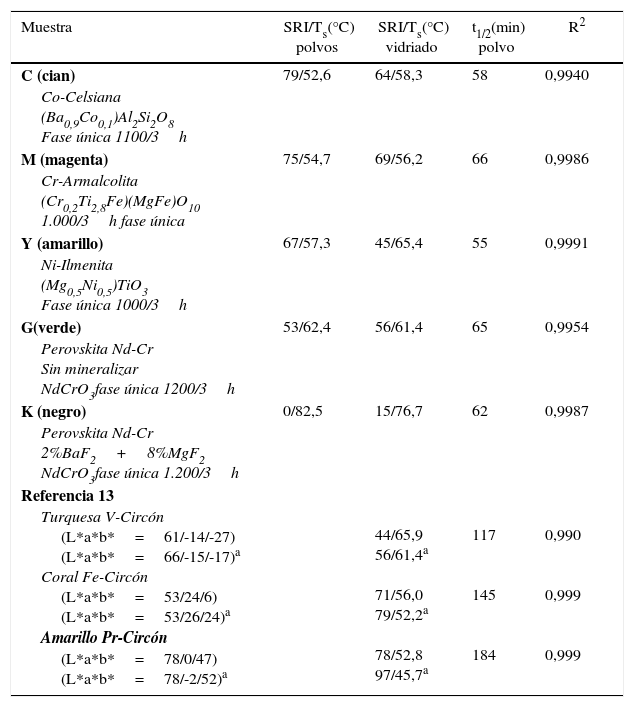
Valores de índice de reflexión solar (SRI), temperatura de equilibrio térmico Ts y parámetros de Langmuir-Hinshelwood en el test fotocatalítico con Naranja II con los polvos de los pigmentos estudiados y los pigmentos CMY de la familia del circón vidriados con esmaltes al 5% en frita de bicocción
| Muestra | SRI/Ts(°C) polvos | SRI/Ts(°C) vidriado | t1/2(min) polvo | R2 |
|---|---|---|---|---|
| C (cian) Co-Celsiana (Ba0,9Co0,1)Al2Si2O8 Fase única 1100/3h | 79/52,6 | 64/58,3 | 58 | 0,9940 |
| M (magenta) Cr-Armalcolita (Cr0,2Ti2,8Fe)(MgFe)O10 1.000/3h fase única | 75/54,7 | 69/56,2 | 66 | 0,9986 |
| Y (amarillo) Ni-Ilmenita (Mg0,5Ni0,5)TiO3 Fase única 1000/3h | 67/57,3 | 45/65,4 | 55 | 0,9991 |
| G(verde) Perovskita Nd-Cr Sin mineralizar NdCrO3fase única 1200/3h | 53/62,4 | 56/61,4 | 65 | 0,9954 |
| K (negro) Perovskita Nd-Cr 2%BaF2+8%MgF2 NdCrO3fase única 1.200/3h | 0/82,5 | 15/76,7 | 62 | 0,9987 |
| Referencia 13 Turquesa V-Circón (L*a*b*=61/-14/-27) (L*a*b*=66/-15/-17)a Coral Fe-Circón (L*a*b*=53/24/6) (L*a*b*=53/26/24)a Amarillo Pr-Circón (L*a*b*=78/0/47) (L*a*b*=78/-2/52)a | 44/65,9 56/61,4a 71/56,0 79/52,2a 78/52,8 97/45,7a | 117 145 184 | 0,990 0,999 0,999 |
Al comparar los valores L*a*b* de la paleta estudiada (fig. 3) con los del circón (tabla 2 y fig. 5) se observa una intensidad de coloración superior (L* inferior) en la paleta objeto de estudio frente a la paleta del circón. En cambio, el chroma de las coloraciones obtenidas con los pigmentos del circón es superior al de la paleta considerada (b* negativo para el cian, a* positivo para el magenta o b* positivo para el amarillo).
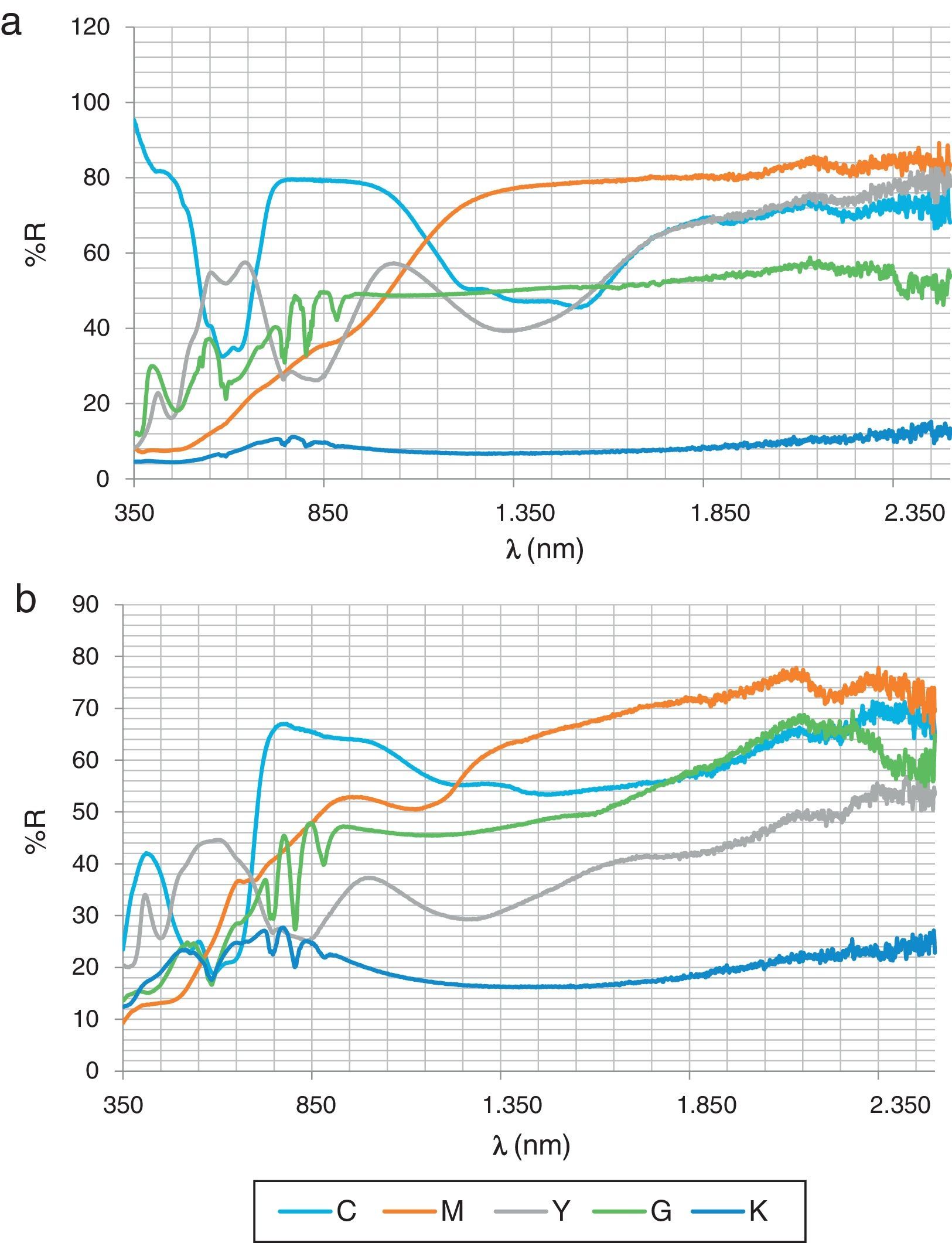
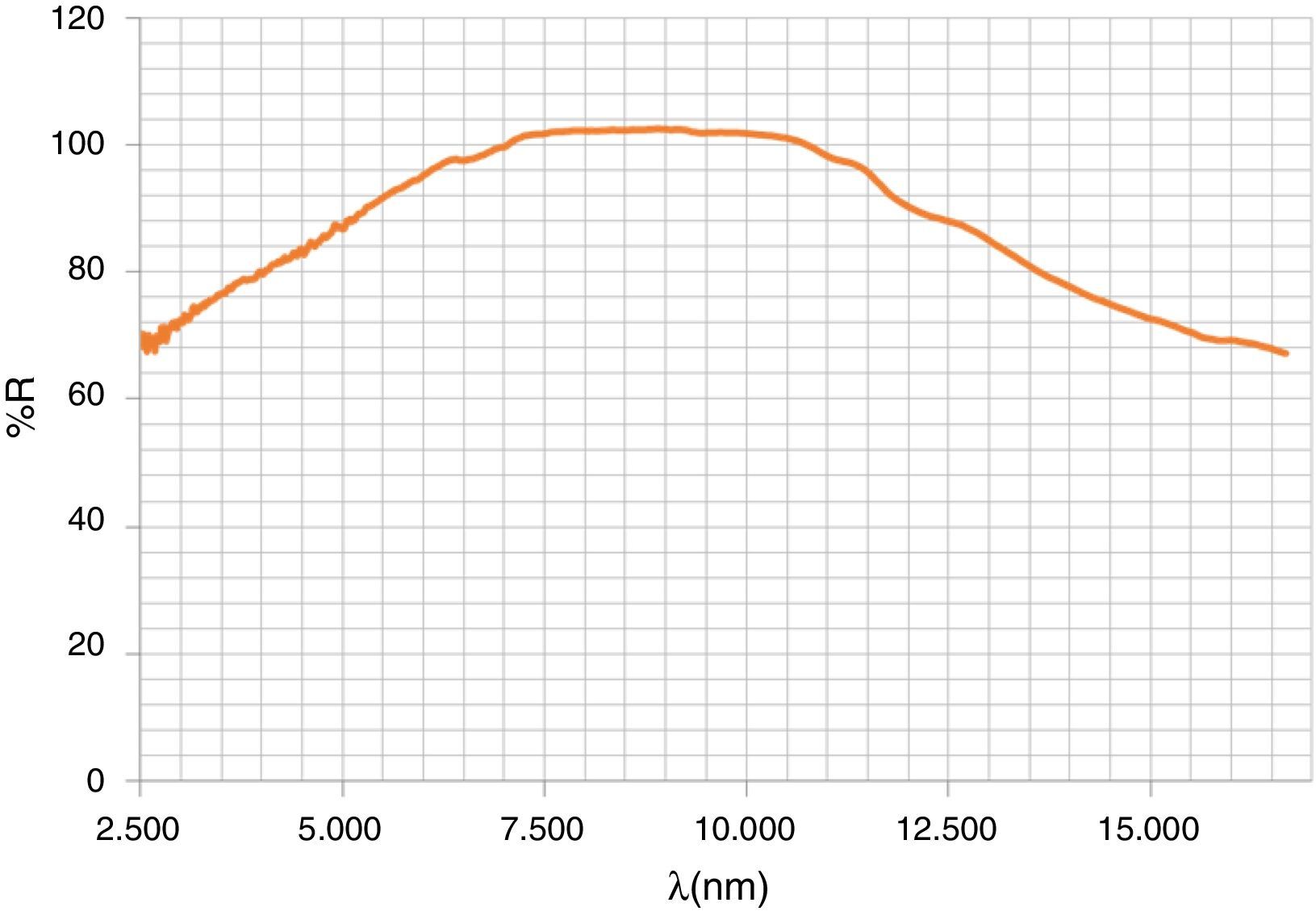
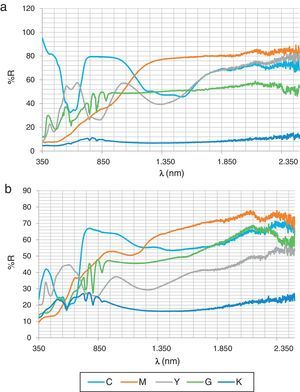
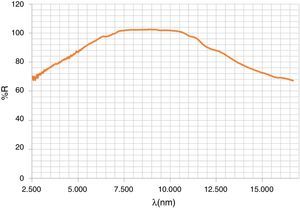
En la figura 4 se presenta el espectro Vis-NIR de los polvos (fig. 4a) y de las baldosas vidriadas con esmaltes al 5% en frita de bicocción (1.050°C) (fig. 4b). A partir de las reflectividades del espectro y mediante la metodología descrita anteriormente, en la tabla 2 se presentan los valores de índice de reflexión solar (SRI), temperatura de equilibrio térmico Ts de los pigmentos estudiados y de los pigmentos CMY de la familia del circón utilizados como en la referencia [14] y los obtenidos con la frita de bicocción. Los resultados indican valores SRI superiores en el caso de magenta y amarillo de los circones de hierro y praseodimio que en el magenta de armalcolita (2 puntos menos en frita de bicocción) y amarillo de geikielita (33 puntos menos en frita de bicocción). En el caso de la celsiana, el valor de SRI supera al del vanadio-circón en 20 puntos al vidriarlos en frita de bicocción. En el caso del verde, el valor de SRI de la perovskita vidriada supera ligeramente a la eskolaita Cr2O3 (Panreac S.A.), cuyo espectro de la pieza vidriada se presenta en la figura 5 (SRI=52) y que se ha tomado como referencia para este color. La perovskita negra NdCrO3 modificada con los mineralizadores fluoruro presenta valores SRI muy bajos (SRI=0 en el caso del polvo), lo que la hace interesante como pigmento para sustratos absorbentes de la radiación en colectores solares de absorción, atendiendo a que su emisividad en el infrarrojo medio es alta, tal y como evidencia el espectro de infrarrojos MIR de la figura 6.
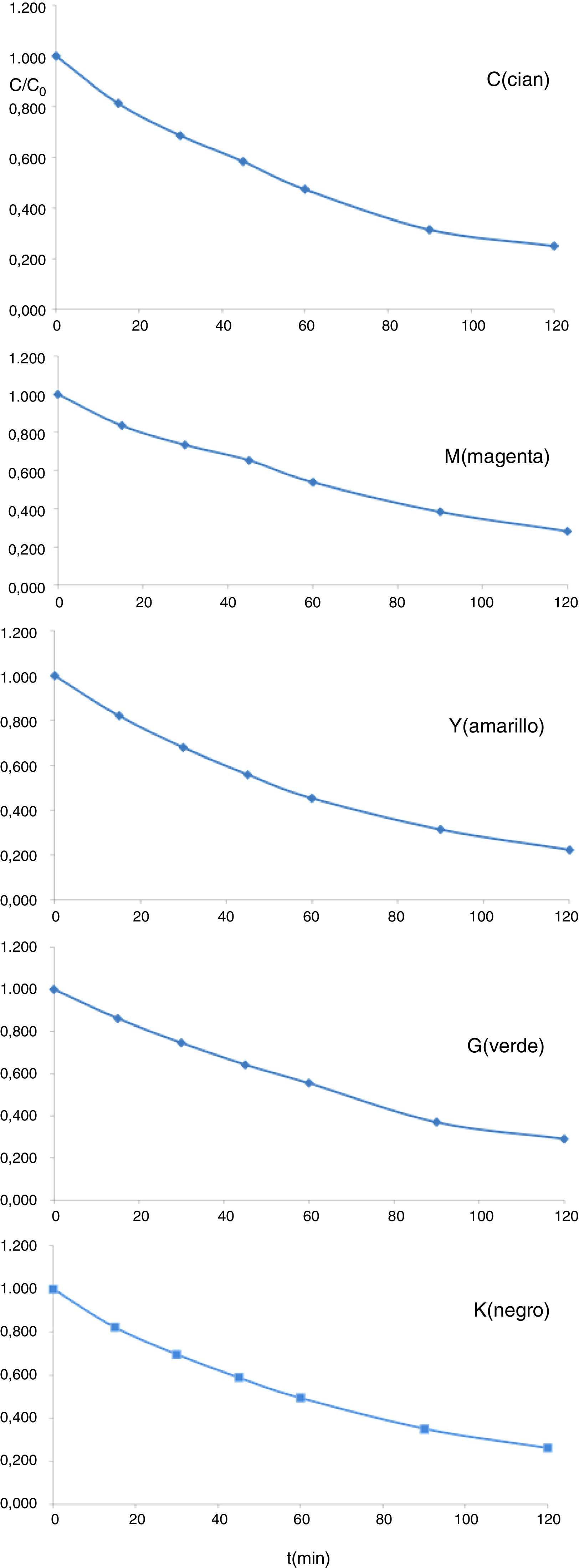
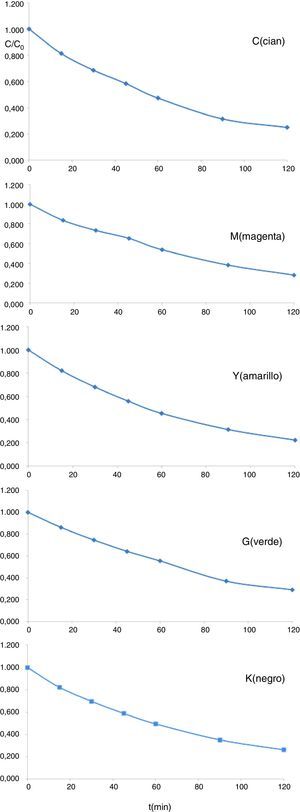
En la figura 7 se presentan las curvas de fotodegradación en el test de degradación fotocatalítica de NaranjaII y en la tabla 2 los parámetros de Langmuir-Hinshelwood (t1/2 y el cuadrado del coeficiente de correlación lineal R2 de la recta obtenida) de los polvos de los pigmentos estudiados y de los pigmentos CMY de la familia del circón descritos en la referencia [14]. En el caso de los polvos objeto de estudio el test da resultados en torno a 55-70min de periodo de semivida que resultan ser inferiores a los medidos con los pigmentos del circón de referencia, con periodos de semidegradación en el intervalo de 110-190min.
En la figura 8 se presentan las micrografías SEM de los polvos lavados, donde se observan partículas finas con tamaños entre 0,5-5μm formando agregados en todos los casos. En el caso de la perovskita negra NdCrO3 modificada con fluoruros, se observa una mayor sinterización del material con tamaños ligeramente mayores de las partículas
ConclusionesSe han preparado por el método cerámico composiciones optimizadas de una cuatricromía CMYK más un pigmento verde basadas en el dopado de cobalto en celsiana (Ba0,9Co0,1)Al2Si2O8 (cian), de cromo en armalcolita (MgFe)(Cr0,2Ti2,8Fe)O10 (magenta), de níquel en geikielita (Mg0,5Ni0,5)TiO3 (amarillo), la perovskita CrNdO3 (verde) y la misma perovskita mineralizada con fluoruros alcalinotérreos (BaF2 y MgF2) (negro). Los pigmentos en polvo y vidriados con un esmalte al 5% en una frita convencional de bicocción (1.050°C) se han caracterizado respecto de su rendimiento colorimétrico mediante el modelo CIEL*a*b*, su capacidad refrigerante (como cool pigments) mediante la medida del índice de reflexión solar SRI y su capacidad fotocatalítica mediante el test de degradación de NaranjaII. Los resultados obtenidos se comparan con los obtenidos con pigmentos comerciales de la familia CMY del circón. La coloración de los polvos y de las plaquetas vidriadas con un esmalte al 5% en frita transparente de bicocción (1.050°C) es intensa, y comparada con la coloración de pigmentos comerciales de la familia CMY del circón, los valores indican una intensidad superior (L* inferior). En cambio el chroma de las coloraciones obtenidas con los pigmentos del circón es superior al de la paleta estudiada (b* negativo para el cian, a* positivo para el magenta o b* positivo para el amarillo). Con relación a su capacidad refrigerante, los resultados indican valores SRI superiores en el caso de magenta y amarillo en los circones de hierro y praseodimio que en el magenta de armalcolita (3puntos menos) y amarillo de geikielita (33puntos menos); en el caso de la celsiana, el valor de SRI supera al del vanadio-circón en 20puntos. En el caso del verde, el valor de SRI de la perovskita vidriada utilizando frita de bicocción supera ligeramente a la eskolaita Cr2O3 que se ha elegido como referencia La perovskita negra presenta valores SRI muy bajos (SRI=0 en el caso del polvo) que, asociados a valores de emisividad altos en el infrarrojo medio MIR, la hace interesante como pigmento para sustratos absorbentes en colectores solares. La capacidad fotocatalítica de los pigmentos analizados, en las condiciones de síntesis descritas, medida por el test de fotodegradación de NaranjaII, indica valores de periodo de semivida en torno a 55-70min, inferiores a los medidos con los pigmentos del circón de referencia (110-190min).
Los autores agradecen la financiación de la Universidad Jaume I (Proyecto P1.1B2015-19) y del Ministerio de Educación (Proyecto MAT2015-69443-P).