La evaluación inicial de la insuficiencia cardíaca apunta a la valoración de la función ventricular, la indagación de la etiología, los factores pronósticos y la decisión terapéutica inicial. El presente artículo evalúa el rol de las principales técnicas de imagen cardíaca no invasiva (excluyendo al ecocardiograma) en cada uno de estos aspectos. Se analiza puntualmente la utilidad de la radiografía de tórax, la angiotomografía coronaria, la resonancia magnética y los estudios de medicina nuclear, tanto para patología isquemiconecrótica como para otras causas no revascularizables.
Initial evaluation of heart failure is directed to ventricular function analysis, etiological investigation, prognostic factors evaluation and initial therapeutic decision. This article summarizes the role of non-invasive cardiac imaging (excluding echocardiogram) in every aspect. Utility of thoracic radiology, coronary computed tomography angiogram, cardiac magnetic resonance and nuclear medicine studies (spect myocardial perfusion and PET-CT) is analyzed, not only in the setting of ischemic cardiomyopathy but also in the rest of the etiological spectrum.
La evaluación inicial de la insuficiencia cardíaca (IC) está orientada a cuatro aspectos principales: determinar la función del ventrículo izquierdo, evaluar la posible etiología, definir el tratamiento inicial y su respuesta y analizar los factores pronósticos. Las imágenes cardíacas no invasivas pueden proporcionar información sobre todas las variables mencionadas.
Radiografía de tóraxLa radiografía de tórax es una herramienta diagnóstica ampliamente utilizada debido a su alta disponibilidad, rapidez, bajo costo y baja exposición a la radiación1.
Las guías de distintas sociedades de cardiología recomiendan la radiografía de tórax para la evaluación inicial de los pacientes con sospecha de insuficiencia cardíaca, ya que permite detectar cardiomegalia, signos de congestión pulmonar o descartar otras condiciones asociadas a la sintomatología del paciente2–4.
El índice cardiotorácico (ICT) medido en la proyección posteroanterior (PA) debe ser menor a 0,5. Sin embargo, un aumento en la silueta cardíaca no siempre indica cardiomegalia, ya que otras condiciones, como el derrame pericárdico, pueden simular un agrandamiento cardíaco. Además, en la proyección anteroposterior (AP) en decúbito utilizada en pacientes hospitalizados, la magnificación del mediastino puede aumentar artificialmente el índice cardiotorácico, lo que debe ser tomado en cuenta en la interpretación1.
La morfología de la silueta cardíaca puede sugerir patologías específicas. Por ejemplo, una silueta en “botella” o “matraz” sugiere la presencia de líquido pericárdico. Asimismo, la visualización de calcificaciones valvulares, miocárdicas o pericárdicas también puede orientar a un diagnóstico específico1.
La congestión pulmonar se manifiesta en la radiografía de tórax a través de hallazgos progresivos, dependiendo de la severidad del compromiso hemodinámico y el aumento de la presión venosa pulmonar:
- 1.
Redistribución vascular: prominencia de las venas pulmonares superiores en relación con las inferiores, lo que indica redistribución del flujo pulmonar debido al aumento de la presión venosa4.
- 2.
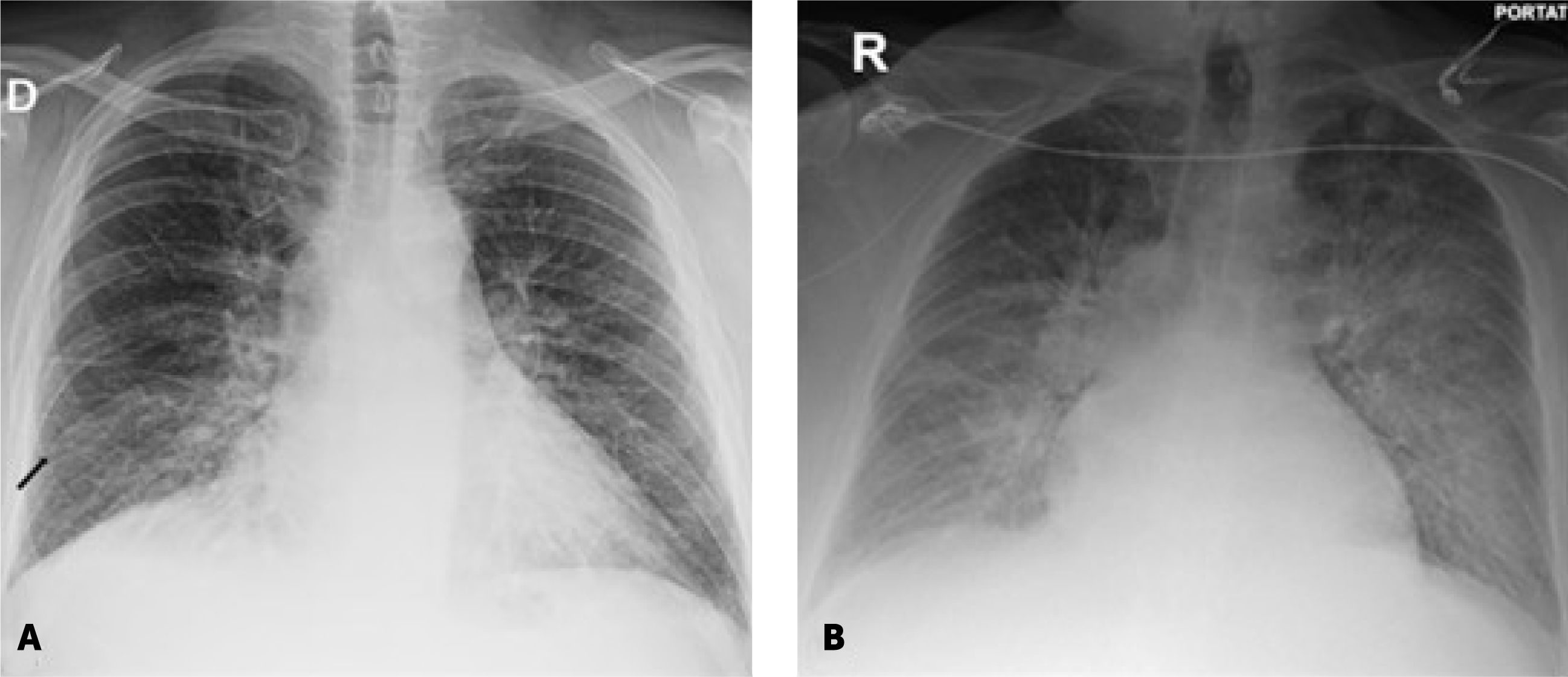
Edema intersticial: los signos radiográficos que sugieren acumulación de líquido en el intersticio pulmonar incluyen: engrosamiento peribronquial, líneas septales (líneas B de Kerley) y engrosamiento de las cisuras pleurales1,4 (figura 1A).
Figura 1.Radiografía de tórax A: En proyección posteroanterior (PA) que muestra opacidades instersticiales de predominio basal, con presencia de líneas B de Kerley (flecha negra), hallazgos compatibles con edema pulmonar intersticial. B: Radiografía portátil de tórax en proyección anteroposterior (AP), que muestra opacidades bilaterales de distribución central predominante, sugestivas de edema pulmonar alveolar, y aumento difuso de la densidad craneocaudal compatible con derrame pleural.
- 3.
Edema alveolar: cuando la presión capilar pulmonar continúa aumentando, el líquido extravasa hacia los alvéolos, lo que provoca edema alveolar. Este se manifiesta en la radiografía como opacidades alveolares bilaterales de predominio central, adoptando una morfología característica en “alas de murciélago”1 (figura 1B).
La insuficiencia cardíaca también puede asociarse a derrame pleural, el cual se detecta en la radiografía como una obliteración de los recesos costofrénicos en proyecciones de pie o como aumento difuso de la densidad del hemitórax comprometido en una proyección en decúbito1.
En el contexto hospitalario, la radiografía de tórax es fundamental para el seguimiento evolutivo de los pacientes con insuficiencia cardíaca congestiva, el control del posicionamiento de tubos y líneas, y la detección de complicaciones asociadas a estos procedimientos o de catéteres o dispositivos no reportados en la anamnesis inicial del paciente5.
Tomografía computada cardíaca (TCC)La TCC juega un rol importante en la evaluación de la insuficiencia cardíaca, principalmente en la detección de patología ateromatosa coronaria como causa de la insuficiencia.
Corresponde a una tomografía computada que se obtiene con sincronización electrocardiográfica, lo que permite reducir los artefactos por movimiento cardíaco, obteniendo así imágenes nítidas; y reconstruir imágenes en las distintas fases del ciclo. Tiene alta resolución espacial, con los equipos de última generación de hasta 0,1mm, y alta resolución temporal, indispensables para evaluar las arterias coronarias, pequeñas y en constante movimiento. Dependiendo de la información requerida, el estudio puede realizarse en una única fase del ciclo, habitualmente diástole para obtener imágenes nítidas quietas, o un estudio con todas las fases del ciclo cardíaco, que logra además reconstrucciones del corazón en movimiento, pudiendo entonces cuantificar función, volúmenes y movimiento valvular.
Un examen de óptima calidad diagnóstica requiere una frecuencia cardíaca idealmente estable y de alrededor de 60-65 latidos por minuto, por lo que habitualmente se premedica con betabloqueadores. Por el pequeño tamaño de las arterias coronarias, es ideal administrar vasodilatadores, habitualmente nitroglicerina sublingual o isosorbida, para mejorar su visualización y aumentar la representación del lecho coronario distal, lo que se lleva a cabo durante el examen. Se inyecta medio de contraste endovenoso para opacificar el lumen de las estructuras cardiovasculares, siendo necesario entonces descartar posibles contraindicaciones como reacciones alérgicas o daño renal importante.
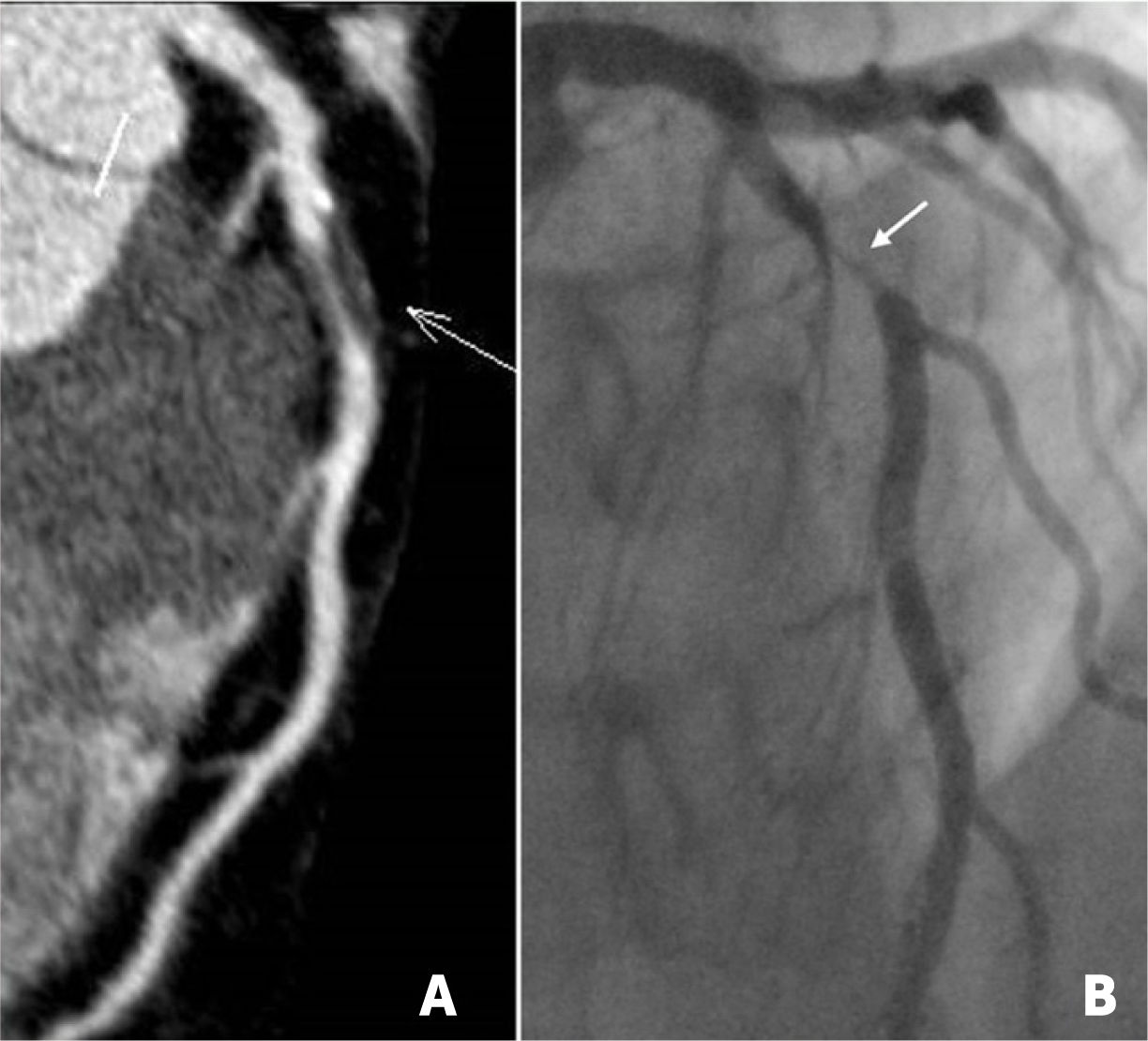
La principal indicación de la TCC es la evaluación de la anatomía coronaria, especialmente para detección y caracterización del compromiso ateromatoso. Tiene alto valor predictivo negativo para excluir la enfermedad coronaria ateromatosa; y en caso de existir, permite cuantificarla y caracterizarla, en cuanto a ubicación, extensión, grado de estenosis, composición de las placas y presencia de características de alto riesgo, información fundamental en el pronóstico y tratamiento de los pacientes (figura 2). Se ha demostrado que un mayor volumen total de placa ateromatosa en el árbol coronario se asocia a mayor riesgo de eventos coronarios, independiente del grado de estenosis que producen6, y que las placas de alto riesgo se asocian a mayor riesgo de síndrome coronario agudo en pacientes con dolor agudo y a mayor riesgo de eventos adversos cardiovasculares en pacientes con dolor estable7.
a y 2b. Ateromatosis de arteria descendente anterior (flechas blancas), con reconstrucción multiplanar en TC cardíaca que demuestra placa fundamentalmente no calcificada que determina estenosis mayor a 70% (a), y angiografía convencional que confirma una estenosis severa (b). Figura 2c. TC con reconstrucción en el eje corto que demuestra placa con características de alto riesgo en arteria descendente anterior (flecha amarilla), con placa de baja densidad con remodelamiento positivo y calcificación puntiforme.
Con el objetivo de lograr una mejor comunicación con el médico tratante, de estratificar el riesgo de los pacientes y facilitar la toma de decisiones, se creó la clasificación CAD-RADS (Coronary Artery Disease-Reporting and Data System), que separa a los pacientes en distintas categorías según la gravedad del compromiso ateromatoso, sugiriendo, además, manejo clínico6,7.
Además de caracterizar anatómicamente las placas ateromatosas con TCC, existe la posibilidad de agregar información fisiológica sobre su significancia hemodinámica, con simulación por tomografía computada de la reserva fraccional de flujo (FFR-CT), o con estudio de perfusión miocárdica por TC con adenosina. La FFR-CT y el estudio de perfusión por TC tendrían resultados comparables, y un rol complementario cuando se agregan a la TC cardíaca convencional, mejorando la especificidad, el valor predictivo positivo y la precisión en el diagnóstico8, al identificar las estenosis hemodinámicamente significativas que se beneficiarían de tratamiento endovascular o quirúrgico.
La TCC permite evaluar también el resto de la anatomía y función cardíaca, incluyendo tamaño de cavidades, grosor y contractilidad miocárdica, anatomía y función valvular, pericardio.
TCC en insuficiencia cardíacaParticularmente en el contexto de insuficiencia cardíaca, la mayor utilidad del examen es la evaluación del compromiso ateromatoso coronario, que permite diferenciar cardiopatía isquémica de no isquémica.
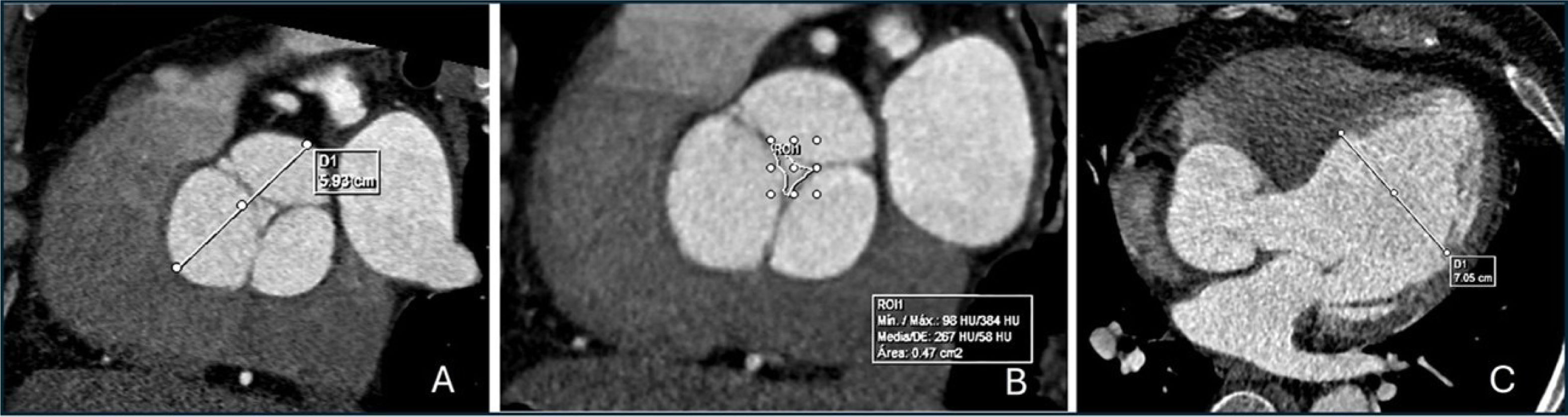
En el caso de valvulopatías, define con alta resolución espacial la anatomía valvular, caracterizando la morfología, presencia de engrosamiento y calcificaciones, medición de áreas de apertura y cierre por planimetría, y además la repercusión de estas alteraciones en el tamaño de las cavidades cardíacas y su función (figura 3).
No es el examen de primera línea en la evaluación de patología valvular, pero estaría indicado cuando las imágenes por ecocardiografía no son óptimas. En casos de estenosis aórtica con bajo flujo y bajo gradiente, la TCC está indicada para cuantificar las calcificaciones valvulares, e identificar así las estenosis que son severas, ya que el grado de calcificación de la válvula se relaciona con el grado de estenosis9. En el contexto de válvulas protésicas, es muy útil para identificar obstrucción y dehiscencia; y en el caso de endocarditis, la presencia de complicaciones como abscesos, pseudo aneurismas, fístulas, leaks o fugas paravalvulares. Además, está indicado como estudio preoperatorio para planificar la instalación de válvulas percutáneas, siendo la más frecuente la aórtica.
La TCC ayuda en la caracterización de patología estructural, como miocardiopatía hipertrófica, hipertrabeculación del ventrículo izquierdo o patología congénita que favorezca la insuficiencia cardíaca. En casos de enfermedades infiltrativas, miocarditis o síndrome Tako-Tsubo, aporta en la evaluación estructural y funcional en general, que puede ser complementaria a ecocardiografía o resonancia.
Otra utilidad descrita es en el mapeo de la anatomía venosa coronaria y venosa pulmonar, para guiar procedimientos.
En resumen, la TCC es un examen diagnóstico no invasivo de primera línea en la evaluación anatómica de la enfermedad coronaria ateromatosa. Además, permite evaluar estructura y función cardíaca, apoyando el diagnóstico y tratamiento de pacientes con insuficiencia cardíaca. Es muy importante conocer la hipótesis diagnóstica antes de realizar el estudio, para programar el examen adecuadamente y responder así a la pregunta clínica.
Resonancia magnética cardíaca (RMC)La RMC es una técnica no invasiva y libre de radiación ionizante que permite evaluar en un solo estudio la estructura y función del corazón.
Se ha transformado en una importante herramienta para la evaluación de la insuficiencia cardíaca por su papel clave en el diagnóstico, pronóstico y tratamiento.
Utiliza un campo magnético y ondas de radio para generar imágenes de alto contraste, de buena resolución espacial (menor que TCC y ecografía) y excelente resolución temporal, superior a la TCC, aunque menor que la ecografía.
Los campos magnéticos más utilizados son de 1,5 y 3 Tesla, equivalentes a 20 000 y 60 000 veces la gravedad terrestre. Este campo es constante, incluso si el equipo está apagado. Esto determina la primera y más importante norma de seguridad en resonancia magnética (RM): ningún objeto ferromagnético puede entrar al área del equipo. Todo debe ser compatible con RM, incluidas camillas, equipos de anestesia, tubos de oxígeno y dispositivos en los pacientes como prótesis, marcapasos, bombas, coils entre otros. Para consultar la seguridad de diferentes dispositivos en RMC, se puede acceder al sitio web mrisafety.com.
Dado que el corazón está en movimiento constante, las imágenes se sincronizan con el ECG. Esto permite obtener imágenes en distintas fases del ciclo cardíaco, tanto dinámicas como estáticas.
Los estudios se componen de una serie de secuencias diseñadas para responder a la pregunta diagnóstica del paciente. Por esta razón, contar con los antecedentes clínicos es esencial para orientar el examen de manera adecuada.
Las aplicaciones generales son diversas, abarcando el estudio de la morfología cardíaca, la función, perfusión y caracterización del miocardio, los flujos a través de vasos y válvulas, y caracterización de tumores.
Es un estudio largo (entre 30 a 45 minutos) y requiere una frecuencia lo más regular posible. Se obtienen imágenes en los planos cardíacos estándar (eje corto, 2, 3 y 4 cámaras), con secuencias rápidas y sincronizadas con ECG, que permiten visualizar en 2D el corazón y los grandes vasos y con las secuencias de cine, el movimiento cardíaco en tiempo real. Estas secuencias, a través de softwares dedicados, permiten analizar cualitativa y cuantitativamente las aurículas y los ventrículos, siendo el gold standard para la evaluación de los volúmenes ventriculares, la fracción de eyección y la masa miocárdica.
Además, es excelente para estudiar contractilidad global y segmentaria, las válvulas cardíacas y el pericardio.
En relación a la caracterización del miocardio, la RMC puede estudiar la estructura del tejido cardíaco mediante secuencias específicas como los mapas paramétricos (MP) y el realce tardío (RT). Cada tejido tiene propiedades únicas de relajación (T1, T2 y T2*) que se modifican con los cambios en su composición y que se cuantifican mediante los mapas paramétricos. Como ejemplos tenemos el valor T2, que aumenta con el edema, el valor de T1 que se eleva en patologías inflamatorias e infiltrativas y disminuye en la enfermedad de Fabry o hemocromatosis y que además permite determinar el volumen extracelular (VEC) que aumenta en enfermedades infiltrativas. Un T2* bajo se asocia a infiltración tisular por fierro.
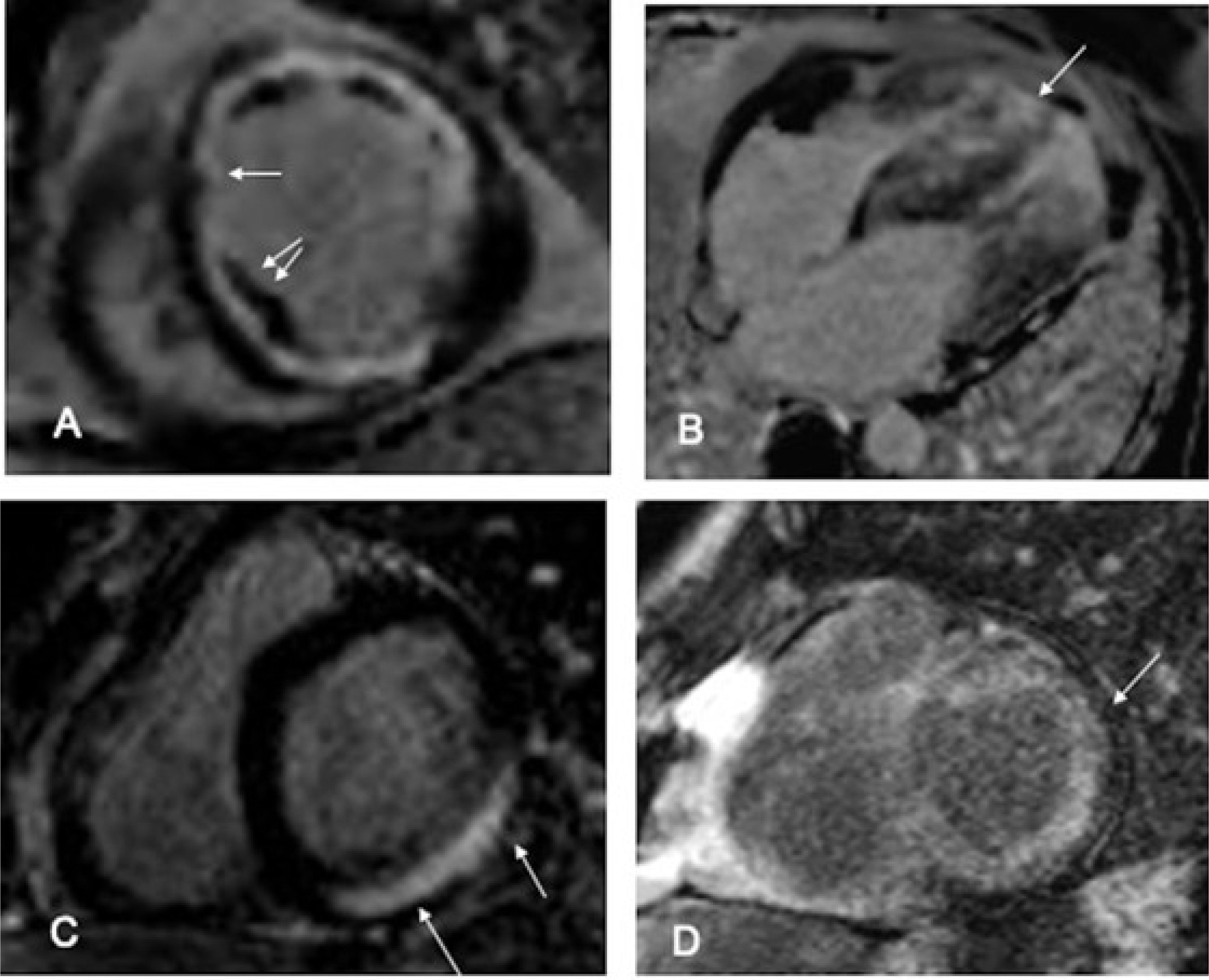
En el realce tardío se administra contraste endovenoso que se elimina rápidamente del tejido sano. Si hay daño celular (ej. infarto, miocarditis) (figuras 4a y 4c) o aumento del espacio extracelular (ej. fibrosis, infiltración), el contraste se retiene (figura 4b y 4d). La localización y patrón del realce orientan el diagnóstico.
Cardio RM Realce Tardío. A- Patrón isquémico, con RT subendocárdico (flecha) que refleja necrosis celular. Las zonas hipointensas en el espesor del realce corresponden a obstrucción microvascular (flecha doble) B- Miocardiopatía hipertrófica, con hipertrofia de pared, con patrón parcheado intramiocárdico (flecha) reflejando fibrosis. C- Miocarditis, con patrón subepicárdico (flechas) que evidencia inflamación con daño celular. D- Amiloidosis, con patrón subendocárdico-transmural difuso (flecha), que refleja la infiltración del miocardio por proteínas de amiloide con aumento del VEC.
La perfusión del miocardio se evalúa en tiempo real con el paso del contraste a través del miocardio. Así se identifican zonas isquémicas o infartadas permitiendo realizar estudios de perfusión de estrés con adenosina. También se observa la vascularización de tumores cardíacos.
Respecto a la evaluación del flujo sanguíneo, mediante secuencias phase contrast se analiza la velocidad y dirección del flujo sanguíneo que permite calcular gradientes de presión, volúmenes de eyección y detectar estenosis o insuficiencia en válvulas y vasos. Asimismo, se pueden realizar secuencias angiográficas.
RMC en insuficiencia cardíaca (IC)La RMC se recomienda cuando la información ecocardiográfica es insuficiente o cuando se sospecha de una miocardiopatía específica, en los síndromes coronarios con coronariografía limpia, y estudio pre trasplante, entre otros. Las últimas guías de consenso de expertos, Europea3 y Americana2, muestran las indicaciones de la RM en la IC, que se resumen en la tabla 1.
Recomendaciones para la evaluación con imágenes cardíacas. Guías ACC-AHA para el manejo de la insuficiencia cardíaca 2022
| CR | Recomendaciones |
|---|---|
| 1 | En pacientes con IC sospechada, de reciente diagnóstico o aguda descompensada, debería realizarse Rx tórax para evaluar tamaño cardíaco, congestión pulmonar y otras enfermedades que pudieran contribuir al cuadro |
| 1 | En pacientes con ETT no adecuado, se recomiendan imágenes alternativas para la evaluación de la función ventricular (resonancia cardíaca, tomografía cardíaca o imágenes nucleares) |
| 2a | En pacientes con IC o miocardiopatía, la RMC puede ser útil para el diagnóstico y manejo |
| 2a | En pacientes con IC, puede ser útil la evaluación de posible enfermedad isquémica para identificar la causa y guiar el manejo |
| 2b | En pacientes con IC y enfermedad coronaria que sean candidatos a revascularización, las imágenes de estrés no invasivas (eco estrés, SPECT, RMC o PET) pueden ser consideradas para la detección de isquemia miocárdica que ayude a guiar la revascularización coronaria |
Abreviaciones: CR: Clase de recomendación; NE: Nivel de evidencia; DL: datos limitados; NR: estudios no aleatorizados; IC: insuficiencia cardíaca; ETT: ecocardiograma transtorácico; RMC: resonancia magnética cardíaca.
En el diagnóstico y etapificación de la IC resulta útil para clasificar y estratificar la gravedad a través de la evaluación de los volúmenes cardíacos, la masa miocárdica y la fracción de eyección de ambos ventrículos. También contribuye al estudio de la disfunción diastólica en pacientes con IC con fracción de eyección conservada10.
Una vez establecido el diagnóstico, las secuencias de RT permiten detectar el origen isquémico, observándose un patrón subendocárdico distribuido en territorio coronario (figura 4a).
Si no es isquémico y se sospecha una miocardiopatía, las secuencias de caracterización (T1, T2 y T2*) y los distintos patrones de RT pueden detectar enfermedades infiltrativas o inflamatorias como miocarditis (figura 4c), sarcoidosis, enfermedad de Fabry, enfermedad de Chagas, sobrecarga de hierro, amiloidosis (figura 4d), etc. También determinan la fibrosis y el VEC en distintos tipos de miocardiopatías (figura 4b).
En cuanto al pronóstico, la detección y cuantificación de la fibrosis y tejido cicatricial mediante RT, se asocia a pronóstico más desfavorable con aumento de efectos adversos y mortalidad10.
Limitaciones de la RMCA pesar de sus ventajas, la RMC tiene algunas limitaciones:
- •
Duración prolongada, requiere un paciente estable y cooperador.
- •
Contraindicada en personas con dispositivos incompatibles o claustrofobia severa (puede requerir anestesia).
- •
El uso de gadolinio no se recomienda en insuficiencia renal grave (filtración glomerular <30ml/min) por riesgo de fibrosis sistémica nefrogénica.
- •
Las arritmias pueden dificultar la adquisición de imágenes, aunque existen técnicas para minimizar este efecto.
La enfermedad coronaria constituye la principal causa de insuficiencia cardíaca con fracción de eyección disminuida11. El deterioro de la función ventricular en estos casos puede ser el resultado de isquemia, necrosis, remodelado ventricular, hibernación miocárdica, disincronía ventricular o una combinación de los mismos.
La evaluación de la etiología isquémica de la insuficiencia cardíaca en la aproximación inicial del paciente con insuficiencia cardíaca resulta esencial, no sólo por su frecuencia, sino por constituir una de las pocas causas con disponibilidad de tratamiento específico, que puede contribuir tanto a mejorar el pronóstico de los pacientes como a disminuir los enormes costos sanitarios que la patología genera.
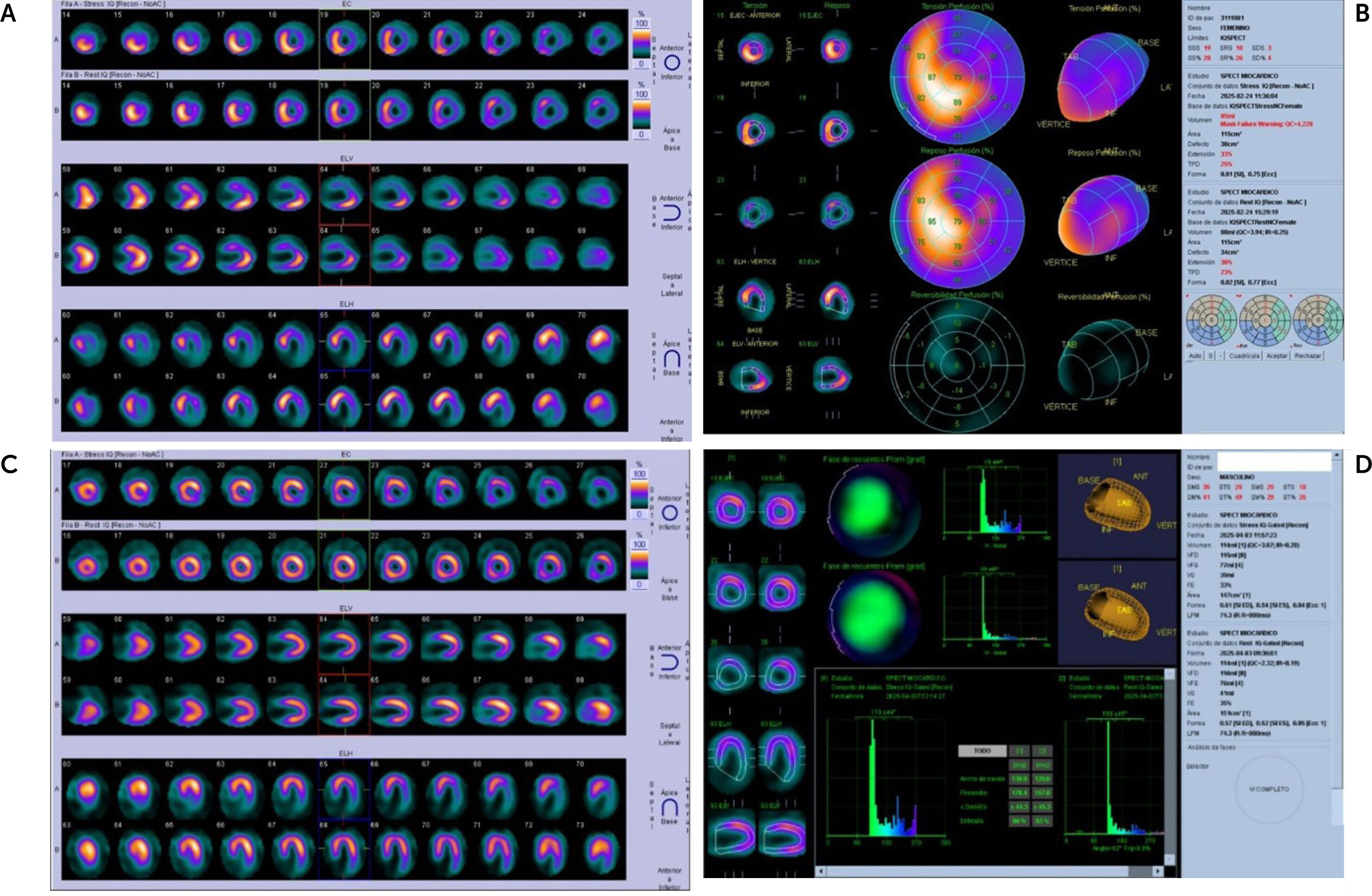
En este contexto, la medicina nuclear ofrece un significativo aporte, permitiendo en un solo estudio evaluar la geometría y función ventricular, confirmar o descartar la etiología isquemiconecrótica, evaluar y cuantificar la extensión y severidad de los defectos de perfusión, estimar pronóstico, diferenciar entre isquemia, necrosis e hibernación, cuantificar viabilidad, contribuir a la decisión terapéutica y guiar la revascularización de acuerdo a los hallazgos de los territorios arteriales comprometidos, y analizar la sincronía ventricular12 (figura 5).
A. Cintigrama miocárdico dobutamina-reposo de paciente con miocardiopatía dilatada isquemiconecrótica: cortes de perfusión con extensa secuela de necrosis transmural en territorios de DA y Cx, sin desarrollo de isquemia. B. Mapa polar con cuantificación de captación, sin evidencia de viabilidad significativa. C. Cintigrama miocárdico esfuerzo-reposo de paciente con deterioro severo de FEVI: desarrollo de extensa isquemia en territorio de Cx. D. Mapa polar de fase e histograma de fase que evidencian disincronía ventricular.
El cintigrama miocárdico gatillado con 99mTc-SestaMIBI se realiza con protocolo de reposo-esfuerzo o apremio farmacológico con dipiridamol, adenosina o dobutamina. La adquisición se sincroniza con el trazado electrocardiográfico permitiendo evaluar la motilidad y el engrosamiento parietal sistólico. Puede realizarse en pacientes con insuficiencia renal o alergia al contraste ya que no requiere inyección de contraste nefrotóxico, así como en pacientes con dispositivos o claustrofobia. Una perfusión miocárdica normal excluye la etiología isquemiconecrótica de la insuficiencia cardíaca, obligando a reorientar la evaluación hacia causas no revascularizables.
La perfusión miocárdica también puede ser medida con trazadores de PET para evaluar flujo miocárdico, aunque su costo y falta de disponibilidad la hace un estudio poco accesible por el momento en la mayoría de los países.
La evidencia del beneficio de la revascularización versus tratamiento médico óptimo en miocardiopatía isquemiconecrótica ha resultado conflictiva en los últimos años, tanto en la evaluación de la isquemia como de la viabilidad13. El estudio más reciente que evaluó la evolución de más de 40 000 pacientes durante 11 años definió que los pacientes con deterioro de la función ventricular presentan beneficios con la revascularización cuando su monto isquémico es mayor al 10%14.
Por el momento, la tendencia a la hora de definir la posibilidad de revascularización continúa considerando el porcentaje de miocardio en riesgo, es decir, la suma del miocardio isquémico más el miocardio viable. Con este fin se utilizan diferentes scores (de suma, de reposo, diferencial) así como la cuantificación del porcentaje de miocardio comprometido.
Numerosos trabajos proporcionan evidencia de beneficio de revascularización sobre tratamiento médico óptimo cuanto mayor es el porcentaje de miocardio viable15,16, a pesar de existir información controversial en otros estudios17.
Es importante considerar factores adicionales en esta evaluación, ya que también se ha demostrado que presentan mayor beneficio con la revascularización pacientes de menor edad, mayor deterioro de la función sistólica, y mayor carga de enfermedad aterosclerótica.
La medicina nuclear ofrece dos tipos de estudios que permiten evaluación de viabilidad miocárdica. El primero, el SPECT gatillado con 99mTc-SestaMIBI, resulta más accesible ya que es el mismo que se utiliza para evaluar isquemia y debería ser el primero en solicitarse de no tener estudios previos de evaluación no invasiva. Existe, sin embargo, un porcentaje de casos en los que el estudio no evidencia viabilidad significativa, que sí puede ser detectada por el PET con 18FFDG, que presenta mayor sensibilidad y ha demostrado mejorar el pronóstico cuando existe adherencia a la recomendación terapéutica18.
El SPECT gatillado, además de evaluar isquemia y viabilidad, permite estimar la fracción de eyección del ventrículo izquierdo, incluso en pacientes con mala ventana ecocardiográfica, y hace posible la visualización dinámica de la geometría ventricular.
Uno de los parámetros evaluados en el estudio es la presencia de disincronía ventricular. A través del análisis del histograma de fase y el mapa polar de fase, es posible brindar información de utilidad a la hora de definir la terapia de resincronización cardíaca (TRC) en pacientes con bloqueo de rama izquierda y deterioro severo de la función sistólica, ya que ha sido demostrado que el beneficio es mayor cuando el catéter de estimulación se coloca en una localización que no tenga necrosis significativa, y preferiblemente en el último segmento viable de activación mecánica del ventrículo izquierdo19,20.
Por último, no debemos olvidar que alrededor del 50% de los pacientes presenta insuficiencia cardíaca con fracción de eyección conservada, con significativa morbilidad y mortalidad y un amplio abanico de etiologías asociadas. En este contexto, las guías recomiendan el estudio de causas con tratamiento específico, como la amiloidosis cardíaca. Las guías 2022 del American College of Cardiology/American Heart Association recomiendan con nivel de evidencia 1b la realización de cintigrama con pirofosfato para aquellos pacientes con sospecha clínica de amiloidosis y estudios negativos para cadenas livianas en sangre y orina2. En estos pacientes la gammagrafía con 99mTc-PYP, DPD o HMDP con SPECT presenta 100% de especificidad y valor predictivo positivo para amiloidosis por transtiretina (ATTR), permitiendo evitar la biopsia endomiocárdica en aquellos con grado 2 o 3 de positividad en el estudio21.
La amiloidosis cardíaca debe sospecharse en pacientes con insuficiencia cardíaca con fracción de eyección preservada que presenten engrosamiento de la pared ventricular, especialmente si se acompaña de voltajes bajos de QRS, estenosis aórtica severa, síndrome del túnel carpiano, o polineuropatía autonómica o sensitiva.
En la tabla 1 se resumen las principales indicaciones de imágenes cardíacas no invasivas en la evaluación inicial de la insuficiencia cardíaca, de acuerdo a las Guías de la American Heart Association y American College of Cardiology2.
ConclusiónUna adecuada evaluación diagnóstica inicial del paciente con insuficiencia cardíaca permite acortar los tiempos diagnósticos, proveer mayor exactitud en el diagnóstico etiológico y la guía terapéutica inicial y optimizar recursos para el sistema sanitario. Para ello es esencial la comunicación entre el médico tratante y el especialista en imágenes, con el fin de definir el mejor método a utilizar, adecuado a las características puntuales y sospecha diagnóstica de cada paciente, planificar y ajustar los protocolos de adquisición para cada paciente según la sospecha clínica.
Como guía general, la evaluación inicial incluye la radiografía de tórax y el ecocardiograma transtorácico. En segundo lugar, es necesario evaluar una posible etiología coronaria. En este sentido es posible realizar una angiotomografía para la evaluación de la anatomía coronaria, o estudios no invasivos funcionales para la evaluación y cuantificación de la isquemia. De acuerdo a las preferencias del médico, las condiciones del paciente y la disponibilidad y costos, se puede optar entre el ecocardiograma de estrés, la RMC y el cintigrama miocárdico. Estos estudios permiten además la evaluación de la viabilidad miocárdica.
En el caso de patologías valvulares, infiltrativas o estructurales, los mayores aportes son proporcionados por la TC y la RMC.
El trabajo en equipo y la permanente comunicación entre los diferentes especialistas involucrados en el diagnóstico y tratamiento de estos pacientes son fundamentales para garantizar la celeridad, selección adecuada de métodos diagnósticos y optimización de recursos necesaria para el abordaje de esta patología.
Consideraciones éticasSe aclara que se han seguido los protocolos institucionales de Clínica Las Condes relacionados con la publicación de datos de pacientes, sujetos a privacidad y con consentimiento informado en los casos pertinentes.
Declaración de conflictos de interesesNo se declaran conflictos de intereses por parte de los autores.
FinanciamientoNo se ha recibido financiamiento en relación al presente artículo.