El síndrome antifosfolípido (SAF) es una enfermedad autoinmune sistémica, caracterizada por trombosis recurrente, que puede afectar la circulación arterial y venosa.
ObjetivoAnalizar las diferencias inmunológicas y farmacológicas, así como los desenlaces clínicos de una cohorte de pacientes con SAF primario y secundario.
Materiales y métodosEstudio de corte transversal que incluyó 352 pacientes con diagnóstico de SAF atendidos entre los años 2014 y 2018. Se analizaron variables sociodemográficas, clínicas e inmunológicas y se realizó un análisis univariado y un análisis bivariado mediante la prueba chi-cuadrado para determinar diferencias entre los pacientes con SAF primario y SAF secundario. Finalmente, se hizo un análisis multivariado para buscar asociaciones con los desenlaces clínicos trombóticos en los pacientes con SAF.
ResultadosLa edad promedio de la población fue de 42,4±14años; el 84,6% correspondió a sexo femenino. El 67,6% de los pacientes tenía diagnóstico de SAF primario y un 32,4% de SAF secundario, siendo el lupus eritematoso sistémico (LES) la enfermedad asociada en un 84%. Dentro de los eventos trombóticos, el más frecuente fue la trombosis venosa profunda (17,3%), seguida por el ataque cerebrovascular (9,9%). En los eventos obstétricos existió una prevalencia del 39,4% para abortos. No se encontraron diferencias en el perfil sociodemográfico ni en el perfil inmunoserológico entre los pacientes con diagnóstico de SAF primario y aquellos con SAF secundario. Los eventos trombóticos tuvieron mayor frecuencia en el grupo de SAF primario, pero solo la tromboembolia pulmonar alcanzó significación estadística. Eventos obstétricos como los abortos no fueron diferentes entre ambos grupos. Dentro de los factores asociados a los eventos trombóticos, se encontró que el sexo femenino tiene una probabilidad 5 veces mayor de accidente cerebrovascular y 3 veces mayor de trombosis venosa profunda. Los anti-β2GPI tipo IgM aumentaron alrededor de 3 veces la probabilidad de presentar abortos en mujeres con SAF.
ConclusiónSe presenta una de las cohortes colombianas más grandes de pacientes con SAF reportadas hasta el momento en la literatura. La población es comparable clínica y sociodemográficamente con lo encontrado en otros estudios, aunque la prevalencia de SAF primario fue mayor y las complicaciones trombóticas fueron menores. La tromboembolia pulmonar fue significativamente mayor en el grupo de SAF primario.
Antiphospholipid syndrome (APS) is a systemic autoimmune disease characterized by recurrent thrombosis that can affect the arterial and venous circulation.
ObjectiveTo analyze the immunological and pharmacological differences, as well as the clinical outcomes of a cohort of patients with primary APS and secondary APS.
Materials and methodsA retrospective cohort study was conducted that included 352 records of patients diagnosed with APS and treated between 2014 and 2018. A description is presented of the sociodemographic, clinical, and immunological profile of the population. A bivariate analysis performed using the chi-squared test to determine differences between groups with primary APS and secondary APS, and finally a multivariate analysis to search for associations with thrombotic clinical outcomes in patients with APS.
ResultsThe mean age was 42.4±14 years, and 84.6% were females. Two-thirds (67.6%) of the patients had a diagnosis of primary APS, and 32.4% of secondary APS, of which 84% were associated with systemic lupus erythematosus (SLE). Among the thrombotic events, the most frequent were deep vein thrombosis (17.3%) and stroke (9.9%). Obstetric events were frequent, with a prevalence of 39.4% for miscarriages. No differences were found in the sociodemographic or immunoserological profile when comparing the group of primary vs. secondary APS. Thrombotic events were more frequent in the primary APS group, although only pulmonary embolism reached statistical significance. There were no differences between the two groups as regards obstetric events, such as miscarriages. Women were found to be 5 times more likely to have a stroke and 3 times more to have deep vein thrombosis. The anti-β2GPI type IgM increased the probability of presenting miscarriages about 3 times in women with APS.
ConclusionThe study contains one of the largest Colombian cohorts with APS reported so far, and although it is both clinically and sociodemographically similar to other cohorts, there is a higher prevalence of primary APS. There was a lower frequency of thrombotic complications compared to other cohorts. Patients with primary APS had a tendency to develop thrombosis, as has already been reported in the literature.
El síndrome antifosfolípido (SAF) es una enfermedad sistémica autoinmune caracterizada por trombosis recurrente que puede afectar la circulación arterial y venosa. Es una de las trombofilias adquiridas más comunes, con una incidencia de 5 casos por 100.000 personas al año. Ocurre en el 1% de la población general, tiene predilección por el sexo femenino y puede ser primario o secundario. Aproximadamente la mitad de los pacientes con SAF tiene una presentación primaria, mientras que la otra mitad se encuentra asociada a otras patologías1, siendo el lupus eritematoso sistémico (LES) la enfermedad asociada más frecuente. Un tercio de los pacientes con LES tiene anticuerpos antifosfolípidos, pero solo el 5-10% de ellos desarrollará un SAF2. Se han encontrado diferencias entre SAF primario y secundario; una de las más importantes radica en que en el SAF asociado a LES existe una mayor frecuencia de artritis, livedo reticularis, trombosis venosa y pérdidas fetales3. Sin embargo, los datos de cohortes que comparen SAF primario y secundario son limitados.
Dentro de las manifestaciones clínicas más frecuentes se encuentran las trombosis del sistema venoso profundo de las extremidades y de la circulación arterial cerebral. De forma menos frecuente, puede ocurrir trombosis en otros sitios como las venas hepáticas, venas viscerales o circulación venosa cerebral. Las manifestaciones obstétricas son igualmente importantes, incluyendo muerte fetal sin otras causas, abortos recurrentes o parto pretérmino4. Otros escenarios como el SAF catastrófico son infrecuentes: se presentan en menos del 1% de los pacientes con SAF y conllevan una alta mortalidad. El SAF catastrófico se caracteriza por el compromiso trombótico en 3 o más órganos de forma simultánea o en rápida sucesión, en presencia de anticuerpos antifosfolípidos y con confirmación histopatológica de trombosis de vaso pequeño en ausencia de inflamación a este nivel. Suele desencadenarse por infecciones y sus principales complicaciones son compromiso cerebral y cardiaco, infecciones y falla multiorgánica5.
Los criterios clasificatorios establecen que debe cumplirse al menos un criterio clínico y uno de laboratorio. Dentro de los criterios clínicos se encuentran los episodios de trombosis y los eventos obstétricos que incluyen muerte fetal luego de la semana 10 de gestación, 3 o más abortos antes de la semana 10 y parto pretérmino antes de la semana 34, relacionado con síndromes hipertensivos del embarazo o restricción del crecimiento intrauterino4. Pueden encontrarse otras manifestaciones clínicas no criterio como trombocitopenia, livedo reticularis, úlceras de piel y ataques isquémicos transitorios5. Dentro de los criterios de laboratorio se encuentra la positividad persistente en el tiempo (mayor de 12 semanas) de anticoagulante lúpico, anti-beta2glicoproteína I (anti-β2GPI) o anticuerpos anticardiolipinas IgG o IgM4.
La evidencia local en este tema es limitada. A la fecha solamente se encuentran reportados en la literatura 3 trabajos de cohortes colombianas con SAF. Dos de los estudios se llevaron a cabo en la ciudad de Medellín6,7 en centros de referencia de enfermedades autoinmunes y el tercero en una población del suroccidente colombiano8. En Medellín, Vargas et al. describieron 62 pacientes con diagnóstico de SAF por criterios de Sapporo y encontraron que aquellos con SAF primario tenían una edad de inicio más tardía y se asociaban con mayor frecuencia de pérdidas fetales. Por otro lado, el SAF secundario en la mayoría de los casos se asoció con LES, siendo los eventos trombóticos de tipo venoso la manifestación más frecuente. Desde el punto de vista inmunoserológico, los anticuerpos anticardiolipinas fueron los más prevalentes en esta cohorte de pacientes, con presencia en el 93,4% de los pacientes6. En el año 2012 Mesa et al. describieron otra cohorte de 100 pacientes con SAF en quienes detallaron las manifestaciones clínicas no criterio, es decir, aquellas que no caben dentro de los criterios diagnósticos pero hacen parte del espectro de la enfermedad. De estas manifestaciones, las de tipo neurológico fueron las más prevalentes (23,9%)7. El objetivo del presente estudio es comparar las características sociodemográficas, clínicas e inmunoserológicas entre SAF primario y secundario en una cohorte colombiana de pacientes con SAF atendidos en un centro de referencia de enfermedades autoinmunes de Colombia.
Materiales y métodosSe hizo un estudio de corte transversal basado en el registro de una cohorte retrospectiva de 352 pacientes con diagnóstico de SAF según criterios clasificatorios de Sapporo, que fueron atendidos en una institución especializada en reumatología entre los años 2014 y 2018. Se describe el perfil sociodemográfico, clínico e inmunológico de la población por medio de proporciones relativas y absolutas, y posteriormente se hace un análisis bivariado para determinar diferencias entre los pacientes con SAF primario y secundario mediante la prueba chi-cuadrado. Finalmente, se realiza un análisis multivariado para identificar factores asociados a los desenlaces clínicos con una regresión logística binaria. Se utilizó el paquete estadístico SPSS versión 21 de la Universidad CES.
ResultadosCaracterísticas generales de la poblaciónLa edad promedio de la población general fue de 42,4±14 años, siendo el 84,6% de sexo femenino. El 67,6% de los pacientes tenía diagnóstico de SAF primario y un 32,3% de SAF secundario, de los cuales un 84% se asoció a LES. Dentro de los eventos trombóticos, el más frecuente fue la trombosis venosa profunda (17,3%), seguida por el ataque cerebrovascular (9,9%). Los eventos obstétricos fueron frecuentes, con una prevalencia de abortos del 39,4%. Desde el punto de vista inmunoserológico, la positividad para anticuerpos anticardiolipina fue lo más prevalente.
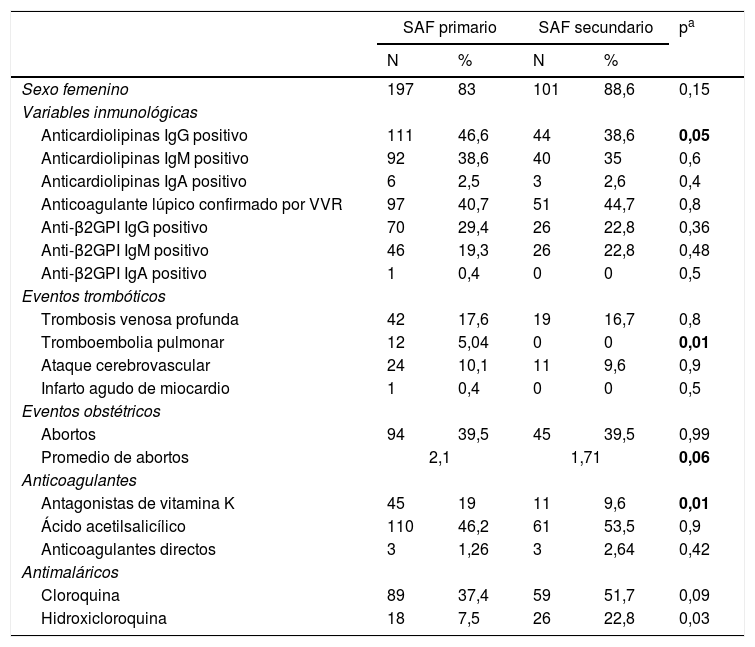
Comparación entre síndrome antifosfolípido primario y secundarioAl comparar la población con diagnóstico de SAF primario y aquella con SAF secundario, no se encontraron diferencias en el perfil sociodemográfico ni en el perfil inmunoserológico. Los eventos trombóticos tuvieron mayor frecuencia en el grupo de SAF primario, pero solamente la tromboembolia pulmonar alcanzó significación estadística. Lo anterior sugiere un curso más grave en este grupo de pacientes, como ha sido reportado en otras cohortes. Eventos obstétricos como los abortos no fueron diferentes entre ambos grupos (véase tabla 1).
Análisis comparativo de pacientes con síndrome antifosfolípido primario y secundario
| SAF primario | SAF secundario | pa | |||
|---|---|---|---|---|---|
| N | % | N | % | ||
| Sexo femenino | 197 | 83 | 101 | 88,6 | 0,15 |
| Variables inmunológicas | |||||
| Anticardiolipinas IgG positivo | 111 | 46,6 | 44 | 38,6 | 0,05 |
| Anticardiolipinas IgM positivo | 92 | 38,6 | 40 | 35 | 0,6 |
| Anticardiolipinas IgA positivo | 6 | 2,5 | 3 | 2,6 | 0,4 |
| Anticoagulante lúpico confirmado por VVR | 97 | 40,7 | 51 | 44,7 | 0,8 |
| Anti-β2GPI IgG positivo | 70 | 29,4 | 26 | 22,8 | 0,36 |
| Anti-β2GPI IgM positivo | 46 | 19,3 | 26 | 22,8 | 0,48 |
| Anti-β2GPI IgA positivo | 1 | 0,4 | 0 | 0 | 0,5 |
| Eventos trombóticos | |||||
| Trombosis venosa profunda | 42 | 17,6 | 19 | 16,7 | 0,8 |
| Tromboembolia pulmonar | 12 | 5,04 | 0 | 0 | 0,01 |
| Ataque cerebrovascular | 24 | 10,1 | 11 | 9,6 | 0,9 |
| Infarto agudo de miocardio | 1 | 0,4 | 0 | 0 | 0,5 |
| Eventos obstétricos | |||||
| Abortos | 94 | 39,5 | 45 | 39,5 | 0,99 |
| Promedio de abortos | 2,1 | 1,71 | 0,06 | ||
| Anticoagulantes | |||||
| Antagonistas de vitamina K | 45 | 19 | 11 | 9,6 | 0,01 |
| Ácido acetilsalicílico | 110 | 46,2 | 61 | 53,5 | 0,9 |
| Anticoagulantes directos | 3 | 1,26 | 3 | 2,64 | 0,42 |
| Antimaláricos | |||||
| Cloroquina | 89 | 37,4 | 59 | 51,7 | 0,09 |
| Hidroxicloroquina | 18 | 7,5 | 26 | 22,8 | 0,03 |
Anti-β2GPI: anti-beta2glicoproteína I; Ig: inmunoglobulinas; SAF: síndrome antifosfolípido; VVR: veneno de víbora de Russell.
En negrita, resultados con valor p ≤0,05.
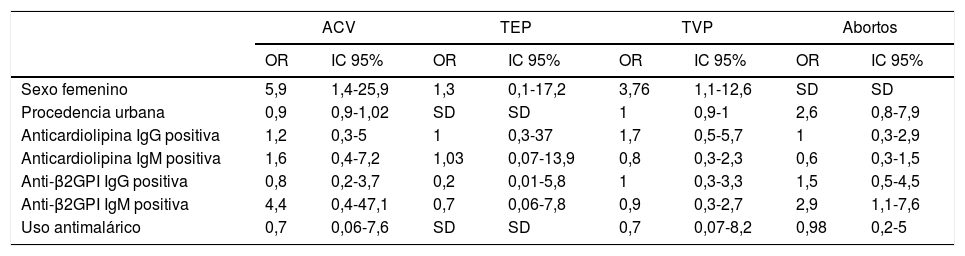
Al buscar asociaciones entre las diferentes variables sociodemográficas, clínicas, inmunológicas y farmacológicas, se encontró que las mujeres tienen una probabilidad 5,9 veces mayor para accidente cerebrovascular (ACV) y 3,7 veces mayor para trombosis venosa profunda en comparación con los hombres. No hubo diferencias significativas en el uso de antimaláricos en ninguno de los desenlaces. Se encontró que la positividad de los anti-β2GPI tipo IgM aumentó 2,9 veces la probabilidad de las mujeres de presentar aborto (véase tabla 2).
Factores asociados a desenlaces trombóticos en pacientes con SAF
| ACV | TEP | TVP | Abortos | |||||
|---|---|---|---|---|---|---|---|---|
| OR | IC 95% | OR | IC 95% | OR | IC 95% | OR | IC 95% | |
| Sexo femenino | 5,9 | 1,4-25,9 | 1,3 | 0,1-17,2 | 3,76 | 1,1-12,6 | SD | SD |
| Procedencia urbana | 0,9 | 0,9-1,02 | SD | SD | 1 | 0,9-1 | 2,6 | 0,8-7,9 |
| Anticardiolipina IgG positiva | 1,2 | 0,3-5 | 1 | 0,3-37 | 1,7 | 0,5-5,7 | 1 | 0,3-2,9 |
| Anticardiolipina IgM positiva | 1,6 | 0,4-7,2 | 1,03 | 0,07-13,9 | 0,8 | 0,3-2,3 | 0,6 | 0,3-1,5 |
| Anti-β2GPI IgG positiva | 0,8 | 0,2-3,7 | 0,2 | 0,01-5,8 | 1 | 0,3-3,3 | 1,5 | 0,5-4,5 |
| Anti-β2GPI IgM positiva | 4,4 | 0,4-47,1 | 0,7 | 0,06-7,8 | 0,9 | 0,3-2,7 | 2,9 | 1,1-7,6 |
| Uso antimalárico | 0,7 | 0,06-7,6 | SD | SD | 0,7 | 0,07-8,2 | 0,98 | 0,2-5 |
ACV: accidente cerebrovascular; Anti-β2GPI: anti-beta2glicoproteína I; IC 95%: intervalo de confianza del 95%; Ig: inmunoglobulinas; OR: odds ratio; SAF: síndrome antifosfolípido; SD: información conflictiva por presencia de cero en los grupos; TEP: tromboembolia pulmonar; TVP: trombosis venosa profunda.
El SAF se caracteriza por el desarrollo de trombosis venosas o arteriales, morbilidad del embarazo y presencia de anticuerpos antifosfolípidos. El Euro-Phospholipid Project ha aportado gran parte de los datos descriptivos desde lo sociodemográfico, clínico e inmunológico9. Los resultados presentados en esta cohorte son similares a los reportados, lo cual confirma varias características de la enfermedad independientes de la localización geográfica.
Al igual que en otros estudios, se encontró una mayor frecuencia de SAF primario al compararlo con el secundario (67,6% vs. 32,3%). El LES fue la principal patología asociada en los pacientes con SAF secundario (84,2%), tal como se reporta en la literatura1. Con respecto a los estudios locales, los datos obtenidos muestran algunas diferencias. Osio et al. reportaron una prevalencia de SAF primario ligeramente menor que la de la presente cohorte (62% vs. 67%)8.
Según el Euro-Phospholipid Project, el 87,9% de la cohorte contaba con anticuerpos anticardiolipina positivos, con una distribución relativamente homogénea entre IgG, IgM e IgA.
En esta cohorte, el 44% presentó positividad para IgG, el 37% para IgM y el 2,5% para IgA, con diferencias estadísticamente no significativas entre SAF primario y SAF secundario. De forma similar, la presencia de anticoagulante lúpico y anti-β2GPI no mostró diferencias estadísticamente significativas entre SAF primario y SAF secundario.
De manera similar a lo publicado por Cervera et al. en el Euro Phospolipid Project9, el evento trombótico más frecuente en nuestra población fue la trombosis venosa profunda, pero en un porcentaje mucho menor que en la cohorte europea, sin diferencias importantes entre el SAF primario y el secundario. En nuestro estudio sí se evidenció una diferencia estadísticamente significativa en la prevalencia de tromboembolia pulmonar en el grupo de SAF primario; sin embargo, esta frecuencia es menor que lo reportado en la literatura10 y es posible que exista un subdiagnóstico que explique tal hallazgo. Dentro de las trombosis arteriales, el ACV fue la manifestación más frecuente aunque con una prevalencia menor que la reportada.
Los eventos obstétricos, al igual que los trombóticos, se presentaron con menor frecuencia que lo reportado en la literatura11, con una tendencia a un mayor promedio de abortos en las pacientes con SAF primario. En nuestra población, las pacientes con anti-β2GPI IgM positivo tenían mayor probabilidad de presentar abortos (OR=2,9; IC 95%=1,1-7,6), lo cual contrasta con lo reportado por Alijotas-Reig et al. en el European Registry on Obstetrical Anti-Phospholipid Antibody Syndrom (Euroaps)12, en el que no se presentó una diferencia significativa con la presencia de este anticuerpo ni con lo reportado por Silver et al., quienes hallaron una mayor probabilidad de abortos con la presencia de β2GPI IgG positivo (OR=3,03; IC 95%=1,20-7,62)13. Un estudio local con población colombiana mostró mayor frecuencia de complicaciones obstétricas que las reportadas en esta cohorte (39% vs. 30%)7. Adicionalmente, reportó una asociación entre anticardiolipinas IgM y trombosis de accesos vasculares y entre positividad del anticoagulante lúpico y compromiso neurológico (p<0,05)7, hallazgos que por el diseño del presente estudio no pueden ser reafirmados.
Si bien el sexo no parece ser una variable que determine diferencias en el riesgo trombótico, en el análisis multivariado del presente estudio se encontró que el sexo femenino, en comparación con el masculino, se asocia con una mayor probabilidad de ACV (OR=5,9, IC 95%=1,4-25,8) y trombosis venosa profunda (OR=2,9; IC 95%=1,1-7,6). En un estudio en el que se evaluó la influencia del sexo en 49 pacientes con SAF primario, se encontró mayor prevalencia de tromboembolia pulmonar en mujeres que en hombres (34,2% vs. 0,0%, p=0,024)14. La asociación del sexo femenino con mayor frecuencia de fenómenos trombóticos pudiera explicarse por una diferente positividad de anticuerpos, sin embargo, ni la muestra del presente estudio ni la de Carvalho son suficientes para llegar a esta conclusión. Dicho desenlace debe evaluarse de manera más amplia en futuros estudios.
Los antagonistas de la vitamina K fueron los principales anticoagulantes administrados en la población de estudio. Los anticoagulantes directos (DOAC, por sus siglas en inglés) se emplearon en el 1,26 a 2,64% de los casos. Los DOAC se han posicionado como la primera línea en muchos escenarios clínicos, sin embargo, en SAF su seguridad es dudosa15. En el estudio RAPS, Cohen et al.16 demostraron que el uso de rivaroxabán se asociaba con un incremento de 2 veces en el potencial de trombina, lo que sugiere un riesgo trombótico alto en comparación con warfarina. La importancia en este efecto fue evaluada en el estudio multicéntrico de no inferioridad publicado por Pengo et al.17, en el que pacientes con SAF de alto riesgo trombótico con perfil inmunológico triple positivo (anticoagulante lúpico, anticardiolipina y β2-glicoproteína), que recibieron rivaroxabán, presentaron mayores tasas de eventos tromboembólicos (12% vs. 0%) y de sangrado mayor (7% vs. 3%) en comparación con warfarina, lo cual llevó a su suspensión temprana. En este mismo sentido, en el 2019 un ensayo clínico de no inferioridad18 reafirmó la inferioridad del rivaroxabán, comparado con warfarina, reportando un incremento de trombosis recurrente de casi 2 veces (11,6% vs. 6,3%). La baja prevalencia del uso de los DOAC en el presente estudio es simplemente un reflejo de que, ante la evidencia actual, no parecen una estrategia segura en este grupo de pacientes.
ConclusiónSe presenta una de las cohortes colombianas más grandes de pacientes con SAF reportadas hasta el momento en la literatura. La población es comparable clínica y sociodemográficamente con lo encontrado en otros estudios6–8, aunque la prevalencia de SAF primario fue mayor y las complicaciones trombóticas menores. La tromboembolia pulmonar fue significativamente mayor en el grupo de SAF primario, en tanto que el sexo femenino se asoció con un mayor riesgo de ACV y trombosis venosa profunda.
FinanciaciónEste trabajo fue desarrollado con recursos propios de la institución.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.