El objetivo de este trabajo fue conocer la seroprevalencia de Neospora caninum en los bovinos de los tambos del Valle del Lerma (Salta, Argentina) y los factores de riesgo asociados a la transmisión de este parásito en esta región. Se tomaron muestras de suero de aproximadamente 40 vacas en cada tambo, que fueron analizadas por ELISA indirecto para detectar anticuerpos contra N. caninum. También se discriminó entre infecciones crónicas y agudas midiendo la avidez de dichos anticuerpos. Todos los tambos presentaron al menos un bovino seropositivo y la media fue de 35,3 ± 14,9% de animales positivos. También se detectaron anticuerpos específicos en caninos presentes en 9 de los 16 tambos, con un valor de seropositividad del 71,7 ± 19,9%. El 56,3% de los bovinos seropositivos cursaban infecciones agudas. Se halló una asociación negativa entre la seroprevalencia y el índice de avidez de los anticuerpos específicos, lo que indica que la presencia de animales con infecciones agudas se asocia a mayor seroprevalencia. Los campos con pastoreo presentaron mayor cantidad de infecciones recientes. Estos resultados revelan por primera vez la importancia de este parásito en los tambos de la región y la necesidad de propiciar el desarrollo de programas de control considerando los distintos factores de riesgo que afectan la situación epidemiológica de la enfermedad.
The objective of this work was to determine the seroprevalence of Neospora caninum in cattle in Valle de Lerma, province of Salta, Argentina, and the risk factors associated with the disease. Serum samples were taken from 40 cows in each dairy herd, which were analyzed by indirect ELISA to detect antibodies against N. caninum. Chronic and acute infections were discriminated by measuring the avidity of these antibodies. All the herds exhibited at least one seropositive animal, the mean being 35.3 ± 14.9% of positive animals. Specific antibodies were also detected in dogs present in 9of the herds, which showed a seropositivity value of 71.7% ± 19.9%. Among the seropositive animals, 56.3% showed acute infections. A negative association was found between seroprevalence and the avidity index of specific antibodies, indicating that the presence of animals with acute infections is associated with higher seroprevalence. Fields with grazing showed more recent infections. These results show for the first time the importance of this parasite in this particular region and the need to promote the development of control programs considering the different risk factors that affect the epidemiological situation of the disease.
La neosporosis bovina es una enfermedad parasitaria producida por el protozoo apicomplejo Neospora caninum, ampliamente distribuido en regiones ganaderas de todo el mundo20. Los cánidos se comportan como hospedadores definitivos7,13, mientras que diversas especies de mamíferos pueden ser hospedadores intermediarios, entre ellos, los bovinos3. En estos animales, el signo clínico más importante es el aborto, aunque también pueden presentarse casos de muerte embrionaria o neonatal20,29. Las fallas reproductivas debidas a neosporosis bovina están asociadas a grandes pérdidas económicas a nivel mundial, que han sido estimadas en alrededor de 1.300 millones de dólares por año, con mayor efecto sobre la industria lechera31.
La transmisión del parásito a los hospedadores intermediarios puede ocurrir horizontalmente, por la ingesta de ooquistes, o verticalmente durante la preñez, por vía transplacentaria. La transmisión vertical, a su vez, puede subclasificarse como endógena o exógena. La vía endógena es causada por la reactivación de quistes tisulares en un animal persistentemente infectado y se asocia a un patrón endémico de fallas reproductivas y al mantenimiento de la infección en el rodeo. La transmisión exógena, en cambio, tiene lugar luego de una infección horizontal primaria causada por la ingesta de ooquistes por un animal preñado y se asocia a un patrón epidémico de abortos20.
Entre los principales factores de riesgo figuran el sistema de producción y manejo21 y las consecuencias directas de las propias infecciones9,32.
Distintos estudios han verificado que el estado serológico de los rodeos infectados con N. caninum es variable entre países y regiones del mismo país, y también entre sistemas productivos32. En América Latina, la neosporosis es considerada una enfermedad emergente en rodeos lecheros, con prevalencias variables9,22.
Según relevamientos realizados en diferentes regiones de la Argentina, se conoce que la enfermedad está ampliamente distribuida tanto en rodeos de cría como en tambos8,10,19,23. En la provincia de Salta, existe un único antecedente sobre un relevamiento efectuado en el Valle de Lerma en 2011, que arrojó una prevalencia del 31% para tambos (comunicación personal). No existe un análisis de seroprevalencia actualizado de esta zona.
La ganadería en el noroeste argentino (NOA) ha crecido, principalmente, debido a la expansión de monocultivos en el centro del país30. Por esta razón, estudiar la epidemiología de las enfermedades reproductivas en esta zona podría redundar en un mayor crecimiento económico estratégico. Se ha reportado que los rodeos lecheros son más proclives a contraer infecciones por N. caninum23,27 y a tener las pérdidas económicas asociadas. Para profundizar al respecto, en este trabajo nos propusimos estimar la seroprevalencia de esta enfermedad en vacas de tambos ubicados en el Valle de Lerma, provincia de Salta, y caracterizar distintos factores de riesgo asociados, con el objetivo de establecer las medidas de control más adecuadas para esta región.
Materiales y métodosEncuesta epidemiológicaSe analizaron en total 16 establecimientos (51,6% del total de tambos de la provincia) ubicados en el Valle de Lerma, Salta, durante el período 2016-2018. Se realizó una encuesta transversal mediante visita a cada establecimiento. Esta contempló preguntas sobre identificación, manejo productivo, datos sanitarios y presencia de cánidos domésticos o silvestres. La vacuna reproductiva utilizada en algunos de los tambos estudiados está incluida dentro de los planes de vacunación regionales y contiene antígenos del herpesvirus bovino (IBR) tipo 1 y tipo 5, del virus de la diarrea viral bovina, de Campylobacter sp., Histophilus sp. y de diversos serovares de Leptospira sp.
Toma de muestraEl tamaño de la muestra se determinó mediante un programa de muestreo estadístico del Instituto Nacional de Tecnología Agropecuaria (INTA) (proMESA 1.3, desarrollado por Emilio A León [Unidad de Epidemiología, CICVyA, INTA], Sergio J. Duffy [Unidad de Epidemiología, CICVyA, INTA], Bryan ÓLeary [EpiCentre, Massey University, Nueva Zelanda] y Mark Stevenson [EpiCentre, Massey University, Nueva Zelanda]), considerando una prevalencia esperada de un 40% (estimada a partir de comunicaciones personales con profesionales de INTA), aceptando un error relativo del 20% y una tasa de homogeneidad baja. Se tomaron por cada tambo alrededor de 40 muestras sanguíneas de hembras adultas raza Holstein en ordeñe, escogidas al azar. En 9 de los tambos fue posible, además, muestrear algunos de los perros (n = 41) que estaban en contacto con las vacas, ya sea en el campo o en los alrededores de las instalaciones de ordeñe.
A los bovinos se les tomaron muestras de 5ml de sangre sin anticoagulante por venopunción coccígea y a los cánidos domésticos se les tomaron 5ml de muestra de sangre sin anticoagulante por venopunción yugular o de vena cefálica antebraquial. Dichas muestras fueron incubadas durante 30 min a 37°C y luego centrifugadas (3.000rpm, 10 min). Se separó el suero en 2alícuotas, que se conservaron a –20°C hasta su análisis.
Técnicas serológicasLa detección en suero de anticuerpos específicos inducidos por la infección se realizó mediante un ELISA indirecto desarrollado en nuestro laboratorio, siguiendo los lineamientos ya establecidos17. Brevemente, las placas fueron sensibilizadas (6h, 4°C) con un extracto soluble de taquizoítos de N. caninum (cepa Nc1, 750 ng/pocillo), que fue obtenido siguiendo procedimientos ya reportados18. Luego de 3 lavados con solución de lavado (PBS-Tween 0,05%; 250μl/pocillo), las placas fueron bloqueadas con 125μl/pocillo de una solución de PBS-caseína al 0,5% (solución bloqueante) durante toda la noche a 4°C. Los sueros problema se diluyeron 1:120 en solución bloqueante y se incubaron durante 30 min a temperatura ambiente (50μl/pocillo). Luego de 3 lavados, se adicionaron 50μl/pocillo (dilución 1:5.000 en solución bloqueante) del anticuerpo conjugado (anti-IgG bovina conjugado a peroxidasa AffiniPure Goat Anti-Bovine IgG [H+L], número de catálogo 101-035-003, Jackson Immuno Reaserch Laboratories Inc., PA, EE. UU.) y se incubó a temperatura ambiente durante 20 min. El sustrato (50μl/pocillo; TMB One Solution, número de catálogo G7431, Promega Biosciences, CA, EE. UU.) fue agregado luego de unos lavados e incubado en oscuridad durante 10 min a temperatura ambiente. Finalmente, se adicionó la solución de frenado (H2SO4 2N, 50μl/pocillo) y las placas fueron leídas a 450nm. Los resultados se calcularon normalizando los valores de densidad óptica (DO) respecto del control positivo (S/P [%]). Se utilizó como control positivo y negativo el suero de un animal infectado y de otro no infectado, respectivamente, caracterizados previamente por inmunofluorescencia indirecta (IFI, estándar de oro) y por ELISA (ID Screen® Neospora caninum Competition, IDVet, Montpellier, Francia).
Para determinar el punto de corte, se evaluaron muestras positivas (n = 307) y negativas (n = 327) (dilución final 1:120) cuyo status fue definido por IFI. Se construyó una curva ROC y se crearon 2histogramas; su punto de intersección se consideró como el valor de corte. Se estableció una relación S/P del 40% como un umbral de corte apropiado, pero, dado que se observó cierta superposición entre ambas curvas, las muestras con valores de S/P entre el 30 y el 40% se consideraron dudosas y se procesaron nuevamente en una dilución final de 1:40. El valor de corte de esta prueba confirmatoria fue establecido en el 30% (datos no publicados).
Para determinar la avidez de los anticuerpos, se agregó un paso de lavado de las muestras de suero con un agente caotrópico (urea 6M en PBS), que despega anticuerpos débilmente unidos al antígeno antes de agregar el conjugado. Esta solución se incubó en la placa durante 20 min a temperatura ambiente (100μl/pocillo). Luego, las placas fueron lavadas 3 veces con solución de lavado y se prosiguió con el protocolo, tal como se describió. El grado de disociación obtenido establece la fuerza de unión de los anticuerpos presentes en el suero al antígeno y se estima mediante el índice de avidez (IA [%]), que se calcula como la relación entre el valor de la DO con el tratamiento con el agente caotrópico y el valor de la DO sin aplicar dicho tratamiento. Se consideran anticuerpos de alta avidez aquellos que presentan IA superiores al 65%17.
Las muestras de los sueros provenientes de los perros fueron procesadas por IFI en un laboratorio privado (BioVet Lab, Rafaela, Santa Fe, Argentina).
Análisis estadísticoSe utilizó un análisis estadístico descriptivo. Se estimó la prevalencia aparente y real en función de la sensibilidad (0,925) y especificidad (0,968) de la prueba de ELISA utilizada, que había sido desarrollada y validada previamente en nuestro laboratorio mediante un análisis ROC17.
La correlación lineal (Pearson) y la regresión lineal simple se emplearon para establecer la relación entre seroprevalencia y porcentaje de infecciones crónicas. Se aplicaron un análisis de varianza y una prueba de Fisher para asociar la presencia de abortos con la seroprevalencia de N. caninum y con la proporción de infecciones crónicas y de infecciones agudas. En todos los casos, el intervalo de confianza (IC) utilizado fue del 95%.
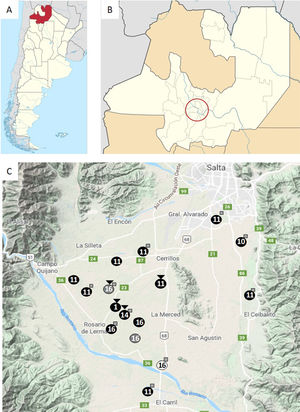
ResultadosSistemas productivosSe realizaron encuestas en 16 tambos ubicados en diferentes puntos del Valle de Lerma, correspondientes a zonas altas sobre las cimas y las laderas de los cerros o en los valles con humedales. Se procesaron como mínimo 38 muestras de suero de vacas de cada tambo. Los tambos evaluados corresponden a la mitad de los tambos de la provincia (fig. 1).
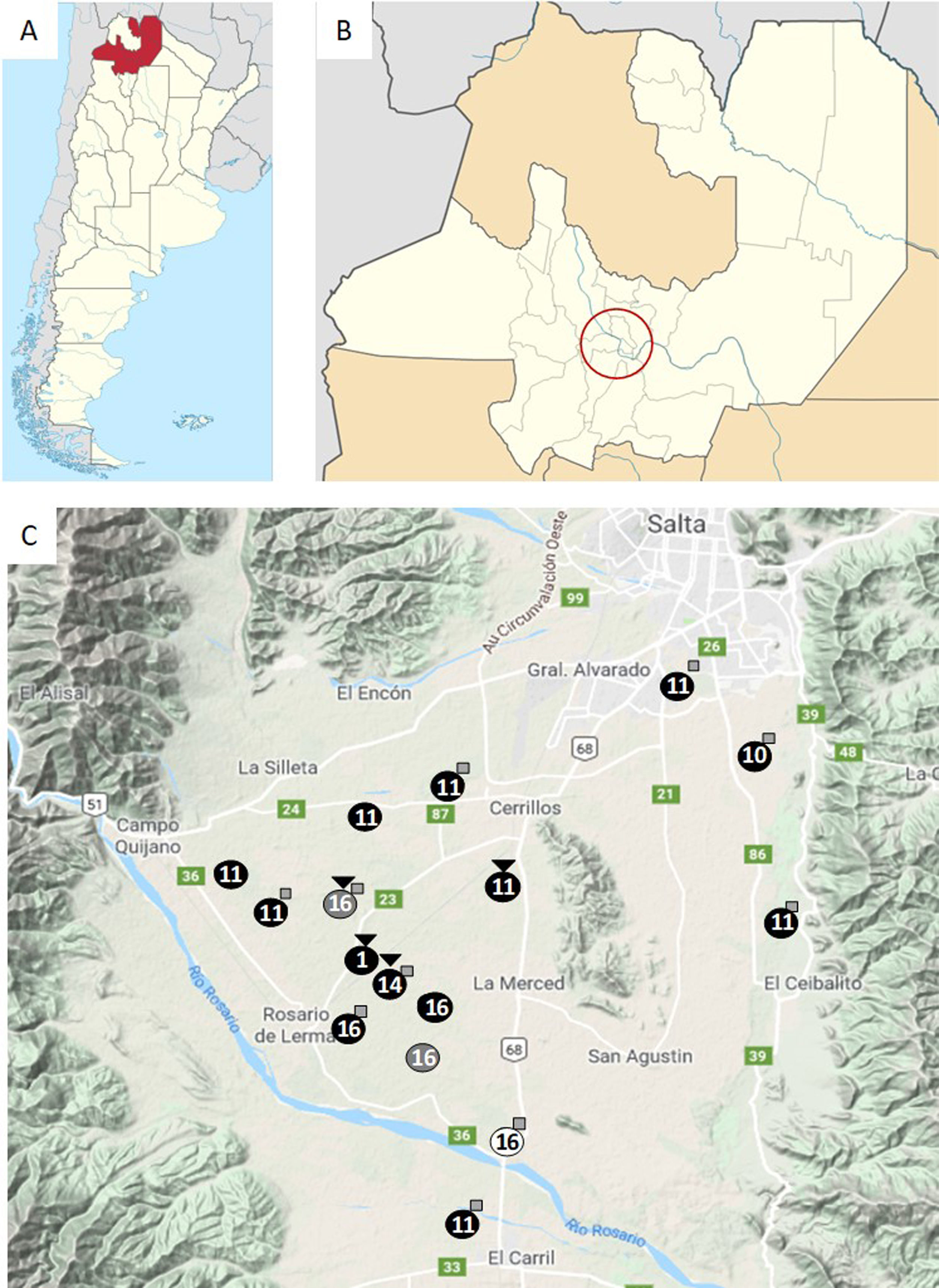
Ubicación geográfica de la Argentina (A) y la provincia de Salta (B); el círculo señala la ubicación del Valle de Lerma. Detalle del Valle de Lerma (C); los círculos señalan la ubicación de los tambos muestreados (enumerados del 1 al 16). El color del fondo del círculo denota el sistema productivo del establecimiento.
●: pastoreo a campo con suplementación (PcS); ●: free stall;○dry lot; □: tambos en donde fue posible muestrear cánidos; ?: tambos que comparten la misma acequia.
El Valle de Lerma se encuentra ubicado entre los paralelos 24° 30’ y 25° 37’ de latitud sur y los meridianos 65° 22’ y 65° 40’ de longitud oeste, lo que representa un área total de 17.000km2 de extensión, que alberga los departamentos de La Caldera, Capital, Rosario de Lerma, Cerrillos, Chicoana, La Viña y parte de General Güemes. La temperatura media es de aproximadamente 23°C en verano y 15°C en invierno. La distribución geográfica de los tambos que formaron parte de este trabajo se muestra en la figura 1C.
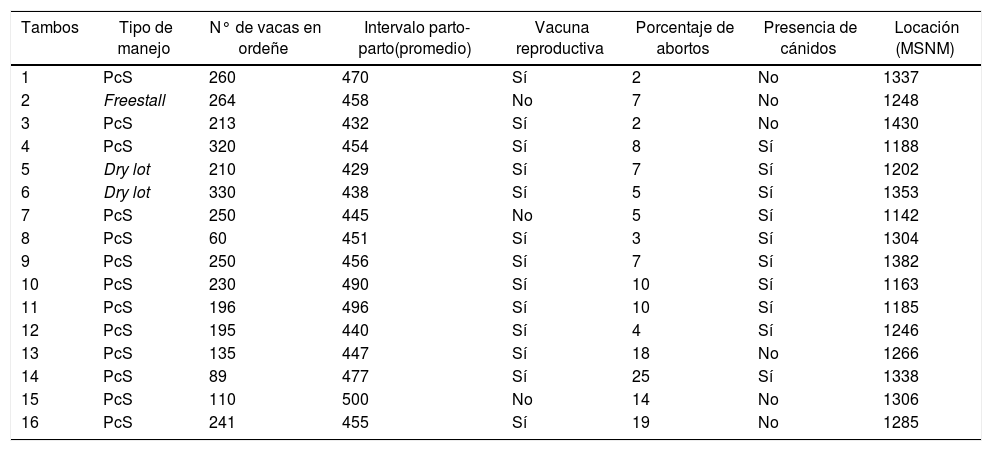
Los resultados de la encuesta realizada en los tambos se resumen en la tabla 1. La mayoría de los establecimientos (13/16) tienen un manejo que complementa al pastoreo, con suplementación con maíz molido y silo más heno de alfalfa, soja, semilla de algodón y afrechillo de trigo. Dos establecimientos (2/16) tienen un sistema de dry lot, en donde los animales también son alimentados con pasturas naturales y suplemento, pero se encuentran en un área elevada con una pendiente que permite evacuar el agua en épocas de lluvia. El establecimiento restante tiene un sistema de free stall, con los animales confinados y un manejo más intensivo.
Características de los tambos encuestados
| Tambos | Tipo de manejo | N° de vacas en ordeñe | Intervalo parto-parto(promedio) | Vacuna reproductiva | Porcentaje de abortos | Presencia de cánidos | Locación (MSNM) |
|---|---|---|---|---|---|---|---|
| 1 | PcS | 260 | 470 | Sí | 2 | No | 1337 |
| 2 | Freestall | 264 | 458 | No | 7 | No | 1248 |
| 3 | PcS | 213 | 432 | Sí | 2 | No | 1430 |
| 4 | PcS | 320 | 454 | Sí | 8 | Sí | 1188 |
| 5 | Dry lot | 210 | 429 | Sí | 7 | Sí | 1202 |
| 6 | Dry lot | 330 | 438 | Sí | 5 | Sí | 1353 |
| 7 | PcS | 250 | 445 | No | 5 | Sí | 1142 |
| 8 | PcS | 60 | 451 | Sí | 3 | Sí | 1304 |
| 9 | PcS | 250 | 456 | Sí | 7 | Sí | 1382 |
| 10 | PcS | 230 | 490 | Sí | 10 | Sí | 1163 |
| 11 | PcS | 196 | 496 | Sí | 10 | Sí | 1185 |
| 12 | PcS | 195 | 440 | Sí | 4 | Sí | 1246 |
| 13 | PcS | 135 | 447 | Sí | 18 | No | 1266 |
| 14 | PcS | 89 | 477 | Sí | 25 | Sí | 1338 |
| 15 | PcS | 110 | 500 | No | 14 | No | 1306 |
| 16 | PcS | 241 | 455 | Sí | 19 | No | 1285 |
PcS: pastoreo con suplementación.
La mayoría de los tambos estudiados (13/16) utilizaban vacunas reproductivas, independientemente del sistema productivo. La presencia de perros se declaró en un 62,5% de los tambos y se registró también la visita nocturna frecuente de zorros (Lycalopex culpaeus) en los silos y las pasturas utilizadas por las vacas, aunque no se procesaron muestras de estos animales.
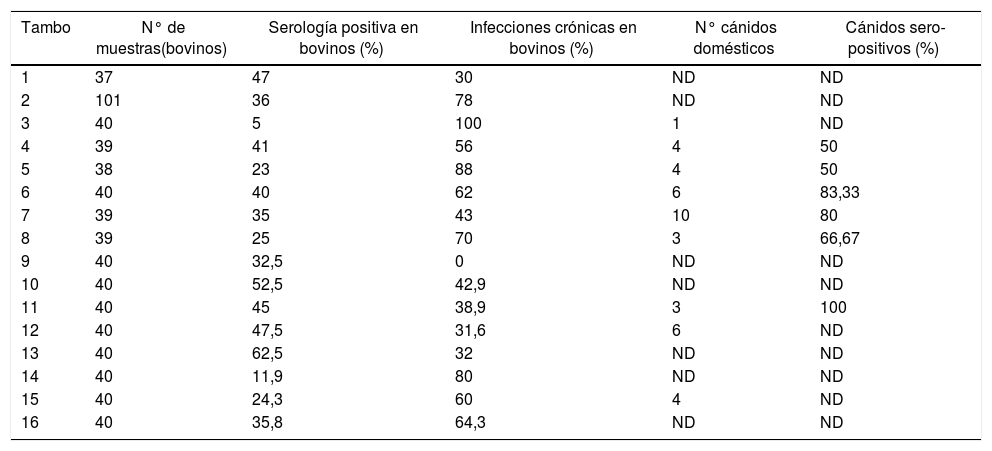
Serología en bovinos y caninos domésticosSe obtuvieron muestras de 693 bovinos (459 vacas y 234 vaquillonas de 2-3 años) y 41 perros. El 100% de los tambos presentó al menos 2bovinos con anticuerpos específicos para N. caninum, lo que evidencia la importante circulación de la enfermedad. Los datos de serología obtenidos para N. caninum en sueros bovinos y caninos se muestran en la tabla 2.
Seroprevalencia de N. caninum y porcentaje de animales con infecciones crónicas
| Tambo | N° de muestras(bovinos) | Serología positiva en bovinos (%) | Infecciones crónicas en bovinos (%) | N° cánidos domésticos | Cánidos sero- positivos (%) |
|---|---|---|---|---|---|
| 1 | 37 | 47 | 30 | ND | ND |
| 2 | 101 | 36 | 78 | ND | ND |
| 3 | 40 | 5 | 100 | 1 | ND |
| 4 | 39 | 41 | 56 | 4 | 50 |
| 5 | 38 | 23 | 88 | 4 | 50 |
| 6 | 40 | 40 | 62 | 6 | 83,33 |
| 7 | 39 | 35 | 43 | 10 | 80 |
| 8 | 39 | 25 | 70 | 3 | 66,67 |
| 9 | 40 | 32,5 | 0 | ND | ND |
| 10 | 40 | 52,5 | 42,9 | ND | ND |
| 11 | 40 | 45 | 38,9 | 3 | 100 |
| 12 | 40 | 47,5 | 31,6 | 6 | ND |
| 13 | 40 | 62,5 | 32 | ND | ND |
| 14 | 40 | 11,9 | 80 | ND | ND |
| 15 | 40 | 24,3 | 60 | 4 | ND |
| 16 | 40 | 35,8 | 64,3 | ND | ND |
Las infecciones crónicas corresponden a un IA > 65%.
ND: no determinado.
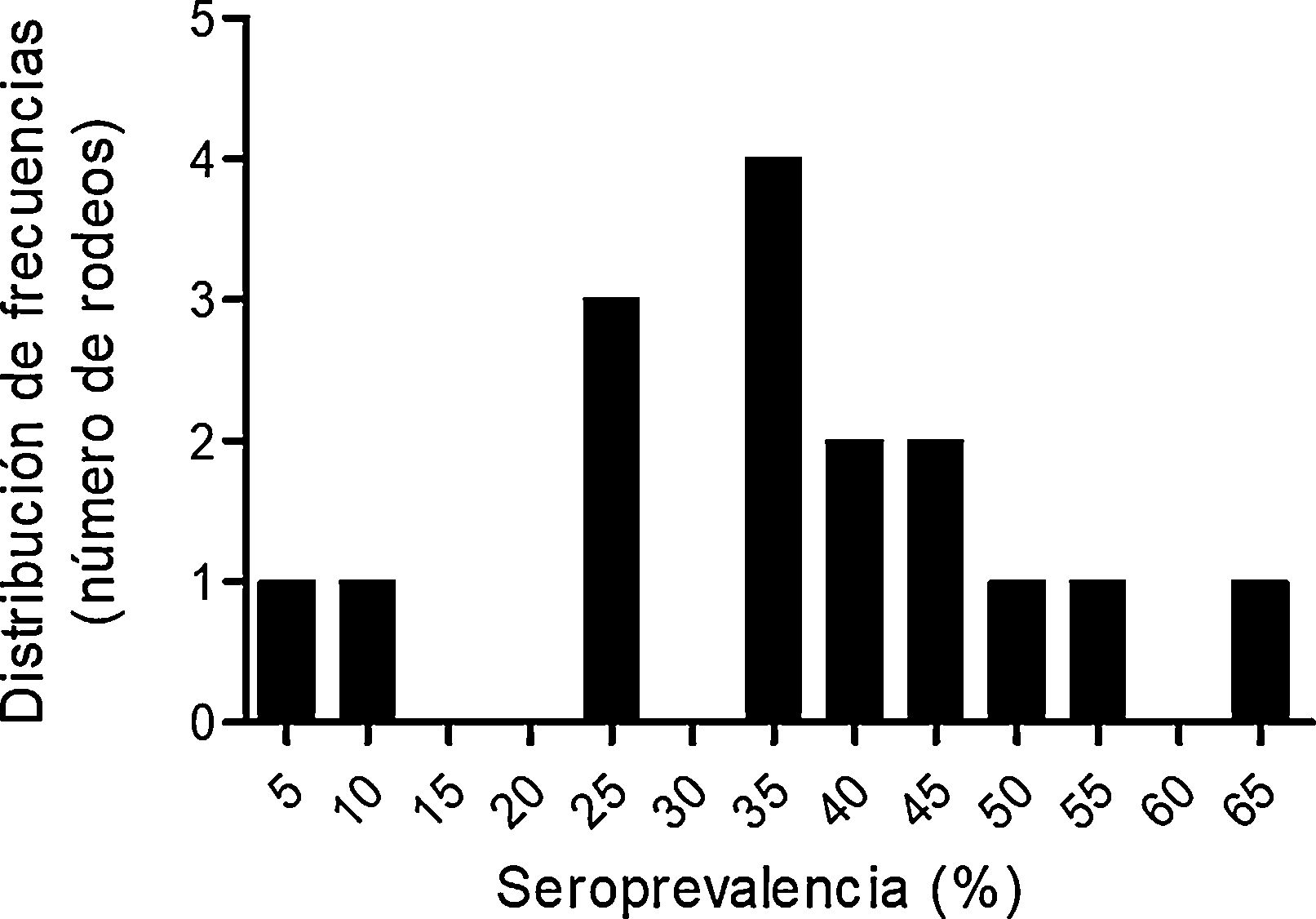
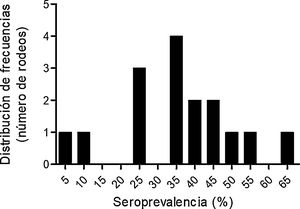
De un total de 693 muestras bovinas analizadas, 244 fueron positivas. Esto arroja una seroprevalencia aparente del 35,5% (IC = 0,32-0,39) y una seroprevalencia verdadera del 35,9% (IC = 0,32-0,40). La media estimada de la seroprevalencia intrarrodeo fue del 35,3 ± 14,9% (límites: 5% al 62,5%). La distribución de la frecuencia de la seroprevalencia de N. caninum en los rodeos estudiados indica que el 43,7% de ellos tiene una prevalencia mayor del 40% (fig. 2).
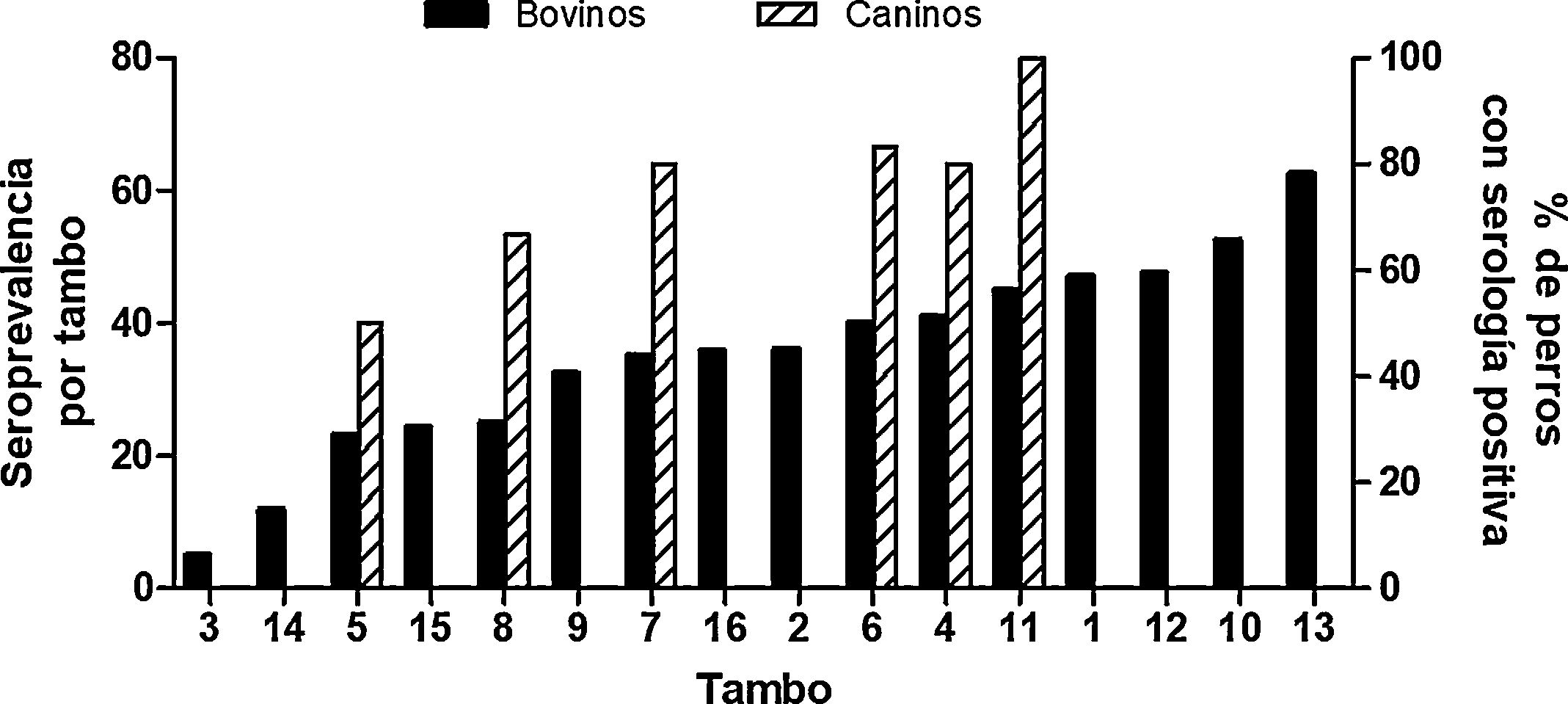
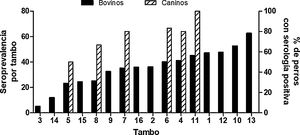
Al menos la mitad de los establecimientos en los que se tomaron muestras de sangre de perros presentaba anticuerpos específicos anti-N. caninum. El promedio de animales seropositivos fue de 71,7 ± 19,9%. Si bien la presencia de perros infectados y la seroprevalencia intrarrodeo no estuvieron asociadas de manera estadísticamente significativa, se detecta una tendencia que podría indicar una relación positiva entre ambas variables. Se necesitan más datos para confirmar esta asociación (fig. 3).
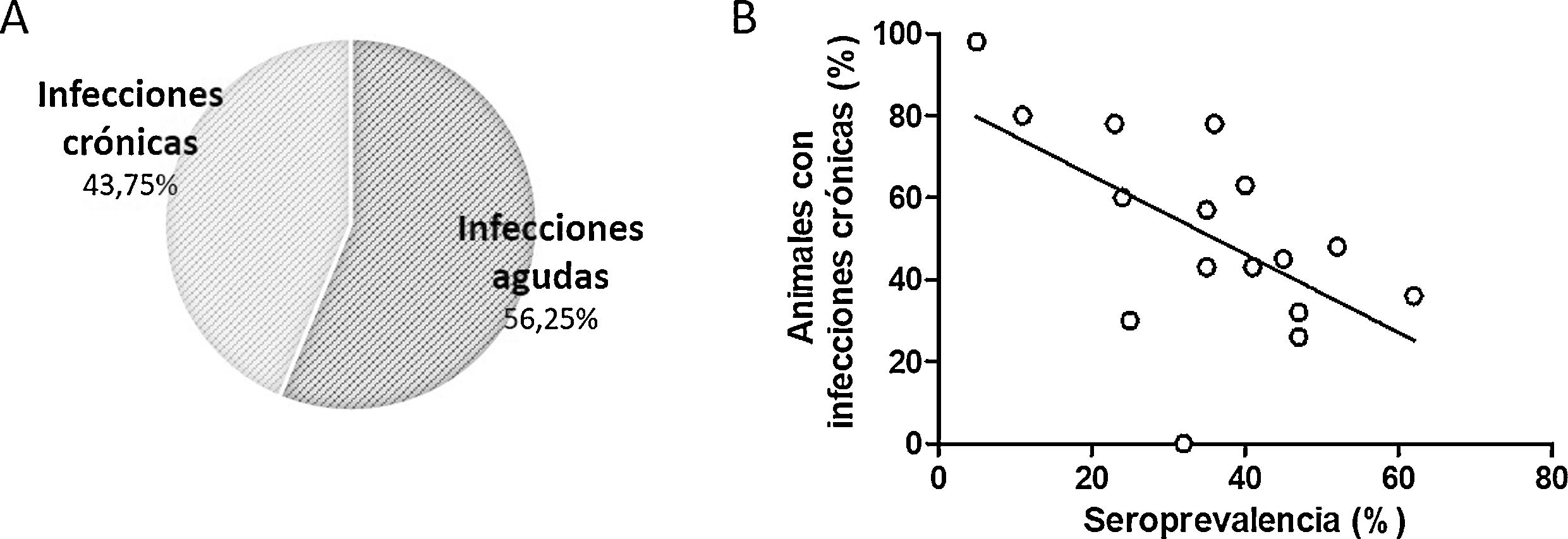
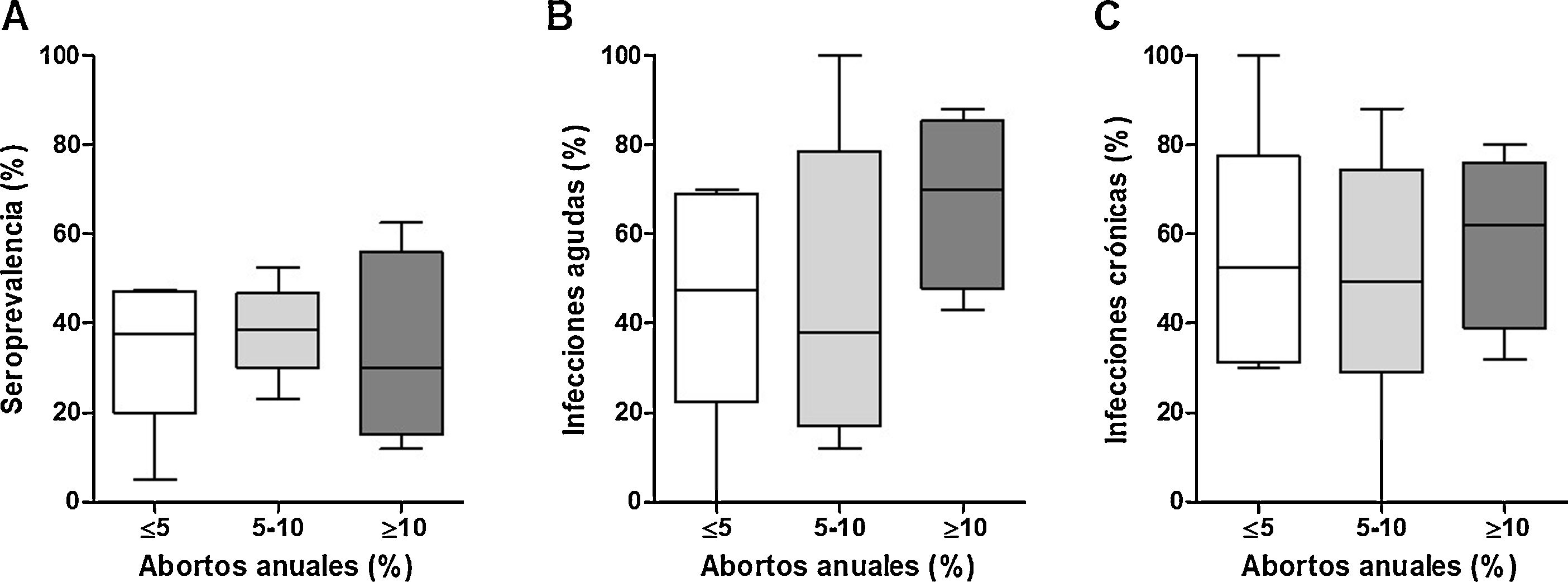
Mediante la aplicación del ELISA de avidez se determinó que el 43,7% de los bovinos positivos presentaban infecciones crónicas (IA mayor del 65%) y, por lo tanto, más de la mitad de los animales estudiados cursaban una infección aguda (fig. 4A). También se encontró una asociación negativa (r2 = 0,33; p < 0,02) entre la seroprevalencia y las infecciones crónicas determinadas según el IA de IgG. Se observa claramente que los establecimientos que poseen menor seroprevalencia son aquellos en los que la incidencia de infecciones crónicas es mayor que la de infecciones agudas (fig. 4B). Además, se observó una asociación positiva entre infecciones agudas y sistema productivo con pastoreo y suplementación (test de Fisher; p = 0,0294).
Porcentaje de animales con infecciones crónicas y agudas, determinado según la avidez de los anticuerpos totales específicos (IA mayor o menor del 65%, respectivamente) (A). Asociación entre el porcentaje de infecciones crónicas intratambo y la seroprevalencia de N. caninum en los rodeos (B).
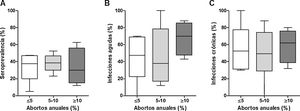
No se encontró asociación entre la seroprevalencia y la tasa de abortos anuales (fig. 5A). Sin embargo, se pudo observar una tendencia a una mayor tasa de abortos en aquellos tambos con mayores niveles de infecciones agudas con N. caninum (fig. 5B), mientras que el porcentaje de infecciones crónicas no guarda relación con la tasa de abortos (fig. 5C).
DiscusiónEn este estudio hemos caracterizado, por primera vez, la seroprevalencia de N. caninum en la cuenca lechera del Valle de Lerma, situado en la provincia de Salta (Argentina), y hemos analizado diferentes factores de riesgo para su transmisión en esta región, incluyendo aspectos geográficos, de manejo productivo y ecológicos.
Detectamos animales seropositivos en la totalidad de los tambos muestreados, con una seroprevalencia alta a nivel rodeo (valor promedio del 35,3% y un valor máximo del 62,5%), sin diferencias entre las prevalencias aparentes y las reales debido a la alta sensibilidad y especificidad de la prueba de ELISA utilizada. Estos valores remarcan la importancia que tiene N. caninum en la sanidad de estos establecimientos.
En la región central de Argentina, estudios previos hallaron también una elevada circulación de N. caninum, con casi la totalidad de los rodeos lecheros muestreados positivos, aunque con prevalencias menores10,23. Resulta importante destacar que el 43,7% de los tambos presentaron seroprevalencias superiores al 40%, con anticuerpos predominantemente de baja avidez, lo que denota la gran dispersión de la enfermedad con carácter epidémico en esta región. Esto remarca la importancia de establecer programas de manejo y control, considerando el escaso número de animales seronegativos presentes para reemplazos y los costos de las vaquillonas a incorporar.
La tasa de transmisión vertical en animales con infecciones crónicas ya fue estudiada por nuestro grupo de trabajo en animales de esta misma cuenca lechera28. En ese trabajo previo, pudimos observar que la mayoría de los bovinos con infecciones crónicas no abortaba y que la transmisión se relacionaba con un perfil particular de respuesta inmunitaria. Dado que la presencia de anticuerpos puede generar protección (se ha visto que vacas multíparas infectadas no abortan26,34), la presencia de una alta tasa de infecciones crónicas podría explicar, al menos parcialmente, la falta de correlación entre seroprevalencia y abortos en algunos casos.
No encontramos asociaciones estadísticamente significativas entre la seroprevalencia de N. caninum en los rodeos y los datos productivos de estos, probablemente debido a que el manejo productivo y reproductivo es similar en la mayoría de los tambos.
Varios trabajos han propuesto al manejo intensivo como un factor de riesgo clave para explicar la mayor prevalencia de N. caninum que se suele observar en los tambos comparados con los rodeos de cría, lo cual se adjudicó a una mayor exposición posnatal a ooquistes que contaminan el agua y el alimento del ganado5,27,33. Otros estudios, por el contrario, han identificado la transmisión vertical endógena como factor de riesgo en tambos con sistemas intensivos1,2,11. En la cuenca del río Salado (principal área de cría de ganado de Argentina), los sistemas extensivos no estarían asociados a la transmisión horizontal del parásito6, aunque se reportó un tambo en la provincia de Buenos Aires con seroprevalencia muy alta (80,9%) y en donde la frecuencia estimada de transmisión horizontal superaba a la de transmisión vertical (el 51 y el 37,1%, respectivamente)24.
En este sentido, nuestros resultados muestran que el tambo con sistema intensivo (free stall) posee una mayor cantidad de infecciones crónicas, lo que sugiere la menor circulación de ooquistes. Lo mismo observamos en los campos con sistema de dry lot, en donde el escurrimiento del agua de lluvia y riego, favorecido por la pendiente de estas zonas, podría limitar el contacto de los quistes con el alimento. Estos datos sugieren que tanto el sistema de manejo (intensivo o extensivo) como las condiciones topográficas (altura, pendiente) y otras particularidades (acequias de agua de lluvia compartidas entre distintos tambos) deberían ser consideradas en futuros estudios que abarquen mayor número de tambos de similares características, ubicados en esta misma región o en otras.
Las características climáticas también podrían comportarse como un factor de riesgo asociado al aborto, aunque hay pocos datos al respecto. Se ha observado que un incremento en el nivel de precipitaciones en ambientes secos puede comprometer el éxito de la gestación en vacas infectadas con N. caninum16.
La transmisión horizontal no ha sido tradicionalmente considerada como la más importante debido a su menor asociación con abortos en comparación con la transmisión vertical4,12,14,20, aunque se ha establecido que también puede contribuir al mantenimiento de una alta seroprevalencia en rebaños infectados endémicamente1,27.
En los tambos en los que se pudieron tomar muestras de perros, se encontró al menos un animal seropositivo, lo que evidencia una posible fuente de contagio importante. Todos los tambos reportaron la presencia de zorros y comadrejas; en muchos casos, se observó incluso la presencia de madrigueras y perros en los depósitos donde se almacena el alimento. Esto sugiere que la presencia de los perros en los rodeos bovinos constituye un factor de riesgo para este tipo de transmisión, tal como se ha informado previamente1,15,25.
En este sentido, nuestros resultados remarcan la importancia que tiene individualizar los distintos factores de riesgo y diferenciar infecciones horizontales de verticales, y, a su vez, determinar si estas son endógenas o exógenas, para caracterizar la situación epidemiológica de una región en particular. Estos datos, sin duda, serán esenciales para la confección de un plan de manejo tendiente al control de esta enfermedad.
ConclusionesEste trabajo demuestra por primera vez la circulación de N. caninum en la cuenca lechera del Valle de Lerma, en la provincia de Salta. Existe una alta prevalencia de neosporosis de carácter epidémico en los tambos de esta región, con un 100% de rodeos positivos y una prevalencia promedio intrarrodeo del 35%. Se encontró una asociación positiva entre la seroprevalencia y la presencia de infecciones agudas en animales adultos, lo que sugiere que el principal mecanismo de dispersión de la enfermedad en esta región es la transmisión horizontal. La presencia de perros infectados, la ubicación geográfica y el libre pastoreo serían los principales factores de riesgo con efecto sobre este tipo de transmisión.
Conflicto de interesesLos autores declaran no tener ningún tipo de conflicto de interés con personas u organizaciones que pudieran sesgar su trabajo.
FinanciaciónEste trabajo se realizó con fondos provenientes del programa de Salud Animal de INTA (PNSA1115053).
Los autores agradecen al personal de los establecimientos donde se realizó el estudio, incluyendo tamberos y veterinarios, por su colaboración con el manejo de los animales.