El ictus isquémico por embolia cálcica como complicación potencial de la cirugía cardiaca es excepcional. El manejo terapéutico en estos casos no está definido. Presentamos nuestra experiencia en la oclusión de la arteria cerebral media (ACM) por un émbolo cálcico tras cirugía de válvula aórtica, que fue tratado con éxito mediante neurointervencionismo.
Mujer de 77años de edad con estenosis aórtica ingresada para el reemplazo de la válvula aórtica. Tenía disnea con el ejercicio 4meses antes de la admisión hospitalaria. Entre sus antecedentes destacan hipertensión y diabetes. La ecocardiografía mostró una fracción de eyección ventricular izquierda normal, leve hipertrofia ventricular izquierda, leve dilatación biauricular y estenosis aórtica severa. Realizaba tratamiento con aspirina, simvastatina, torasemida y metformina. En el examen preoperatorio estaba alerta y orientada, no tenía déficits sensitivos o motores y la marcha era normal. Los parámetros de laboratorio fueron también normales. Fue sometida a una toracotomía y reemplazo valvular aórtico con prótesis porcina. Un ecocardiograma transesofágico intraoperatorio no reveló trombos en la aurícula izquierda.
El día 1 postoperatorio, tras ser extubada, al despertar en la unidad de cuidados postoperatorios cardiacos presenta somnolencia, hemiparesia derecha y afasia global, episodio clínico compatible con ictus isquémico completo de ACM izquierda. Se activa el código ictus intrahospitalario. La NIHSS fue de 18 puntos en ese momento. Se realiza TC cerebral urgente, que muestra una masa redondeada de alta densidad en la localización teórica del segmento proximal de la ACM izquierda. El mapa TC de perfusión muestra una extensa área de penumbra isquémica en el territorio de la ACM izquierda. La angiografía por RM muestra una discontinuidad inmediatamente distal al origen de la ACM izquierda (fig. 1). Debido a su reciente cirugía, se descartó el tratamiento trombolítico. Se procedió a terapia endovascular con anestesia general, utilizando un dispositivo stentriever. el procedimiento cursa con éxito tras un solo pase (fig. 2). El examen histológico del fragmento fue compatible con un émbolo cálcico. Fue dada de alta a los 7días, y el resultado fue muy favorable: a los 3meses la escala modifica de Rankin era de 1 punto.
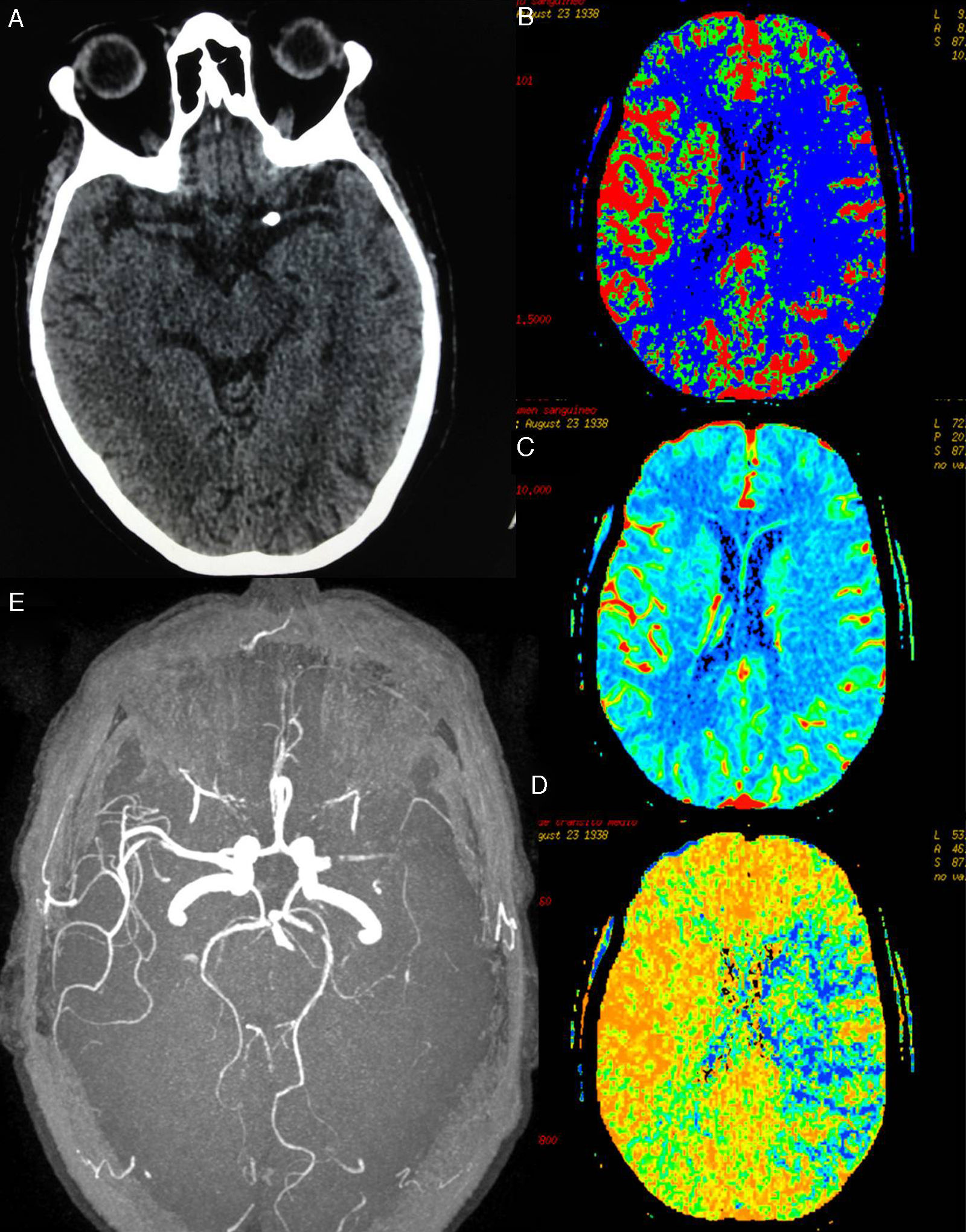
A) TC cerebral. Se aprecia calcio endoluminal en la ACM proximal izquierda. B-D) En los mapas TC-perfusión de flujo, volumen y tiempo de tránsito medio se identifica una amplia área del territorio de la ACM izquierda afectada que presenta un aumento del TTM (zona azul en D) y una disminución del flujo (zona azul en B). El mapa de volumen (C) no identifica zona de volumen disminuido significativo, el área afectada corresponde con amplia zona de penumbra. E) Estenosis preoclusiva del segmento M1 izquierdo, en secuencias angiográficas de RM 3D.
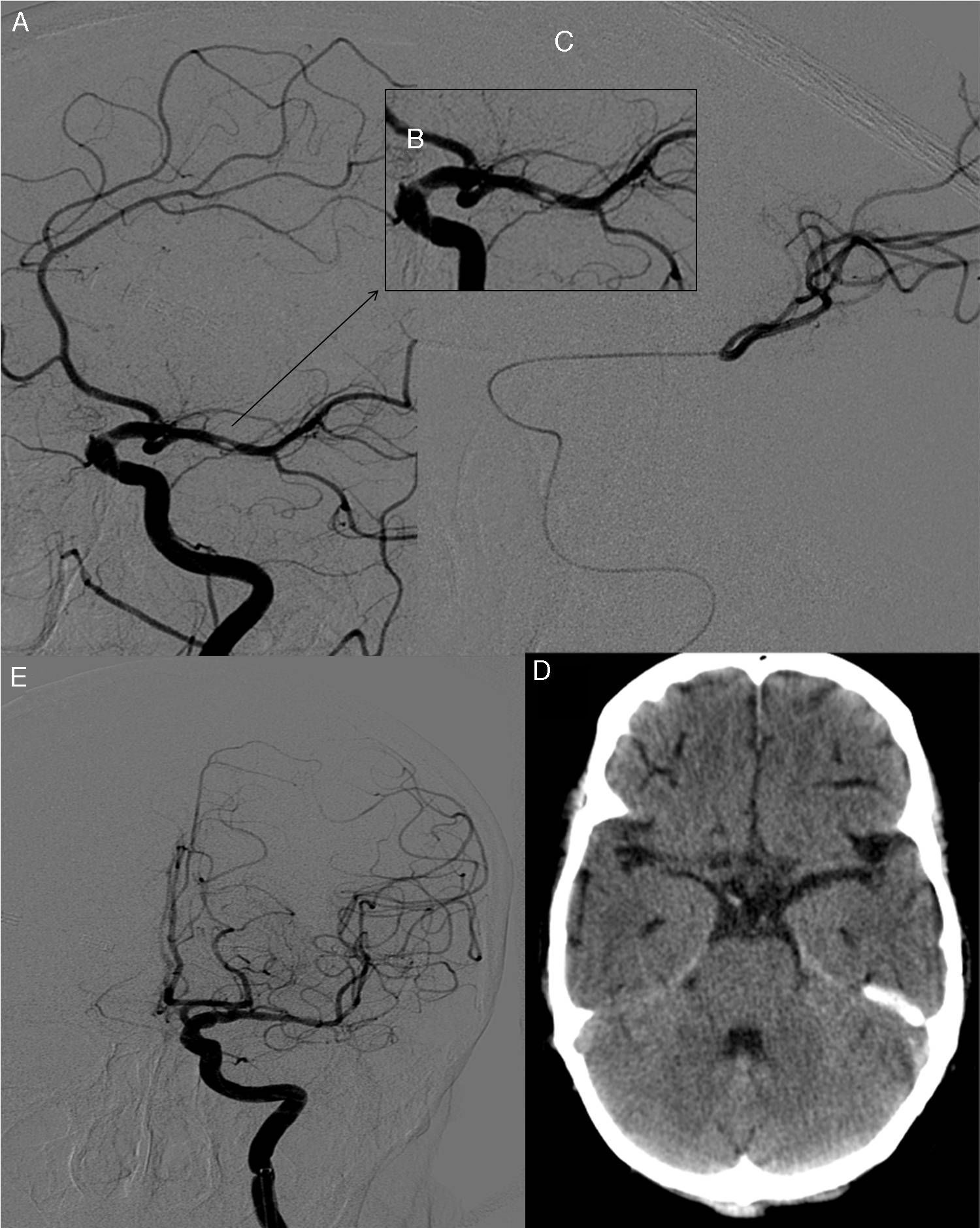
A) Angiografía selectiva de la carótida interna izquierda. Se observa un émbolo cálcico en la ACM izquierda. B) Imagen angiografía aumentada en la que se observa la casi oclusión del vaso. C) Embolectomía mediante dispositivo TREVO, procedimiento que cursa con éxito tras un solo pase, como se observa en la angiografía de control tras el procedimiento (D). E) TC cerebral de control con ausencia de material cálcico en el área teórica de la ACM izquierda.
La estenosis de la válvula aórtica calcificada es el trastorno valvular-cardíaco adquirido más común en los países desarrollados, y la intervención quirúrgica es a menudo indicada para resolver los síntomas y la mortalidad asociada1. Las válvulas aórticas calcificadas pueden ser una fuente de émbolos al cerebro. Los factores que predisponen a la embolia cerebral cálcica incluirían la manipulación mecánica de las válvulas durante los procedimientos diagnósticos o terapéuticos, aunque también pueden aparecer espontáneamente o rara vez por endocarditis2,3.
El 20% de los pacientes con prótesis valvulares cardiacas presentarán un ictus cardioembólico dentro de los 15años tras el reemplazo de la válvula4. Por otra parte, el ictus isquémico por tromboembolia perioperatoria o por hipoperfusión es una complicación bien conocida de la cirugía cardiovascular. Esta cirugía conlleva un riesgo considerable de ictus perioperatorio, potencialmente atribuible al aumento de partículas y embolización de aire, siendo la embolización por calcio excepcional5. En una serie prospectiva de más de 16.000 pacientes de cirugía cardiaca, que fueron seguidos una media de 12días tras la intervención, el riesgo de ictus a corto plazo fue del 4,8% tras la sustitución aislada de la válvula aórtica, del 8,8% después de la sustitución de la válvula mitral y del 9,7% después de una intervención multiválvula6.
El ictus perioperatorio se pueden dividir en 2 categorías: precoz, presente en la extubación (intraoperatoria), y tardío, que ocurre posterior a la extubación (postoperatorio). Tarakji et al.7 estudiaron más de 45.000 pacientes y documentaron factores de riesgo diferenciales asociados al ictus precoz y al tardío, lo que podría corresponderse con mecanismos patogénicos distintos.
La demostración de una embolia cerebral calcificada por TC fue documentada por primera vez por Yock en 19818. La TC es generalmente menos sensible que la resonancia magnética en la identificación del ictus isquémico agudo, pero la TC sí es más sensible en la detección de la embolia por calcio9.
Aunque el diagnóstico de este tipo de ictus suele ser rápido, ya que se produce en pacientes hospitalizados, estrechamente monitorizados hemodinámica y neurológicamente, dentro de unidades de cuidados intensivos o unidades de reanimación de cirugía cardiaca, el manejo terapéutico es complicado y controvertido. Las guías de ictus existentes recomiendan evitar la trombólisis sistémica dentro de los 14días de la cirugía mayor10, lo que impide su uso en la mayoría de los casos de ictus perioperatorios, y en caso de poder utilizarse probablemente sería poco efectivo por la esencia misma del material embólico11. La terapia más prometedora para el ictus inmediatamente después de la cirugía mayor es la terapia endovascular utilizando dispositivos de recuperación de trombos. En este sentido, 5 ensayos clínicos aleatorizados recientemente publicados (MR CLEAN, EXTEND IA, ESCAPE, SWIFT PRIME y REVASCAT) han demostrado que la terapia endovascular es altamente beneficiosa en pacientes con oclusión de la arteria carótida interna intracraneal o ACM hasta 6h después de la aparición de los síntomas del ictus. El beneficio de la terapia endovascular con medios extractores de trombos, con respecto a un resultado de independencia funcional a 90días en términos de número necesario de pacientes a tratar, es de 3 a 7sujetos12-16. La extrapolación de estos datos para el período perioperatorio es obviamente especulativo, ya que hay muy pocos casos de embolia cálcica cerebral tratados con éxito mediante dispositivos extractores de trombos17,18. Este procedimiento presentaría el riesgo potencial de provocar la migración del material cálcico y hacer oclusiva la lesión. Algún grupo ha empleado con éxito sistemas de stent coronario montado sobre balón de angioplastia rechazando el émbolo contra la pared, aunque este procedimiento no está exento de riesgo de rotura del vaso19. En nuestro caso, la extracción mediante dispositivo stentriever fue exitosa, sin complicaciones y tras un solo pase.
Este caso ilustra, por un lado, la utilidad de la TC en la detección de embolia cerebral calcificada tras la sustitución de la válvula aórtica, y por otro, la necesidad de activar el Código ictus siempre que haya un ictus en el entorno hospitalario, ya que el diagnóstico rápido y exhaustivo de estos pacientes asociado al desarrollo presente de la terapia endovascular puede mejorar el pronóstico final de estos pacientes.
Este trabajo fue presentado de forma parcial en la LXVII Reunión Anual de la Sociedad Española de Neurología.