Las fístulas arteriovenosas espinales (FAVE) son excepcionales y representan el 3% de las lesiones espinales. Asocian gran morbilidad sin tratamiento precoz, pero el diagnóstico constituye un reto. Nuestro objetivo es evaluar sus características clínicas y revisar la evolución tras el tratamiento. ¿Puede ser tarde para tratar?
MétodosPresentamos una serie retrospectiva de 10 casos diagnosticados y tratados en 3 años en un hospital terciario.
ResultadosSe observó un predominio masculino (80%). La edad media fue de 65,4 años. El síntoma inicial predominante fue la claudicación de la marcha/paraparesia (70%). En la mayoría de los pacientes la clínica fue lentamente progresiva. Al diagnóstico, lo habitual fue la combinación de síntomas motores, sensitivos y esfinterianos. El tiempo medio desde el inicio de los síntomas hasta el diagnóstico fue de 24,3 meses. El 60% tenía un diagnóstico inicial erróneo. La RM espinal fue diagnóstica en el 90% de los casos; la arteriografía, en el 100%. La localización más frecuente fue dorsal baja y el tipo anatómico predominante fue FAVE dural (7 pacientes). Todas fueron tratadas con embolización, cirugía o con ambas y el 70% mejoró tras su cierre, independientemente del tiempo de evolución.
ConclusionesEl diagnóstico de las FAVE es difícil y generalmente tardío, lo que empeora el pronóstico de los pacientes. Se debe tener un alto nivel de sospecha ante síntomas de mielopatía o claudicación de la marcha exacerbadas con el ejercicio e intentar tratamiento precoz. Consideramos que el tratamiento siempre está indicado, independientemente del tiempo de evolución, al mejorar la calidad de vida o conseguir la estabilización.
Spinal arteriovenous fístulas (SAVF), a rare type of vascular malformation, account for 3% of all spinal cord lesions. Without early treatment, the associated morbidity is high; furthermore, SAVF pose a major diagnostic challenge. Our purpose was to evaluate the clinical characteristics of SAVF and review their progress after treatment to determine whether it may be too late for treatment in some cases.
MethodsWe present a retrospective series of 10 patients diagnosed with SAVF and treated at a tertiary hospital during a 3-year period.
ResultsIn our sample, SAVF were found to be significantly more frequent in men (80%). Mean age in our sample was 65.4 years. The most common initial symptom was intermittent claudication/paraparesis (70%). In most patients, symptoms appeared slowly and progressively. At the time of diagnosis, the most common symptoms were motor, sensory, and sphincter disorders. Mean time from symptom onset to diagnosis was 24.3 months. Initial diagnosis was erroneous in 60% of the patients. Spinal MRI was diagnostic in 90% of these cases and arteriography in 100%. The most common location of the fistula was the lower thoracic region and the most frequent type was dural (7 cases). All patients were treated with embolisation, surgery, or both and 70% improved after fistula closure regardless of progression time.
ConclusionsDiagnosis of SAVF is difficult and often delayed, which leads to poorer patient prognosis. We should have a high level of suspicion for SAVF in patients with intermittent claudication or paraparesis exacerbated by exercise. Early treatment should be started in these patients. Treatment should always aim to improve quality of life or stabilise symptoms, regardless of progression time.
Las fístulas arteriovenosas espinales (FAVE) son excepcionales. A pesar de representar el tipo de malformaciones vasculares espinales más frecuentes —agrupan el 70%—, únicamente alcanzan el 3% de todas las lesiones de la médula espinal1,2. Se consideran anomalías adquiridas, y es inusual encontrarlas en individuos menores de 50 años, aunque la etiología exacta aún es desconocida. Fisiopatológicamente consisten en un desarrollo anormal de una comunicación o shunt arteriovenoso de bajo flujo, pero con potenciales complicaciones graves. La llamada FAVE dural (también conocida como fístula dorsal intradural o dural raquídea) es el subtipo anatómico más frecuente, en el que el shunt se localiza en el trayecto de la raíz nerviosa correspondiente, dentro de la duramadre, y con suplencia a través de una arteria radiculomeníngea que drenará en venas radiculares, conectadas a su vez de forma centrípeta con venas perimedulares. Aunque menos frecuentes, existen otros 2subtipos: las FAVE piales (perimedulares o intradurales ventrales) y las fístulas epidurales (extradurales), con suplencia a través de una arteria radiculomedular y una arteria segmentaria, respectivamente3,4.
El mecanismo principal de daño en las FAVE durales y piales es el drenaje anómalo a través de venas perimedulares, lo que produce hipertensión venosa retrógrada y pérdida de regulación de los vasos medulares con disrupción de la barrera hematoencefálica y, consecuentemente, edema medular progresivo5. Con el tiempo, disminuye el gradiente de presión arteriovenosa, lo que conduce a la isquemia medular y, por tanto, a la mielopatía progresiva, que será más o menos reversible según el tiempo de evolución. No se ha dilucidado por completo el mecanismo patológico de estos shunts, pero se hipotetiza con que, una vez presentes, una progresiva fibrosis o una trombosis de venas radiculares (por la edad y acelerada por el shunt), que actuarían hasta entonces como rutas de drenaje alternativas desde las venas perimedulares arterializadas, podría ser un factor importante en la inducción de la hipertensión, al disminuir el flujo de salida6,7. Dado que la región toracolumbar presenta menor número de canales de drenaje venoso en comparación con otras regiones espinales, la congestión venosa es transmitida en dirección caudocraneal a lo largo de la médula espinal, lo que explica que en la mayoría de las ocasiones los primeros síntomas reflejen disfunción del cono medular8. Clínicamente se presentan con síntomas vagos de lento desarrollo (claudicación con el ejercicio, parestesias…) antes de producir una mielopatía severa con paraplejía y disfunción esfinteriana. Con mucha menos frecuencia cursan de forma aguda en forma de sangrado subaracnoideo o hematomielia, casi exclusiva de las piales, fístulas habitualmente de mayor flujo. En las FAVE epidurales, los síntomas por efecto de masa y compresión de estructuras vecinas (raíces y médula espinal), dado el tamaño que pueden llegar a adquirir, es el mecanismo principal de daño, aunque también la hipertensión venosa retrógrada juega un papel3,4.
La localización es típicamente toracolumbar; las cervicales son infrecuentes, sobre todo las inferiores a C2, prácticamente anecdóticas. Las superiores a C2 o craneocervicales pueden presentarse con congestión venosa, que incluso puede alcanzar al cono medular, o con sangrado subaracnoideo, mucho más frecuente que las toracolumbares, dependiendo del patrón de drenaje9.
Es conocido que, sin tratamiento, las FAVE asocian gran morbilidad2,10–13. Sin embargo, su historia natural y manejo siguen siendo temas controvertidos, con recomendaciones diversas según 2puntos de vista: el de la cirugía y el de la terapia endovascular. Con el presente artículo, queremos dar una visión intermedia desde una planta de Neurología, en la que en pocos años se han diagnosticado un número reseñable de casos. Los objetivos de nuestro trabajo son evaluar sus características clínicas y revisar la evolución tras el tratamiento, intentando responder a la siguiente pregunta: ¿Puede ser demasiado tarde para tratar?
Pacientes y métodosSe recopiló a un total de 10 pacientes mayores de 18 años con diagnóstico de FAVE realizado a lo largo de 3años (2012-2015) en la planta de Neurología del Hospital Clínico San Carlos de Madrid. Varios de estos pacientes acudieron al neurólogo como segunda e incluso tercera opinión desde otros centros y especialistas. Se ha realizado una recogida de datos clínicos de la historia hospitalaria y un seguimiento a largo plazo de los pacientes a través de consulta externa hospitalaria y por vía telefónica. Todos los pacientes fueron evaluados por neurólogos y tratados en nuestro centro, y han presentado un mínimo de seguimiento de 6 meses tras el tratamiento. Tras la obtención de todos los datos clínicos, se ha realizado un análisis descriptivo de los casos así como una revisión de la literatura consultando la base de datos Pubmed a través de las siguientes palabras clave: «spinal arteriovenous lesions», «spinal arteriovenous fistulas», «spinal dural arteriovenous fistulas», «spinal vascular malformations» «spinal vascular disorder», «mielopathy», «spinal angiography».
ResultadosFormas de presentación y características clínicasDe los 10 pacientes incluidos, 8 (80%) eran varones. La edad media al diagnóstico fue de 65,4 años (intervalo de 50 a 80). Las características de todos los pacientes se detallan en la tabla 1. Siete pacientes (70%) se presentaron con síntomas lentamente progresivos, 2 pacientes (20%) tuvieron un inicio agudo y un paciente (10%) se presentó con sintomatología fluctuante. Uno de los pacientes con inicio ictal cursó con una monoparesia crural aguda y desarrolló posteriormente una afectación bilateral y, el otro, presentó una paraplejía aguda por hemorragia subaracnoidea tras realización de una punción lumbar indicada por otro motivo.
Características clínicas y evolución de los 10 pacientes diagnosticados de fístulas arteriovenosas espinales
| Pte. n.° | Sexo/edad (años) | Tiempo hasta el diagnóstico | Curso clínico | Síntomas iniciales | Estado funcional al diagnóstico | RM espinal | Diagnóstico inicial | Tipo y localiza-ción de la FAVE | Tto. | Evolución clínica/estado funcional tras Tto | RM medular tras Tto |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H/72 | 48 meses | Agudo y posteriormente progresivo | Monoparesia MMII y claudicación de la marcha | G5, M2, B2 | Edema+FV | Síndrome pospolio y siringomielia | Dural/T7 izquierda | E+Qx | Mejoría/G4, M2, B0 | Mejoría del edema |
| 2 | H/78 | 84 meses | Progresivo | Claudicación de la marcha | G5, M2, B0 | Edema+FV+hemosi-derina saco tecal | ECL | Dural/l4 izquierda | E | Estable/G5, M2, B0 | Mejoría del edema y desaparición de FV |
| 3 | H/51 | 3 meses | Progresivo | Trastorno sensitivo de MMII | G1, M2, B2 | Edema+FV | Cefalea mixta | Dural/FM-C1 bilateral | 2 Qx | Empeoramiento/ G2, M1, B1 | Mejoría del edema y de FV |
| 4 | H/80 | 2 meses | Progresivo | Dolor cervical | G1, M0, B0 | Edema+FV | No | Dural/FM | 2 E+2 Qx | Empeoramiento/ G5, M2, B0 | Mejoría del edema |
| 5 | H/72 | 24 meses | Progresivo | Claudicación de la marcha | G5, M2, B2 | Edema+FV | Síndrome de piernas inquietas | Dural/T8 derecha | E+Qx | Mejoría/G3, M2, B0 | Igual |
| 6 | H/53 | 2 meses | Progresivo | Claudicación de la marcha | G4, M0, B1 y disfunción eréctil | Edema+FV | No | Epidural/l4 y T10-11 bilaterales | 4 E | Mejoría/G1, M0, B0 | Desaparición del edema, persistencia de FV |
| 7 | M/79 | 2 días | Agudo | Paraparesia grave y retención urinaria tras PL | G5, M2, B0 | HSA T9-saco y coágulos+edema cono | No | Epidural/T12-L1 izquierda | E | Mejoría/G3, M0, B0 | Igual |
| 8 | H/54 | 24 meses | Fluctuante | Torpeza de la marcha | G1, M0, B0 | Edema | EM | Perimedu-lar/T12 izquierda | Qx | Mejoría/G0, M0, B0 | Desaparición del edema |
| 9 | M/50 | 48 meses | Progresivo | Dolor lumbar | G2, M1, B0 | Edema+FV | ECL | Dural/T12 izquierda | E | Mejoría/G0, M1, B0 | Mejoría del edema y desaparición de FV |
| 10 | H/65 | 8 meses | Progresivo | Claudicación de la marcha | G2, M0, B0 | Edema+FV | No | Dural/l2 derecha | 2 E | Mejoría/G0, M0, B0 | Mejoría del edema y desaparición de FV |
Estado funcional medido según escala Aminoff-Logue (G: gait, M: micturition; B: bowel).
E: embolización; ECL: estenosis de canal lumbar; EM: esclerosis múltiple; FM: foramen magno; FV: flow voids; H: hombre; HSA hemorragia subaracnoidea; M: mujer; MMII: miembros inferiores; PL: punción lumbar; Qx: cirugía; Tto: tratamiento.
Al inicio, lo más frecuente fue la presentación con síntomas de una única modalidad: 7 pacientes (70%) con síntomas motores, 2 pacientes (20%) con dolor y un paciente (10%) con alteración sensitiva (tabla 2). La claudicación de la marcha o la paresia dependiente del ejercicio fue la presentación más frecuente. Como ejemplo representativo, el paciente 10, jugador de golf habitual, era capaz de describir la distancia exacta en forma de número de hoyos a la que le obligaba esa claudicación a detener la actividad cada día, con recuperación en minutos u horas. Los 2 pacientes que consultaron por dolor, uno de ellos con lumbalgia aislada y otro con cervicalgia irradiada a hombros, reportaron también empeoramiento con la actividad física y bipedestación así como mejoría significativa con el reposo y decúbito. El paciente que se presentó con síntomas sensitivos lo hizo en forma de parestesias en ambas piernas así como con fenómeno de Lhermitte reverso, desencadenado con la extensión cervical. Ningún paciente presentó disfunción esfinteriana como queja inicial.
Síntomas al inicio y al diagnóstico
| Síntoma | Inicial | Al diagnóstico |
|---|---|---|
| Claudicación de la marcha/paresia | 7 | 9 |
| Alteración sensitiva | 1 | 6 |
| Dolor | 2 | 0 |
| Disfunción de esfínteres | 0 | 6 |
| Otros | 0 | 1a |
Número de pacientes que presentaban dichos síntomas respecto al total (N=10).
Al diagnóstico, lo habitual fue la suma de síntomas: paresia, alteración sensitiva y disfunción esfinteriana. Nueve pacientes (90%) presentaron alteración motora (5 con afectación grave de la marcha, con uso de 2apoyos instrumentales o silla de ruedas, con puntuación media en la escala Aminoff-Logue 3,1); 6 pacientes (60%), alteración sensitiva y 6 pacientes (60%), disfunción esfinteriana (6 urinaria y 4 fecal). Un paciente (10%) asoció además disfunción eréctil (tabla 2).
Tiempo transcurrido hasta el diagnósticoUna vez iniciados los primeros síntomas, el tiempo medio hasta el descubrimiento de la FAVE (considerando este último su diagnóstico inequívoco por arteriografía espinal) fueron 24,3 meses, con mediana de 24 meses. Cinco pacientes (50%) fueron diagnosticados con más de un año de duración de los síntomas.
Se encontraron diagnósticos iniciales erróneos en 6 pacientes (60%). Se consideró diagnóstico inicial erróneo cuando la resonancia magnética (RM) medular inicial mostraba signos característicos de FAVE (hiperseñal del cordón en T2 o vasos serpinginosos o flow voids, con o sin realce poscontraste), pero el paciente recibió el diagnóstico de otra entidad. El más frecuente fue la enfermedad degenerativa lumbar, en 2 pacientes. Uno de ellos incluso fue tratado mediante cirugía de estenosis de canal lumbar, sin mejoría clínica ni radiológica. Otros diagnósticos fueron esclerosis múltiple, síndrome de piernas inquietas refractario a tratamiento, cefalea mixta, y en el paciente 1 coexistían los diagnósticos de síndrome pospoliomielitis y siringomielia. Todos estos pacientes son los que presentaron un mayor retraso en el diagnóstico.
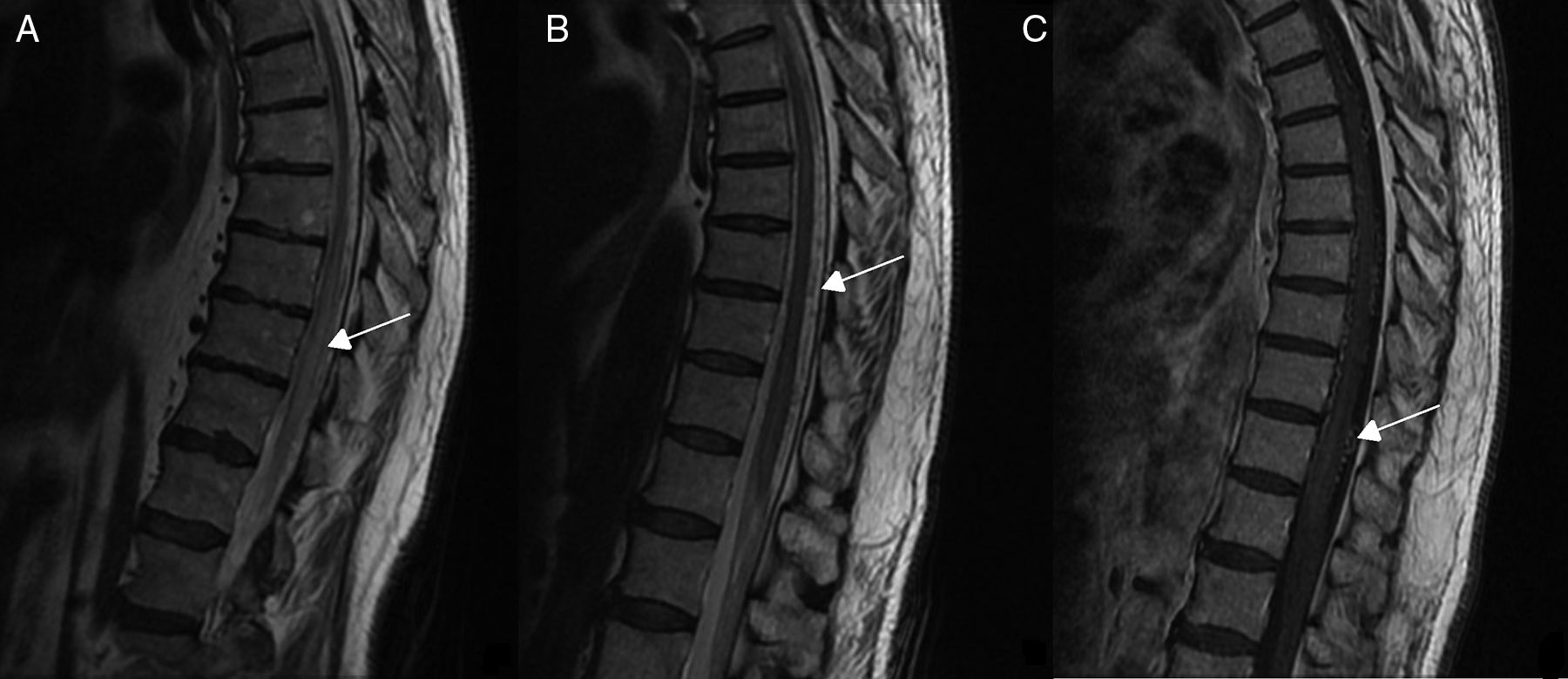
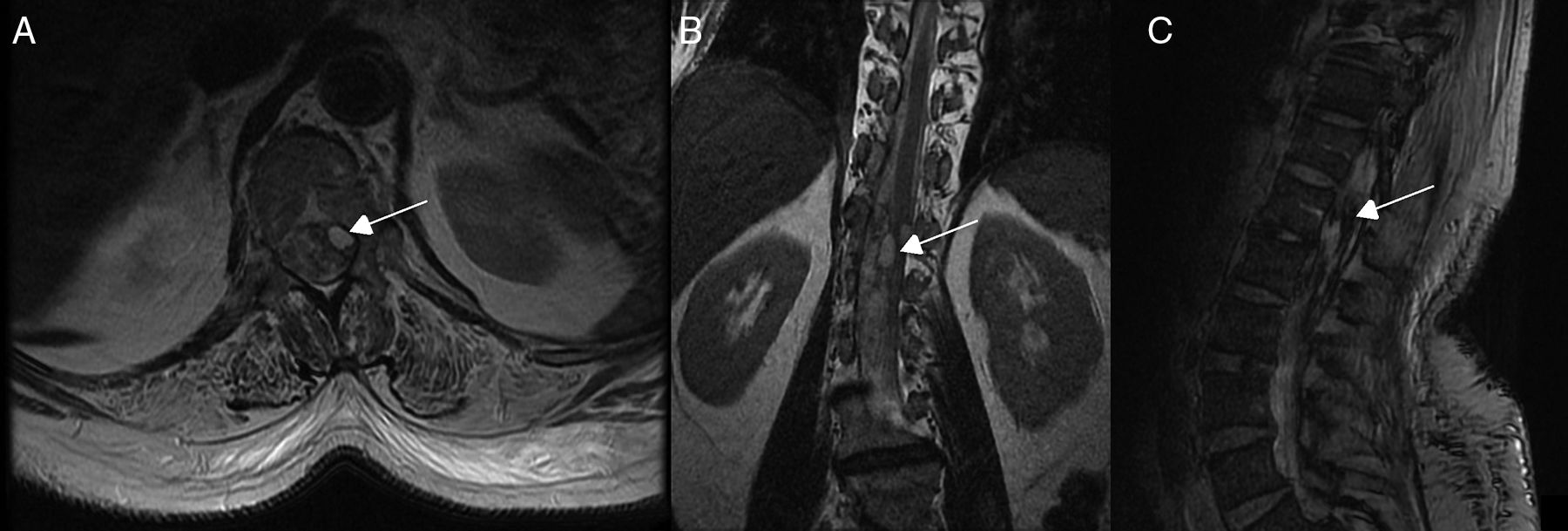
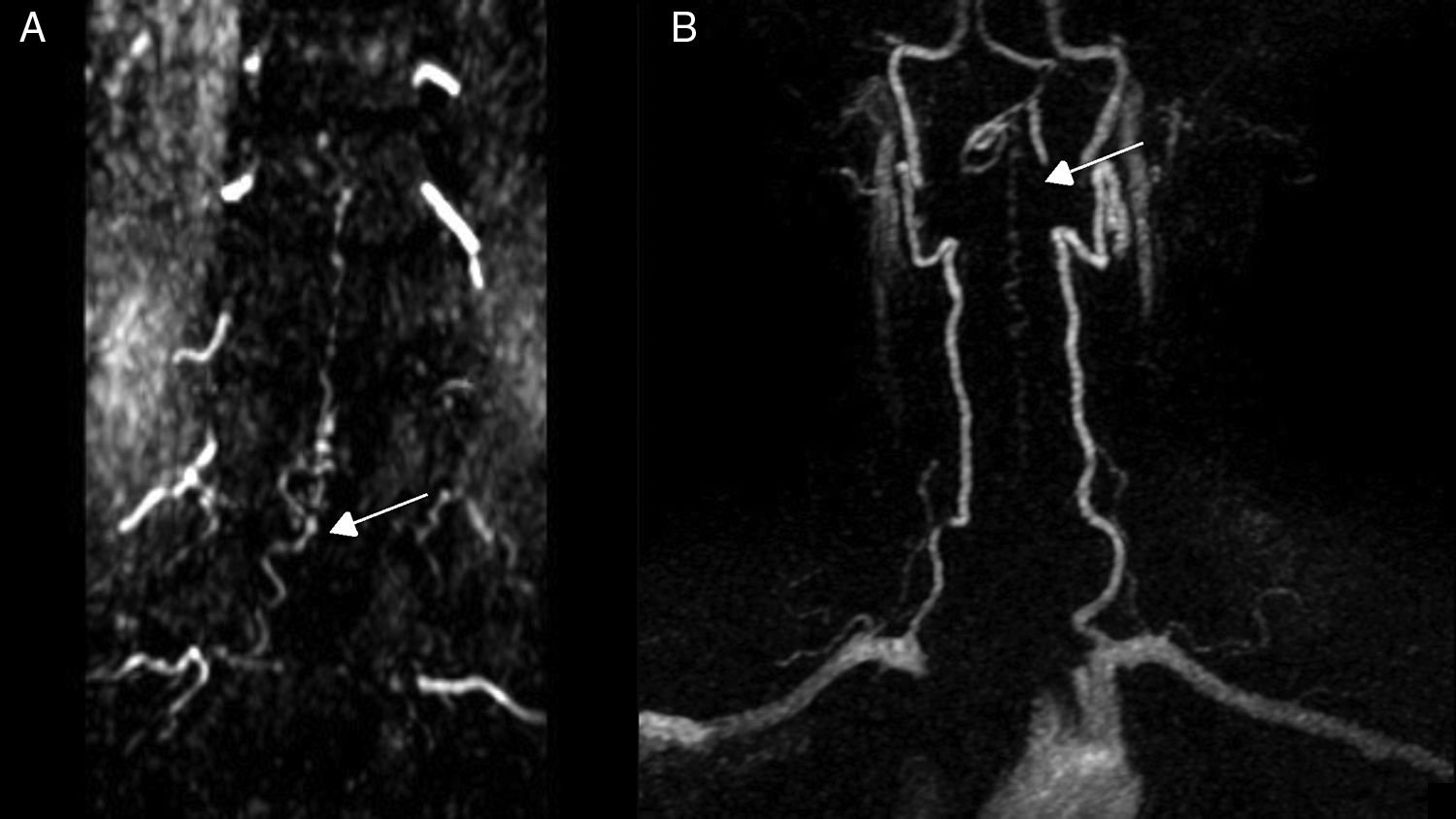
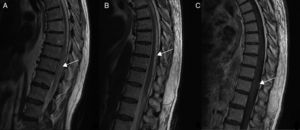
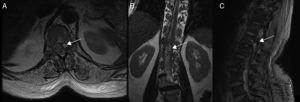
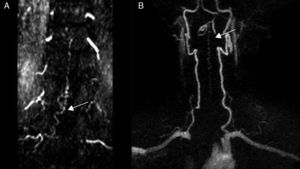
Pruebas diagnósticas y anatomía de las fístulas arteriovenosas espinalesSe realizó RM medular en todos los pacientes, que fue diagnóstica en 9 de ellos (90%). Los 9 mostraron hiperseñal en secuencias T2, con longitud media de 7,6 cuerpos vertebrales, en 8 de los cuales se involucraba al cono medular. Por otro lado, 8 de esos 9 pacientes presentaron los flow voids, con una media de 6,6 cuerpos vertebrales de longitud, únicamente ausente en el caso de fístula perimedular (fig. 1). En uno de los pacientes se encontraron signos de sangrado antiguo en el saco tecal. La RM no fue diagnóstica únicamente en el paciente que se presentó con un sangrado tras punción lumbar, artefactuando en gran medida la imagen (fig. 2). En 5 pacientes se incluyeron secuencias time-resolved imaging of contrast kinetics (TRICKS) en la RM diagnóstica: en 4 de ellos (80%) se pudo precisar el nivel exacto de la fístula (fig. 3).
RM medular del paciente 7. Múltiples imágenes de morfología irregular en el interior del saco tecal. A y B) Algunas imágenes son pseudonodulares e hiperintensas en T2. C) Otras son de baja intensidad evidentes en la secuencia de eco gradiente T2, con extensión aproximada desde T9 hasta saco tecal, así como hiperintensidad de señal difusa del LCR en T1, con coágulos que distorsionan la dirección de la salida de las raíces de la cola de caballo e hiperintensidad del cono medular, todo ello compatible con hemorragia subaracnoidea lumbar.
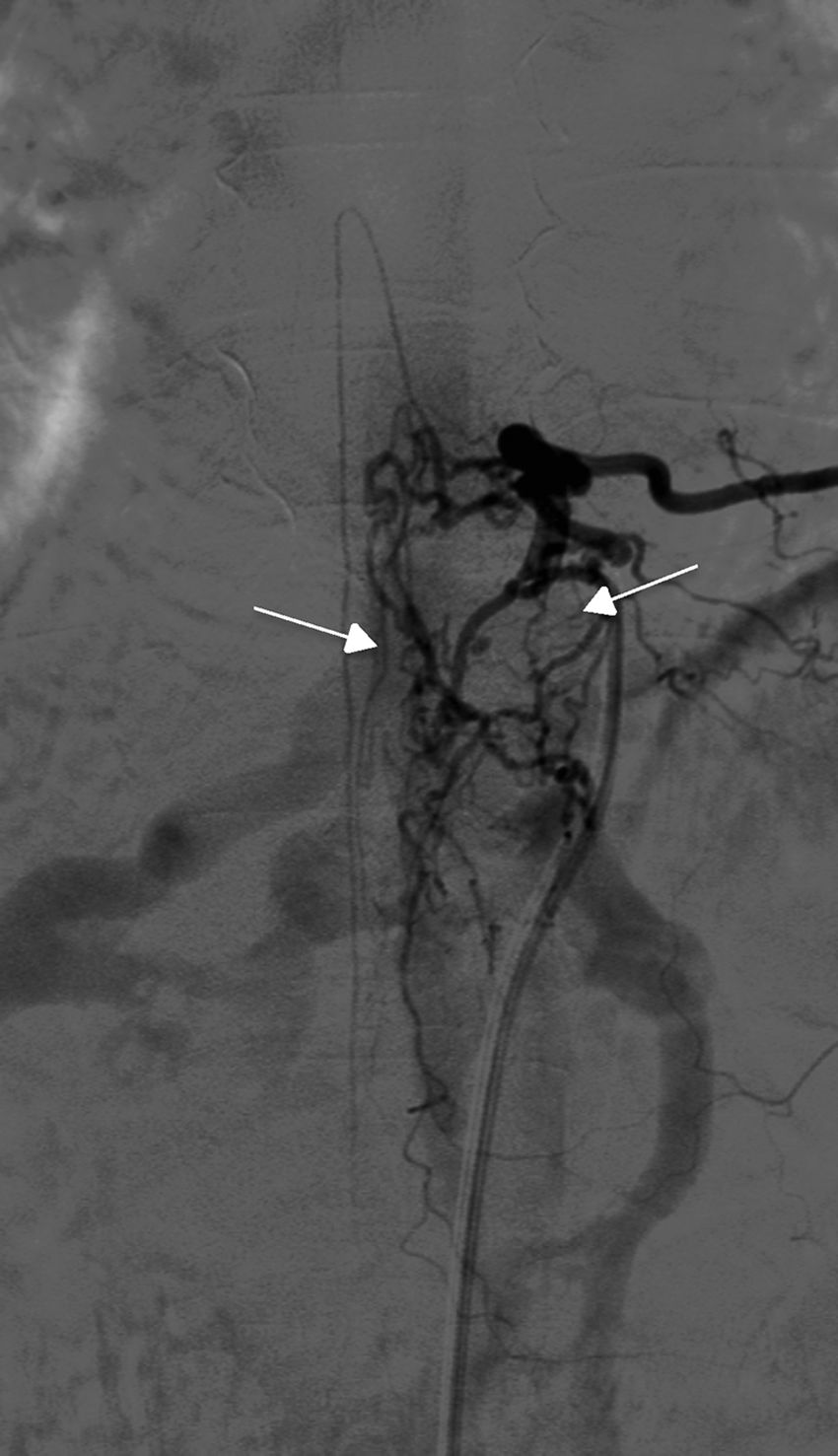
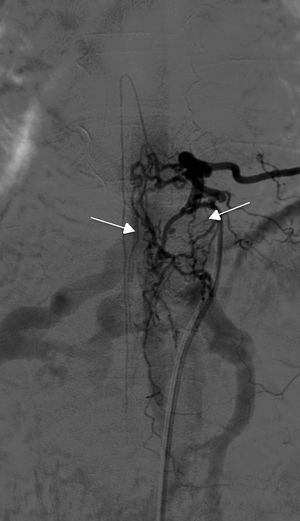
La arteriografía fue diagnóstica en los 10 pacientes (100%) en un único procedimiento, con identificación del subtipo anatómico: 7 fueron durales, 2 epidurales y una perimedular. En cuanto a la localización anatómica, 2 fueron cervicales (unión cráneo-cervical), 6 dorsales (todas por debajo de T7) y 3 lumbares. La localización más frecuente fue la dorsal baja. Un paciente cursó con 2fístulas simultáneas a 2niveles diferentes: dorsal y lumbar, ambas bilaterales (fig. 4). Según la lateralidad, 5 fístulas fueron izquierdas, 2 derechas y 3 bilaterales.
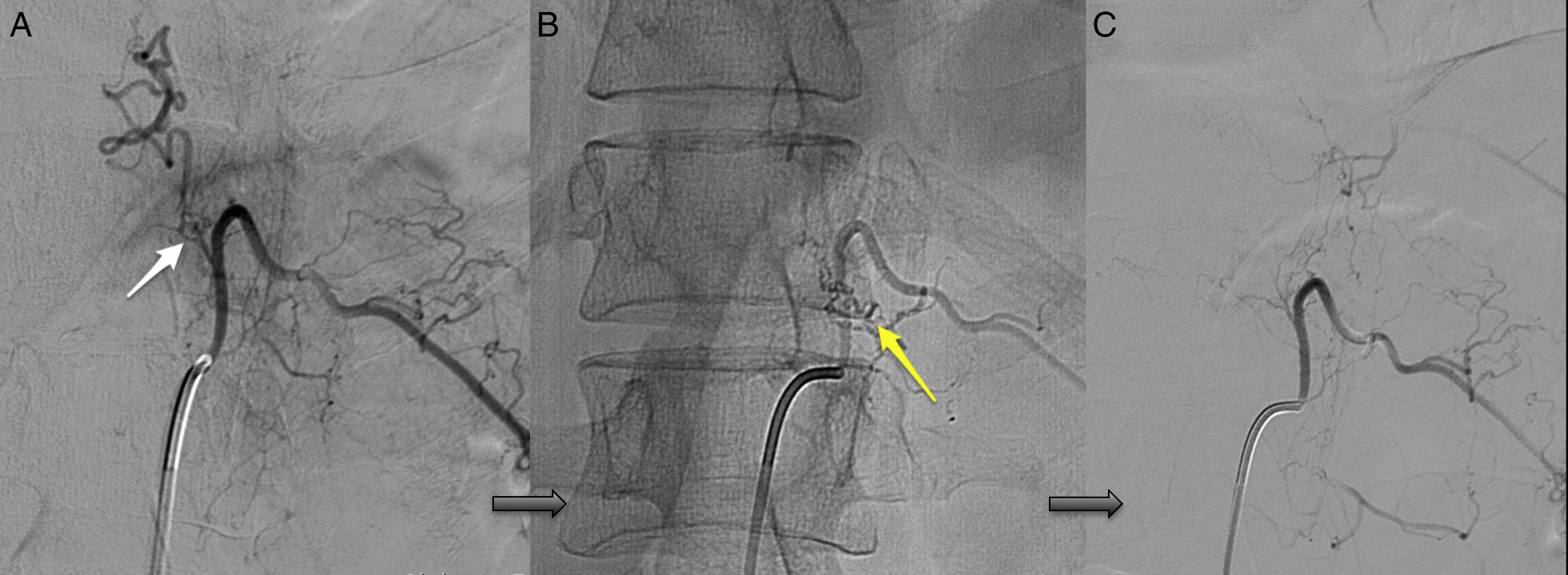
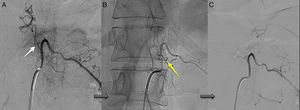
TratamientoLa estrategia empleada fue la terapia endovascular como primera elección en los casos técnicamente posibles y cirugía en el resto. De esta forma, 5 (50%) pacientes se trataron exclusivamente con embolización endovascular (fig. 5) y 2 (20%) con cirugía; fue necesario en 3 casos (30%) un abordaje combinado endovascular-cirugía. Los casos en los que se optó por la cirugía de entrada fueron una FAVE cervical, con angioarquitectura demasiado compleja para la embolización y una FAVE alimentada desde la arteria espinal anterior, contraindicación formal para la terapia endovascular. Seis de los pacientes (60%) requirieron varios intentos de cierre de la fístula en diferentes tiempos, ya fuese con el mismo procedimiento, ya fuese combinado. Concretamente, los 2 pacientes que presentaban FAVE cervicales requirieron varias intervenciones: uno de ellos, 2cirugías y el otro, 2embolizaciones y una cirugía. Solo 4 de los pacientes (40%) obtuvieron una obliteración completa con un único tratamiento y en un solo tiempo.
Evolución clínica y radiológicaEl parámetro utilizado para medir la evolución tras el tratamiento fue la escala Aminoff-Logue, por ser la empleada en la mayoría de las revisiones clínicas de FAVE (tabla 3). A pesar del elevado tiempo de evolución en muchos casos, se obtuvieron mejorías significativas con el cierre de las fístulas. En cuanto a la marcha —el parámetro más importante para la autonomía de los pacientes—, 7 (70%) de los pacientes afectados mejoraron en un grado significativo con el tratamiento (al menos variación en 1 punto en la escala) y un paciente (10%) permaneció estable, que fue aquel con más tiempo de evolución (84 meses). Solo 2 pacientes (20%) presentaron empeoramiento tras el tratamiento, ambos con FAVE cervicales y requerimiento de varias intervenciones por reaperturas hasta conseguir la oclusión total. En todos los pacientes se realizó un programa de rehabilitación mantenida en forma de cinesiterapia con movimientos pasivos o activos de las extremidades afectas según el grado de paresia y colaboración, así como mejoría de la marcha mediante hidroterapia y técnicas de control del equilibrio. Algún paciente recibió también electroestimulación. De los 7 pacientes con disfunción esfinteriana, 5 (71,4%) mejoraron de forma significativa sus síntomas (variación 1 punto en la escala), fundamentalmente a expensas de mejoría del esfínter fecal; la disfunción vesical fue la menos reversible.
Escala Aminoff-Logue
| Marcha (G) | Micción (M) | Defecación (B) |
|---|---|---|
| G0: sin déficit motor | M0: normal | B0: normal |
| G1: debilidad sin restricción de la actividad física | M1: urgencia o dificultad para iniciar la micción pero continente | B1: incontinencia ocasional o estreñimiento persistente |
| G2: debilidad con restricción de la actividad física | M2: incontinencia o retención ocasionales | B2: incontinencia persistente |
| G3: necesidad de un apoyo para la deambulación | M3: totalmente incontinente o retención persistente | |
| G4: necesidad de 2apoyos para la deambulación | ||
| G5: dependencia de silla de ruedas |
B: bowel; G: gait; M: micturition.
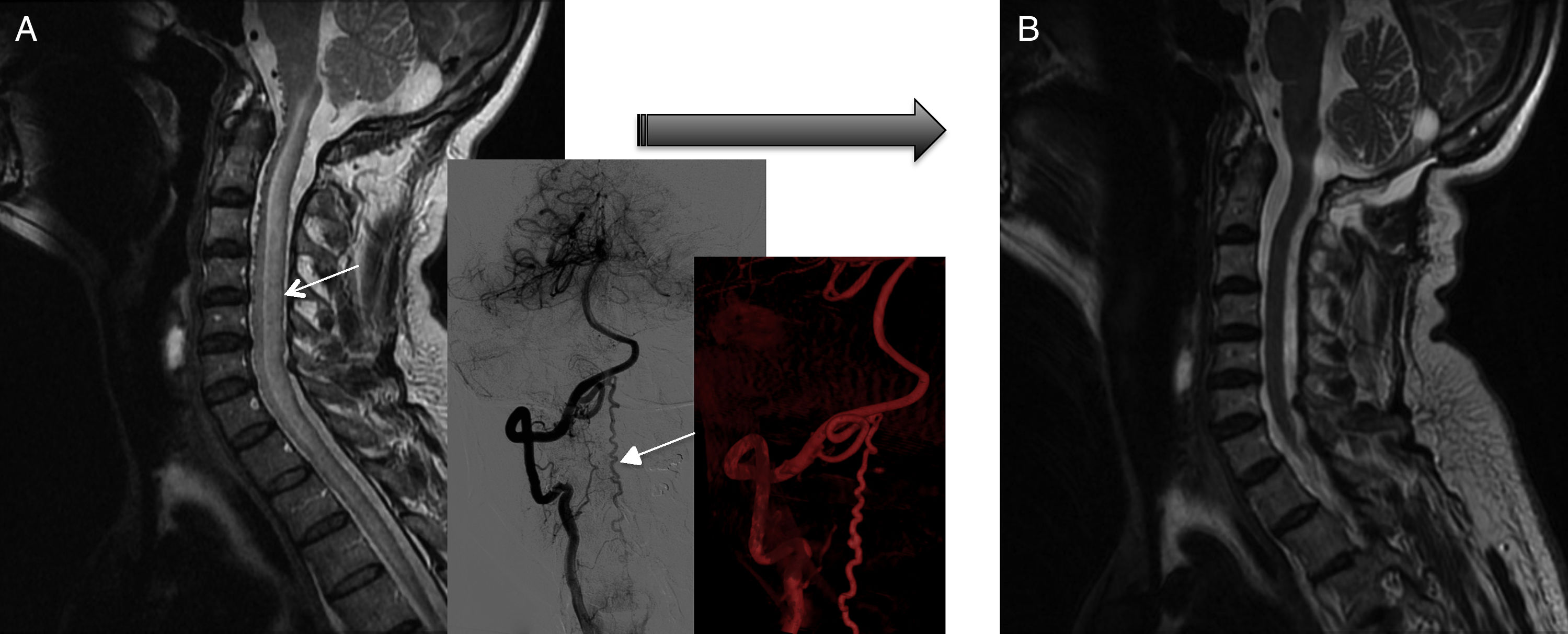
Todos los pacientes tuvieron confirmación angiográfica del cierre de la fístula. En la RM, 8 de los pacientes (80%) presentaron mejoría tras el cierre completo de la fístula, todos ellos con reducción del edema medular y 5 de ellos, además, con disminución significativa o desaparición de los signos de congestión venosa, aunque en 2 de ellos no se tradujo en mejoría clínica (ambos correspondían a los casos de fístulas cervicales, fig. 6). En 2 pacientes (20%) del total no se objetivaron cambios radiológicos: uno de ellos por reapertura recurrente y en el otro por hemorragia subaracnoidea; sin embargo, ambos experimentaron una mejoría clínica significativa.
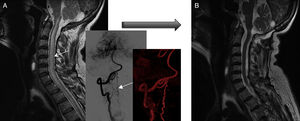
RM pre- y postratamiento quirúrgico del paciente 3. A) Se observa RM al diagnóstico con edema medular desde la unión bulbomedular hasta niveles torácicos (y reconstrucciones angiográficas). B) RM postratamiento (2 cirugías) con normalización de la señal. A pesar de ello, el paciente deterioró en un punto su estado funcional en la marcha.
Nuestra serie de pacientes con FAVE refleja unos datos demográficos superponibles a los descritos, con predominancia en varones, la mayoría en la sexta y séptima décadas de la vida1,2. Las características clínicas son también equiparables. La mayoría de los pacientes cursaron con síntomas lentamente progresivos, simétricos e inicialmente de una única modalidad, en su mayoría claudicación de la marcha o paresia de miembros inferiores exacerbada con el ejercicio, bipedestación prolongada o maniobra de Valsalva, debida al empeoramiento de la hipertensión venosa de la vena de drenaje arterializada. Este dato se ha asociado en la literatura sobre todo con fístulas torácicas14. Dos de nuestros pacientes aquejaron solo dolor durante meses, sin otros déficits añadidos, por lo que se debe considerar la existencia de una FAVE ante una cervicalgia o lumbalgia persistente, con o sin dolor radicular, en pacientes sin claros signos de enfermedad degenerativa espinal. La disfunción esfinteriana al inicio, al igual que en estudios previos, fue extremadamente infrecuente. Sin embargo, al diagnóstico lo habitual fue la combinación de síntomas (paresia, alteración sensitiva y disfunción esfinteriana) y mayores grados de discapacidad15–17. Lo habitual es encontrar signos de disfunción de motoneurona superior e inferior; la superior es la más relacionada con la discapacidad14. En cuanto a la posibilidad de cursar de forma asintomática, es una cuestión controvertida: se han descrito escasos casos diagnosticados por arteriografía que hayan cursado sin signos ni síntomas de mielopatía18–20.
Es conocido que el diagnóstico de las FAVE es difícil y tardío debido a la ausencia de características clínicas específicas, con tiempos largos hasta el diagnóstico en todas las series, lo que nos alerta de su pobre reconocimiento11–17. Es habitual el diagnóstico inicial, sobre todo en los pacientes de mayor edad, de otras entidades más prevalentes, como la enfermedad degenerativa lumbar, mielitis inflamatoria o incluso enfermedad nerviosa periférica4,10,11, al igual que lo ocurrido en nuestra muestra, e incluso el recorrido por diversos especialistas y la realización de múltiples pruebas hasta el diagnóstico.
En nuestra muestra, la RM espinal obtuvo una elevada sensibilidad (90%) en el diagnóstico de la FAVE. En algunos casos se realizaron secuencias TRICKS que demostraron un alto valor localizador al comparar los resultados con los hallados en la arteriografía espinal, considerada como prueba gold standard en el diagnóstico, lo que la coloca en un lugar muy prometedor. Consisten en una variación de la secuencia 3D TOF dinámica con contraste que permite la adquisición de múltiples fases con un único bolo de contraste, muchas de ellas con llenado venoso, lo que permite obtener una fase óptima para el diagnóstico respecto al 3D TOF convencional. Consideramos que la RM medular es una prueba diagnóstica fundamental para facilitar la toma de decisión al neurólogo de pedir una arteriografía (prueba compleja, invasiva e incluso con potencial de agravar la congestión venosa en algunos casos), orientar el nivel anatómico de la fístula y, por tanto, acortar el tiempo de arteriografía, e incluso como control evolutivo tras el tratamiento. Se debe realizar completa en todos los casos en los que se sospecha una fístula espinal, debido a la disociación de los niveles clínicos y radiológicos. Existen estudios que demuestran que los niveles de pinprick, muy frecuentes en la exploración, se corresponden en menos del 50% de los casos con el nivel de la fístula14 y que en muchas ocasiones tampoco se relaciona o no se suele incluir dentro de los niveles de hiperseñal en RM21. Uno de los estudios más largos realizados para estimar la sensibilidad y especificidad de la RM en el diagnóstico de las FAVE no encontró ningún caso diagnosticado por arteriografía que no presentase alguno de los signos radiológicos característicos: hiperintensidad en T2 correspondiente al edema medular o los flow voids correspondientes a la congestión y tortuosidad venosa18. En ese estudio, la hiperintensidad del cordón medular fue el hallazgo más frecuente (90% de los pacientes), seguido de los flow voids (80%), datos similares a los nuestros. Cuando ambos signos estaban presentes, la especificidad para el diagnóstico alcanzaba el 97%. Creemos, por tanto, obligada la realización de angiografía espinal ante la detección de alguno de estos 2signos en la RM y, sobre todo, ante la presencia de ambos. Probablemente se podría evitar si ninguno de ellos estuviese presente, y considerar entonces otros posibles diagnósticos. Otros hallazgos menos frecuentemente reportados, como la hiperseñal del cono medular, el realce poscontraste o la expansión del cordón medular, se consideran menos sensibles en el diagnóstico. Sin embargo, en nuestros pacientes, la hiperseñal del cono medular se objetivó en el 100% de las fístulas dorsales y lumbares —solo estuvo ausente en las 2cervicales—, por lo que es probable que la sensibilidad sea mayor a la descrita. Aunque es, por tanto, indiscutible la alta sensibilidad de la RM en el diagnóstico de las FAVE, no es absoluta, ya que existen estudios que han reportado un pequeño porcentaje de pacientes sin alteraciones en T2 (que se asoció además con una menor discapacidad)14,22, por lo que es fundamental un alto grado de sospecha de los clínicos.
Se han intentado establecer asociaciones entre los hallazgos radiológicos y la clínica de los pacientes en diversos estudios. Una mayor longitud de hiperseñal en T2 en la RM pretratamiento se ha relacionado con el empeoramiento de los síntomas con el ejercicio (lo que refleja el grado de médula espinal vulnerable a la isquemia ante mayores demandas energéticas), así como con el estado funcional pre- y postratamiento23,24, sin embargo, no se ha podido establecer relación entre la hiperseñal postoperatoria y el estado funcional o la discapacidad tras el tratamiento14,23. En nuestra serie, obtuvimos una disociación clínico-radiológica en algunos pacientes: casos que tras el cierre de la fístula presentaron mejoría clínica significativa (en 2 puntos de la escala Aminoff-Logue en la marcha) a pesar de no presentar mejoría radiológica, y pacientes que no experimentaron mejoría clínica pero sí en la RM. La RM tras tratamiento no parece, por tanto, ser buena predictora de la evolución.
Lo que sí parece claro es que el mal pronóstico funcional se asocia con tiempos de evolución mayores y, por tanto, con retraso en el diagnóstico, y que el estado funcional postratamiento se asocia con el estado funcional pretratamiento10,12,13. Los artículos más antiguos ya observaron que tratamientos por encima de los 3años desde el inicio de los síntomas se asociaban con peor evolución25, de lo que se concluye que el tratamiento debe ser lo más precoz posible.
El objetivo del tratamiento de las FAVE es eliminar la congestión venosa con el cierre completo de la comunicación arteriovenosa. Existen 2tipos de abordajes posibles: la cirugía, primera técnica empleada, consistente en laminectomía o laminoplastia con sección/desconexión de la vena de drenaje, y la embolización endovascular de los vasos nutricios o de la propia vena de drenaje. A pesar de que la mayoría de los estudios a lo largo del tiempo han reflejado una mayor efectividad de la cirugía respecto a la embolización, con hasta un 98% de éxitos quirúrgicos frente al 25-75% de las embolizaciones15,16,21,26,27, cada vez existe una mayor tendencia al abordaje endovascular por su menor agresividad, avances en la técnica con empleo de agentes embolizantes nuevos como el onyx y menores tiempos de recuperación y hospitalización3,28–32, si bien es cierto que no es posible su realización en todos los casos debido a la variabilidad de la vasculatura espinal o a un origen común de la arteria nutricia y la arteria de Adamkiewicz. En nuestros pacientes, se empleó la embolización endovascular como primera línea de tratamiento ante fístulas técnicamente posibles. No podemos comparar la efectividad de la embolización y la cirugía, ya que muchos de nuestros casos precisaron el abordaje combinado para su total cierre, lo que, por otra parte, suele ser una necesidad frecuente. Es fundamental una cooperación entre el neurocirujano y el neurorradiólogo para decidir el mejor tratamiento de estos pacientes32 y la actitud dependerá de forma importante de la experiencia de cada centro en ambos abordajes. Se ha reportado algún caso en los últimos tiempos de obliteración mediante «cirugía mínimamente invasiva», con ligadura endoscópica interlaminar guiada con microscopia de la vena de drenaje proximal, como técnica innovadora y poco agresiva en casos seleccionados; sin embargo, está por determinar aún su utilidad y efectividad en esta dolencia33. Por otro lado, se debe recordar que, ante un empeoramiento de los síntomas, siempre se debe descartar una recanalización de la FAVE, hecho relativamente frecuente y que se asocia con una peor evolución de los pacientes. También en esos casos es conveniente descartar la existencia de FAVE múltiples, bien sincrónicas o metacrónicas34.
Las fístulas de la unión craneocervical, aún más infrecuentes, probablemente correspondan a un subgrupo de lesiones diferentes, con presentación clínica que puede variar desde la mielopatía crónica hasta la hemorragia subaracnoidea intracraneal, o incluso disfunción de tronco. Por su menor prevalencia, establecer cuál es el mejor tratamiento para ellas aún es más controvertido. En la actualidad no hay estudios que comparen la eficacia de la cirugía y la embolización en ellas, por lo que creemos que el abordaje dependerá en gran medida de la angioarquitectura de la lesión y, como en todos los casos, de la experiencia del centro. En una de las últimas revisiones, la presentación hemorrágica y la obliteración quirúrgica fueron los factores asociados a un mejor pronóstico en este subgrupo35. Lo que está claro es la necesidad de tratamiento precoz, o incluso urgente, en aquellos casos con una mielopatía preexistente que presenten una exacerbación aguda.
La indicación de tratamiento preventivo en el caso de descubrir una FAVE asintomática por el momento es controvertido, dada su historia natural incierta, aunque creemos que, con el tiempo, todas acaban generando síntomas y probablemente el tratamiento en un estadio precoz o incluso asintomático sería lo correcto19. Una buena estrategia sería la monitorización estrecha con RM y la realización de tratamiento precoz ante la aparición de los primeros síntomas o alteraciones radiológicas.
En cuanto al uso de esteroides en el intento de mejorar los síntomas de mielopatía en estos pacientes, debe evitarse: se ha publicado en diversos estudios el empeoramiento de los déficits neurológicos durante la administración intravenosa u oral (o menos frecuentemente, epidural) o en la primeras 24 h desde su administración, que pueden no ser reversibles36,37. Se cree que podría deberse al aumento de la hipertensión venosa por los cambios osmóticos inducidos con la reabsorción renal de agua, o incluso se postula que podrían favorecer las trombosis venosas radiculopiales, al aumentar la congestión. Probablemente, se trate de una combinación de ambos mecanismos36,37. Un empeoramiento de los síntomas mielopáticos en un paciente tras la administración de esteroides debe hacernos sospechar una FAVE.
En la evolución tras el tratamiento, el 70% de nuestros pacientes presentó una mejoría significativa de la marcha, dato similar a la literatura13,28: fueron las fístulas craneocervicales las que presentaron peor pronóstico y manejo más complicado. Creemos que la medición de la discapacidad con escalas clínicas es de gran utilidad en el seguimiento. Al margen del objetivo del cierre fistuloso, el papel de la rehabilitación precoz y sostenida fue fundamental en todos los casos. A pesar de que en la mayoría de los estudios se ha hablado de una peor recuperación de la disfunción esfinteriana, la cual suele ser una manifestación tardía13,38, en nuestra serie, como en alguna otra11, la mayoría de los pacientes afectados experimentó una mejoría de los síntomas, sobre todo la disfunción fecal. Existen estudios que, a pesar de no encontrar relación entre el tiempo hasta el diagnóstico con los síntomas motores o sensitivos, sí han encontrado relación con una disfunción vesical grave. Este hecho probablemente sea debido a la hipertensión y congestión del cono medular, área más vulnerable a la isquemia por el menor número de canales venosos en comparación con áreas espinales superiores14. Por otro lado, es razonable pensar que aquellos pacientes con mayor duración de los síntomas hasta el diagnóstico tendrán una mayor discapacidad (reportado en numerosos estudios) y, consecuentemente, una peor evolución, y, sin embargo, en otros estudios se ha demostrado que la capacidad de mejoría tras el tratamiento no parece depender tanto del tiempo de duración de los síntomas como del estado clínico pretratamiento13. En cuanto a la localización anatómica, parece que las FAVE de localización torácica baja son las que presentan mayor capacidad de mejoría en la funcionalidad en comparación con fístulas en cualquier otro nivel, con diferencias significativas en el pronóstico motor. El hecho de presentar una vascularización más rica podría explicar esta diferencia, considerando el rol de la isquemia en la génesis del daño espinal en estos pacientes13.
Para concluir, el diagnóstico de las FAVE continúa siendo un reto, lo que las convierte en una entidad infradiagnosticada, pero a la vez son una causa tratable y curable de mielopatía. Consideramos que ante una claudicación de la marcha o una mielopatía de causa desconocida, el neurólogo siempre debe sospecharlas y buscarlas. La demora en su diagnóstico será lo que conferirá un peor pronóstico para los pacientes. Sin embargo, afirmamos que nunca es demasiado tarde para tratar, por mucho tiempo de evolución que presenten, ya que en un elevado porcentaje obtendremos la mejoría o, al menos, la estabilización de los síntomas. El tipo de tratamiento empleado dependerá sobre todo de la experiencia del centro y es fundamental en todos los casos el diálogo multidisciplinar.
Conflictos de interesesNo existen conflictos de intereses.