Los traumatismos craneoencefálicos leves (TCE-L) han sido tradicionalmente considerados acontecimientos sin repercusiones cerebrales significativas, cuya sintomatología remite espontáneamente en unos días. Sin embargo, estos hechos son cada vez más cuestionados. Este estudio pretende objetivar la existencia de alteraciones cognitivas precoces en una serie de pacientes con TCE-L y relacionar los hallazgos con distintos marcadores de lesión cerebral.
MétodosEstudio prospectivo de una cohorte de pacientes con un TCE-L valorados de forma consecutiva durante 12 meses. De un total de 1.144 pacientes, se seleccionó a 41 (3,7%) que habían presentado una conmoción cerebral. Además de la valoración clínica habitual y de la práctica de una tomografía computarizada (TC) cerebral, los pacientes fueron estudiados mediante un test estandarizado para síntomas posconmocionales en las primeras 24h después del TCE-L y al cabo de 1-2 semanas y, coincidiendo con la segunda valoración, mediante una batería neuropsicológica. Los resultados se compararon con los de un grupo de 28 voluntarios sanos de características parecidas. En 20 pacientes se practicó una resonancia magnética (RM) craneal.
ResultadosEn este análisis exploratorio, la memoria y el aprendizaje verbal fueron las funciones cognitivas más afectadas después del TCE-L. Siete de los 20 pacientes con TC cerebral normal presentaron alteraciones estructurales visibles por RM, que en 2 casos fueron compatibles con la presencia de lesión axonal difusa.
ConclusionesLos resultados de este estudio piloto sugieren la presencia de alteraciones cognitivas precoces y lesiones cerebrales estructurales en un porcentaje no despreciable de pacientes que han presentado una conmoción cerebral recuperada después de un TCE-L.
Mild traumatic brain injury (mTBI) has traditionally been considered to cause no significant brain damage since symptoms spontaneously remit after a few days. However, this idea is facing increasing scrutiny. The purpose of this study is to demonstrate the presence of early cognitive alterations in a series of patients with mTBI and to link these findings to different markers of brain damage.
MethodsWe conducted a prospective study of a consecutive series of patients with mTBI who were evaluated over a 12-month period. Forty-one (3.7%) of the 1144 included patients had experienced a concussion. Patients underwent a routine clinical evaluation and a brain computed tomography (CT) scan, and were also administered a standardised test for post-concussion symptoms within the first 24hours of mTBI and also 1 to 2 weeks later. The second assessment also included a neuropsychological test battery. The results of these studies were compared to those of a control group of 28 healthy volunteers with similar characteristics. Twenty patients underwent an MRI scan.
ResultsVerbal memory and learning were the cognitive functions most affected by mTBI. Seven out of the 20 patients with normal CT findings displayed structural alterations on MR images, which were compatible with diffuse axonal injury in 2 cases.
ConclusionsResults from this pilot study suggest that early cognitive alterations and structural brain lesions affect a considerable percentage of patients with post-concussion syndrome following mTBI.
Los traumatismos craneoencefálicos (TCE) constituyen un problema de elevada prevalencia, tanto en las sociedades industrializadas como en países en vías de desarrollo, con una incidencia estimada entre 150 y 250 casos al año por cada 100.000 habitantes1. Un 10% de los TCE son graves (puntuación en la escala de coma de Glasgow [ECG] ≤ 8), un 10% moderados (puntuación en la ECG entre 9 y 13) y un 80% de los afectados presentan un TCE leve (TCE-L), con una puntuación de 14 o 15 en la ECG2.
Tradicionalmente, se ha concedido poca importancia al estudio de las repercusiones de los TCE-L, al considerarse que se trata de un problema esencialmente reversible, sin patología cerebral detectable y con pocas o ninguna secuela residual. Sin embargo, en los últimos años los resultados de múltiples estudios cuestionan este hecho. En el contexto hospitalario, los protocolos habituales de manejo de los TCE-L establecen que cuando estos pacientes presentan una TC cerebral normal pueden ser dados de alta hospitalaria, frecuentemente sin seguimiento clínico. No obstante, existe evidencia reciente de que hasta un 25% de los TCE-L con tomografía computarizada (TC) normal presentan alteraciones en la resonancia magnética (RM) craneal3.
Además de la puntuación en la ECG (14-15), los criterios diagnósticos que se contemplan tradicionalmente en el diagnóstico de los TCE-L son la pérdida de consciencia (PDC) —que debe ser inferior a 30 min— y la presencia de una posible amnesia postraumática (APT) de duración inferior a 24h. Cuando alguno de estos criterios está presente, se considera que el paciente presenta una «conmoción cerebral»4. Las consecuencias de un TCE-L pueden ser muy variables y van desde una ausencia absoluta de síntomas residuales hasta la presencia de un cortejo sintomático florido que incluye cefaleas, mareos, náuseas, inestabilidad de la marcha, irritabilidad, alteraciones de memoria o dificultades de concentración. Tres meses después del traumatismo, aproximadamente un 30% de los afectados sigue sin recuperarse ad integrum5, presentando lo que se conoce como un síndrome posconmocional (SPC)6.
A pesar de los avances en las técnicas de identificación del daño cerebral, la mayoría de los estudios reconocen la existencia de un porcentaje de personas que después de un TCE-L presenta síntomas persistentes e incapacitantes, en ausencia de alteraciones evidentes en las pruebas de neuroimagen. Esto explica porque muchos autores consideran que la lesión cerebral puede no ser la única causa de las alteraciones a largo plazo detectadas en algunos pacientes después de un TCE-L. En estos casos, las secuelas residuales podrían estar influidas por una serie de condicionantes como rasgos de personalidad, enfermedades mentales o sistémicas preexistentes, comorbilidad asociada (dolor crónico, trastornos ansioso-depresivos, etc.), factores sociopsicológicos y la implicación del paciente en algún tipo de reclamación o demanda judicial7.
Según los paradigmas clásicos, la gran mayoría de las alteraciones neuropsicológicas secundarias a un TCE moderado o grave pueden explicarse por la localización de las lesiones cerebrales8. Sin embargo, en ausencia de lesiones focales evidentes en la TC cerebral, las disfunciones cognitivas de estos pacientes pueden deberse a la desconexión de diversas estructuras anatómicas cerebrales, debido a la presencia de una lesión axonal difusa (LAD)5. Este fenómeno puede constituir también el sustrato que explica la presencia de síntomas y alteraciones cognitivas residuales en algunos pacientes que han presentado un TCE-L. Entre las consecuencias neuropsicológicas más frecuentes asociadas a los TCE-L se encuentran alteraciones en la velocidad de procesamiento de la información, atención y memoria9-12.
Para facilitar el diagnóstico de posibles lesiones estructurales en los TCE-L, los protocolos de RM más recientes incluyen secuencias de ponderación de la susceptibilidad de los tejidos (SWI, por su nomenclatura en inglés, susceptibility weighted imaging)13. El SWI es una técnica extremadamente sensible a elementos paramagnéticos, especialmente útil en la identificación de microhemorragias, habiéndose constatado en algunos estudios que esta técnica es muy superior (hasta 6 veces más)14 a las secuencias potenciadas en T2* para la detección de microsangrados puntiformes que se asocian a la LAD.
El objetivo de este estudio piloto es valorar la presencia de alteraciones cognitivas y síntomas afectivos y conductuales precoces (antes de los 14 días después del traumatismo) en una serie de pacientes que han presentado una conmoción cerebral secundaria a un TCE-L respecto de un grupo control de voluntarios sanos, y explorar si existen relaciones entre los déficits cognitivos objetivados y los síntomas clínicos. De forma adicional, para determinar la severidad de la lesión encefálica, se pretende analizar la presencia de lesiones estructurales mediante RM en un subgrupo de pacientes incluidos en el estudio.
Pacientes y métodosPacientes y grupo controlLos pacientes incluidos en este estudio fueron atendidos en el servicio de Urgencias de Neurotraumatología del Hospital Universitario Vall d’Hebron (HUVH) entre abril del 2013 y abril del 2014. Para ser incluidos en este estudio, los pacientes debían cumplir todos los criterios de inclusión y ninguno de los de exclusión siguientes:
- –
Criterios de inclusión: a) edad comprendida entre los 18 y los 65 años; b) ser catalán y/o castellanoparlantes; c) haber presentado un TCE-L con una puntuación de 14 o 15 en la ECG dentro de las 24 h previas a la inclusión en el estudio; d) haber presentado una conmoción cerebral, identificada por la presencia de una pérdida transitoria de consciencia<30 min —verificada mediante la presencia de algún testigo—, vómitos, crisis comiciales, APT inferior a 24h o síntomas posconmocionales intensos (tabla 1); e) exploración neurológica normal, y f) TC cerebral normal.
Tabla 1.Criterios empleados para la identificación de una conmoción cerebral en pacientes atendidos en las primeras 24h después de un traumatismo craneoencefálico leve (TCE-L). En el presente estudio se exigía presencia de por lo menos uno de los siguientes indicadores, clasificados de manera dicotómica (sí/no)
Indicador Comentario Pérdida de consciencia Requería la confirmación por un testigo. Debe diferenciarse de episodios sincopales Amnesia postraumática Evalúa la evocación detallada de los acontecimientos de justo antes y después del TCE-L Crisis Signos posconmocionales objetivos Vómitos Síntomas posconmocionales severos Registro de la severidad de los siguientes síntomas, mediante una escala de 0 a 4:
Cefalea, náuseas, sensación de inestabilidad, hipersensibilidad a la luz, hipersensibilidad a los ruidos, desorientación, visión borrosa y mareos
Los síntomas se clasificaron como severos si cualquiera de ellos tenía una intensidad ≥ 3, o la suma de la intensidad de todos los síntomas era ≥ 5 puntos - –
Criterios de exclusión: 1) TCE previo que hubiera requerido atención hospitalaria; 2) antecedentes de abuso crónico de sustancias psicoactivas; 3) enfermedad psiquiátrica o neurológica conocida; 4) enfermedad sistémica crónica con potenciales repercusiones cognitivas (insuficiencia renal, hepática, síndrome metabólico, etc.), y 5) politraumatismo con un índice en la escala de severidad superior a 6.
La exploración neurológica de los pacientes y la interpretación inicial de la TC cerebral fueron llevadas a cabo por el neurocirujano de guardia, puesto que se trata de procedimientos rutinarios en la evaluación del TCE-L. Las TC cerebrales realizadas en urgencias fueron posteriormente revaluadas por los neurorradiólogos del HUVH.
El grupo control fue reclutado a partir de los acompañantes y familiares de los pacientes ingresados en el servicio de neurocirugía del HUVH. De las personas interesadas en formar parte del grupo control, se seleccionó a aquellas que cumplían los criterios de inclusión (a) y (b) y ninguno de los criterios de exclusión (1-4) antes mencionados. Además de los criterios anteriores, se seleccionaron aquellos casos con edades y nivel de estudios paralelos a las de los pacientes. El grupo control final quedó constituido por 28 voluntarios (18 varones y 10 mujeres), con una mediana de edad de 29 años (rango intercuartil [RIC] 21, mínimo: 18, máximo: 64).
Todos los pacientes y los participantes del grupo control firmaron el consentimiento informado aceptado por el Comité de Ética del HUVH (PR-AG-47-2013).
Procedimientos de evaluación y seguimientoAdemás de la valoración clínica inicial, todos los pacientes fueron evaluados dentro de las primeras 24h del traumatismo. Adicionalmente, 34 pacientes fueron estudiados en un segundo tiempo, dentro de las 2 primeras semanas post-TCE. Un subgrupo de 20 pacientes se exploró también mediante RM craneal (14 varones y 6 mujeres, con una mediana de edad de 29, RIC 21, mínimo: 18 y máximo 64). Todos los participantes del grupo control fueron valorados en una ocasión.
Evaluación estandarizada de la conmociónDurante su estancia en Urgencias de Neurotraumatología, dentro de las primeras 24h después del TCE-L, y en una segunda ocasión, coincidiendo con la exploración neuropsicológica, los pacientes fueron evaluados mediante la prueba Sport Concussion Assessment Tool Second Edition (SCAT2)15. El SCAT2 es una herramienta de evaluación estandarizada diseñada para medir los efectos agudos de las conmociones cerebrales producidas en un contexto deportivo. Este test registra la presencia de síntomas posconmocionales, la pérdida de consciencia (debe ser confirmada por testigos), la puntuación en la ECG y exige una evaluación del equilibrio y coordinación, así como una valoración cognitiva mediante el Standardized Assessment of Concussion (SAC). El SAC incluye la evaluación de la orientación temporal, memoria —inmediata y diferida— y concentración. El SCAT2 constituye una herramienta especialmente útil en el ámbito clínico debido a sus características de valoración multidimensional y a su brevedad16. Las puntuaciones máximas son de 30 puntos para el SAC y de 100 puntos para el SCAT2 total.
Valoración neuropsicológicaTodos los participantes fueron evaluados neuropsicológicamente en una ocasión y en el caso de los pacientes se realizó dentro de las primeras 2 semanas después del TCE-L. Para la evaluación de las funciones cognitivas se empleó una batería neuropsicológica específica formada por pruebas de valoración de la atención, memoria, velocidad del procesamiento de la información y funciones ejecutivas complejas (tabla 2). Para la elección de las pruebas se siguieron las recomendaciones del National Institute of Neurological Disorders and Stroke americano2. Los test seleccionados forman parte del Core Data Elements recomendado para el estudio de este tipo de pacientes2. Además, los pacientes realizaron una prueba de valoración de esfuerzo (TOMM)17 para identificar posibles intentos de simulación de síntomas o una mera falta de colaboración durante la exploración, y respondieron a un cuestionario de sintomatología ansioso-depresiva (HAD)18, dado que la presencia de estos síntomas puede influir en los perfiles cognitivos. La exploración cognitiva completa requería un tiempo aproximado de 120 min e incluía un periodo de 5-10 min de descanso, si era necesario. Estos estudios se llevaron a cabo por investigadoras específicamente formadas en neuropsicología (AR y VC).
Lista de pruebas de la batería de evaluación neuropsicológica
| Objetivo de su aplicación | Nombre de la prueba |
|---|---|
| Memoria | Test de aprendizaje verbal auditorio de Rey19 Brief Visual Memory Test-Revised20 |
| Atención y velocidad de procesamiento | Trail MakingTest21, Parte A Conner's Continuous Performance Test-II, v. 5.222 Subtest Clave de números de la batería Wechsler de inteligencia para adultos (WAIS-III)23 Subtest Búsqueda de símbolos de la WAIS-III |
| Funciones ejecutivas | Test oral de asociación controlada de palabras21 Trail Making Test, Parte B Subtests de memoria de trabajo de la WAIS-III (Letras y números; Dígitos) |
| Valoración del esfuerzo | Test of Memory Malingering17 |
Los estudios por RM se realizaron en un equipo SIEMENS Magnetom TrioTim syngo 3-tesla, en el Centro para el Diagnóstico por Imagen del Hospital Clínic de Barcelona y fueron analizados por una colabora externa al proyecto, experta en neurorradiología (NB). En cada caso, se obtuvo una imagen estructural potenciada en T1, de alta resolución (3D Magnetization Prepared Rapid Gradient Echo, MP-RAGE), además de secuencias mediante los protocolos Fluid Attenuated Inversion Recovery (FLAIR) y de gradiente echo en T2. Para la identificación de microsangrados se adquirieron secuencias de SWI. El orden de las secuencias fue el mismo para todos los participantes y las exploraciones se realizaron antes de 14 días desde el TCE-L.
Análisis estadísticoEl análisis de todas las variables se realizó mediante el paquete estadístico SPSS (versión 22, SPSS, Chicago, Illinois, EE. UU.). Debido a que la gran mayoría de las variables no siguen una distribución normal, la comparación y el análisis de asociaciones entre las diferentes variables registradas se realizaron mediante pruebas no paramétricas (test de la ji al cuadrado y el test de Mann-Whitney-Wilcoxon).
Con respecto a la evaluación neuropsicológica, donde el análisis implica muchas variables relacionadas, es conocido que la probabilidad de error de tipo i aumenta al realizar comparaciones estadísticas múltiples y se podría argumentar el uso de la corrección de Benjamini y Hochberg24 para la tasa de descubrimientos falsos o directamente un p-valor más conservador de 0,01. No obstante, el tamaño muestral pequeño reduce considerablemente el poder estadístico. Por lo tanto, se decidió seguir un abordaje estadístico más liberal, asumiendo en la interpretación de todos los resultados presentados una probabilidad de error del 5%. Para describir mejor la intensidad de las diferencias estadísticamente significativas encontradas, se calculó el tamaño del efecto mediante el indicador r.
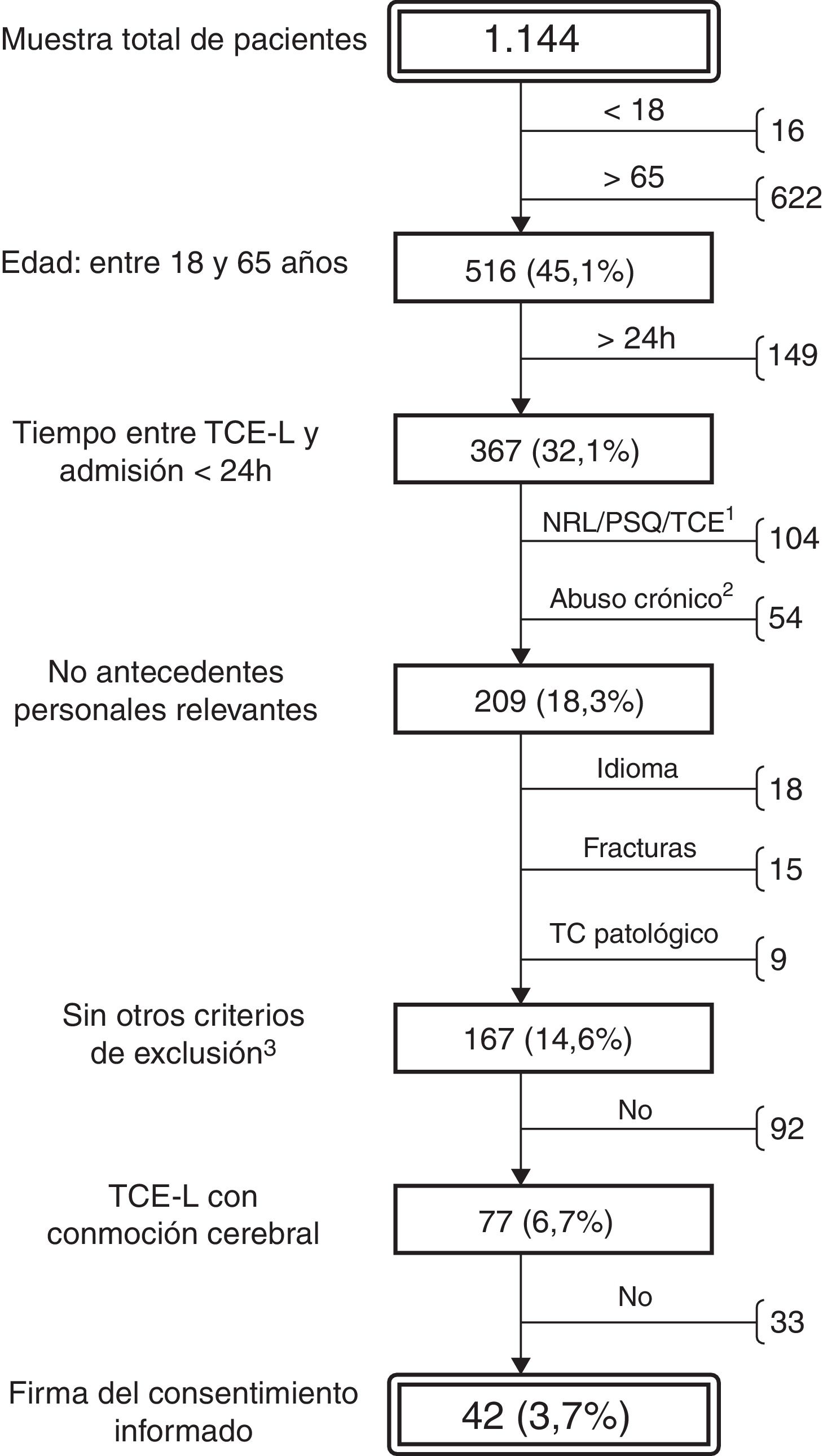
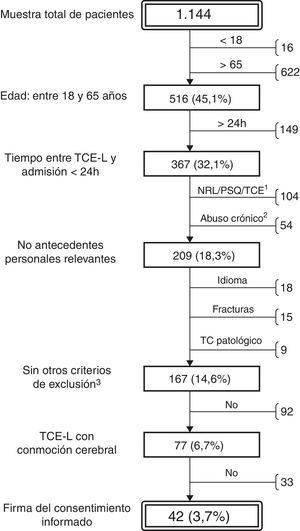
ResultadosDurante el periodo de estudio, el Servicio de Neurocirugía atendió a 1.144 pacientes con el diagnóstico de TCE-L. La mayor parte de estos pacientes tenían una edad avanzada o habían presentado un traumatismo craneal banal, sin pérdida de consciencia, ni APT ni otros síntomas relevantes asociados. De los 1.144 pacientes, se seleccionó a un total de 41 (16 mujeres y 25 varones, con una mediana de edad de 34 años, RIC de 24 y un rango de 18-64 años) (fig. 1) que cumplían los criterios de inclusión y ninguno de los de exclusión. En todos ellos se realizó una evaluación cognitiva breve y el registro de síntomas posconmocionales el mismo día del traumatismo mediante el SCAT2 y los resultados se compararon con los del grupo control. No obstante, 7 de estos 41 pacientes (17%) no acudieron a la visita de seguimiento, por lo que la valoración cognitiva extensa de seguimiento se redujo a los 34 pacientes restantes (12 mujeres y 22 varones, con una mediana de edad de 32,5 años, RIC 23, mínimo de 18 y máximo de 64).
Algoritmo de selección de pacientes con un traumatismo craneoencefálico (TCE) leve atendidos en Urgencias de Neurotraumatología del Hospital Universitario Vall d’Hebron durante un año. Los porcentajes se refieren al número total de pacientes. Motivos de exclusión: enfermedades neurológicas, psiquiátricas o TCE previo (1); abuso crónico de alcohol o drogas (2); otros (3): conocimiento insuficiente de castellano o catalán, fracturas que requirieron ingreso y hallazgos patológicos en la TC cerebral inicial.
Como era esperable, a pocas horas del TCE-L, los pacientes presentaron un número significativamente mayor de síntomas y una mayor gravedad de los mismos que los participantes sanos (z=−4,44, p<0,001, r=0, 53 y z=−4,88, p<0,001, r=0,58, respectivamente; tabla 3). Asimismo, el indicador global del SCAT2 mostró diferencias significativas entre los 2 grupos (z=3,46, p<0,001, r=0,43).
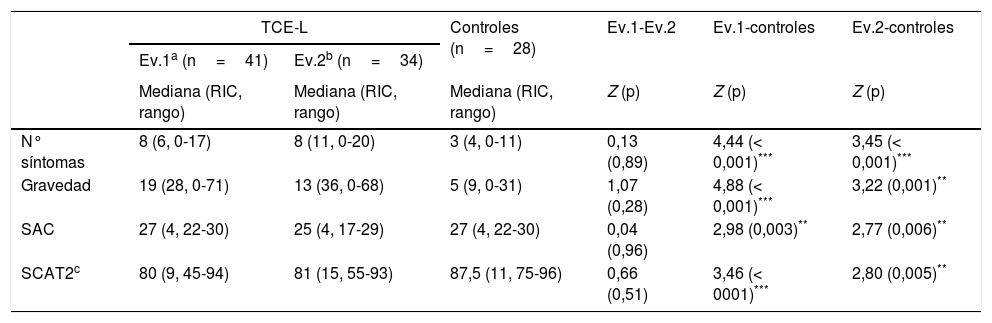
Evaluación longitudinal del SCAT2 en el grupo de TCE-L y resultados en el grupo control
| TCE-L | Controles (n=28) | Ev.1-Ev.2 | Ev.1-controles | Ev.2-controles | ||
|---|---|---|---|---|---|---|
| Ev.1a (n=41) | Ev.2b (n=34) | |||||
| Mediana (RIC, rango) | Mediana (RIC, rango) | Mediana (RIC, rango) | Z (p) | Z (p) | Z (p) | |
| N° síntomas | 8 (6, 0-17) | 8 (11, 0-20) | 3 (4, 0-11) | 0,13 (0,89) | 4,44 (< 0,001)*** | 3,45 (< 0,001)*** |
| Gravedad | 19 (28, 0-71) | 13 (36, 0-68) | 5 (9, 0-31) | 1,07 (0,28) | 4,88 (< 0,001)*** | 3,22 (0,001)** |
| SAC | 27 (4, 22-30) | 25 (4, 17-29) | 27 (4, 22-30) | 0,04 (0,96) | 2,98 (0,003)** | 2,77 (0,006)** |
| SCAT2c | 80 (9, 45-94) | 81 (15, 55-93) | 87,5 (11, 75-96) | 0,66 (0,51) | 3,46 (< 0001)*** | 2,80 (0,005)** |
Ev.1 representan las evaluaciones agudas, realizadas en las primeras 24h después del traumatismo craneoencefálico leve (TCE-L).
Ev.2 representan las segundas evaluaciones, realizadas a una mediana de 5 días después del TCE-L, con un mínimo de 2 y un máximo de 13 días después del traumatismo.
El SCAT2 no puede calcularse en los casos en los que no se ha aplicado la evaluación del equilibrio, por lo que los valores corresponden a una n=35 de pacientes en la exploración aguda y a una n=31 en la exploración de seguimiento.
Ev.: evaluación; SAC: Standardized Assessment of Concussion; SCAT2: Sport Concussion Assessment Tool versión 2.
En la valoración clínica de seguimiento realizada varios días después del traumatismo, el número y la gravedad de los síntomas, así como el valor total del SCAT2, seguían mostrando diferencias estadísticamente significativas entre los pacientes traumáticos y los del grupo control (z=−3,45, p<0,001; r=0,44; z=3,22, p=<0,001; r=0,41; z=2,80, p=0,005, r=0,36, respectivamente). En cambio, los resultados del cuestionario específico para síntomas de depresión y ansiedad HAD objetivaron que no existían diferencias significativas entre los 2 grupos en las subescalas de ansiedad (z=−0,59, p=0,55) y depresión (z=−0,68, p=0,50).
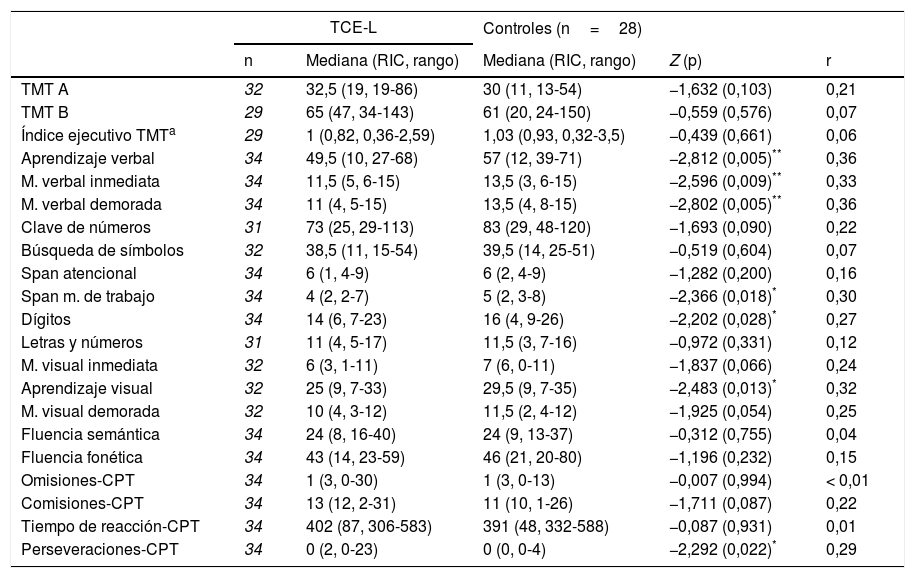
Valoración neuropsicológicaEn los 34 pacientes que acudieron a la visita de seguimiento se realizó una valoración neuropsicológica extensa, cuyos resultados se compararon con los del grupo control (n=28). La mayoría de los pacientes se valoraron durante la primera semana después del TCE-L (mediana: 5 días, mínimo 2 y máximo 13 días, tabla 4). La tabla 5 muestra los resultados más relevantes de la evaluación cognitiva de los 2 grupos estudiados. En la tabla puede observarse que el tamaño muestral varió entre test, dado que en los pacientes que presentaban lesiones leves de la extremidad superior dominante no se aplicaron las pruebas que requerían actividades manuales como realizar dibujos o valorar la velocidad psicomotora.
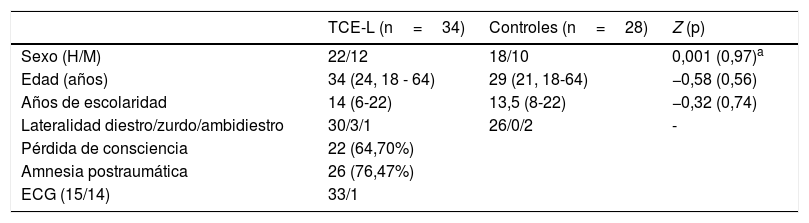
Descriptores sociodemográficos y clínicos relevantes en los pacientes evaluados neuropsicológicamente y en el grupo control
| TCE-L (n=34) | Controles (n=28) | Z (p) | |
|---|---|---|---|
| Sexo (H/M) | 22/12 | 18/10 | 0,001 (0,97)a |
| Edad (años) | 34 (24, 18 - 64) | 29 (21, 18-64) | −0,58 (0,56) |
| Años de escolaridad | 14 (6-22) | 13,5 (8-22) | −0,32 (0,74) |
| Lateralidad diestro/zurdo/ambidiestro | 30/3/1 | 26/0/2 | - |
| Pérdida de consciencia | 22 (64,70%) | ||
| Amnesia postraumática | 26 (76,47%) | ||
| ECG (15/14) | 33/1 |
Mediana, rango intercuartil y valores mínimo y máximo entre paréntesis.
ECG: escala de coma de Glasgow; TCE-L: traumatismo craneoencefálico leve.
Análisis comparativo de la evaluación neuropsicológica realizada en los pacientes evaluados y el grupo control
| TCE-L | Controles (n=28) | ||||
|---|---|---|---|---|---|
| n | Mediana (RIC, rango) | Mediana (RIC, rango) | Z (p) | r | |
| TMT A | 32 | 32,5 (19, 19-86) | 30 (11, 13-54) | −1,632 (0,103) | 0,21 |
| TMT B | 29 | 65 (47, 34-143) | 61 (20, 24-150) | −0,559 (0,576) | 0,07 |
| Índice ejecutivo TMTa | 29 | 1 (0,82, 0,36-2,59) | 1,03 (0,93, 0,32-3,5) | −0,439 (0,661) | 0,06 |
| Aprendizaje verbal | 34 | 49,5 (10, 27-68) | 57 (12, 39-71) | −2,812 (0,005)** | 0,36 |
| M. verbal inmediata | 34 | 11,5 (5, 6-15) | 13,5 (3, 6-15) | −2,596 (0,009)** | 0,33 |
| M. verbal demorada | 34 | 11 (4, 5-15) | 13,5 (4, 8-15) | −2,802 (0,005)** | 0,36 |
| Clave de números | 31 | 73 (25, 29-113) | 83 (29, 48-120) | −1,693 (0,090) | 0,22 |
| Búsqueda de símbolos | 32 | 38,5 (11, 15-54) | 39,5 (14, 25-51) | −0,519 (0,604) | 0,07 |
| Span atencional | 34 | 6 (1, 4-9) | 6 (2, 4-9) | −1,282 (0,200) | 0,16 |
| Span m. de trabajo | 34 | 4 (2, 2-7) | 5 (2, 3-8) | −2,366 (0,018)* | 0,30 |
| Dígitos | 34 | 14 (6, 7-23) | 16 (4, 9-26) | −2,202 (0,028)* | 0,27 |
| Letras y números | 31 | 11 (4, 5-17) | 11,5 (3, 7-16) | −0,972 (0,331) | 0,12 |
| M. visual inmediata | 32 | 6 (3, 1-11) | 7 (6, 0-11) | −1,837 (0,066) | 0,24 |
| Aprendizaje visual | 32 | 25 (9, 7-33) | 29,5 (9, 7-35) | −2,483 (0,013)* | 0,32 |
| M. visual demorada | 32 | 10 (4, 3-12) | 11,5 (2, 4-12) | −1,925 (0,054) | 0,25 |
| Fluencia semántica | 34 | 24 (8, 16-40) | 24 (9, 13-37) | −0,312 (0,755) | 0,04 |
| Fluencia fonética | 34 | 43 (14, 23-59) | 46 (21, 20-80) | −1,196 (0,232) | 0,15 |
| Omisiones-CPT | 34 | 1 (3, 0-30) | 1 (3, 0-13) | −0,007 (0,994) | < 0,01 |
| Comisiones-CPT | 34 | 13 (12, 2-31) | 11 (10, 1-26) | −1,711 (0,087) | 0,22 |
| Tiempo de reacción-CPT | 34 | 402 (87, 306-583) | 391 (48, 332-588) | −0,087 (0,931) | 0,01 |
| Perseveraciones-CPT | 34 | 0 (2, 0-23) | 0 (0, 0-4) | −2,292 (0,022)* | 0,29 |
CPT: Continuous Performance Test; M.: memoria; TCE-L: traumatismo craneoencefálico leve; TMT: Trail Making Test.
La prueba que mejor permitió discriminar entre los 2 grupos fue la Lista de aprendizaje verbal auditivo de Rey. El rendimiento de los pacientes fue significativamente inferior que el observado en el grupo control en la capacidad de aprendizaje y la memoria verbal inmediata y diferida, con un tamaño del efecto mediano (con r>0,3). También estaban por debajo del grupo de referencia la capacidad de aprendizaje visual y la memoria visual diferida, aunque esta última diferencia solo tendía a la significación estadística (p=0,054). Además, los pacientes obtuvieron puntuaciones significativamente inferiores en 3 indicadores: span de memoria de trabajo, subtest de Dígitos y en el número de perseveraciones del CPT. Estas variables ofrecen información sobre aspectos de la atención y funciones ejecutivas (por el componente de memoria de trabajo y de inhibición) que aparecen alteradas a pocas semanas después del TCE-L.
Cabe destacar que debido al número elevado de variables introducidas en el análisis, cualquier estrategia estadística más conservadora, que implemente una corrección por comparaciones múltiple, establecería el umbral de significación por debajo de p=0,003, aproximadamente, mientras que las alteraciones que se han objetivado en esta cohorte de pacientes tienen un nivel de significación de 0,005 o superior.
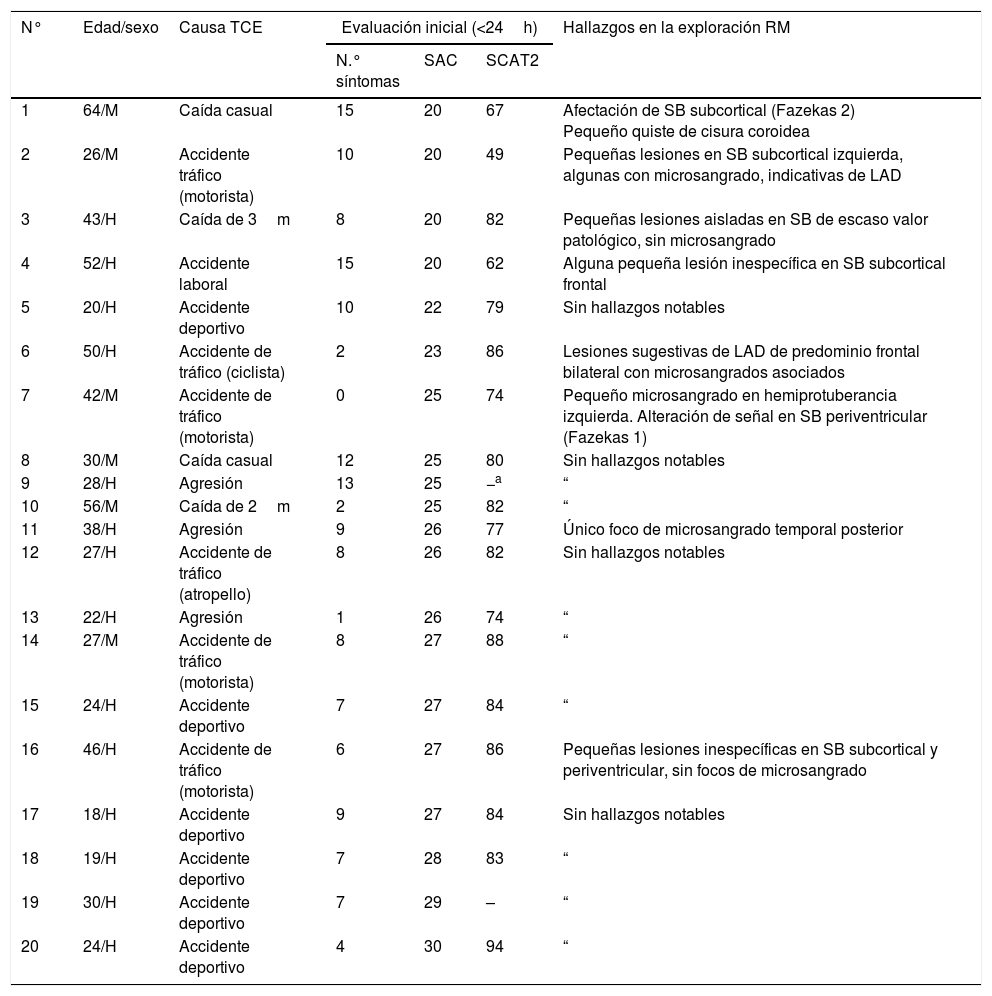
Resultados de la resonancia magnéticaLas exploraciones mediante RM craneal se realizaron a un subgrupo de 20 pacientes, seleccionados según su disponibilidad para la realización de la prueba. La mediana de días después del traumatismo en el que se realizó la RM fue de 6, con un valor mínimo de 1 día y un máximo de 13. La tabla 6 muestra una descripción detallada de los datos demográficos de este subgrupo de 20 pacientes, junto con los hallazgos neurorradiológicos objetivados.
Características demográficas, clínicas y neurorradiológicas de los 20 pacientes evaluados mediante RM, ordenados por la puntuación del SAC
| N° | Edad/sexo | Causa TCE | Evaluación inicial (<24h) | Hallazgos en la exploración RM | ||
|---|---|---|---|---|---|---|
| N.° síntomas | SAC | SCAT2 | ||||
| 1 | 64/M | Caída casual | 15 | 20 | 67 | Afectación de SB subcortical (Fazekas 2) Pequeño quiste de cisura coroidea |
| 2 | 26/M | Accidente tráfico (motorista) | 10 | 20 | 49 | Pequeñas lesiones en SB subcortical izquierda, algunas con microsangrado, indicativas de LAD |
| 3 | 43/H | Caída de 3m | 8 | 20 | 82 | Pequeñas lesiones aisladas en SB de escaso valor patológico, sin microsangrado |
| 4 | 52/H | Accidente laboral | 15 | 20 | 62 | Alguna pequeña lesión inespecífica en SB subcortical frontal |
| 5 | 20/H | Accidente deportivo | 10 | 22 | 79 | Sin hallazgos notables |
| 6 | 50/H | Accidente de tráfico (ciclista) | 2 | 23 | 86 | Lesiones sugestivas de LAD de predominio frontal bilateral con microsangrados asociados |
| 7 | 42/M | Accidente de tráfico (motorista) | 0 | 25 | 74 | Pequeño microsangrado en hemiprotuberancia izquierda. Alteración de señal en SB periventricular (Fazekas 1) |
| 8 | 30/M | Caída casual | 12 | 25 | 80 | Sin hallazgos notables |
| 9 | 28/H | Agresión | 13 | 25 | −a | “ |
| 10 | 56/M | Caída de 2m | 2 | 25 | 82 | “ |
| 11 | 38/H | Agresión | 9 | 26 | 77 | Único foco de microsangrado temporal posterior |
| 12 | 27/H | Accidente de tráfico (atropello) | 8 | 26 | 82 | Sin hallazgos notables |
| 13 | 22/H | Agresión | 1 | 26 | 74 | “ |
| 14 | 27/M | Accidente de tráfico (motorista) | 8 | 27 | 88 | “ |
| 15 | 24/H | Accidente deportivo | 7 | 27 | 84 | “ |
| 16 | 46/H | Accidente de tráfico (motorista) | 6 | 27 | 86 | Pequeñas lesiones inespecíficas en SB subcortical y periventricular, sin focos de microsangrado |
| 17 | 18/H | Accidente deportivo | 9 | 27 | 84 | Sin hallazgos notables |
| 18 | 19/H | Accidente deportivo | 7 | 28 | 83 | “ |
| 19 | 30/H | Accidente deportivo | 7 | 29 | – | “ |
| 20 | 24/H | Accidente deportivo | 4 | 30 | 94 | “ |
LAD: lesión axonal difusa; RM: resonancia magnética; SAC: Standardized Assessment of Concussion; SB: sustancia blanca; SCAT2: Sport Concussion Assessment Tool versión 2.
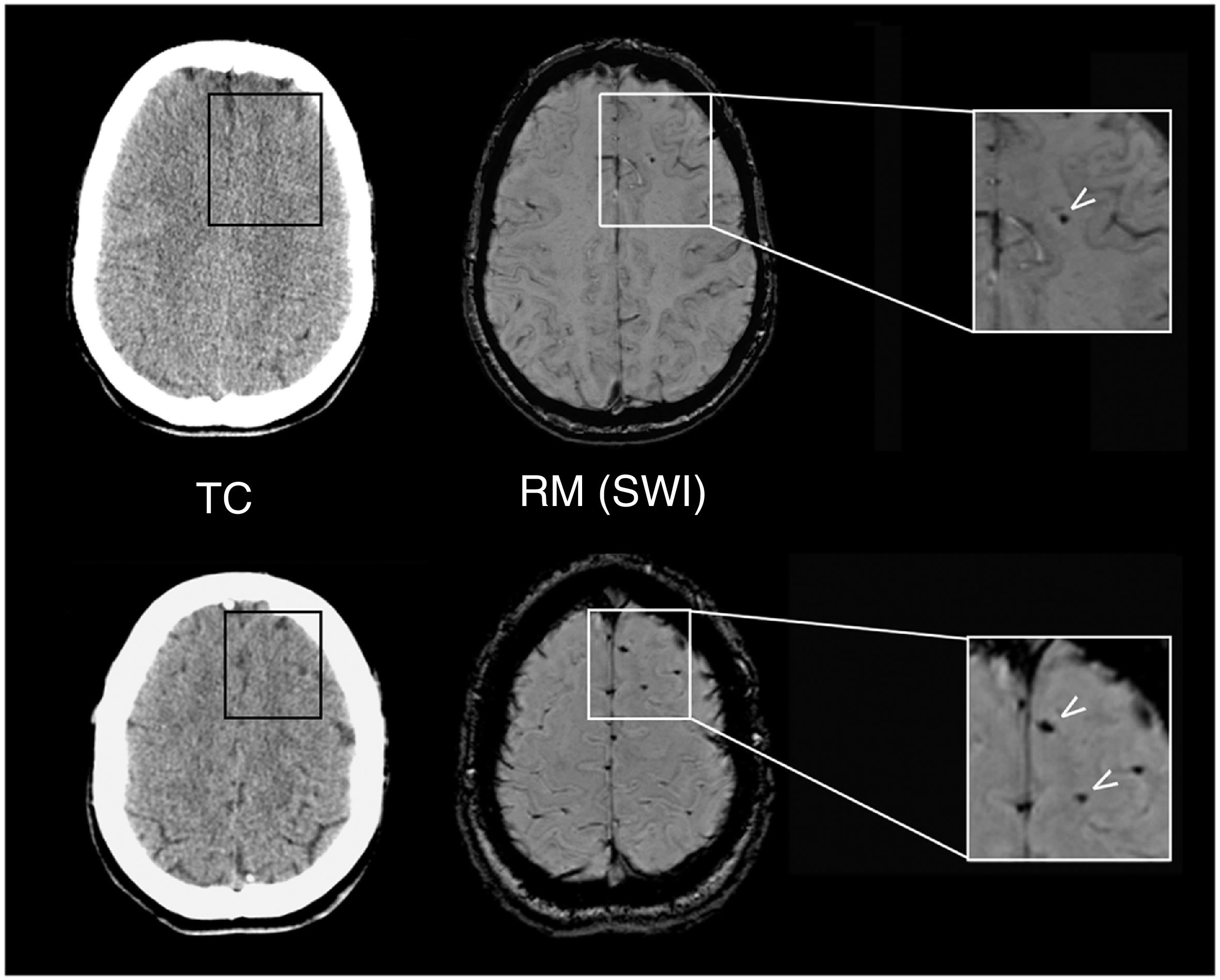
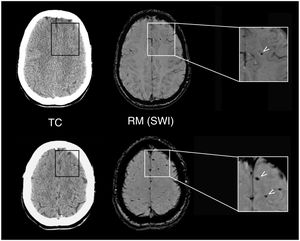
A pesar de que en todos los casos la TC cerebral inicial fue normal, la RM objetivó lesiones sugestivas de LAD en 2 de los 20 pacientes evaluados (10%). La figura 2 muestra las lesiones observadas en una paciente de 26 años que presentó un TCE-L con PDC y APT debido a accidente de motocicleta. De manera adicional, en otros 5 pacientes (25%) se objetivaron focos de alteraciones de la señal de etiología que podría ser traumática, aunque este hecho no pudo precisarse con certeza en todos los casos.
Hallazgos neurorradiológicos en un paciente de 26 años que presentó un traumatismo craneoencefálico leve. La tomografía computarizada (TC) cerebral, practicada a las 2 h del traumatismo, fue normal (izquierda), mientras que la resonancia magnética (RM) craneal (derecha) practicada a los 10 días objetivó focos de alteración de la señal en la secuencia Susceptibility Weighted Imaging (SWI) (flechas), correspondientes a microsangrados indicativos de lesión axonal difusa leve.
Los resultados de este estudio piloto demuestran que los pacientes que han presentado una conmoción cerebral secundaria a un TCE-L pueden presentar síntomas que perduran días después del traumatismo, lo que puede interferir en la incorporación del paciente al ámbito laboral o dificultar su rendimiento académico. Más allá de los síntomas habituales de una conmoción cerebral (cefalea, vértigo…), estos pacientes pueden presentar alteraciones cognitivas objetivables mediante las herramientas adecuadas. Por último, en un porcentaje no despreciable de pacientes se identificaron alteraciones estructurales en la RM compatibles con una LAD o microsangrados, a pesar de que en todos ellos se había objetivado inicialmente una TC cerebral normal.
Aspectos a considerar en la inclusión de los pacientes del estudioUno de los hallazgos más llamativos del presente trabajo ha sido el elevado número de pacientes que acudieron al centro hospitalario para ser valorados después de presentar un TCE-L y que finalmente no fueron candidatos para el estudio. La edad fue el criterio de exclusión más frecuente. El 55% de los pacientes atendidos durante el año de desarrollo del proyecto fueron mayores de 65 años. Esta cifra concuerda con los cambios observados recientemente en los patrones epidemiológicos del TCE. A nivel mundial se ha objetivado que la edad de los pacientes traumáticos se ha incrementado de manera muy significativa y que las caídas han superado las cifras de accidentes de tráfico como causa principal del traumatismo en este grupo de edad1. Los estrictos criterios de cribado aplicados, elegidos específicamente para eliminar factores de confusión conocidos, redujeron el número potencial de participantes hasta el 6,9%. Por otra parte, solo el 60% de los que cumplían los criterios de inclusión accedieron a participar de forma no remunerada en el estudio. De esta forma, el porcentaje de participación final se redujo a menos del 4% de todos los pacientes atendidos durante un año en un hospital de nivel tres. En un estudio publicado en 2013, Luoto et al. advertían sobre este hecho y afirmaban que muchos de los estudios hospitalarios que se dirigen a temas específicos de investigación sobre los TCE-L reclutan muestras que pueden estar sesgadas y que sus resultados no pueden generalizarse a toda la población de traumáticos25.
Criterios diagnósticos del traumatismo craneoencefálico leveDe acuerdo con los criterios clásicos de la Organización Mundial de la Salud en 20044, el diagnóstico de un TCE-L exige que el paciente presente una puntuación de 13, 14 o 15 en la ECG. Sin embargo, siguiendo criterios diagnósticos más actuales, en el presente estudio se han descartado aquellos pacientes que presentaban una puntuación de 13. Diversos autores señalan que la evolución de los pacientes con una puntuación de 13 en la ECG es más comparable con la de los TCE moderados que con la de los leves, sobre la base de indicadores de mortalidad y complicaciones26. Stein y Ross compararon los hallazgos en la TC cerebral inicial de un grupo de 106 pacientes que presentaban una puntuación de 13 en la ECG con la de 341 pacientes etiquetados de TCE moderado de acuerdo con los criterios clásicos (puntuaciones entre 9 y 12 en la ECG)27. El porcentaje de lesiones objetivadas en la TC cerebral de ambos grupos fue superponible (44,3% vs. 40,3%, respectivamente). Estos autores encontraron, además, que un 20% de los pacientes con una TC cerebral patológica requirieron intervención quirúrgica, por lo que proponen, ya en 1992, que los pacientes traumáticos con una puntuación de 13 en la ECG deberían ser reclasificados como moderados y no leves27.
En el presente estudio también se exigía que la TC cerebral fuera normal. La exclusión de los pacientes con una exploración tomográfica patológica asegura una mayor homogeneidad de la muestra, puesto que en los pacientes con lesiones en la TC cerebral se utilizan protocolos de seguimiento distintos, más cercanos a los de los TCE moderados. La ausencia de lesiones cerebrales en los estudios convencionales que se practican en Urgencias permite centrar el estudio en el extremo más benigno de esta patología (pacientes con una puntuación de 14 o 15 y TC cerebral normal).
Valoración clínica en el traumatismo craneoencefálico leve. Herramientas actualesPara profundizar en el estudio de por qué algunos pacientes presentan un SPC, es necesario conocer mejor la traducción clínica de los TCE-L en la fase aguda. El valor pronóstico de descriptores tradicionales, como la presencia y la duración de la PDC y de la APT, no está bien establecido y el conocimiento fisiopatológico de ambos fenómenos en el contexto de los TCE-L es aún limitado. En estos pacientes, la validez y el poder predictivo de la APT están ampliamente cuestionados, a pesar de ser un signo definitorio de la conmoción y un elemento crítico de la evaluación hospitalaria de rutina16.
Con el objeto de registrar de forma exhaustiva la información clínica de los pacientes con un TCE-L estudiados, se utilizó una escala inicialmente diseñada para valorar traumatismos en el ámbito deportivo (SCAT2), observándose que los pacientes valorados seguían presentando un número elevado de síntomas posconmocionales al cabo de 1-2 semanas después del traumatismo, aunque su severidad tendía a reducirse respecto a la valoración inicial. Los resultados obtenidos de la aplicación del SCAT2, tanto el día del traumatismo como 1-2 semanas después, avalan el uso de esta herramienta en la monitorización estandarizada de la sintomatología posconmocional, dado que también ofrece una cuantificación global del estado cognitivo de estos pacientes. No obstante, la evaluación de los síntomas clínicos —PDC y pérdida de equilibrio— en el contexto de los TCE-L valorados es este estudio es menos fiable que en el contexto deportivo, ya que en muchos casos se basa en información proporcionada por el propio paciente o relatada por testigos. Además, la exploración del equilibrio no se puede realizar en aquellos pacientes con lesiones en extremidades inferiores que dificulten la bipedestación. Por otra parte, los resultados en la valoración del equilibrio son más variables en la población adulta general que en los jóvenes deportistas: el 10% de una muestra de población canadiense sana y aproximadamente el 65% de un grupo control finlandés obtuvieron puntuaciones bajas en las pruebas de equilibrio16. Estos resultados indican que el valor de este subtest de equilibrio dentro del SCAT2 debería ser reconsiderado en futuros estudios dirigidos a validar el uso de esta escala fuera del contexto deportivo.
Resultados de la valoración neuropsicológicaA pesar de que el TCE puede alterar casi cualquier aspecto del funcionamiento encefálico, posiblemente la afectación clave de estos pacientes sea la disfunción de los sistemas frontales, donde se centran especialmente las funciones ejecutivas (capacidad de planificación y organización, memoria de trabajo, flexibilidad e inhibición de conductas, entre otras). Esta perspectiva ha hecho que autores como Chen y d’Esposito (2010)28 y Stuss (2011)29 definan el TCE como un trastorno del control cognitivo.
Los resultados de la evaluación neuropsicológica detallada realizada en este estudio indican que durante las primeras semanas posteriores a un TCE-L la capacidad de aprendizaje y la memoria se encuentren levemente alteradas, en comparación con los hallazgos de un grupo de control. Otros indicadores de atención, que incluyen también un componente ejecutivo puesto que requieren memoria de trabajo e inhibición, se añaden a los resultados que describen la presencia de déficits cognitivos sutiles en este grupo de pacientes.
Estos resultados son fruto de un análisis exploratorio y las diferencias entre los pacientes y el grupo de control han sido consideradas significativas estadísticamente a un p<0,05, sin una corrección post hoc estricta. No obstante, concuerdan con los resultados de una revisión sistemática reciente, que concluyó que la asociación entre el TCE-L y los déficits cognitivos en las primeras 2 semanas es un hallazgo consistente11. En este periodo de seguimiento, la PDC se asoció, aunque de forma limitada, a una reducción en la velocidad de procesamiento de la información. Sin embargo, aunque casi el 70% de los pacientes incluidos en nuestro estudio habían presentado una PDC, los resultados obtenidos no confirman de manera clara la existencia de un déficit específico de velocidad de procesamiento.
Tomografía computarizada normal y lesiones en la resonancia magnéticaLos pacientes con un TCE-L, y especialmente aquellos con sintomatología persistente, podrían presentar lesiones cerebrales que pueden pasar desapercibidas en la TC cerebral. La secuencia SWI identificó la presencia de lesiones traumáticas estructurales en un 10% de los 20 pacientes estudiados por RM. De forma adicional, en otros 5 casos (25% de los pacientes estudiados) se objetivaron lesiones en la RM que no se visualizaron en la TC cerebral convencional, aunque en algunos casos la etiología de estas lesiones fue incierta.
A pesar de que en otros estudios el volumen total de las lesiones que se identifican en las secuencias SWI se correlaciona con indicadores clínicos de severidad30, no se ha establecido una relación clara entre la presencia de estas lesiones y la recuperación cognitiva después del traumatismo. Diversos estudios han objetivado que la existencia de lesiones en las exploraciones de neuroimagen de pacientes con un TCE-L se asocia a peores resultados en funciones cognitivas como la memoria. Sin embargo, debido a que la gran mayoría de las pruebas neuropsicológicas aplicadas no discriminan entre los grupos de pacientes con y sin lesiones neurorradiológicas, hay autores que opinan que estos pacientes no deberían tratarse de forma distinta31.
La identificación de estas lesiones cerebrales regionales, que aparecen en el momento agudo del TCE-L y persisten de forma indefinida, aporta información no solo de la severidad de la lesión, sino también sobre qué sistemas neuroconductuales pueden haber sido afectados. Las exploraciones de RM avanzada mejoran la compresión de la distribución de la lesión encefálica y, en última instancia, permiten el desarrollo de estrategias de evaluación y tratamiento más efectivas, de forma análoga a como ocurre el proceso de rehabilitación de los pacientes que han presentado un accidente vascular isquémico.
En conclusión, a pesar de que este estudio presenta una serie de limitaciones, los resultados obtenidos confirman que, en contra de la creencia ampliamente extendida en el ámbito clínico, determinados TCE-L no deberían considerarse acontecimientos banales. A pesar de presentar una TC normal, los estudios de RM avanzada objetivaron que entre el 10 y el 35% de los pacientes estudiados presentaban lesiones que podían ser indicativas de una LAD. Tanto en la fase aguda como a 1-2 semanas después del traumatismo, los pacientes evaluados presentaban alteraciones del estado neurocognitivo global, en comparación con el grupo control. Los resultados de la valoración neuropsicológica indican que a medio plazo el estado cognitivo de estos pacientes sigue alterado y que presentan problemas de memoria y de atención ejecutiva. Una de las principales limitaciones del estudio es el periodo relativamente corto de seguimiento. Después de un TCE-L los síntomas podrían persistir durante meses después del traumatismo o incluso, en algunos aspectos, hacerse permanentes. Esto implica la necesidad de extender el periodo de seguimiento de los enfermos. Este aspecto deberá ser incluido en futuros estudios.
El conjunto de esta información pone de manifiesto que el manejo que suele hacerse en un medio hospitalario del paciente con un TCE-L (habitualmente valoración y alta hospitalaria sin seguimiento) puede no ser adecuado en algunos casos. El registro estructurado de la sintomatología posconmocional y la evaluación neuropsicológica aportan información muy relevante sobre las alteraciones que estos pacientes pueden presentar durante al menos las 2 primeras semanas después del traumatismo. A pesar de que es necesario ampliar la muestra de pacientes, los resultados obtenidos hasta el momento permiten afirmar que el cuestionario SCAT2 utilizado en este estudio constituye una herramienta útil, por lo que debería considerarse su incorporación en la asistencia clínica rutinaria.
FinanciaciónEste trabajo ha sido parcialmente financiado por las siguientes entidades: Fundación MAPFRE (proyecto 2012-04 a MAP), Fondo de Investigación Sanitaria (proyecto PI13/02397, investigador principal MAP) e Institut de Recerca Vall d’Hebron (beca PRED-VHIR-2012-26 concedida a AR). El presente estudio forma parte de la tesis doctoral de AR.
Conflicto de interesesNinguno de los autores presenta conflictos de intereses.
A la Dra. Núria Bargalló, por su inestimable ayuda en la valoración de las exploraciones de RM. A todo el equipo de enfermería de Urgencias de Neurotraumatología, por su colaboración en la selección de pacientes. A Noelia Montoya, Lourdes Expósito y Mercedes Arribas, por su apoyo constante.