Editado por: Dr. Mariano de la Figuera von Wichmann
(Clínica Olivé Gumà, Barcelona, Spain)
Prof. Dr. Elena Segura-Grau
(Tondela Viseu Hospital Center, Viseu, Portugal)
Última actualización: Diciembre 2024
Más datosLa disnea es un síntoma frecuentemente consultado en atención primaria y de amplia diversidad etiológica (respiratoria, cardiovascular, obesidad, etc.). Ocasiona unos 3-4 millones de consultas urgentes al año. Entre un 9-13% de la población ambulatoria refiere disnea, llegando hasta un 37% en adultos≥70 años.
En atención primaria, donde las pruebas complementarias son limitadas, la ecografía clínica, es decir, la realizada a pie de cama por el médico directamente responsable del paciente, como complemento a una correcta anamnesis y exploración física, facilita el diagnóstico precoz del enfermo con disnea, así como su seguimiento.
En diversos estudios se ha demostrado que la ecografía pulmonar en manos de un operador bien entrenado tiene mayor precisión diagnóstica.
Dyspnea is a symptom frequently consulted in primary care and has a wide range of etiologies (respiratory, cardiovascular, obesity, etc.). It causes 3-4 million emergency consultations per year. Approximately 9-13% of the ambulatory population reports dyspnea, getting up to 37% in adults aged≥70 years.
In primary care, where complementary tests are limited, clinical ultrasound is performed at bedside by the doctor directly responsible for the patient, as a complement to a thorough medical assessment and physical examination, that facilitates the early diagnosis of patients with dyspnea as well as their follow-up.
In various studies, it has been shown that lung ultrasound in the hands of a well-trained operator has greater diagnostic accuracy.
La disnea es un síntoma frecuente en nuestras consultas y con una amplia variedad de posibilidades etiológicas, resultando a veces desafiante establecer un diagnóstico preciso. La disnea puede tener su origen en procesos potencialmente graves en los que un diagnóstico precoz e inicio de tratamiento adquieren gran relevancia. La mayoría de los casos de disnea están relacionados con afección respiratoria (enfermedades pulmonares obstructivas, enfermedades de la caja torácica, enfermedad pleural y enfermedades del parénquima pulmonar) o cardiovascular (insuficiencia cardiaca, enfermedad del pericardio y enfermedades vasculares pulmonares como la embolia o la hipertensión pulmonar), aunque existen otras, como la obesidad, la anemia o una baja forma física1,2.
La base del diagnóstico del paciente con disnea se centra en la historia clínica y la exploración física, y en función de esta valoración inicial, se solicitan pruebas complementarias1.
En diversos estudios se ha demostrado que la ecografía pulmonar en manos de un operador bien entrenado tiene una mayor precisión diagnóstica. La sensibilidad y la especificidad de la ecografía pulmonar son variables en función de la enfermedad analizada: 85 y 93% para neumonía; 80 y 99% para neumotórax, y 94 y 92% en el diagnóstico de descompensación de insuficiencia cardiaca, respectivamente1–4.
El desarrollo de equipos ecográficos de calidad, tanto de consola como portátiles, ha permitido la expansión de la ecografía en múltiples especialidades (medicina de familia, medicina interna, urgencias, cuidados intensivos, reumatología, neumología, etc.)1,5.
Centraremos nuestro artículo en la exploración pulmonar del paciente con disnea, sin profundizar en los hallazgos ecográficos respecto de la congestión sistémica en la insuficiencia cardiaca, ya que se abordarán en un artículo específico.
IndicacionesEn la evaluación diagnóstica del paciente con disnea, la ecografía clínica sirve para complementar la exploración física tradicional y permite establecer el diagnóstico etiológico en un número significativo de enfermos, incluso antes de disponer de pruebas complementarias como la radiografía de tórax o las determinaciones analíticas. No obstante, es preciso recalcar que la anamnesis y la exploración física tradicionales constituyen el eje de la orientación diagnóstica del paciente con disnea y que, junto con la ecografía clínica, nos permiten confirmar o descartar una sospecha clínica de manera más fiable. Para la valoración ecográfica completa del enfermo con disnea debemos realizar ecografía pulmonar, ecocardiograma básico y ecografía de las extremidades inferiores. La ecografía permite distinguir un origen cardiaco o respiratorio, por ejemplo, para diferenciar una insuficiencia cardiaca de una enfermedad pulmonar obstructiva crónica o una neumonía5–8.
Técnica de exploraciónConfiguración del ecógrafoEl equipo de ecografía para la realización de la técnica solo precisa de imagen bidimensional y en modo M. Seleccionar una configuración adecuada es fundamental para garantizar una resolución de imagen óptima. Seleccionaremos el preset o configuración preestablecida de pulmón y, en ausencia de este, se podrá utilizar el preset de abdomen desactivando los atenuadores de artefactos, ya que la ecografía pulmonar se basa en estos artefactos. Posteriormente, ajustaremos la profundidad a unos 8-12cm y posicionaremos el foco en la línea pleural. La ganancia la vamos subiendo desde cero hasta lograr que la sombra de las costillas se vea de color negro y la línea pleural blanca.
Selección del transductorSe necesita un transductor de baja frecuencia tipo convex o microconvex, de entre 3,5-5MHz, que permita la visualización de las estructuras profundas del tórax y caracterizar las consolidaciones y el derrame pleural.
Para las estructuras más superficiales, es decir, la pleura y los signos y artefactos que se generan en ella, las sondas de frecuencia superior a 5MHz, como es el transductor lineal, proporcionan mejor resolución. Estas sondas se emplean, además, para el estudio vascular, lo cual nos sirve de complemento en el diagnóstico de la trombosis venosa profunda ante la sospecha de un tromboembolismo pulmonar.
Manejo de la sondaSe recomienda sostener la sonda como un bolígrafo sobre un espacio intercostal, perpendicular a la pared torácica y con el marcador de la sonda hacia craneal. El marcador de la pantalla deberá ajustarse en el lado superior izquierdo de la pantalla. De esta manera, las sombras de las costillas se verán a ambos lados de la pantalla y, al interpretar las imágenes ecográficas, la parte izquierda de la pantalla indicará superior, y la derecha, inferior.
Posicionamiento del pacienteLa ecografía pleuropulmonar se puede realizar con el enfermo en prácticamente cualquier posición; variará mucho en función de la situación clínica del paciente.
En la consulta de atención primaria, con el paciente sentado, la exploración más común consiste en dividir cada hemitórax («R» de right=derecho/«L» de left=izquierdo) en 6 segmentos, e ir comparando la pared torácica de ambos lados durante el examen. Para ello, pediremos al paciente que colabore cruzando sus brazos por delante para desplazar ambas escápulas hacia externo. Los segmentos estarían limitados en la parte frontal por la línea paraesternal y el quinto espacio intercostal (R1-R2 y L1-L2); en el lateral, por la línea axilar anterior, la línea axilar posterior y el quinto espacio intercostal (R3-R4 y L3-L4), y en la parte posterior, por las líneas paravertebrales y la línea subescapular (R5-R6 y L5-L6).
Por otro lado, a la hora de evaluar la presencia de síndrome alvéolo-intersticial, como es en el caso de la insuficiencia cardiaca, Volpicelli propone en su protocolo 8 zonas ecográficas para examinar el tórax: 4 correspondientes a cada hemitórax, divididas por la línea paraesternal, axilar anterior y posterior5,9–14.
Hallazgos normales y patológicosSignos de normalidad- •
Signo del murciélago: es la imagen inicial que debemos obtener al realizar una ecografía pulmonar, semejante a la forma de un murciélago. Las costillas se identifican fácilmente por la sombra acústica que reflejan, y la presencia entre ellas de una línea hiperecoica horizontal corresponde a la línea pleural. Estrictamente hablando, la pleura no se ve con ecografía, sin embargo, se ven sus artefactos. La línea pleural incluye la pleura parietal, el espacio pleural y la pleura visceral. La línea hiperecoica que se visualiza corresponde a la parte más superficial de los alvéolos, que, como el aire no deja pasar los ultrasonidos, se reflejan masivamente en la sonda y dibujan esta línea, que en condiciones normales es móvil (fig. 1b)15,16.
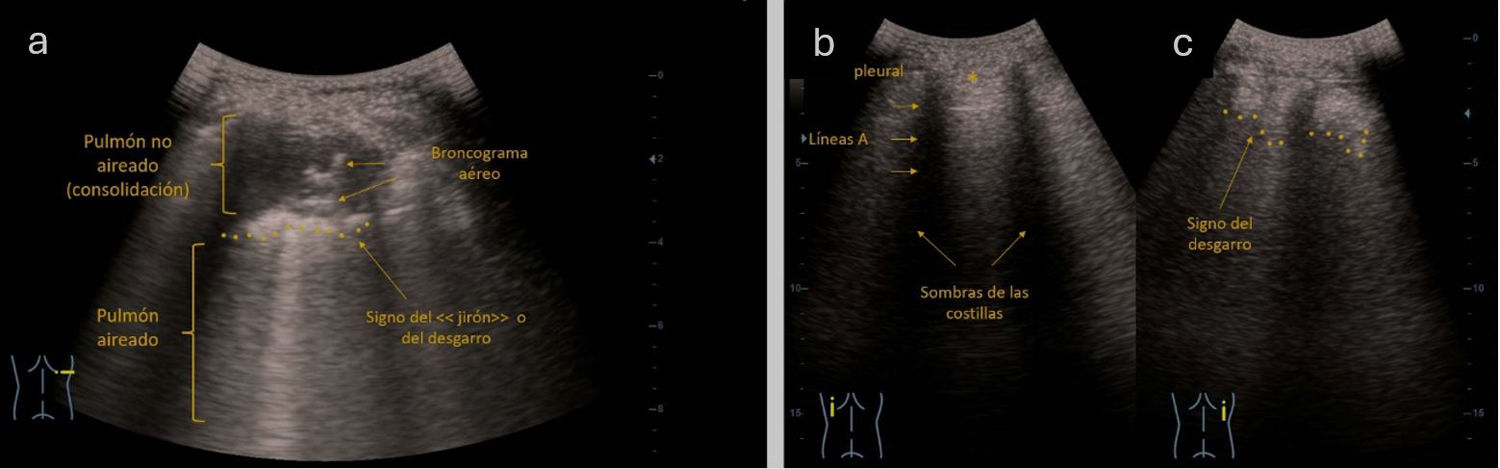
Figura 1.Consolidación no translobar de unos 4cm en lóbulo inferior derecho (LID) en contexto de neumonía de la comunidad. a: en la imagen ecográfica, según el pictograma, se aprecia en un corte transversal (intercostal) en LID, una imagen hipoecogénica de 3-4cm de bordes irregulares, compatible con consolidación pulmonar. En el interior de la lesión, se aprecian líneas hiperecogénicas horizontales de aspecto lenticular, móviles con la respiración; muy indicativas del broncograma aéreo. En área adyacente, perilesional, vemos algunas líneas B o artefacto en cola de cometa. b: comparativa de ambos hemitórax en un corte longitudinal. Según se refleja en el pictograma, en hemitórax izquierdo, se aprecian signos de normalidad: signo del murciélago, patrón de líneas A; además, la imagen en dinámico confirmaba la existencia de deslizamiento pleural y signo de la cortina. c: en hemitórax derecho, según se refleja en el pictograma, la pleura se visualiza como desgarrada, signo conocido como «shred sign».
Fuente: Grupo de Trabajo Ecografía de SEMERGEN.
- •
Deslizamiento pleural: la pleura se visualiza como una línea hiperecogénica única de hasta 2-3mm de grosor que se mueve con la respiración, ofreciendo una imagen de desplazamiento horizontal similar a un «camino de hormigas», y que representa el movimiento de la pleura visceral contra la parietal. Es importante recordar que en condiciones normales las hojas pleurales están pegadas y no se visualiza el espacio pleural14,17.
- •
Signo de la orilla del mar: en un pulmón sano, se pueden diferenciar las áreas inmóviles habituales que corresponden a la pared torácica, mediante líneas horizontales paralelas («mar»), de las áreas móviles, que corresponden al deslizamiento pleural y se visualizan en forma de punteado («orilla»). Este signo, que se visualiza en modo M, puede ser útil si se tienen dudas sobre la presencia de deslizamiento pleural18.
- •
Líneas A: son imágenes lineales hiperecoicas, paralelas a la línea pleural y estáticas, que se visualizan a intervalos regulares equidistantes y cuya distancia se debe a la reflexión de las ondas de ultrasonidos desde la piel hasta la pleura, por lo que cuanto más profundos son los haces de ultrasonidos, más tiempo tardan en regresar al transductor. Se trata de artefactos, generalmente sin significación patológica, que se ocasionan por la interfase gaseosa que presenta el parénquima pulmonar normal; es decir, en presencia de aire en contacto con la línea pleural (fig. 1b y fig. 2a).
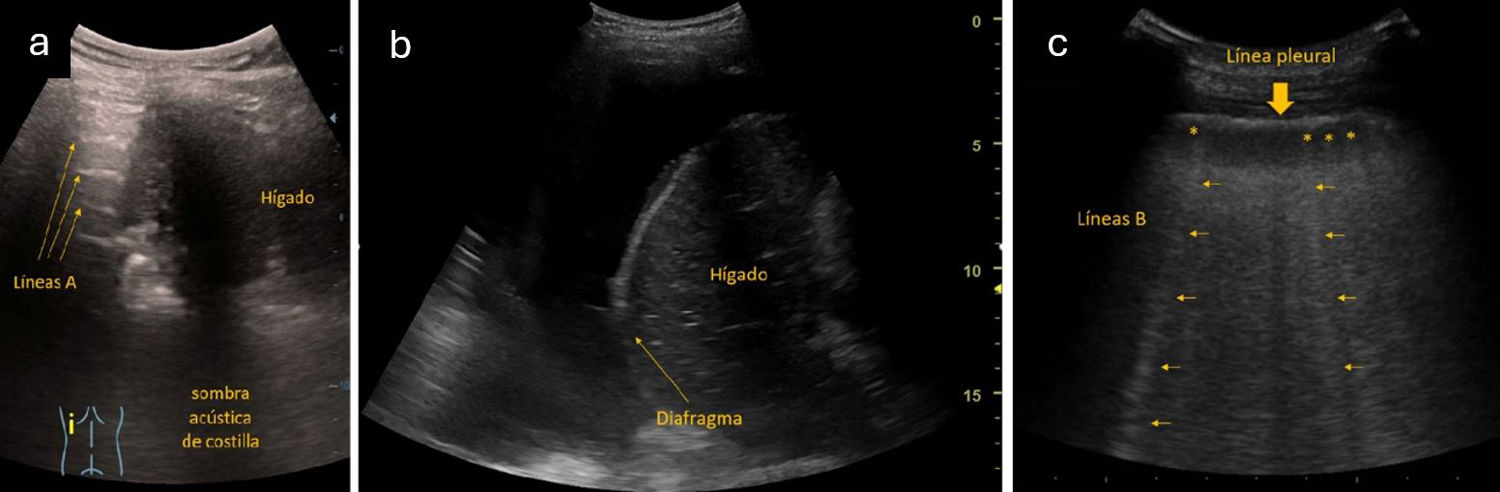
Figura 2.a: signo de la cortina en un corte longitudinal en base pulmonar derecha de un paciente sano: en inspiración, los artefactos de normalidad pulmonar producen un borramiento del órgano abdominal situado caudalmente al pulmón (hígado en este caso). b: derrame pleural en corte longitudinal en base pulmonar derecha: vemos como la ausencia del signo de la cortina nos orienta a la presencia de un derrame pleural en dicha zona. Paciente con diagnóstico final de tuberculosis pulmonar. c: múltiples líneas B (*) en paciente con aumento de su disnea basal en contexto de agudización de su insuficiencia cardiaca en un corte transversal/oblicuado a nivel intercostal: se visualizaban más de 3 líneas B en cada espacio intercostal en más de 2 campos pulmonares de cada hemitórax. Las líneas B (*) parten desde la pleura (flecha gruesa) y llegan hasta el final de la pantalla (flechas finas).
Fuente: Grupo de Trabajo Ecografía de SEMERGEN.
En algunas situaciones patológicas, como tromboembolismo pulmonar, asma o enfermedad pulmonar obstructiva crónica, visualizamos líneas A debido a la existencia de aire. Si tenemos un contexto clínico compatible, sería necesario realizar otras pruebas para el diagnóstico (en tromboembolismo pulmonar, ecografía de extremidades inferiores; en asma/EPOC, espirometría)2,18,19.
- •
Signo de la cortina: consiste en la visualización de los artefactos pulmonares de normalidad (líneas A y deslizamiento pleural) en las bases pulmonares, produciendo con la inspiración un borramiento/impedimento para visualizar los órganos abdominales situados caudalmente al pulmón (hígado y bazo, según corresponda). Su visualización descarta la presencia de derrame pleural (fig. 2 a y b) (ver vídeo 1).
- •
Líneas B: se definen como artefactos hiperecogénicos, bien definidos, verticales, en imagen de cola de cometa, que se inician en la línea pleural hasta el final de la pantalla, borran las líneas A y se mueven de forma sincrónica con el deslizamiento pleural, cuando está presente. La presencia de 3 o menos se puede dar en condiciones normales, sin embargo, más de 3 líneas B indican enfermedad intersticial en la zona que estamos visualizando, por presencia de líquido y aire en el alvéolo15,18,19 (fig. 2c) (ver vídeos 1 y 2).
- •
Líneas Z: se trata de líneas hiperecoicas verticales, cortas y mal definidas, que surgen de la línea pleural y, a diferencia de las líneas B, no llegan al borde inferior de la pantalla (alcanzan 2-5cm en profundidad). Además, no borran las líneas A ni siguen al deslizamiento pulmonar. Carecen de significado patológico16.
- •
Signo de la estratosfera o código de barras: patrón lineal por encima y por debajo de la línea pleural. Se visualiza si hay ausencia de deslizamiento pleural. Tiene significación patológica y su afectación más común es el neumotórax. Sin embargo, aunque la presencia de deslizamiento pleural nos descarta el neumotórax, su ausencia no es patognomónica, ya que puede haber ausencia de deslizamiento pleural en otras dolencias, como la obstrucción bronquial18,20.
- •
Signo del punto pulmón: se trata de un artefacto dinámico y es patognomónico de neumotórax. Se define como el punto en el que empieza el pulmón sano y acaba el neumotórax, y una imagen ecográfica donde visualizamos deslizamiento pleural en un lado de la pantalla y al otro lado ausencia de deslizamiento20 (ver vídeo 3).
- •
Signo del tejido (tissue-like): artefacto que se produce cuando existe una falta de aireación importante del parénquima pulmonar, como ocurre en la neumonía o la atelectasia, y este adquiere una ecogenicidad similar a la del hígado (hepatización pulmonar)16,18,19 (fig. 3b).
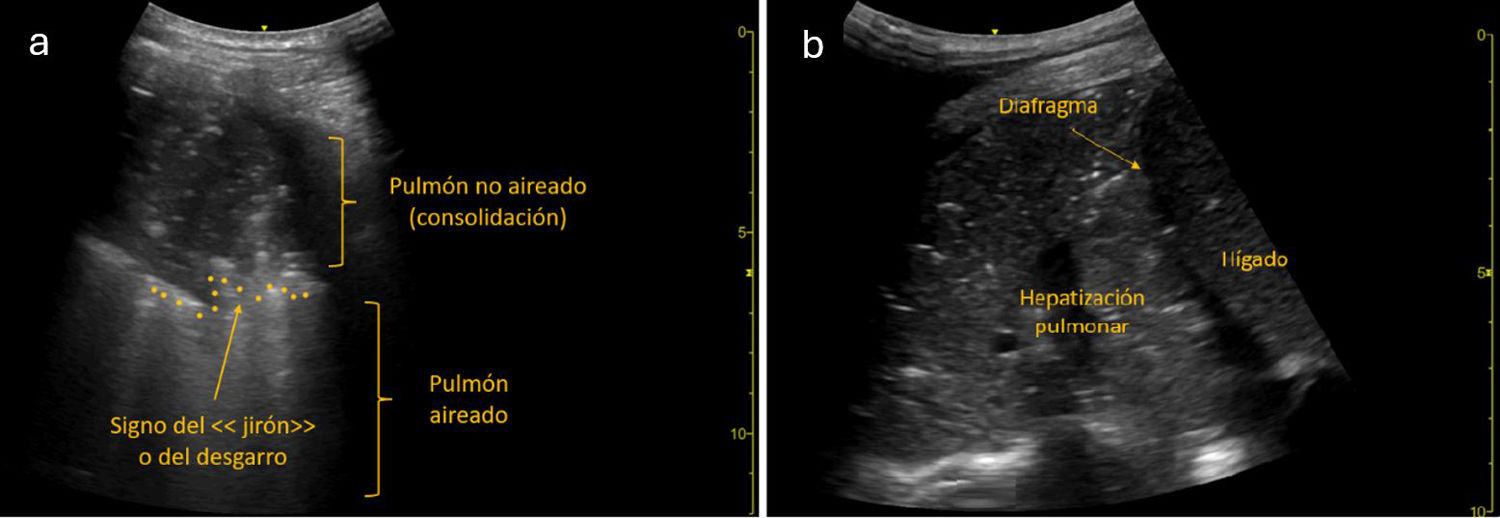
Figura 3.a: consolidación no translobar (signo del desgarro): se objetiva imagen hipoecogénica, de unos 6cm, con imágenes hiperecogénicas en su interior, compatible con consolidación pulmonar con broncograma aéreo en dicho nivel y delimitada del resto del pulmón aireado por una línea fractal (signo del desgarro). b: consolidación translobar (hepatización): en un corte intercostal en base pulmonar derecha se objetiva una imagen de gran tamaño, unos 10cm, con hepatización pulmonar y broncograma aéreo, de un paciente con una neumonía que precisó ingreso en UCI.
Fuente: Grupo de Trabajo Ecografía de SEMERGEN.
- •
Signo de la medusa o de la lengua: artefacto dinámico que se produce por el movimiento del parénquima pulmonar al expandirse y colapsarse en el derrame que lo rodea, creando un efecto de aleteo en la zona colapsada. Aunque la ecografía pulmonar puede detectar pequeños volúmenes (20ml) de derrame, este signo se visualiza en derrame pleural, al menos, moderado. En presencia de un derrame pleural bilateral, sería recomendable la realización de una ecografía cardiaca15,21 (ver vídeo 4).
- •
Líneas E: líneas verticales, hiperecogénicas y asíncronas con los movimientos respiratorios, que pueden borrar las líneas A, y se inician en la pared torácica (a diferencia de las líneas B que parten de la línea pleural). Estos artefactos surgen del tejido celular subcutáneo en los pacientes con enfisema subcutáneo20.
- •
Signo del desgarro o del jirón: artefacto que se produce cuando parte del lóbulo pulmonar está aireado, siendo este signo el límite entre la consolidación y el pulmón aireado adyacente. También se conoce como «fragmentación o línea fractal». Se produce cuando hay una consolidación subpleural o consolidación no translobar17 (fig. 1 y fig. 3a) (ver vídeo 5).
- •
Broncograma aéreo: consiste en la visualización de líneas hiperecogénicas, en el interior de una consolidación pulmonar, a veces ramificadas y móviles con la respiración, correspondientes al atrapamiento de burbujas aéreas en el interior de los bronquios o bronquiolos14,16,17 (fig. 1a) (ver vídeo 5).
- •
Broncograma líquido: se caracteriza por estructuras tubulares hipoecoicas o anecoicas, sin signos de perfusión en el Doppler color. Muy indicativo de neumonía secundaria a obstrucción bronquial central14,17,18.
La ecografía se ha utilizado para caracterizar diferentes estructuras por su visualización anatómica según los diferentes tejidos y la composición de estos. Parece paradójico que podamos utilizar la ecografía en el tórax, puesto que el aire del pulmón nos dispersa y refleja las ondas de ultrasonidos. Por tanto, no nos dará imágenes anatómicas, aunque sí imágenes artefactuales, es decir, no reales, que podremos utilizar según los hallazgos y patrones que encontremos, para predecir y diagnosticar determinadas enfermedades como las que quedan reflejadas en la tabla 1.
Entidades clínicas detectables por ecografía pulmonar (ver tabla 1 material complementario)
| Asma/EPOC |
| Deslizamiento pleural |
| Líneas A |
| Signo de la cortina |
| Neumotórax |
| Ausencia de deslizamiento pleural |
| Presencia de punto-pulmón |
| Presencia de líneas A |
| (Ver vídeo 3) |
| Insuficiencia cardiaca |
| Deslizamiento pleural conservado |
| >3 líneas B por campo en al menos 2 campos de cada hemitórax |
| Algunas veces se acompaña de derrame |
| (Ver vídeos 1 y 2) |
| Edema pulmonar no cardiogénico, neumopatía intersticial (viral o bacteriana atípica) |
| Línea pleural irregular |
| Consolidaciones subpleurales |
| Líneas B multifocales |
| Distribución multilobar, alternando zonas sanas con zonas afectadas |
| TEP/infarto pulmonar+trombosis venosa profunda |
| Consolidación hipoecoica en forma de cuña con base pleural y vértice hacia el hilio. Doppler negativo (joroba de Hampton) |
| Ausencia de broncograma aéreo. Imagen ecográfica puntiforme, centrado y aislado |
| Se observan líneas A (porque el problema es de perfusión, no de ventilación) |
| Neumonía focal |
| Consolidación lobar |
| Signos de desgarro |
| Broncograma aéreo |
| Líneas B focales |
| Derrame pleural en PLAPS, signo de la medusa |
| Si no toca pleura, patrón normal |
| (Ver vídeo 5) |
EPOC: enfermedad pulmonar obstructiva crónica; PLAPS: síndrome alvéolo-pleural; TEP: tromboembolismo pulmonar.
Fuente: Grupo de Trabajo Ecografía de SEMERGEN5,9,10,12,18.
Es indispensable conocer estos artefactos y saber interpretarlos para que no nos induzcan a error.
Los artefactos generados a través de la línea pleural, junto con las distintas densidades pulmonares que nos podemos encontrar, generan unos signos ecográficos que se correlacionan con distintas enfermedades, tanto pleurales como pulmonares, aunque no son específicos de ninguna en concreto. Siempre será la clínica la que nos oriente para el diagnóstico (tabla 2).
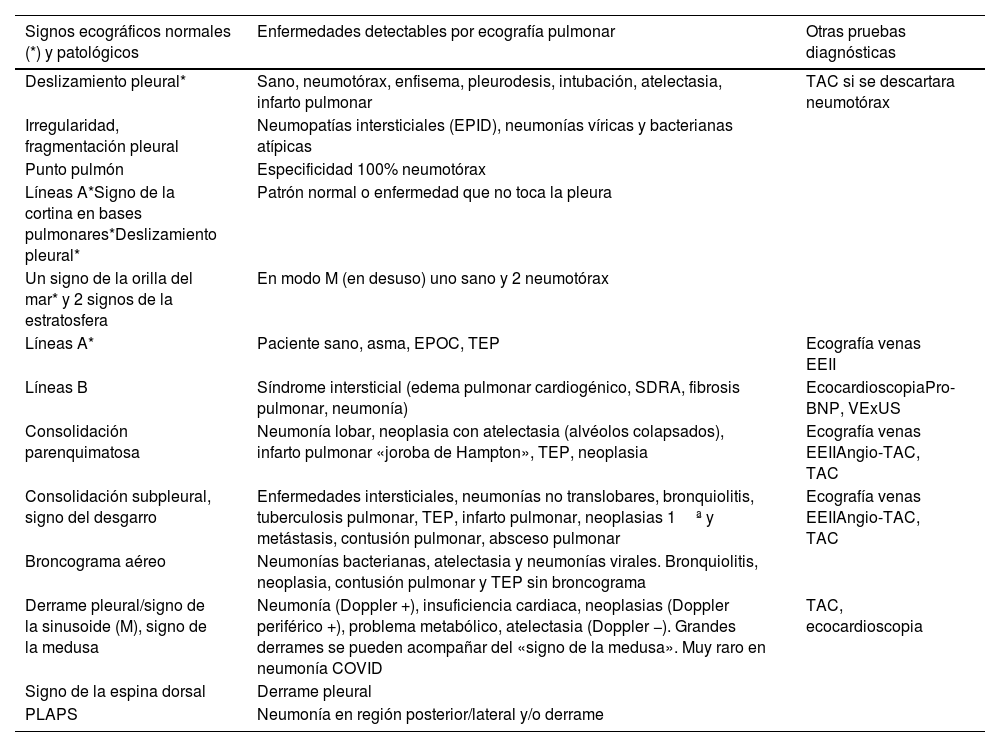
Según signos ecográficos, posibles enfermedades y ayuda con otras pruebas diagnósticas
| Signos ecográficos normales (*) y patológicos | Enfermedades detectables por ecografía pulmonar | Otras pruebas diagnósticas |
|---|---|---|
| Deslizamiento pleural* | Sano, neumotórax, enfisema, pleurodesis, intubación, atelectasia, infarto pulmonar | TAC si se descartara neumotórax |
| Irregularidad, fragmentación pleural | Neumopatías intersticiales (EPID), neumonías víricas y bacterianas atípicas | |
| Punto pulmón | Especificidad 100% neumotórax | |
| Líneas A*Signo de la cortina en bases pulmonares*Deslizamiento pleural* | Patrón normal o enfermedad que no toca la pleura | |
| Un signo de la orilla del mar* y 2 signos de la estratosfera | En modo M (en desuso) uno sano y 2 neumotórax | |
| Líneas A* | Paciente sano, asma, EPOC, TEP | Ecografía venas EEII |
| Líneas B | Síndrome intersticial (edema pulmonar cardiogénico, SDRA, fibrosis pulmonar, neumonía) | EcocardioscopiaPro-BNP, VExUS |
| Consolidación parenquimatosa | Neumonía lobar, neoplasia con atelectasia (alvéolos colapsados), infarto pulmonar «joroba de Hampton», TEP, neoplasia | Ecografía venas EEIIAngio-TAC, TAC |
| Consolidación subpleural, signo del desgarro | Enfermedades intersticiales, neumonías no translobares, bronquiolitis, tuberculosis pulmonar, TEP, infarto pulmonar, neoplasias 1ª y metástasis, contusión pulmonar, absceso pulmonar | Ecografía venas EEIIAngio-TAC, TAC |
| Broncograma aéreo | Neumonías bacterianas, atelectasia y neumonías virales. Bronquiolitis, neoplasia, contusión pulmonar y TEP sin broncograma | |
| Derrame pleural/signo de la sinusoide (M), signo de la medusa | Neumonía (Doppler +), insuficiencia cardiaca, neoplasias (Doppler periférico +), problema metabólico, atelectasia (Doppler −). Grandes derrames se pueden acompañar del «signo de la medusa». Muy raro en neumonía COVID | TAC, ecocardioscopia |
| Signo de la espina dorsal | Derrame pleural | |
| PLAPS | Neumonía en región posterior/lateral y/o derrame |
Angio-TAC: angiografía por tomografía axial computarizada; EEII: extremidades inferiores; EPID: enfermedad intersticial pulmonar difusa; EPOC: enfermedad pulmonar obstructiva crónica; PLAPS: síndrome alvéolo-pleural; Pro-BNP: propéptido natriurético cerebral; SDRA: síndrome de distrés respiratorio; TAC: tomografía axial computarizada; TEP: tromboembolismo pulmonar; VExUS: Venous Excess Ultrasound Score.
Fuente: Grupo de Trabajo Ecografía de SEMERGEN5,9,10,12,18.
Aunque la ecografía es de gran ayuda, en algunas ocasiones, sobre todo en el diagnóstico de la disnea aguda, vamos a necesitar de otras pruebas complementarias para finalizar la evaluación del paciente.
ConclusionesLa ecografía pulmonar se basa en la interpretación de artefactos originados por la interacción entre el aire y los haces de ultrasonidos. A medida que se producen cambios en el tejido pulmonar, observaremos nuevos artefactos que nos harán sospechar diferentes enfermedades.
Es una técnica diagnóstica sencilla, precisa y costo-eficiente que ha demostrado ser superior a la radiografía de tórax en la sospecha de neumonía, congestión pulmonar, derrame pleural y neumotórax.
La ecografía clínica otorga al médico de atención primaria una mayor independencia y seguridad en la toma de decisiones, lo que permite priorizar la derivación de los pacientes con enfermedades graves y evitar derivar a los leves que no lo precisen.
FinanciaciónEl artículo se ha financiado exclusivamente con el patrimonio propio de los autores.
Consideraciones éticasSe ha contado con el consentimiento del paciente y se han seguido los protocolos de los centros de trabajo sobre tratamiento de la información de los pacientes.
Vídeo 1. En un corte intercostal en base derecha con sonda convex, se visualiza deslizamiento pleural y>3 líneas B por campo y signo de la cortina. Se confirman estos hallazgos en 2 áreas en cada hemitoráx (áreas 4, 6, 10 y 12).
Vídeo 2. Mismo paciente que en vídeo 1. Con sonda sectorial a nivel de corte subxifoideo se aprecia aumento del calibre de la vena cava, así como pérdida de su variabilidad con la inspiración.
Vídeo 3. Utilizando la sonda lineal en modo B, podemos visualizar, en un corte longitudinal en área 1 de hemitórax derecho, 2 partes bien definidas. En la mitad derecha del vídeo se objetiva ausencia de deslizamiento pleural con presencia de una línea A. En la mitad izquierda del vídeo se confirma existencia de deslizamiento pleural, y también se visualiza una línea B aislada. En mitad de la pantalla, apreciamos la presencia del signo del punto pulmón. La presencia de punto pulmón es 100% específica de neumotórax.
Vídeo 4. En un corte longitudinal a nivel de seno costofrénico derecho, utilizando la sonda convex, vemos la presencia de una imagen anecoica por encima del diafragma que corresponde a un derrame pleural. En su interior se aprecia la imagen del pulmón colapsado, cuyo movimiento crea un efecto de aleteo en el interior del derrame que se conoce como «signo de la medusa».
Vídeo 5. En un corte intercostal con sonda convex, en el área 10 en hemitoráx izquierdo, se visualiza una consolidación triangular de 4×2,5cm heterohipoecoica acompañada del signo del desgarro, así como de imágenes lenticulares hiperecogénicas, móviles con la respiración indicativas de broncograma aéreo. El resto de los campos pulmonares presentaban signos de normalidad.