Patients with non-idiopathic interstitial lung diseases can develop progressive pulmonary fibrosis (PPF-ILD). The study objectives were to define the profile of patients with PPF-ILD treated with nintedanib and to assess the effectiveness and safety of this drug in a real-world setting.
MethodsThis was a multicenter, prospective, observational study of adult patients with PPF-ILD that initiated treatment with nintedanib in ten Andalusian hospitals (Spain). Demographic data, smoking habit, underlying disease, and diagnosis criteria were recorded. Pulmonary function test results, the dyspnea scale score, and the number of hospitalizations related to PPF-ILD were evaluated at baseline and after 6 and 12 months. Adverse events were recorded.
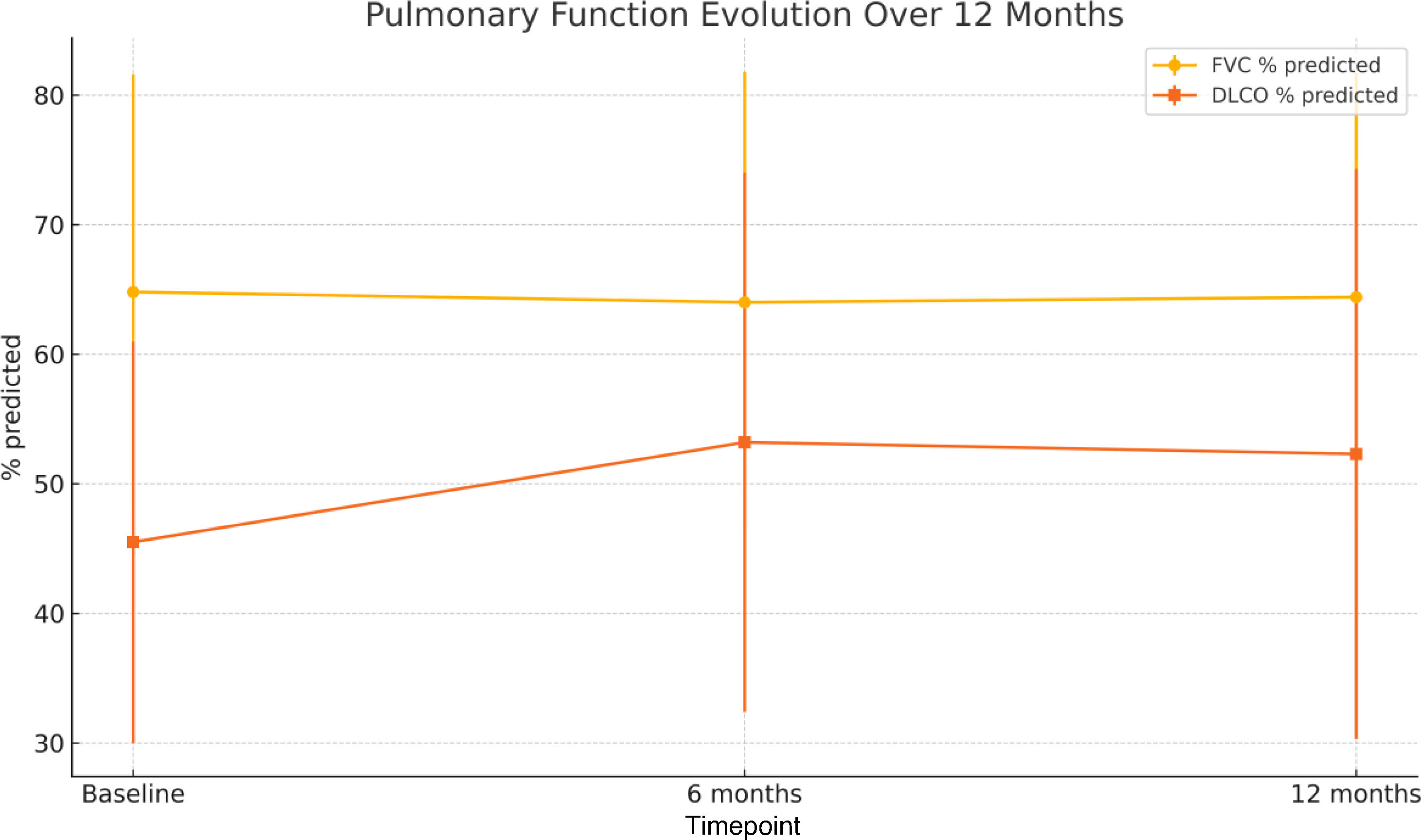
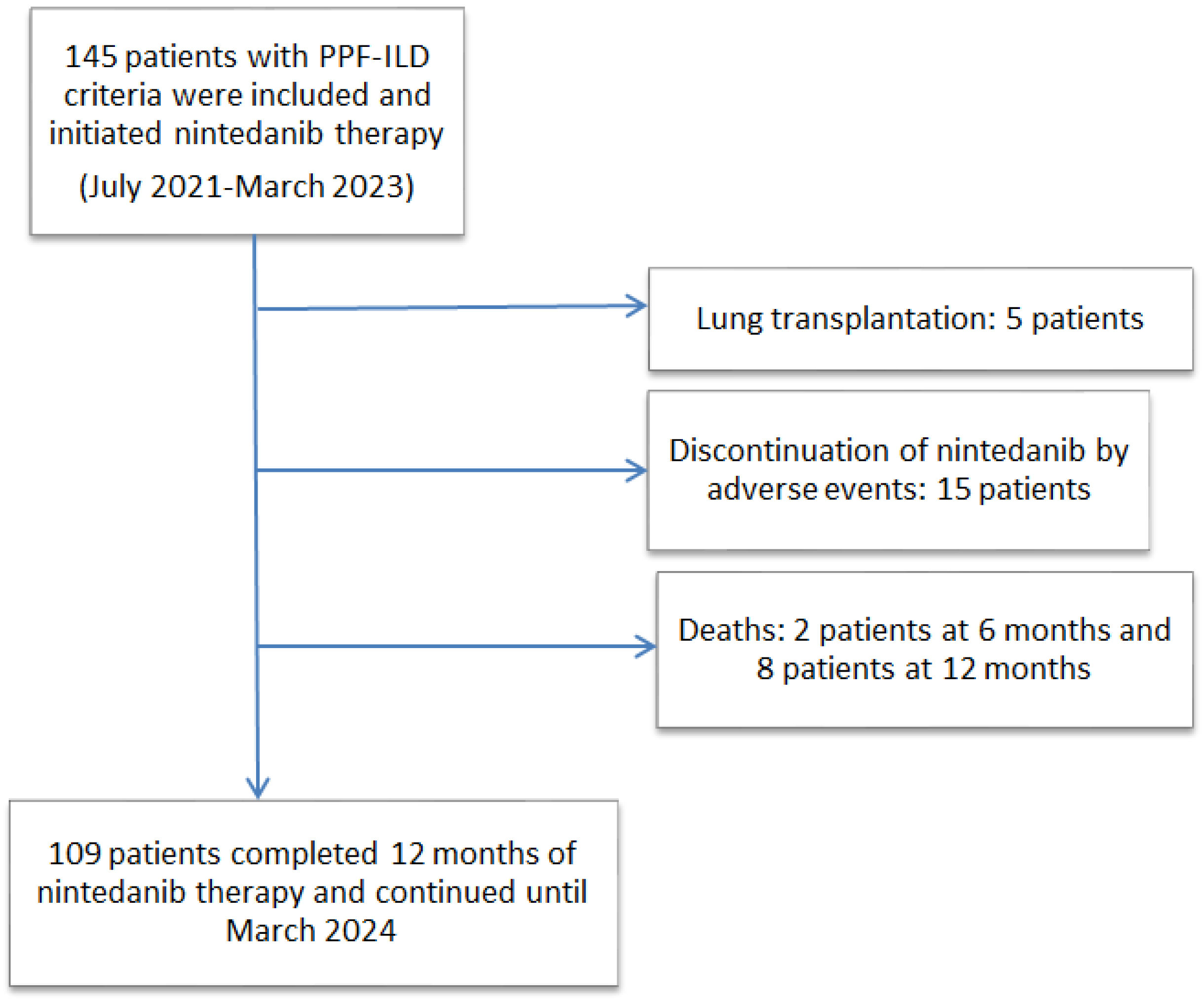
ResultsBetween July 2021 and March 2023, a total of 145 patients entered the study and were followed up until March 2024; 55% were men and the mean age was 66.6±11.5 years. PPF-ILD was diagnosed based on clinical, radiological and pulmonary function test findings in 97 patients (66.9%). The mean±SD duration of nintedanib therapy was 13.3±10.1 months. Dyspnea improved, although the difference was not statistically significant. FVC % and DLCO % stabilized. The number of hospitalizations related to PPF-ILD was reduced (p<0.0001) after 12 months of therapy. Diarrhea was the most common adverse event.
ConclusionsIn this real-world study, the profile of PPF-ILD patients treated with nintedanib was consistent with the approved therapeutic indications. Nintedanib reduced the decline in pulmonary function and the number of hospitalizations, and it was well tolerated. At 12 months, 75.1% of patients remained on treatment; treatment discontinuation occurred in 24.9% due to adverse events, death, or lung transplantation.
Los pacientes con enfermedades pulmonares intersticiales no idiopáticas pueden desarrollar fibrosis pulmonar progresiva (FPP-EPI). Los objetivos del estudio fueron definir el perfil de los pacientes con FPP-EPI tratados con nintedanib y evaluar la eficacia y la seguridad de este fármaco en un entorno de práctica clínica real.
MétodosEstudio multicéntrico, prospectivo y observacional realizado en pacientes adultos con FPP-EPI que iniciaron tratamiento con nintedanib en 10 hospitales andaluces (España). Se recogieron datos demográficos, hábito tabáquico, enfermedad de base y criterios diagnósticos. Se evaluaron los resultados de las pruebas de función pulmonar, la escala de disnea y el número de hospitalizaciones relacionadas con FPP-EPI al inicio del estudio y a los 6 y 12 meses. Se registraron los eventos adversos.
ResultadosEntre julio de 2021 y marzo de 2023 se incluyeron 145 pacientes, que fueron seguidos hasta marzo de 2024; el 55% eran varones y la edad media fue de 66,6±11,5 años. El diagnóstico de FPP-EPI se basó en hallazgos clínicos, radiológicos y funcionales en 97 pacientes (66,9%). La duración media±DE del tratamiento con nintedanib fue de 13,3±10,1 meses. La disnea mejoró, aunque la diferencia no fue estadísticamente significativa. El porcentaje de FVC y DLCO se estabilizó. El número de hospitalizaciones relacionadas con FPP-EPI se redujo (p<0,0001) tras 12 meses de tratamiento. La diarrea fue el evento adverso más frecuente.
ConclusionesEn este estudio de vida real, el perfil de los pacientes con FPP-EPI tratados con nintedanib fue coherente con las indicaciones terapéuticas aprobadas. Nintedanib redujo el deterioro de la función pulmonar y el número de hospitalizaciones, y fue bien tolerado. A los 12 meses, el 75,1% de los pacientes continuaba en tratamiento; la interrupción del tratamiento ocurrió en el 24,9% de los casos, debido a eventos adversos, fallecimiento o trasplante pulmonar.