En los últimos años se han realizado grandes esfuerzos en el programa de prevención de la transmisión de la madre al hijo (PTMH) de VIH en Guinea Ecuatorial (GE). El objetivo de este estudio fue describir los resultados del programa de PTMH en 2 centros sanitarios de Guinea Ecuatorial.
MétodosEstudio observacional prospectivo realizado en el Hospital Regional de Bata y Centro de Salud María Rafols en Bata, GE. Se analizaron las características epidemiológicas, clínicas y microbiológicas de las madres infectadas por el VIH-1 y de sus hijos. Se recogieron muestras sanguíneas en papel de filtro (DBS) en los lactantes expuestos (noviembre de 2012-diciembre de 2013) y se analizaron con la técnica Siemens VERSANT HIV-1 RNA v1.0 (kPCR).
ResultadosSesenta y ocho pares de madres y niños fueron incluidos. La mayoría de las mujeres estaban asintomáticas (88,2% con estadio clínicoi de la OMS). Cuarenta y siete mujeres (69,2%) recibieron tratamiento antirretroviral durante el embarazo. Cuarenta y cinco niños (66,1%) recibieron profilaxis posnatal con antirretrovirales. La mediana de edad en el momento de inclusión fue de 2,4meses (rango 1,2-4,9). Se confirmó la infección en 2 niños, y un niño falleció antes de poder descartarse la infección. La tasa de transmisión del VIH-1 fue del 2,9% (IC95%: 0,2-10,5).
ConclusionesEste estudio ha permitido evaluar el programa de PTMH en base a las técnicas de diagnóstico precoz. La identificación precoz de los pacientes infectados por el VIH-1 es fundamental para el inicio oportuno del tratamiento y evitar la mortalidad asociada a la infección.
Great efforts have been made in the last few years in order to implement the prevention of mother-to-child transmission (PMTCT) program in Equatorial Guinea (GQ). The aim of this study was to evaluate the rates of mother-to-child HIV transmission based on an HIV early infant diagnosis (EID) program.
MethodsA prospective observational study was performed in the Regional Hospital of Bata and Primary Health Care Centre Maria Rafols, Bata, GQ. Epidemiological, clinical, and microbiological characteristics of HIV-1-infected mothers and their exposed infants were recorded. Dried blood spots (DBS) for HIV-1 EID were collected from November 2012 to December 2013. HIV-1 genome was detected using Siemens VERSANT HIV-1 RNA 1.0 kPCR assay.
ResultsSixty nine pairs of women and infants were included. Sixty women (88.2%) had WHO clinical stage 1. Forty seven women (69.2%) were on antiretroviral treatment during pregnancy. Forty five infants (66.1%) received postnatal antiretroviral prophylaxis. Age at first DBS analysis was 2.4 months (IQR 1.2-4.9). One infant died before a HIV-1 diagnosis could be ruled out. Two infants were HIV-1 infected and started HAART before any symptoms were observed. The rate of HIV-1 transmission observed was 2.9% (95%CI 0.2-10.5).
ConclusionsThe PMTCT rate was evaluated for the first time in GQ based on EID. EID is the key for early initiation of antiretroviral therapy and to reduce the mortality associated with HIV infection.
La infección por el virus de la inmunodeficiencia humana (VIH) se manifiesta en Guinea Ecuatorial (GE) como una epidemia generalizada y constituye una de las causas más importantes de morbimortalidad en la población1. Los estudios de prevalencia de la infección muestran un incremento progresivo en la última década, tanto en población de 15 a 49años (3,2% en 2004; 6,2% en 2011) como en mujeres embarazadas (1,5% en 1997; 7,3% en 2008)1.
Se estima que en el país viven aproximadamente 2.900 niños con infección por VIH, habiéndose infectado por vía perinatal la gran mayoría1.
El Plan Nacional de Lucha contra el Sida de GE, con el apoyo técnico del Centro Nacional de Medicina Tropical del Instituto de Salud CarlosIII de España, actualizó el protocolo nacional de prevención de la transmisión de madre a hijo (PTMH) de VIH en 20082. Siguiendo los protocolos internacionales, en esta primera actualización se recomendaba el cribado de infección VIH en toda mujer embarazada. En caso de confirmarse la infección en la gestante, se valoraba la indicación de tratamiento antirretroviral (TAR) de gran efectividad o de profilaxis con antirretrovirales según recomendaciones de la Organización Mundial de la Salud (OMS) entonces vigentes3. De igual forma, este protocolo incluía recomendaciones para el seguimiento del niño expuesto, así como un protocolo diagnóstico de infección por VIH en el hijo de madre infectada por VIH basado en técnicas serológicas. En una evaluación inicial del programa de PTMH en GE, que incluyó a 103 pares de madres y niños nacidos desde 2008 a 2011, observamos que el cumplimiento del protocolo de PTMH era todavía bajo, con un porcentaje muy alto de niños expuestos perdidos en el seguimiento antes de confirmar o descartar la infección4.
El diagnóstico precoz de la infección por VIH antes de los 18meses de vida se basa en la detección por técnicas moleculares del material genético del VIH (ARN viral o ADN proviral)5,6. Sin embargo, dicha técnica no está disponible de manera rutinaria en la práctica clínica habitual en GE. La aplicación de estas técnicas en la sangre total seca recogida en papel de filtro (dried blood spots [DBS]) ha demostrado su eficacia para el diagnóstico precoz de la infección por VIH en países de recursos limitados7-9. Además, esta técnica ha sido utilizada en la evaluación de los programas de PTMH en estos contextos10,11. El objetivo de nuestro estudio fue describir los resultados del programa de PTMH en 2 centros sanitarios de GE en el periodo de noviembre de 2012 hasta diciembre de 2013.
MetodosSe realizó un estudio observacional prospectivo en el Hospital Regional de Bata y en el Centro de Salud María Rafols, Bata, GE. En estos centros se realiza el seguimiento de los niños expuestos, y es a ellos donde acuden las madres con sus hijos para valoración, una vez que sus hijos ya han nacido. Se incluyeron los hijos de las madres con infección por VIH-1, con edades comprendidas entre las 6 semanas y los 6 meses, durante su seguimiento en estas consultas. Se registraron las características epidemiológicas y clínicas de las madres infectadas por el VIH-1 y los lactantes expuestos. Las madres fueron clasificadas según los estadios clínicos e inmunológicos de la OMS para la infección por VIH12. El TAR de primera línea recomendado incluía zidovudina (AZT), lamivudina (3TC) y nevirapina (NVP). En los casos de mujeres en estadios clínicosi o ii y con linfocitos CD4 ≥350/mm3 se recomendaba la profilaxis con AZT desde la semana 28 de gestación, la administración de AZT, 3TC y NVP en el momento del parto, y finalmente la administración de AZT y 3TC durante una semana en el postparto para evitar la selección de resistencias a NVP en dosis única (opciónA de la OMS).
El protocolo recomendaba que, tras el nacimiento, el niño reciba dosis única de NVP y profilaxis con AZT durante 1 a 4semanas, según el tiempo total de TAR que recibiese la madre durante la gestación.
Los tipos de alimentación recomendados para el recién nacido eran lactancia materna exclusiva o lactancia artificial. En GE existe un programa de lactancia artificial gratuito para estas madres coordinado y financiado por el gobierno. En caso de que la madre optase por la lactancia artificial, se valoraba que se cumplieran los criterios AFASS (aceptable, factible, asequible, sostenible, segura) acorde con la recomendación de la OMS13.
Todas las madres de los pacientes fueron informados del estudio y dieron el consentimiento informado por escrito para su participación y la de sus hijos. El estudio fue aprobado por todos los centros participantes y aprobado por el Comité Ético y de Investigación Clínica del Hospital Universitario de Getafe.
Todos los datos previos a la inclusión de los pacientes en el estudio fueron obtenidos a partir de la entrevista clínica y de los informes que aportaban las madres. En todas las madres se confirmó la infección por VIH-1 tras positividad de 3 test rápidos en el laboratorio de los centros del estudio, Determine® (Abbott Laboratories, EE.UU.), Unigold® (Michigan Regional Laboratory System) y Hexagon® (Acon Laboratories, San Diego, California, EE.UU.), o tras el resultado confirmatorio del test Bio-Rad Geenius HIV 1/2®.
Se recogió información sobre el tipo de parto y alimentación del recién nacido.
Se recogieron muestras de sangre en 2 tarjetas de papel de filtro 903 (Whatman, Schleicher & Schuell, BioScience GmbH, Barcelona, España) (dried blood spot [DBS]) de los lactantes expuestos y sus madres. En los niños se requirió un pinchazo con lanceta en el talón para impregnar cada uno de los 5 círculos que tiene cada tarjeta (1 o 2 gotas de sangre en cada círculo, aproximadamente 70μl de sangre/círculo). De la madre se tomó sangre directamente por venopunción posteriormente a la muestra del niño, y se procesaron de forma independiente. Los DBS se mantuvieron en posición horizontal a temperatura ambiente toda la noche hasta asegurar su secado. Posteriormente los DBS de cada paciente se introdujeron en una bolsa plástica diferente con zip junto con 2 desecantes y fueron almacenados a −20°C hasta su envío a España por mensajería internacional. Las muestras fueron analizadas en el Laboratorio de Epidemiología Molecular del VIH del Hospital Ramón y Cajal-IRYCIS. El proceso de extracción, amplificación y detección del genoma por la técnica Siemens VERSANT VIH-1 RNA 1.0 ensayo (kPCR) ya ha sido previamente descrito14,15. Todo niño en seguimiento con una detección positiva en la prueba molecular confirmada en una segunda visita, al menos 4 semanas posterior a la primera, fue diagnosticado de infección por VIH-13,13. Se descartó la infección por VIH-1 en todo niño con un resultado negativo en el primer DBS que no recibiese lactancia materna3,16.
De acuerdo con las recomendaciones del «Protocolo Nacional de Manejo de la Prevención Materno Infantil de VIH de Guinea Ecuatorial», los niños expuestos continuaron su seguimiento acorde al calendario que incluye visitas a las 10 semanas, 14 semanas, 6 meses, 9 meses, 12 meses y 18 meses de vida. En cada visita se realizaba una valoración clínica del paciente, se daban consejos sobre alimentación y se actualizaba el calendario vacunal. A partir de la sexta semana de vida se recomendaba profilaxis con cotrimoxazol a todos los niños expuestos. Según las recomendaciones de este protocolo se consideraba descartada la infección por VIH tras el resultado negativo del test rápido (Determine®) a partir del sexto mes de vida en al menos 2 ocasiones, siempre y cuando el niño no recibiera lactancia materna. Se consideró como fecha de desaparición de anticuerpos la primera fecha en la que el test fue negativo. Se consideraba confirmada la infección por VIH cuando los 3 test rápidos (Determine®, Unigold® y Hexagon®) eran positivos a los 18 meses.
El análisis estadístico fue realizado con el soporte informático del programa SPSS 15.0 para Windows. Se analizaron la mediana y el rango intercuartílico de las variables cuantitativas. Con las variables cualitativas se obtuvieron las frecuencias absolutas y los porcentajes correspondientes a cada una de las categorías que componían dichas variables. Se utilizó el test exacto de Fisher para el análisis de variables cualitativas. Para el análisis de las curvas de supervivencia se aplicó el método de Kaplan-Meier.
ResultadosSetenta y cuatro madres y sus hijos fueron invitados a participar. Tres madres rechazaron la participación de sus hijos en el estudio. En el caso de otros 2 niños no se obtuvieron muestras adecuadas en DBS y fueron excluidos de este análisis. Otro paciente falleció por causas desconocidas antes de que se obtuviese una muestra adecuada en DBS para el análisis y también fue excluido. Sesenta y ocho niños (45,6% varones) fueron incluidos en el estudio. Las características epidemiológicas y clínicas de las madres y los niños quedan recogidas en la tabla 1. En su gran mayoría, las madres eran mujeres jóvenes en estadios no avanzados de la enfermedad. Cuarenta y siete mujeres (69%) recibieron bien profilaxis con AZT o bien tratamiento combinado para la prevención de la transmisión maternoinfantil. La mayoría de los partos fueron vaginales. Cuarenta y cinco niños (66,1%) recibieron profilaxis posnatal con antirretrovirales de forma adecuada: AZT con o sin NVP. Ningún niño estaba recibiendo profilaxis con antirretrovirales en el momento de la extracción del DBS. Durante las visitas de seguimiento ninguna madre refirió que alimentase a su hijo con lactancia materna.
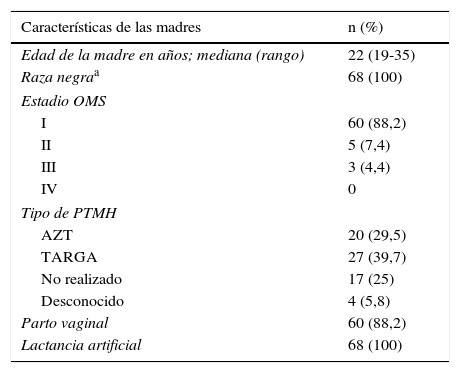
Características de las madres con infección VIH-1 y de los hijos expuestos
| Características de las madres | n (%) |
|---|---|
| Edad de la madre en años; mediana (rango) | 22 (19-35) |
| Raza negraa | 68 (100) |
| Estadio OMS | |
| I | 60 (88,2) |
| II | 5 (7,4) |
| III | 3 (4,4) |
| IV | 0 |
| Tipo de PTMH | |
| AZT | 20 (29,5) |
| TARGA | 27 (39,7) |
| No realizado | 17 (25) |
| Desconocido | 4 (5,8) |
| Parto vaginal | 60 (88,2) |
| Lactancia artificial | 68 (100) |
| Características de los niños | n (%) |
|---|---|
| Edad del niño en meses; mediana (rango) | 2,3 (1,2-4,5) |
| Peso al nacimiento en gramos; mediana (RIQ) | 2.950 (2.300-3.200) |
| Sexo masculino | 31 (45,6) |
| Lugar de nacimiento | |
| Hospital de Bata | 32 (47,0) |
| Otro hospital | 24 (35,4) |
| Parto extrahospitalario | 12 (17,6) |
| Profilaxis neonatal adecuada | |
| Sí | 45 (66,1) |
| No | 15 (22,1) |
| Desconocida | 8 (11,8) |
| Seguimiento de los niños (n, % del total de niños)b | |
|---|---|
| Niños con estudio serológico a los 6 meses (40, 60,6%) Serología VIH negativa (%) | 2,5 |
| Niños con estudio serológico a los 9 meses (30, 45,4%) Serología VIH negativa (%) | 46,6 |
| Niños con estudio serológico a los 12 meses (26, 39,3%) Serología VIH negativa (%) | 57,7 |
| Niños con estudio serológico a los 18 meses (24, 36,3%) Serología VIH negativa (%) | 100 |
AZT: zidovudina; OMS: Organización Mundial de la Salud; PTMH: prevención de la transmisión de la madre al hijo de VIH-1; RIQ: rango intercuartílico; TARGA: tratamiento antirretroviral de gran actividad.
Para cada una de las visitas se muestra el porcentaje de pacientes con serología para el VIH negativa (test rápido Determine® negativo en 2 determinaciones). El análisis se realiza en los pacientes que se mantienen en seguimiento, y se incluyen también los pacientes con diagnóstico de confirmación de no infección por técnicas serológicas con seguimiento ya completo. Se excluyen los 2 pacientes con diagnóstico confirmado de VIH por técnicas virológicas.
Los resultados de la técnica virológica en el primer DBS mostraron un resultado negativo en 66 pacientes y un resultado positivo en 2 pacientes. La tasa de transmisión perinatal de VIH-1 observada en nuestro estudio fue del 2,9% (IC95%: 0,2-10,5). El primer caso se trataba de un varón que nació por parto vaginal de una madre con infección por VIH-1 y que inició profilaxis con AZT en la semana 28 de la gestación. El niño no recibió lactancia materna y realizó profilaxis posnatal con AZT durante 4 semanas. La primera carga viral de VIH-1 en DBS mostró un resultado de 4,53log y la prueba confirmatoria, 4 semanas después, de 4,65log. El segundo paciente era una niña nacida por cesárea de una madre infectada por VIH-1 que inició profilaxis con AZT en el tercer trimestre del embarazo. La paciente no recibió lactancia materna y tomó AZT posnatal durante una semana. Las cargas virales para el VIH-1 fueron de 3,57 y 2,9log en la primera y segunda muestra, respectivamente. Ambos pacientes se encontraban asintomáticos en el momento de la extracción sanguínea del segundo DBS para la confirmación de la infección, e iniciaron TAR de forma inmediata en esa visita.
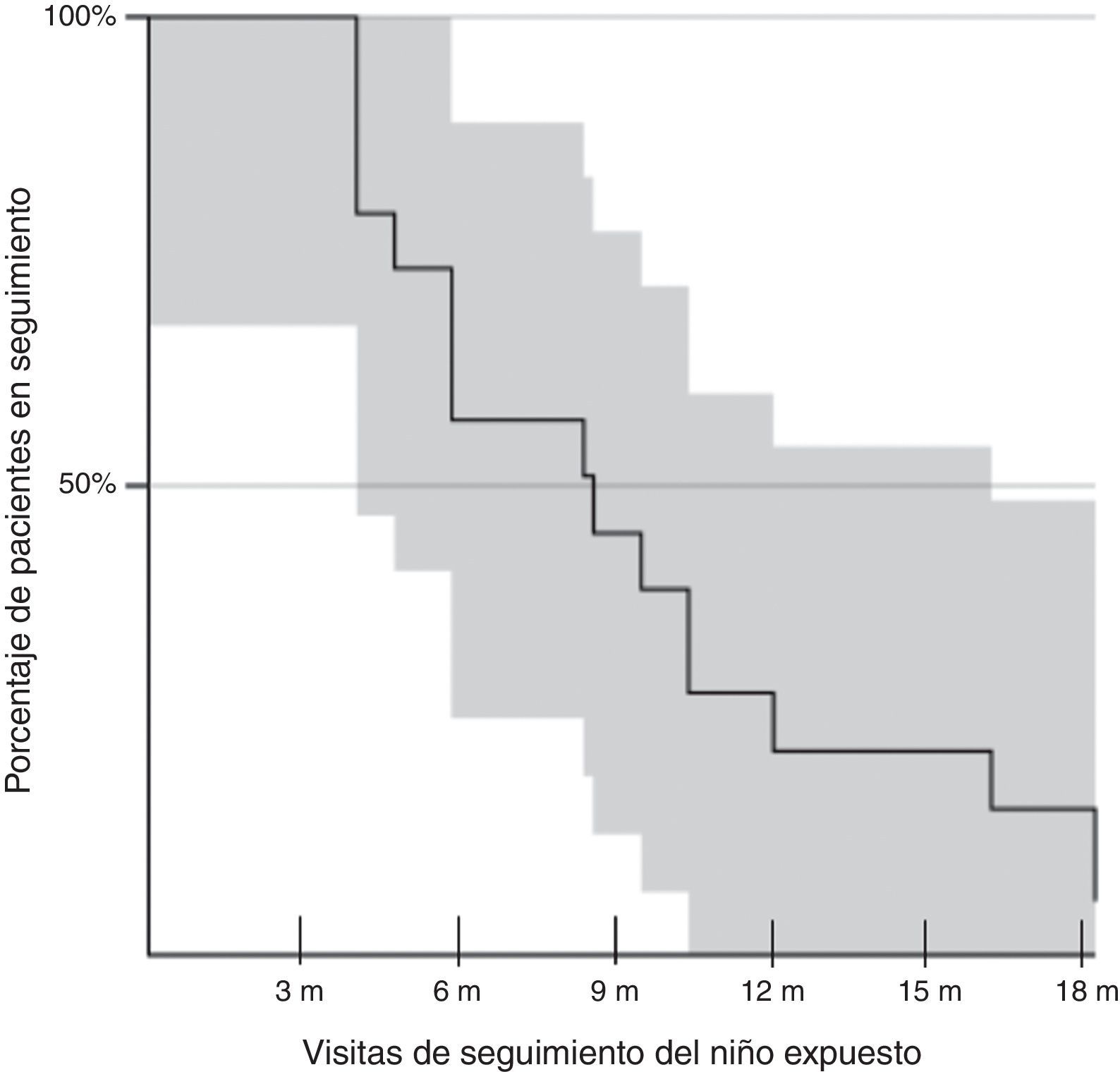
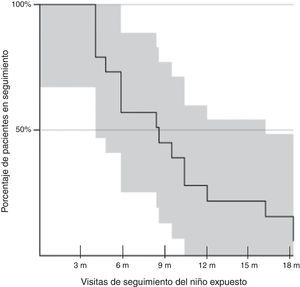
En la figura 1 se observan las pérdidas de seguimiento de los pacientes acorde con las visitas del programa. La mediana de seguimiento fue de 9meses (rango intercuartílico 6-12meses). El número de pacientes perdidos en el seguimiento en las visitas de los 12 y 18meses fue del 77,8 y del 95,8%. No se observaron diferencias en los porcentajes de pacientes perdidos para el seguimiento a los 12meses cuando comparamos estos resultados con los del análisis del periodo 2008-2011 (72 vs. 77,8%).
Acorde a las visitas del programa, solamente se pudo descartar la infección en 24 niños (36,3%) durante el seguimiento. No se observó ningún caso de transmisión posnatal de VIH.
DiscusiónEste estudio ha permitido evaluar el programa de PTMH en un área urbana de GE. En el África subsahariana los programas de PTMH presentan importantes limitaciones en su implementación17,18. A pesar de ello, en los últimos años se han producido grandes avances en la expansión del TAR en estos países19.
En estudios poblacionales en el África subsahariana, las coberturas de TAR en la gestación se correlacionan de forma inversa con las tasas de transmisión perinatal de VIH20. Durante el periodo estudiado observamos un aumento en la cobertura antirretroviral durante la gestación (52% [54/103] vs. 69,2% [47/68], p=0,02) respecto al análisis realizado en el período 2008-2011 en estos mismos centros4. También observamos un aumento significativo en el porcentaje de niños que recibían profilaxis posnatal entre los 2 periodos (41% [42/103] vs. 66,1% [45/68], p=0,001). Aunque previamente no se habían podido evaluar las tasas de transmisión perinatal de VIH-1 en GE de forma fidedigna, estos resultados sugieren avances en la implementación del programa, al menos a nivel local en los centros evaluados en Bata4. Aun así, son necesarios esfuerzos adicionales para aumentar aún más las tasas de cobertura antirretroviral en la gestación. Por otro lado, la adherencia al TAR es un factor crítico para el control adecuado de la carga viral y la prevención de la trasmisión perinatal de VIH. Sin embargo, el diseño de este estudio no permitió analizar la adherencia al TAR durante la gestación.
En hijos de madres con infección por VIH, el diagnóstico precoz es fundamental para un inicio precoz del TAR y así disminuir la morbimortalidad asociada a la infección21,22. Además, las técnicas de diagnóstico precoz en DBS de la infección por VIH han sido consideradas como una herramienta para evaluar los programas de PTMH10. La transmisión perinatal de VIH a las 6 semanas de vida en recién nacidos expuestos ha sido evaluada en Zambia por este método, donde se observaron tasas de transmisión del 4,2% en el caso de que la madre recibiese TARGA y del 6,8% en caso de que recibiese profilaxis con AZT11. Además, las tasas de transmisión perinatal observadas previamente en los estudios que evaluaban la opciónA en el África subsahariana y Asia son similares a las que observamos en nuestro estudio23-25. Aunque el valor de estas técnicas para el diagnóstico precoz de la infección por VIH en DBS ha sido reconocido por la OMS, es importante destacar que, a pesar de que la sensibilidad y la especificidad de estas técnicas pueden ser altas en nuestro medio, pueden presentar limitaciones en la detección de recombinantes del virus o subtipos noB del virus, más frecuentes en otros medios15.
Es importante reseñar que en nuestro estudio solo se evalúa la infección en un primer momento, cercano al nacimiento del niño. Según datos de ONUSIDA, en el contexto del África subsahariana las tasas de transmisión perinatal son del 7% cuando se analizan a las 6 semanas de vida del niño, y hasta del 16% cuando se analizan tras el fin de la lactancia materna19. Las altas pérdidas observadas en el seguimiento no permiten conocer de forma adecuada el número de niños que serorrevierten en los primeros 18meses de vida en nuestro estudio. Sin embargo todas las madres refirieron que la única forma de alimentación del niño fue la lactancia artificial en las visitas de seguimiento del estudio. En cada una de estas visitas se comprobó que las madres tenían los conocimientos y habilidades necesarios para la preparación de fórmula artificial. En GE, la lactancia artificial a los hijos de madre con infección por VIH está garantizada por un programa nacional, y la fórmula se reparte de forma gratuita en múltiples centros sanitarios2. Sin embargo, a pesar de ello, no podemos asegurar que no hubiese casos de lactancia materna o lactancia mixta, y por tanto que hubiese casos de transmisión posnatal de la infección por VIH. Aun así, no observamos ningún caso de transmisión posnatal entre los pacientes que terminaron el seguimiento.
Las altas pérdidas en el seguimiento impiden conocer la evolución de los niños no infectados. La lactancia artificial se ha relacionado con mayor morbimortalidad en los niños expuestos en los países con recursos limitados26. Además, independientemente del tipo de alimentación, la morbilidad de los niños expuestos no infectados puede ser superior a la observada en niños de la población general27-29.
Una de las limitaciones más importantes en la evaluación de los programas de PTMH son las pérdidas del seguimiento observadas en la cascada de atención sanitaria30. Nuestro estudio aporta datos del seguimiento de los hijos de las madres con infección por VIH que acuden a 2 centros sanitarios en Bata, pero no conocemos cuáles son las características y la evolución de las gestantes desde su primera visita en la gestación. Por tanto, este trabajo no permite evaluar de una forma global el programa de PTMH en GE, pero sí que ha permitido evaluar de una forma más detallada una parte de esta cascada de atención en las consultas seleccionadas para el estudio en Bata. Aunque el número de pacientes incluidos en nuestro estudio es pequeño, más de la mitad de los niños no habían nacido en ninguno de los centros donde se realizó la evaluación. Estos datos apoyan una expansión más rápida del programa de PTMH en GE por todo el país y abren la oportunidad para el desarrollo de nuevas estrategias de PTMH.
En conclusión, este estudio aporta los primeros datos en las tasas de transmisión maternoinfantil de VIH-1 en GE basados en el diagnóstico precoz de la infección por VIH de los lactantes expuestos usando una técnica molecular. Además pone de relieve la importancia del diagnóstico precoz para el inicio oportuno del TAR en los niños infectados, para así reducir la mortalidad asociada a la infección VIH-1 en el país.
FinanciaciónEste estudio fue financiado por el Instituto de Salud CarlosIII a través del Plan Nacional de I+D+I 2008-2011 (FIS PI12/00240) y por la 24.ª Beca DODOT 2012 de Investigación Pediátrica de la Asociación Española de Pediatría.
Conflicto de interesesLuis Manuel Prieto Tato, Sara Guillén, Pablo Rojo, José Tomás Ramos y Antonio Vargas participaron como asesores técnicos de Ministerio de Sanidad de Guinea Ecuatorial en la elaboración de las guías nacionales para la prevención maternoinfantil de VIH. Esta actividad no afecta a la calidad del presente documento ni entra en conflicto de intereses con lo recomendado en él. El resto de autores declaran no tener ningún conflicto de intereses.
A todas las madres y los niños, por su participación en el estudio.