La tecnología recombinante del ADN ha permitido disponer de análogos de insulina humana para el tratamiento de la diabetes mellitus, cuya eficacia y seguridad han permitido mejorar el tratamiento de esta enfermedad. En este trabajo se revisan de forma breve las características principales de los análogos de insulina disponibles actualmente. Se incluyen tanto los análogos de insulina de acción rápida (lispro, aspártica y glulisina) como los de acción prolongada (glargina y determir). Se describen las características farmacológicas de cada análogo de insulina, sus diferencias con respecto a la insulina humana, su forma de administración, indicación, eficacia y seguridad. Además se discuten las principales controversias del uso de estos análogos de insulina. En concreto, los referidos al riesgo de cáncer y retinopatía y su utilización en mujeres gestantes.
Recombinant DNA technology has provided insulin analogues for the treatment of diabetes mellitus, with an efficacy and safety that has improved the treatment of this disease. We briefly review the principal characteristics of the insulin analogues currently available. Both rapid-acting (lispro, aspart and glulisine) and long acting (glargine and determir) insulin analogues are included in this review. We describe the pharmacology of each insulin analogue, their differences with the human insulin, the administration, indication, efficacy and safety. In addition we discussed the main controversies of the use of these insulin analogues. In particular, those related with the risk of cancer and retinopathy, and their use in pregnant women.
La insulina es la hormona «anabólica» por excelencia, que permite a nuestras células el aporte necesario de glucosa. A partir de esta glucosa, mediante los procesos de glucólisis y respiración celular, se obtendrá la energía necesaria en forma de trifosfato de adenosina (ATP). La insulina se produce en el páncreas en los islotes de Langerhans, más concretamente en las células llamadas beta. La insulina posee una importante función reguladora sobre el metabolismo, sobre el que tiene los siguientes efectos:
- •
Promueve la glucólisis.
- •
Estimula la glucogenogénesis e inhibe la glucogenólisis.
- •
Favorece la síntesis de triacilgliceroles, estimulando la producción de acetil coenzima A (CoA) (al acelerar la glucólisis), y también estimula la síntesis de ácidos grasos a partir de acetil-CoA.
La conformación estructural de la insulina es muy importante para poder desarrollar su actividad como hormona. Dentro del aparato de Golgi, la proinsulina es introducida en el interior de vesículas secretoras y de almacenamiento ricas en Zn++ y Ca++. Una vez en la vesícula se forman estructuras hexaméricas de la proinsulina con 2 átomos de cinc por cada hexámero de proinsulina: (Zn++)2(Ca++)(Proin), las cuales son posteriormente convertidas en el hexámero de insulina: (Zn++)2(Ca++)(In), produciendo también el péptido C, quedando libres los extremos C-terminal y N-terminal. Estos extremos libres tienen 51 aminoácidos en total y se denominan cadenas A (21 aminoácidos) y B (30 aminoácidos), los cuales terminan unidos entre sí por medio de enlaces disulfuro. De modo que la proinsulina consta de las cadenas B-C-A y los gránulos secretorios liberan las 3 cadenas de forma simultánea.
Por tanto, la insulina es sintetizada y almacenada en forma de un hexámero, es decir, un complejo compuesto por 6 moléculas de insulina, pero su forma activa es la de una hormona monomérica. Este hexámero de insulina permanece inactivo, como forma de almacenamiento con una rápida disponibilidad. El hexámero es mucho más estable que la hormona monomérica, sin embargo, el monómero es la forma más reactiva de la hormona porque su difusión es mucho más rápida.
Teniendo en cuenta esas premisas fisiológicas, debemos pensar que el paciente con diabetes mellitus tipo 1 es un paciente con insulinopenia y el paciente con diabetes mellitus tipo 2 presenta una resistencia a la insulina que acabará generando un cuadro de insulinopenia. Es decir, ambos tipos de diabetes mellitus, el primero desde un inicio y el segundo en una mayoría de los casos, van a precisar del uso de insulina para su tratamiento.
La tecnología recombinante del ADN ha permitido disponer de insulina de una manera fácil y económica1. Por tanto, estas tecnologías se han aplicado para crear unos análogos de insulina, modificando la molécula de insulina humana. Estas modificaciones alteran la farmacocinética y farmacodinámica, intentando imitar la actividad basal y el pico de actividad de la insulina, de forma similar a la producida por las células beta del páncreas. A continuación revisaremos las modificaciones de los análogos de insulina, tanto rápidos (lispro, aspart, glulisina) como basales (glargina y determir), así como su efecto sobre el control glucémico.
Análogos de insulina de acción rápidaInsulina lisproHace 15 años (1996) apareció el primer análogo de la insulina, la insulina lispro (insulina humana Lis B28, Pro B29). Esta molécula se logró con la inversión de 2 aminoácidos, prolina y lisina, en las posiciones 28 y 29 de la cadena B de la molécula de insulina humana. Este cambio produce una variación en la conformación del carbono terminal de la cadena B, que impide la formación de dímeros a partir de los monómeros de insulina2. Desde el punto de vista farmacocinético, la insulina lispro tiene un inicio de acción rápida de aproximadamente 5-15min y una duración de acción reducida de 2-4h. Los estudios experimentales3 en diabéticos tipo 1 muestran como la concentración máxima de la insulina lispro plasmática se alcanza a los 41 min. Tenemos que pensar que inicialmente esta insulina se diseñó con el propósito de imitar las concentraciones fisiológicas de la insulina en la sangre en respuesta al aumento de la glucemia posprandial. Por tanto, la insulina lispro se puede administrar inmediatamente antes de las comidas principales e incluso inmediatamente después. A pesar de estos datos farmacocinéticos, tenemos que recordar que existen otros factores que influyen sobre la absorción subcutánea de la insulina lispro, como sucede con la insulina regular humana. Por ejemplo, la tasa de absorción de insulina aumenta cuando se aplica en la región abdominal y por el efecto del calor4. Otras características que podemos comentar, son una mayor concentración plasmática pico en la insulina lispro y la insulina regular humana1 y una potencia hipoglucemiante de la insulina lispro equivalente a la insulina regular5. En la tabla 1 se muestran las características farmacocinéticas de la insulina lispro (acción rápida de aproximadamente 5-15min y una duración de acción reducida de 2-4h). El tiempo para alcanzar la actividad pico de la insulina humana regular es dependiente de la dosis, a diferencia de la insulina lispro que no depende de esta6.Uno de los temores que todos los médicos hemos tenido en un inicio con estos análogos es el desarrollo de anticuerpos frente a la administración exógena de estas moléculas, con el consiguiente retraso en el inicio de su acción, pudiendo, por tanto, teóricamente, modificar el pico máximo de acción y la duración del tiempo de acción. Con respecto a este primer análogo comercializado (insulina lispro) no se ha conseguido demostrar un aumento de la respuesta inmunológica7, mostrando en los diferentes estudios8, al comparar este análogo de insulina con la insulina humana regular, una tasa similar de de reacciones alérgicas y títulos de anticuerpos antiinsulínicos.
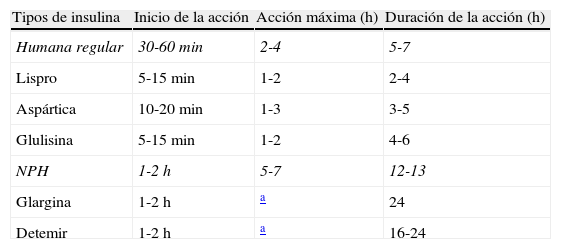
Farmacocinética de los diferentes tipos de insulina
| Tipos de insulina | Inicio de la acción | Acción máxima (h) | Duración de la acción (h) |
| Humana regular | 30-60min | 2-4 | 5-7 |
| Lispro | 5-15min | 1-2 | 2-4 |
| Aspártica | 10-20min | 1-3 | 3-5 |
| Glulisina | 5-15min | 1-2 | 4-6 |
| NPH | 1-2h | 5-7 | 12-13 |
| Glargina | 1-2h | a | 24 |
| Detemir | 1-2h | a | 16-24 |
NPH: Neutral Protamin Hagedorn o isofana.
Fuente: tabla elaborada por los autores a partir de información técnica de diferentes tipos de insulina.
Todos estos cambios farmacocinéticos y farmacodinámicos se traducen en unas modificaciones en las pautas de uso del análogo frente a la insulina regular humana, así como una mejoría en determinados resultados clínicos. Por ejemplo, cuando usamos insulina lispro en régimen terapéutico de dosis múltiples se recomienda, teniendo en cuenta su comienzo de acción más rápido, que se administre justamente antes de iniciar la ingesta, a diferencia de la insulina humana regular que debe inyectarse de 30-60min antes de la ingestión de los alimentos9.
Los estudios clínicos que han comparado el efecto de este análogo con la insulina regular humana demuestran cómo las concentraciones de glucosa posprandiales son de 20-70mg/dl más bajas con insulina lispro10, sin embargo las concentraciones medias de glucosa preprandiales son más elevadas en los que reciben insulina lispro. Por tanto, los valores de hemoglobina glucosilada A1c (HbA1c) disminuyen menos durante el tratamiento con este tipo de análogo. Debemos tener en cuenta que en este control de la glucemia posprandial también van a intervenir el tipo de alimentos que comemos; de este modo, con los alimentos grasos el vaciamiento gástrico se hace más lento. Por ejemplo, Strachan et al.11 realizaron un estudio mediante el uso de alimentos con diferente composición, demostrando que cuando se consumen alimentos con alto contenido en hidratos de carbono, el momento ideal para administrar la insulina lispro es preprandial; sin embargo, cuando los alimentos tienen un alto contenido en grasas es preferible indicar la insulina lispro posprandial. Es importante pensar que la posibilidad de poder administrar la insulina lispro en el período posprandial en niños con diabetes tipo 1 permite dosificar la dosis de acuerdo con la cantidad de alimentos que el niño finalmente come, lo que reduce la posibilidad de episodios hipoglucémicos ante la negativa del niño a realizar una ingesta completa.
Otra de las características de esta insulina es la menor tasa de hipoglucemias. En un trabajo realizado en pacientes diabéticos tipo 112, se comparó la insulina lispro con la insulina humana regular. Después de 3 meses de tratamiento, los niveles de HbA1c disminuyeron a un 0,4%, y presentó menos episodios hipoglucémicos el grupo tratado con insulina lispro. Como último comentario, con los datos que disponemos no tenemos información hasta el momento que justifique el empleo de la insulina lispro en niños < 6 años, personas de la tercera edad, embarazadas y en la lactancia. En tabla 2 se muestran las ventajas y desventajas potenciales de la insulina lispro cuando se compara con la insulina regular humana.
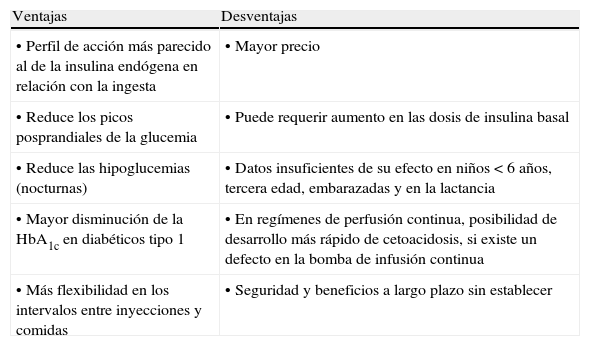
Análogos de insulina rápida (lispro, aspártica, glulisina) al compararlos con la insulina humana regular
| Ventajas | Desventajas |
| • Perfil de acción más parecido al de la insulina endógena en relación con la ingesta | • Mayor precio |
| • Reduce los picos posprandiales de la glucemia | • Puede requerir aumento en las dosis de insulina basal |
| • Reduce las hipoglucemias (nocturnas) | • Datos insuficientes de su efecto en niños < 6 años, tercera edad, embarazadas y en la lactancia |
| • Mayor disminución de la HbA1c en diabéticos tipo 1 | • En regímenes de perfusión continua, posibilidad de desarrollo más rápido de cetoacidosis, si existe un defecto en la bomba de infusión continua |
| • Más flexibilidad en los intervalos entre inyecciones y comidas | • Seguridad y beneficios a largo plazo sin establecer |
Es el segundo análogo de insulina de acción rápida que apareció en el mercado español. Se diferencia estructuralmente de la insulina humana regular, en la sustitución de prolina en la posición 28 de la cadena B de la insulina por ácido aspártico. Esta sustitución disminuye la tendencia de la molécula de insulina a formar hexámeros, lo cual determina sus características farmacocinéticas13. Su acción se inicia a los 10-20min tras la inyección; alcanza un pico máximo de acción a la 1-3h, con una duración entre 3 y 5h (tabla 1). Si la comparamos con la insulina humana regular alcanza una concentración sérica dos veces mayor y dura la mitad del tiempo14. Lo mismo que sucedía con la insulina lispro, se puede inyectar antes de las comidas principales, o incluso después de comer ante situaciones como pueden ser los niños de corta edad o pacientes con demencia, donde no se puede asegurar a priori la ingesta. Con respecto a la farmacocinética, los mismos factores que hemos enumerado que pueden influir en la insulina lispro son capaces de influir en la insulina aspártica. Merece la pena recordar que la afinidad de la insulina aspártica por el receptor de la insulina y por el receptor de IGF-1 es el 80% a la observada con la insulina regular humana15. Su perfil inmunológico es similar al de la insulina regular humana. No se posee suficiente información acerca del uso de este análogo de la insulina en niños < 2 años, personas de la tercera edad y en la lactancia, sin embargo sí que tiene aprobada su indicación en mujeres embarazadas16 y ha demostrado su eficacia en niños mayores de 2 años17.
Estos cambios en su farmacocinética han tenido como implicaciones clínicas mejorías en algunos parámetros habituales que utilizamos para el control de los pacientes diabéticos en la consulta de atención primaria. De este modo, en una comparación con insulina humana regular, Raskin et al.18 demostraron en su trabajo que el grupo tratado con insulina aspártica tuvo valores de HbA1c más bajos y una reducción de las hipoglucemias nocturnas. La insulina aspártica proporciona un mejor control de la glucemia en ayunas y posprandial tanto en diabéticos tipo 1 como tipo 2, en comparación con la insulina humana regular13. Algunos investigadores han demostrado que con el empleo de insulina aspártica se logran obtener valores de glucemia posprandial y de HbA1c más bajos que los obtenidos con la insulina humana regular19,20.
En una revisión Cochrane21 que evaluó 42 ensayos clínicos en los que se comparaban los análogos de insulina de acción rápida con la insulina humana regular, demostró que los análogos de insulina disminuyen los valores de HbA1c un 0,1% más que las insulinas convencionales en personas con diabetes mellitus tipo 1, lo que no ocurría en los diabéticos tipo 2. En ambos tipos de diabetes mellitus parecía disminuir la incidencia de hipoglucemia severa19.
Insulina glulisinaLa insulina glulisina es el más reciente de los análogos de insulina de acción rápida que ha aparecido en nuestro mercado. Este análogo se produce modificando en la molécula de insulina humana del aminoácido aspargina en la posición B3 por lisina, y la lisina en la posición B29 por glutamina. Los datos disponibles de estudios farmacocinéticos de la insulina glulisina son comparables con los obtenidos con la insulina lispro y la duración de su acción es entre 5 y 6h (tabla 1)22. La insulina glulisina presenta una opción novedosa frente a otros análogos de acción rápida, por su única actividad preferencial sobre la fosforilación del IRS-2 (sustrato-2 del receptor de la insulina), proporciona una actividad antiapoptótica de la célula betapancreática frente a los ácidos grasos y a las citocinas23.
Este análogo de insulina rápida, al igual que los otros análogos de acción corta, mimetiza mejor la secreción de insulina endógena que la insulina regular humana. Por ello, este preparado, como hemos comentado previamente, puede administrarse incluso después de las comidas sin riesgo de hipoglucemias. El único contratiempo que podemos comentar en este tipo de insulina es el radical (COOH de la porción terminal de la cadena B de la insulina, que parece estar relacionado con su afinidad con el receptor IGF-1). La mayor afinidad con este receptor IGF-1, incrementa potencialmente el efecto mitogénico, lo cual debe evaluarse en estudios a largo plazo24.
Análogos de insulina de acción prolongadaLa otra necesidad en la insulinización de un paciente diabético es el mantenimiento de una insulinemia basal para mantener un control preprandial adecuado. De este modo, los preparados de insulina de larga acción (NPH y NPL) ponen de manifiesto en la práctica clínica algunos defectos farmacocinéticos y farmacodinámicos que los alejan del objetivo ideal de una insulinemia basal, más o menos constante. Con el fin de obtener este objetivo han aparecido en el mercado análogos de insulina de acción prolongada (insulina glarglina e insulina detemir).
Insulina glarginaLa primera de las moléculas análogas de la insulina de larga acción aprobada para su uso clínico fue la insulina glargina. Esta insulina se obtiene al añadir 2 moléculas de arginina en la región C terminal de la cadena B y la sustitución de la arginina por glicina en la posición A21 de la cadena A25. Estas modificaciones generan la adición de 2 cargas positivas en la molécula, cambiando el punto isoeléctrico de pH 5,4 a 6,7; esto hace que la molécula sea menos soluble al pH fisiológico del tejido subcutáneo, creando microprecipitados de glargina que se van absorbiendo lentamente. Además, a este análogo se le añade cinc, haciendo que cristalice en el tejido subcutáneo, lo que retrasa aún más su absorción. Estas características mencionadas hacen que nos encontremos una insulina totalmente transparente, que a diferencia de la insulina rápida, «también transparente», no puede ser mezclada con ninguna otra preparación de insulina26.
El aspecto más interesante de este análogo de insulina basal es que tras su administración por vía subcutánea se produce un perfil de concentración plasmática, sin picos a lo largo de 20-24h; su acción comienza 1-2h después de administrarse por vía subcutánea27. Es necesario recordar que la insulina glargina puede interactuar con diferentes fármacos, lo que puede modificar sus efectos farmacológicos (tabla 3).
Interacciones con otros fármacos de la insulina glargina
| • Reducen el efecto hipoglucemianteCorticoesteroides, danazol, diazóxido, diuréticos, glucagón, isoniacida, estrógenos y progestágenos, derivados de la fenoticina, somatotropina, simpaticomiméticos (p. ej., adrenalina, salbutamol, terbutalina) y hormonas tiroideas |
| • Potencian el efecto hipoglucemianteAntidiabéticos orales, inhibidores de la enzima conversora de la angiotensina, disopiramida, inhibidores de la monoaminooxidasa, disopiramida, fibratos, fluoxetina, pentoxifilina, propoxifeno, salicilatos, antibióticos tipo sulfamidas |
Las indicaciones clínicas de este análogo de insulina nos permiten utilizarlo en pacientes con diabetes mellitus tipo 1 y diabetes mellitus tipo 2, en estos últimos puede utilizarse con sulfonilureas, acarbosa y metformina. Los datos de su utilidad en mujeres embarazadas y madres lactantes son insuficientes.
Una de las preocupaciones con este análogo de insulina basal es su potencial inmunogenicidad. La mayor afinidad de esta insulina por el receptor IGF-1 también generó precauciones iniciales con respecto a su influencia en la progresión de la retinopatía diabética, sin embargo no existen datos que haga pensar que esta insulina se asocie a un mayor riesgo28.
Los datos más relevantes de este análogo se relacionan con su experiencia clínica. Los ensayos clínicos que han comparado la insulina glargina administrada a la hora de acostarse con la insulina NPH administrada tanto una como dos veces al día han demostrado que la insulina glargina produce valores de glucemias en ayunas menores y menos episodios hipoglucémicos que en los pacientes tratados con insulina NPH29. La disminución del número de hipoglucemias es una constante en los estudios realizados en diabéticos tipos 1 y 2, sobre todo los episodios hipoglucémicos nocturnos son menos frecuentes en comparación con NPH30–34.
Insulina detemirEsta molécula es un análogo de insulina de acción prolongada obtenido mediante la adición de un ácido graso de 14 carbonos (ácido mirístico) en posición B29, además se elimina el aminoácido treonina en la posición 30. Esto permite que la molécula se una en forma reversible a la albúmina; de este modo la insulina detemir circulante está unida a albúmina en más del 98% y solo su fracción libre puede unirse a los receptores de insulina de las células diana, un mecanismo que permite prolongar la duración de su acción. Por tanto, es una molécula que, como la glarglina, no presenta un pico máximo de acción y se puede aplicar de forma única matinal o al acostarse. Como diferencias frente a la insulina NPH y la glarglina, produce menor ganancia de peso que la insulina NPH y posee menor poder mitogénico por ser menos potente en su capacidad de unión al receptor IGF-1, en torno a un 16% de la insulina humana13.
La duración de la máxima de la insulina detemir es de 24h, con un perfil más plano que la insulina NPH y con una menor variabilidad de la absorción35. La respuesta farmacodinámica es proporcional a la dosis (efecto máximo, duración de acción y efecto total).
Los efectos clínicos35–37 muestran cómo con insulina detemir se obtiene el control glucémico, se reduce el riesgo de hipoglucemias sin aumentar significativamente el peso y permite una mayor flexibilidad a la hora de su administración, al compararla con la insulina NPH. A diferencia de lo que sucede con la insulina glarglina, en niños menores de 6 años sí ha sido evaluada positivamente la eficacia y seguridad de insulina detemir38,39. Esta insulina puede interactuar con otros fármacos y modificar su respuesta metabólica (tabla 4).
Insulina detemir: interacción con otros fármacos
| • Aumenta el efecto hipoglucemianteAntidiabéticos orales, inhibidores de la monoaminooxidasa, betabloqueantes no selectivos, inhibidores de la enzima conversora de angiotensina, salicilatos y alcohol |
| • Reducen el efecto hipoglucemianteTiacidas, glucocorticoides, hormonas tiroideas, betasimpaticomiméticos, hormona del crecimiento, octreótido y danazol |
Existe un amplio debate con respecto al riesgo de cáncer y el uso de insulina en los pacientes con diabetes mellitus tipo 2. Debemos tener en cuenta que tanto la obesidad como la diabetes son 2 factores de riesgo para el desarrollo de cáncer. La insulina puede incrementar potencialmente el riesgo de cáncer a través de sus efectos anabólicos y promotores del crecimiento mediados a través de la unión al receptor IGF40,41. Los análogos existentes en la actualidad presentan una afinidad por el receptor de IGF-1 que oscila desde el 16 hasta el 641% comparado con la insulina humana, dependiendo de la línea celular estudiada y del tipo de análogo42–44, así como de la velocidad de disociación de la insulina del receptor.
Una serie de estudios epidemiológicos han tratado de investigar los efectos del uso de insulina en el riesgo de cáncer45–51. Estos estudios han generado resultados variables. El estudio con mayor número de pacientes (n=127.031), un estudio de cohorte retrospectivo, después de ajustar los resultados por la dosis de insulina, detectó un aumento en el riesgo de cáncer dependiente de la dosis con la insulina glarglina en comparación con la insulina humana45; en este estudio, el riesgo de cáncer también aumentaba con el incremento de la duración de la exposición a insulina glargina. Otro estudio de cohorte en el que se incluyeron 114.841 pacientes encontró un mayor riesgo de cáncer de mama con insulina glargina en comparación con los otros tipos de insulina estudiados46. Currie et al.50, en otro estudio de cohorte retrospectivo en 62.809 pacientes, también demostraron una asociación entre el uso de insulina y el riesgo de cáncer en relación con los pacientes que recibieron tratamiento antidiabético oral, sin riesgo adicional atribuible de la insulina glargina sobre otros preparados de insulina. Por último, también en un estudio de cohorte retrospectivo con 12.842 pacientes seguidos durante 4 años, también se encontró una asociación entre el uso de la insulina glargina y el riesgo de cáncer en comparación con los pacientes que utilizaban otras insulinas, aunque los autores señalan que estos resultados podían deberse a un sesgo de selección47. Estos estudios epidemiológicos, sin embargo, están sujetos a una serie de debilidades inherentes al diseño del estudio. La principal limitación es la incapacidad para controlar factores de confusión importante como son el peso, la duración de la diabetes y el tabaquismo. En la actualidad no se ha detectado que exista evidencia de mayor riesgo de cáncer en un extenso estudio diseñado para investigar los efectos de la NPH y la insulina glargina sobre el desarrollo de la retinopatía48 o en un análisis combinado de 31 ensayos con insulina glargina49. Sin embargo, dado que este último análisis post hoc se basa en ensayos con una duración limitada, que no fueron diseñados específicamente para investigar el potencial mitogénico, estos resultados deben interpretarse con precaución. Las recientemente publicadas guías de consenso de la American Diabetes Association (ADA) y la American Cancer Society (ACS) concluyen que las evidencias acerca de que los fármacos específicos para la diabetes afecten al riesgo de cáncer es limitada, y que las indicaciones primordiales de diabetes, en lugar de supuestos problemas con el cáncer, deben seguir siendo los criterios para seleccionar la terapia más adecuada, debiendo ser el médico extremadamente cuidadoso en los pacientes de riesgo50,51.
Uso en gestaciónComo hemos comentado a lo largo del artículo, excepto la insulina aspártica, el resto de análogos de insulina no tienen aprobada su utilización en mujeres gestantes. A este respecto es interesante el metanálisis de Singh et al.52, que analizó 68 ensayos clínicos aleatorios con el objetivo de comparar la eficacia de los análogos de insulina de acción rápida y de larga duración con la de la insulina convencional en el tratamiento, tanto de las diabetes mellitus tipos 1 y 2 como de la gestacional. A modo de resumen, se puede indicar que el uso de análogos de insulina de acción prolongada en la diabetes gestacional es muy reciente, y hasta la fecha los estudios son de corta duración. Teniendo en cuenta los estudios analizados, en términos de HbA1c y de incidencia de hipoglucemia, los autores concluyen que los análogos de insulina de acción rápida y de acción prolongada ofrecen pocos beneficios en relación con insulinas convencionales, excepto la insulina aspártica que ha demostrado claramente sus beneficios y seguridad en este tipo de pacientes16.
ConclusionesEn resumen, los análogos de insulina, tanto rápidos como basales, han aportado algunos beneficios sobre la insulina regular y NPH que veníamos utilizando. Estos beneficios van desde posologías de inyección preprandial, e incluso posprandial, más cómodas y versátiles en los análogos de insulina rápida. También existe una clara disminución del riesgo de hipoglucemias nocturnas con los análogos de insulina basal, incluso la ganancia de peso al insulinizar con detemir es menor que con otras insulinas. No obstante, existen áreas donde debemos profundizar nuestro conocimiento sobre el uso de estas moléculas como son las mujeres con diabetes mellitus en periodo de gestación y la diabetes gestacional. Así mismo, la diferente afinidad por el receptor de IGF-1 de este grupo de moléculas, debe hacernos pensar en esta familia de moléculas no como un grupo homogéneo, debiendo estar atentos a futuros hallazgos en relación con la seguridad de alguno de los análogos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.