En las fases avanzadas de la demencia, los objetivos deberían ser el confort, el adecuado control de los síntomas y evitar el sufrimiento inducido por los procedimientos fútiles, intrusivos o desproporcionados que no benefician al paciente.
La vía subcutánea constituye una herramienta útil en la asistencia a estos pacientes, lo que permite la administración de líquidos y de un gran número de fármacos necesarios para conseguir estos objetivos.
Su buena tolerancia y la gran facilidad de manejo hacen que pueda utilizarse sin problemas fuera del hospital, lo que permite mantener al paciente en su entorno habitual limitando los riesgos derivados de la hospitalización.
Aunque un gran número de fármacos utilizados en este contexto no tienen especificada en su ficha técnica la posibilidad de administración subcutánea, existe una creciente evidencia derivada de su uso y de publicaciones médicas que es recogida en diferentes guías de práctica clínica en cuidados paliativos. Las nuevas regulaciones simplifican la implementación de estos estándares de práctica clínica.
In advanced dementia, the therapeutic goals should be patient comfort, adequate symptom control, and the prevention of suffering due to futile, intrusive or disproportionate procedures. To attain these goals, the subcutaneous route is a useful tool, since it allows fluid administration and the delivery of many drugs. Because it is well tolerated and easy to apply, this route can be safely used in non-hospital settings, allowing patients to stay in their environment and avoiding the risks resulting from hospitalization. Although subcutaneous administration is outside the approved label of many drugs, clinical experience and the medical literature have produced sound evidence that has been incorporated into a number of practice guidelines in palliative care. The recent regulations simplify the implementation of these standars of clinical practice.
Los pacientes con demencia en la fase avanzada de la enfermedad presentan, además del deterioro cognitivo y funcional severos que la definen, alteraciones de conducta y múltiples problemas médicos que, con frecuencia, coexisten y son causa de sufrimiento, generalmente infravalorado1,2. Al igual que otros pacientes en situación de final de vida, estos pacientes, uno de los grupos más vulnerables de la sociedad, necesitan y merecen ser tratados con respeto y asegurar que sus derechos y dignidad sean respetados en todos los estadios de la enfermedad, incluida la etapa terminal. Las personas con demencia próximas al final de su vida deberían tener derecho a recibir los cuidados necesarios que garanticen el adecuado control de síntomas y el alivio del sufrimiento, independientemente del nivel en el que se realice la asistencia sanitaria3. La vía subcutánea permite la administración de fármacos y de líquidos con una excelente tolerancia, facilidad y mínimos riesgos, en situaciones donde otras vías se muestran ineficaces, son imposibles o se consideran desproporcionadas, lo que la constituye como una alternativa eficaz4. Este hecho es más evidente en los pacientes con demencia avanzada, donde frecuentemente se plantean situaciones agudas, derivadas de problemas intercurrentes que imposibilitan o dificultan la utilización de la vía oral5.
HipodermoclisisLos pacientes con demencia avanzada, además de cambios en los mecanismos reguladores de la sed y de la función renal asociados con el envejecimiento, de la posible coexistencia de comorbilidades o fármacos que puedan contribuir a la deshidratación, presentan alteraciones en la deglución y el lenguaje que dificultan la ingestión de líquidos y limitan su capacidad de demanda. Además, al ser dependientes, necesitan de terceras personas para su adecuada hidratación. Todo ello los convierte en un grupo especialmente vulnerable para el desarrollo de deshidratación, sobre todo en situaciones donde la demanda de líquidos necesita ser incrementada6.
La administración de líquidos por vía subcutánea o hipodermoclisis, durante años en el olvido por problemas derivados de un uso inadecuado, es redescubierta en la década de 1980 como alternativa a la hidratación intravenosa, especialmente en el ámbito de los cuidados paliativos y la geriatría7.
Varios trabajos han mostrado la eficacia de esta vía de administración para la absorción de diferentes soluciones en los ancianos8–11. Existen tres revisiones sistemáticas que han mostrado la utilidad de la hipodermoclisis en el tratamiento de la deshidratación leve a moderada en el anciano. Estas revisiones, además de varios estudios de cohortes, incluyen cuatro ensayos controlados randomizados que la comparan con la hidratación intravenosa. La evidencia indica que es, al menos, tan segura y eficaz como la hidratación intravenosa en el tratamiento de la deshidratación leve a moderada del anciano, pero con un menor coste, mayor confort para el paciente y una necesidad de tiempo menor para su colocación y mantenimiento, lo que facilita su utilización ambulatoria12–14.
En uno de estos ensayos, O’Keeffe et al compararon el uso de hipodermoclisis frente a la hidratación intravenosa en 60 ancianos con deterioro cognitivo y una edad media de 80 años que precisaron hidratación parenteral durante al menos 48h. No hubo diferencias en la cantidad de volumen administrado en ambos grupos. A las 48h no se objetivaron diferencias en las cifras de urea y creatinina, mostrando una eficacia de hidratación similar. Sin embargo, los pacientes que recibieron hipodermoclisis tuvieron menos agitación (p<0,005) y los costes fueron significativamente inferiores15.
En otro estudio retrospectivo de Hussain et al en una cohorte de 36 ancianos institucionalizados con una edad media de 85 años, de los que el 86% tenía deterioro cognitivo significativo y en los que la indicación de hipodermoclisis generalmente estuvo relacionada con la presencia de un cuadro infeccioso, ésta se asoció con un retorno a la situación funcional en el 71% de los casos. La hipodermoclisis tuvo una excelente tolerancia y se tradujo en una reducción en los traslados hospitalarios y los costes derivados16.
Además de su utilidad en el tratamiento de la deshidratación leve a moderada y en su prevención en situaciones de demanda incrementada de líquidos, algunos autores han sugerido la utilidad de la vía subcutánea en la prevención, no en el tratamiento, de la malnutrición o su agravamiento a corto plazo en situaciones de estrés, mediante la administración de soluciones de aminoácidos10.
La hipodermoclisis tiene limitaciones que vienen determinadas por el volumen, la velocidad de perfusión y el tipo de soluciones en que pueden administrarse. Se pueden administrar diariamente hasta 1.500ml por sitio de perfusión, con un máximo de 3.000ml a través de dos sitios. Las soluciones que se han empleado con seguridad incluyen el suero salino al 0,9 y al 0,45%, el suero glucosalino isotónico y, aunque se ha referido en el pasado el riesgo de administrar soluciones libres de electrolitos, la administración de suero glucosado al 5% también es considerada segura siempre que no se superen los 2.000ml diarios y/o un ritmo de perfusión de 2ml/h7,12,14. Se ha administrado potasio en concentraciones no superiores a 35mmol/l con buena tolerancia local17.
El problema secundario más frecuente derivado del uso de hipodermoclisis es el desarrollo de edema local que condiciona el cambio de lugar de perfusión. Las reacciones locales suelen ser leves y menos frecuentes que las asociadas con la vía intravenosa. El riesgo de hipervolemia y de cambios en la concentración de electrolitos séricos, habitualmente son menores que con la administración intravenosa de líquidos14,18.
Es importante añadir que la indicación de hipodermoclisis, como otras formas de hidratación parenteral, debe realizarse considerando los riesgos y los beneficios para cada caso concreto, respetando las voluntades anticipadas si las hubiere y sin olvidar las creencias y expectativas de los familiares de estos pacientes sobre los beneficios de la hidratación en las fases terminales de la enfermedad19.
Administración de fármacos por vía subcutáneaClásicamente empleada para la administración de insulina y vacunas, en la década de 1970, Russell en Reino Unido comenzó a utilizarla para la administración de morfina en el tratamiento del dolor en los pacientes con cáncer terminal20. Desde entonces, el interés suscitado por esta vía para la atención a los pacientes en el final de la vida y el número de fármacos administrados a través de ella, ha ido incrementándose de forma progresiva en los últimos años.
Los pacientes con demencia avanzada, generalmente con grandes limitaciones de movilidad y disfagia, sufren problemas como incontinencia, malnutrición, deshidratación, episodios repetidos de broncoaspiración, neumonías aspirativas y otras infecciones recurrentes, así como úlceras por presión. Estos y otros problemas médicos que surgen en estas fases de la demencia, determinan que puedan experimentar síntomas como dolor, disnea, aumento de secreciones respiratorias, fiebre, confusión, agitación y otras alteraciones de conducta, entre otros, que se traducen en altos niveles de sufrimiento2. No debe obviarse que su incapacidad de expresión verbal no es sinónimo de incapacidad de sufrir y experimentar disconfort21. Las frecuentes limitaciones que exhiben, especialmente en situaciones agudas, para la vía oral limitan las posibilidades de tratamiento5.
Cuando la vía oral no es posible o no permite un adecuado tratamiento y control sintomático, la alternativa que dispone de más recursos farmacológicos y es mejor tolerada por el paciente es la vía subcutánea. Las características de esta vía permiten, además, la posibilidad de asistencia al paciente en su domicilio. La vía intravenosa es técnicamente más complicada, se asocia con mayor necesidad de restricción física y generalmente condiciona el ingreso hospitalario. La vía intramuscular necesita múltiples inyecciones y es dolorosa e incómoda. Las vías rectal y transdérmica pueden ser una opción fácil y cómoda, pero tienen una gran limitación en la disponibilidad de fármacos, restringida a la administración de algunos fármacos analgésicos-antipiréticos por vía rectal, y a la administración de opioides por vía transdérmica22,23.
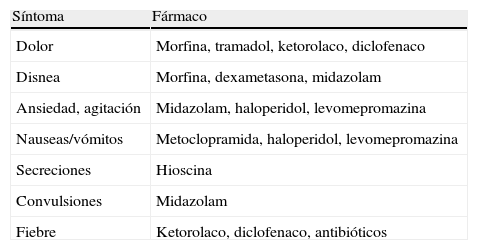
Fármacos para el control de síntomasExiste actualmente una larga lista de fármacos que han sido utilizados en este contexto de final de la vida para su administración por vía subcutánea y que incluyen diferentes opioides, sedantes, antieméticos, anticolinérgicos, antiinflamatorios no esteroideos, diuréticos, protectores gástricos y otros4,24. No es objeto de este artículo hacer una exhaustiva revisión de todos ellos, sino destacar aquéllos más frecuentemente utilizados y que pueden tener especial relevancia en el tratamiento de los problemas surgidos en las fases avanzadas de la demencia (tabla 1).
Síntomas frecuentes en el final de la vida y fármacos útiles para su control
| Síntoma | Fármaco |
| Dolor | Morfina, tramadol, ketorolaco, diclofenaco |
| Disnea | Morfina, dexametasona, midazolam |
| Ansiedad, agitación | Midazolam, haloperidol, levomepromazina |
| Nauseas/vómitos | Metoclopramida, haloperidol, levomepromazina |
| Secreciones | Hioscina |
| Convulsiones | Midazolam |
| Fiebre | Ketorolaco, diclofenaco, antibióticos |
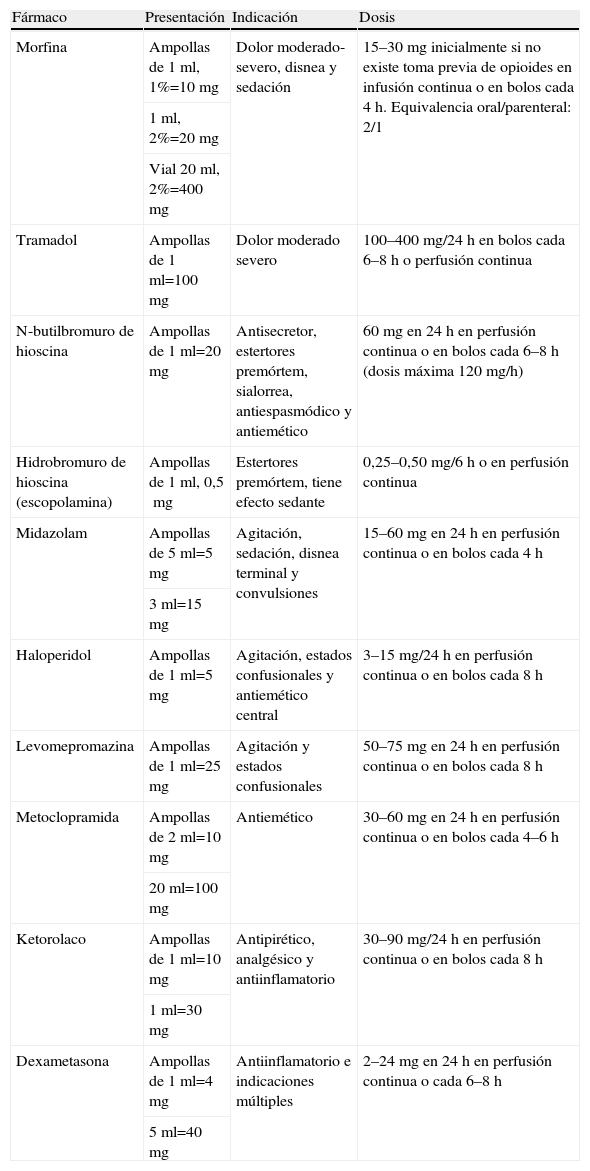
La experiencia en la administración de fármacos por vía subcutánea deriva de su uso, mayoritariamente, en el tratamiento del paciente oncológico terminal y su utilización está recomendada en diferentes publicaciones, libros y guías de práctica clínica en cuidados paliativos en la atención al paciente terminal (tabla 2).
Fármacos más frecuentemente empleados para el control sintomático del paciente en el final de la vida
| Fármaco | Presentación | Indicación | Dosis |
| Morfina | Ampollas de 1ml, 1%=10mg | Dolor moderado-severo, disnea y sedación | 15–30mg inicialmente si no existe toma previa de opioides en infusión continua o en bolos cada 4h. Equivalencia oral/parenteral: 2/1 |
| 1ml, 2%=20mg | |||
| Vial 20ml, 2%=400mg | |||
| Tramadol | Ampollas de 1ml=100mg | Dolor moderado severo | 100–400mg/24h en bolos cada 6–8h o perfusión continua |
| N-butilbromuro de hioscina | Ampollas de 1ml=20mg | Antisecretor, estertores premórtem, sialorrea, antiespasmódico y antiemético | 60mg en 24h en perfusión continua o en bolos cada 6–8h (dosis máxima 120mg/h) |
| Hidrobromuro de hioscina (escopolamina) | Ampollas de 1ml, 0,5mg | Estertores premórtem, tiene efecto sedante | 0,25–0,50mg/6h o en perfusión continua |
| Midazolam | Ampollas de 5ml=5mg | Agitación, sedación, disnea terminal y convulsiones | 15–60mg en 24h en perfusión continua o en bolos cada 4h |
| 3ml=15mg | |||
| Haloperidol | Ampollas de 1ml=5mg | Agitación, estados confusionales y antiemético central | 3–15mg/24h en perfusión continua o en bolos cada 8h |
| Levomepromazina | Ampollas de 1ml=25mg | Agitación y estados confusionales | 50–75mg en 24h en perfusión continua o en bolos cada 8h |
| Metoclopramida | Ampollas de 2ml=10mg | Antiemético | 30–60mg en 24h en perfusión continua o en bolos cada 4–6h |
| 20ml=100mg | |||
| Ketorolaco | Ampollas de 1ml=10mg | Antipirético, analgésico y antiinflamatorio | 30–90mg/24h en perfusión continua o en bolos cada 8h |
| 1ml=30mg | |||
| Dexametasona | Ampollas de 1ml=4mg | Antiinflamatorio e indicaciones múltiples | 2–24mg en 24h en perfusión continua o cada 6–8h |
| 5ml=40mg |
La morfina por vía subcutánea ha mostrado su eficacia en el tratamiento del dolor moderado a severo25. Además de su utilización como analgésico, la morfina está indicada en la sedación y en el tratamiento de la disnea en el paciente terminal26–31. La eficacia en el tratamiento de la disnea ha sido refrendada en una revisión Cochrane, aunque el mecanismo por el cual la alivia no se conoce con exactitud. Es posible que la morfina reduzca los efectos del dióxido de carbono y el oxígeno sobre la ventilación. Algunos estudios han mostrado en sujetos sanos que la morfina disminuye el consumo de oxígeno en reposo y durante el ejercicio, aunque otros no lo han confirmado32. A pesar de los temores suscitados por su capacidad de producir depresión respiratoria, Bruera et al han mostrado que la morfina mejora la disnea sin causar un deterioro significativo de la función pulmonar en los pacientes oncológicos terminales33 y Good et al han evidenciado que su uso no necesariamente se asocia con una disminución de la supervivencia34.
Tanto el N-butilbromuro de hioscina como el hidrobromuro de hioscina son eficaces en el tratamiento de las secreciones respiratorias y estertores premórtem35. La escopolamina (hidrobromuro de hioscina), además, al atravesar la barrera hematoencefálica, tiene un efecto sedante que puede resultar deseable en determinadas situaciones26–31.
Dos neurolépticos, el haloperidol y la levomepromazina, pueden administrarse por vía subcutánea y son de utilidad en los pacientes agitados y en los estados confusionales. Ambos, al igual que la metoclopramida, tienen un efecto antiemético. El haloperidol se ha mostrado eficaz, también, en el tratamiento de los vómitos inducidos por opioides y en los secundarios a alteraciones metabólicas26–31,36.
El midazolam, debido a su hidrosolubilidad y excelente biodisponibilidad, es la benzodiacepina de elección para su administración por vía subcutánea37. Su administración es útil, además de como anticonvulsivante, en estados de gran ansiedad y agitación y en la disnea que no responde a otros tratamientos26–31.
El ketorolaco, también el diclofenaco, además de su actividad analgésica antiinflamatoria, se utiliza por vía subcutánea en el tratamiento sintomático de la fiebre26–31.
La dexametasona tiene múltiples indicaciones en los cuidados paliativos. Su utilidad viene derivada de su potente actividad antiinflamatoria. Los corticoides están indicados en el tratamiento de la disnea secundaria al asma, a la enfermedad pulmonar obstructiva crónica o a otras circunstancias que causan broncoespasmo26–31. Aunque no se ha demostrado la utilidad de los corticoides en el tratamiento de la aspiración pulmonar38, el broncoespasmo y la disnea secundaria que frecuentemente condicionan puede hacerles, junto a otras medidas, útiles en el control sintomático de la disnea en estas circunstancias.
La administración de fármacos por vía subcutánea puede realizarse en perfusión continua o de forma intermitente, en bolos. La administración en bolos es más sencilla, tiene un coste menor y es más útil en situaciones de necesidad de control sintomático rápido. Sin embargo, necesita un mayor número de manipulaciones locales, está limitada a pequeños volúmenes, generalmente menos de 3ml, tiene efecto pico-valle con niveles altos iniciales que incrementan el riesgo de efectos adversos y niveles bajos al final del efecto de la dosis que pueden determinar un mal control sintomático. La perfusión subcutánea continua permite administrar volúmenes totales mayores, mantiene concentraciones plasmáticas uniformes, evita manipulaciones y presenta mayor comodidad para el paciente y para el equipo sanitario. En el lado negativo está su coste más elevado al requerir dispositivos y sistemas para la perfusión. Estos dispositivos, sin embargo, bien sean electrónicos, mecánicos o elastoméricos permiten la administración simultánea de varios fármacos, lo que posibilita el control de varios síntomas22,31.
Compatibilidad y estabilidad de mezclas de fármacosLa combinación de fármacos para su administración simultánea exige que éstos sean compatibles y permanezcan estables en la mezcla. Negro et al analizaron la compatibilidad física de una mezcla de dosis fijas de fármacos que incluían un opioide (morfina hidrocloruro o tramadol), haloperidol lactato, N-butilbromuro de hioscina, midazolam hidrocloruro, dexametasona fosfato sódico y metoclopramida hidrocloruro. Realizaron mezclas de 2, 3, 4 y 5 fármacos y evaluaron su eficacia y tolerancia. Hubo 52 mezclas compatibles. Solamente aquellas que contenían dexametasona-haloperidol y dexametasona-midazolam se mostraron incompatibles (desarrollo de precipitación o turbideces). De todas las combinaciones que resultaron compatibles, 18 fueron administradas a los pacientes con cáncer en cuidados paliativos consiguiendo un buen control sintomático. La combinación más utilizada fue la que incluía morfina, midazolam, haloperidol y hioscina39.
En este trabajo se evaluaba solamente la compatibilidad física de las distintas combinaciones de fármacos. Sin embargo, es posible no detectar problemas físicos de compatibilidad y, a pesar de ello, que exista degradación de alguno de sus componentes, esto es, que existan problemas de estabilidad química y, por tanto, pérdida de eficacia. Una mezcla de fármacos se considera químicamente estable si la degradación de cualquiera de sus componentes es inferior al 10%40.
Existen cada vez más publicaciones que evalúan, además de la compatibilidad física, la estabilidad química de diferentes combinaciones de fármacos para uso subcutáneo mediante técnicas de cromatografía líquida de alto rendimiento. Así, la combinación de la morfina hidrocloruro y el N-butilbromuro de hioscina en diferentes concentraciones, en condiciones de temperatura variable y protegidos de la luz, es compatible y permanece químicamente estable a lo largo de 15 días41. Igualmente se ha demostrado la compatibilidad y la estabilidad de la combinación de la morfina con el hidrobromuro de hioscina, la dexametasona o la metoclopramida en condiciones variables de temperatura durante 7 días40. También, las mezclas del tramadol con el haloperidol o con el N-butilbromuro de hioscina son compatibles y permanecen estables durante 15 días a diferentes temperaturas42,43. Asimismo, la combinación del tramadol y la dexametasona permanece estable durante 5 días a 25°C14. De igual manera, la combinación de la morfina, el haloperidol y el butilbromuro de hioscina es físicamente compatible y químicamente estable durante 15 días a 25°C.45
Es importante recordar que la compatibilidad y la estabilidad de una mezcla viene determinada no solo por los fármacos que la componen, sino también por otros factores que son determinantes. Así, la concentración, la proporción, el orden en que se realiza la combinación, el tipo de diluyente empleado, el pH, las condiciones ambientales de luz, la temperatura y el tiempo transcurrido tras la mezcla, entre otros, condicionan la compatibilidad y la estabilidad química de la combinación farmacológica40–45.
Por tanto, se recomienda utilizar la combinación del menor número de fármacos posible. Combinaciones de más de tres fármacos tienen más riesgo de incompatibilidad y de inestabilidad. En general, se recomienda no mezclar la dexametasona ni el ketorolaco con otros fármacos. Se debe revisar periódicamente la mezcla para identificar precipitaciones, turbideces o pérdidas de volumen y monitorizar frecuentemente al paciente para evaluar la existencia de pérdida de eficacia o de reacciones indeseables30,31.
AntibióticosLa presencia de aspiraciones repetidas, el deterioro inmunitario condicionado por la propia demencia y la frecuente malnutrición, la inmovilidad, la incontinencia esfinteriana y otros factores hacen que, en esta fase final de la demencia, el desarrollo de fiebre e infecciones constituyan un problema frecuente y la utilización de antibióticos constituya un hecho cómun46,47.
Varios antibióticos han sido utilizados por vía subcutánea: ceftriaxona, cefepima, ampicilina, amikacina, gentamicina, tobramicina y teicoplanina4,24,48. De todos ellos, la ceftriaxona es la más evaluada. Varios autores han propuesto su administración por esta vía en el manejo de la neumonía y otras infecciones en los pacientes ancianos, especialmente aquéllos con enfermedad avanzada, demencias, agitación, coagulopatías o con imposibilidad de utilización de vías alternativas49–51. Estudios de farmacocinética muestran que la ceftriaxona consigue unos niveles plasmáticos similares a los obtenidos tras su administración intravenosa, con una biodisponibilidad próxima al 100%, aunque con un pico plasmático más tardío y sin diferencias significativas en los parámetros farmacocinéticos evaluados, como la semivida de eliminación, el volumen de distribución y el área bajo la curva52,53. La tolerancia local tras la inyección de dosis de 0,5 o 1 g de ceftriaxona es buena (la administración de dosis de 2 g conlleva un mayor riesgo de necrosis cutánea)54.
No existen guías que orienten sobre el manejo de las infecciones en pacientes terminales. Todavía más difícil resulta esta decisión en pacientes con demencia, en los que no existe una frontera clara que delimite la certeza de una muerte próxima y las posibilidades de prolongación de la vida, y donde las decisiones deben ser tomadas por terceros, generalmente la familia, que con un paternalismo bien intencionado no siempre satisfacen los mejores intereses del paciente.
Kruse et al han mostrado que la mortalidad a los tres meses tras un episodio de infección del tracto respiratorio inferior, se relacionaba mejor con la severidad de la demencia que con la agresividad del tratamiento antibiótico55. Otros autores han objetivado que un manejo intensivo de la fiebre y las infecciones no prolonga la supervivencia en aquellos pacientes con demencia en fases muy avanzadas que permanecen mutistas y encamados56,57.
Sin embargo, es necesario recordar que además de su intención terapéutica curativa fundamental, el uso de antibióticos en los pacientes en situación de final de la vida puede tener una utilidad paliativa. Algunos autores han mostrado que los antibióticos mejorarían los síntomas derivados de las infecciones urinarias en pacientes que reciben cuidados paliativos por cáncer terminal58. Recientemente, Van der Steen et al han mostrado que los antibióticos pueden tener utilidad en el control sintomático en los pacientes con demencia que sufren neumonía59. Es importante no olvidar que la neumonía es causa de gran sufrimiento en el paciente con demencia y que, independientemente del uso de antibióticos, es necesario un adecuado tratamiento sintomático60.
Indicación de uso por vía subcutánea: hacia una progresiva normalizaciónAunque en algún país de nuestro entorno algunos antibióticos (ceftriaxona) especifican la posibilidad de administración por vía subcutánea24, en España ninguno de ellos tiene aprobado su uso por esta vía. Asimismo, de la lista de 10 fármacos que figuran en la tabla 2 y que constituyen aquéllos más frecuentemente empleados en la atención a los pacientes en el final de la vida, solamente el cloruro mórfico, el tramadol, el N-butilbromuro de hioscina y el hidrobromuro de hioscina tienen aprobada y especificada en su ficha técnica esta posibilidad de administración. Igualmente, sólo el suero salino fisiológico tiene especificada esta posibilidad de administración61.
Además, existe una asimetría de disponibilidad de fármacos para su uso por esta vía en los diferentes países de la Unión Europea. Si se revisan aquellos fármacos frecuentemente utilizados en el entorno de los cuidados paliativos, únicamente la morfina tiene aprobada esta vía de forma universal24.
Esta falta de indicación probablemente venga condicionada porque el desarrollo de muchos de estos fármacos fue previo a la generalización del uso de la vía subcutánea y no fue testada en el proceso de licencia. Sin embargo, su uso está refrendado en diferentes libros y guías de práctica clínica en cuidados paliativos, en un mayor número de publicaciones biomédicas y en una creciente experiencia de uso, no necesariamente comunicada.
Es obligatorio recordar que en España la utilización de un medicamento para indicaciones o en condiciones de uso distintas a las aprobadas y que aparecen reflejadas en la ficha técnica del medicamento estaba regulada por el Real Decreto 223/2004 que hace referencia a los ensayos de medicamentos y por la Ley 29/2006 de Garantías y Uso Racional de los Medicamentos que determinan su uso solamente dentro de un ensayo clínico o como uso compasivo. Evidentemente, los trámites necesarios no eran los más eficaces y satisfactorios para determinadas situaciones de la práctica clínica como así sucede en la atención a los pacientes terminales30.
Existe un interés creciente de las organizaciones sanitarias en el desarrollo de programas de atención a los pacientes en el final de la vida62. Por tanto, había necesidad de un esfuerzo de estandarización y normalización en el uso de la vía subcutánea. En este sentido, como desarrollo de la Ley de Garantías y Uso Racional de los Medicamentos, recientemente, ha sido publicado el Real Decreto 1015/2009, de 19 de junio, por el que se regula la disponibilidad de medicamentos en situaciones especiales. En ella se diferencian claramente los requisitos para el uso compasivo (utilización de medicamentos en fase de investigación clínica en pacientes que no forman parte de un ensayo clínico) de las condiciones necesarias para la prescripción de medicamentos autorizados cuando se utilicen en condiciones distintas de las incluidas en la ficha técnica autorizada. Para estos últimos se elimina la necesidad de autorización previa individual en cada caso por parte de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) y se refuerza la responsabilidad de los centros sanitarios, la información a los pacientes, y la vigilancia de su uso. La AEMPS podrá emitir recomendaciones, que deberán considerarse en los protocolos elaborados por los centros sanitarios. Para aquellos medicamentos que estén comercializados en otros países y que su utilización sea necesaria, la norma también actualiza el procedimiento63.
ConclusiónLa vía subcutánea constituye una alternativa de administración útil en el paciente con demencia avanzada. Esta vía ha demostrado su eficiencia en la perfusión de líquidos para la prevención y tratamiento de la deshidratación leve a moderada y constituye una opción cómoda y eficaz para la administración de determinados fármacos necesarios en estas fases de la demencia próximas al final de la vida. Dado que muchos de ellos no tienen aprobada esta vía de administración era necesario un esfuerzo de adaptación entre las guías de práctica clínica y las regulaciones administrativas. En este sentido el nuevo real decreto de acceso a medicamentos en situaciones especiales aporta ventajas, elimina cargas administrativas y facilita la atención a los pacientes en el final de su vida.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.