El infarto agudo de miocardio representa la primera causa de muerte no trasmisible en el mundo. Una de las herramientas que sirven como soporte a las decisiones en su diagnóstico son las redes neuronales, de las cuales se ha demostrado un buen nivel de precisión.
MétodosSe realizó el entrenamiento y la prueba de varias redes neuronales, con diferentes arquitecturas para el diagnóstico del infarto, a partir de los datos de la escala de clasificación de la probabilidad de angina de Braunwald en un grupo de pacientes que ingresaron por dolor torácico al servicio de urgencias del Hospital San José de Bogotá.
ResultadosSe generaron 40 redes que fueron probadas en 5 experimentos de los cuales se obtuvo mayor precisión diagnóstica con el modelo de 5 entradas electrocardiográficas más troponina, aunque el mejor valor predictivo negativo se alcanzó en el modelo con 10 variables clínicas, electrocardiográficas y troponina. Varias de las redes diseñadas tuvieron una sensibilidad y una especificidad del 100%. Se requiere un estudio de validación para comprobar estos hallazgos.
ConclusionesCon los resultados encontrados para las redes neuronales en la literatura y en este estudio se puede considerar el uso de esta estrategia de inteligencia computacional en la práctica.
Myocardial infarction represents the leading cause of death by a noncommunicable disease worldwide; one of the tools that serve as decision support for establishing a diagnosis are neural networks. They have been shown to have a good level of accuracy.
MethodsTraining and testing of several neural networks was performed with different architectures for the diagnosis of the myocardial infarction in a group of patients admitted with chest pain emergency room in the Hospital de San José, Bogotá. This was carried out according to data from the incidence scale of Braunwald's classification of unstable angina.
ResultsForty networks were generated and tested in five experiments obtaining an accurate diagnostic with the electrocardiographic pattern of five entries and troponin. The negative predictive value was 100% in the model with ten clinical variables, electrocardiogram and troponin. Some of the designed networks had a sensitivity and specificity of 100%. A validation study to verify these findings is required.
ConclusionsWith the results found for neural networks in the literature and in the present study, we should consider the practical use of this computational intelligence strategy in daily practice.
El infarto agudo de miocardio (IAM) es una de las condiciones que se manifiestan con dolor torácico y ponen en riesgo la vida; de ahí que su diagnóstico apropiado y oportuno determine la instauración de una serie de medidas que pueden cambiar su historia natural.
Gran parte de los esfuerzos diagnósticos para dolor torácico en el servicio de urgencias se encaminan a esta entidad, teniendo en cuenta que sus síntomas son variables y los pacientes los perciben de maneras muy diferentes1.
Una condición particular en la práctica clínica son los errores en el proceso de atención médica2, motivo por el cual se ha hecho prioritaria la búsqueda de medidas para controlar esta situación. El diagnóstico y el tratamiento de la isquemia coronaria no escapan a ello3,4. Ante este hecho y con la necesidad consiguiente de contar con un mayor sustento del conocimiento en la práctica diaria, junto con el ambiente propiciado por el uso de nuevas tecnologías, se ha intentado dar un estímulo para la generación y la utilización de sistemas de soporte en la toma de decisiones clínicas encaminados a esta condición5. Uno de estos son las redes neuronales.
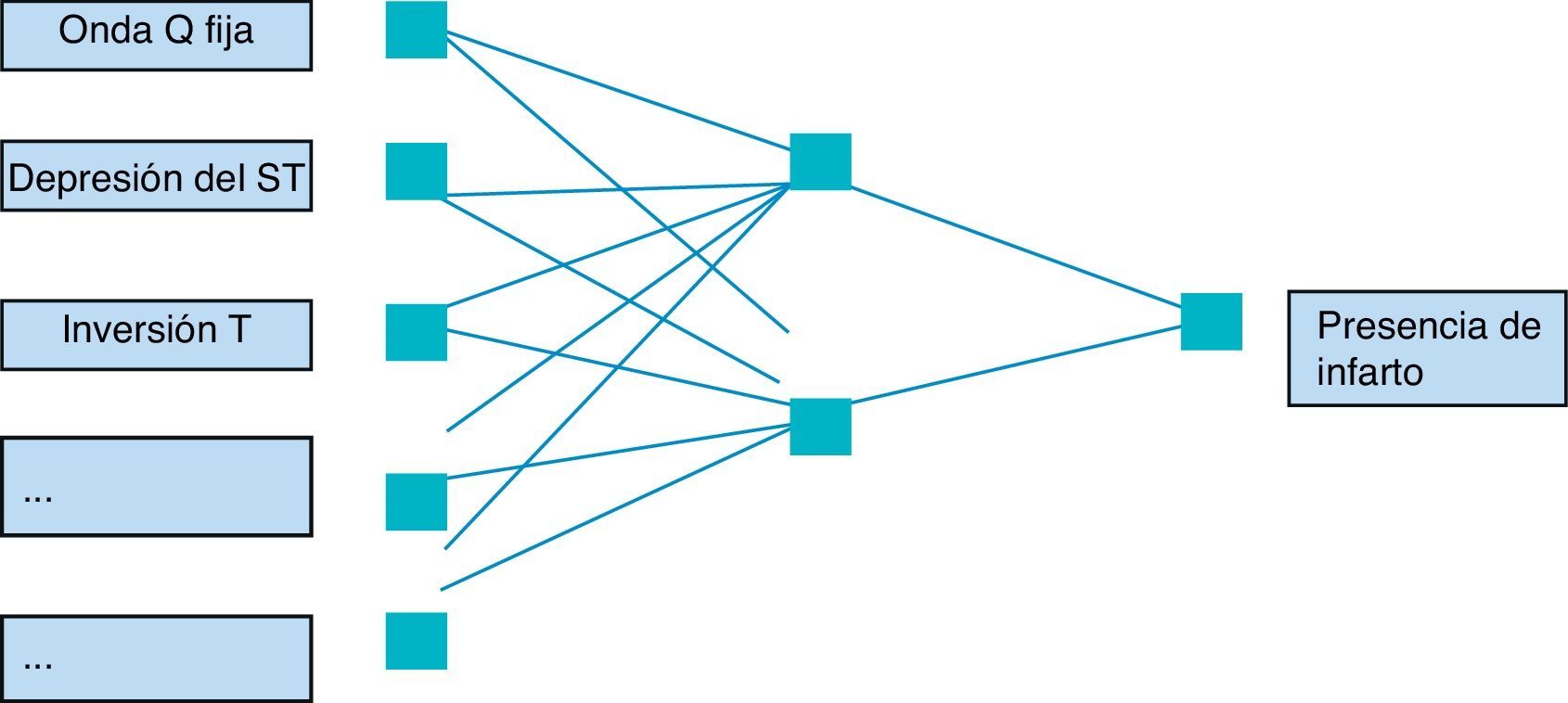
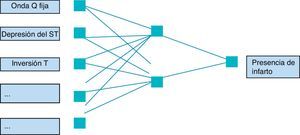
De acuerdo con la Computational Intelligence Society del Institute of Electrical and Electronics Engineers (IEEE), las redes neuronales son paradigmas computacionales basados en modelos matemáticos con capacidad de un fuerte patrón de reconocimiento. Una red neuronal es un algoritmo de cálculo que se basa en una analogía del sistema nervioso6. Se intenta imitar la capacidad de aprendizaje de este, haciendo que reconozca gradualmente patrones de asociación entre las entradas (variables predictivas) y los estados dependientes de ellas (salidas)7,8. La señal progresa desde las entradas, luego por la capa oculta, hasta obtener una respuesta traducida en el nivel de activación de los nodos de salida, los cuales predicen el resultado con base en las variables de entrada7. En la figura 1 se ejemplifica una red neuronal con 5 neuronas de entrada, 2 neuronas en la capa oculta y una neurona de salida, aplicada al diagnóstico del infarto.
De otro lado, se han publicado gran cantidad de estudios que utilizan redes neuronales, con diferentes aproximaciones para apoyar el diagnóstico de los síndromes coronarios agudos9–23. En el artículo que se publica en este número se efectúa una descripción del desempeño de varias redes neuronales en el diagnóstico del IAM, a partir de los datos obtenidos de las 18 variables de la escala de valoración de la probabilidad de angina descrita por Braunwald et al.24 en 1994, aplicada a una población de pacientes que consultaron por dolor torácico al hospital San José de Bogotá.
MetodologíaBase de datosSe tomó la base de datos de una población compuesta por pacientes mayores de 18años que consultaron al servicio de urgencias del Hospital San José por dolor torácico como motivo de consulta principal, entre el 20 febrero y el 30 de octubre de 2012. Esta base de datos hacía parte del estudio «Estructuración e implementación de una ruta crítica para el manejo de pacientes con síndrome coronario agudo en el servicio de urgencias del hospital San José de Bogotá». El muestreo de los casos elegidos de la base de datos se realizó por conveniencia, a partir de aquellos en que se diligenció correctamente la ruta crítica; estuvo compuesta por 159 pacientes, de los cuales 37 tuvieron diagnóstico de IAM.
Descripción de la red neuronalSe usó NEUROSOLUTIONS®, un ambiente de desarrollo de redes neuronales creado por NeuroDimension Inc., el cual se comercializa bajo licencia EULA (End-user license agreement). Se diseñó un grupo de experimentos consistentes en distintas variaciones de la estructura de redes neuronales, que tenían en común una capa oculta, una neurona de salida, la tasa de aprendizaje y el uso de back propagation con momentum (el algoritmo que permite el entrenamiento de la red). Se varió el número de neuronas (variables) de entrada, escogidas a partir de diferentes criterios o heurísticas:
- a)
Cinco neuronas: provenientes de los datos del ECG consignados en la escala de Braunwald.
- b)
Seis neuronas: la anterior más el resultado de la troponina.
- c)
Diez neuronas: las que se presentaban con mayor frecuencia entre quienes se diagnosticó un infarto.
- d)
Dieciocho neuronas: todos los componentes de la escala de Braunwald.
Los otros aspectos que se variaron fueron el número de neuronas en la capa oculta (2, 3, 4, 6 y 10) y el momentum escogido (0,3 y 0,5). Cada una de las redes fue probada en 5 experimentos. De cada uno de ellos se construyó una tabla de 2×2 calculando, a partir de estos resultados, sensibilidad, especificidad, valores predictivos y precisión. Se obtuvieron los promedios y su respectiva desviación estándar para graficar finalmente los resultados obtenidos.
El estudio fue aprobado por el comité de investigaciones y el comité de ética en investigación con seres humanos de la Facultad de Medicina de la Fundación Universitaria Ciencias de la Salud, Hospital San José de Bogotá. No se requirió la obtención de un consentimiento informado.
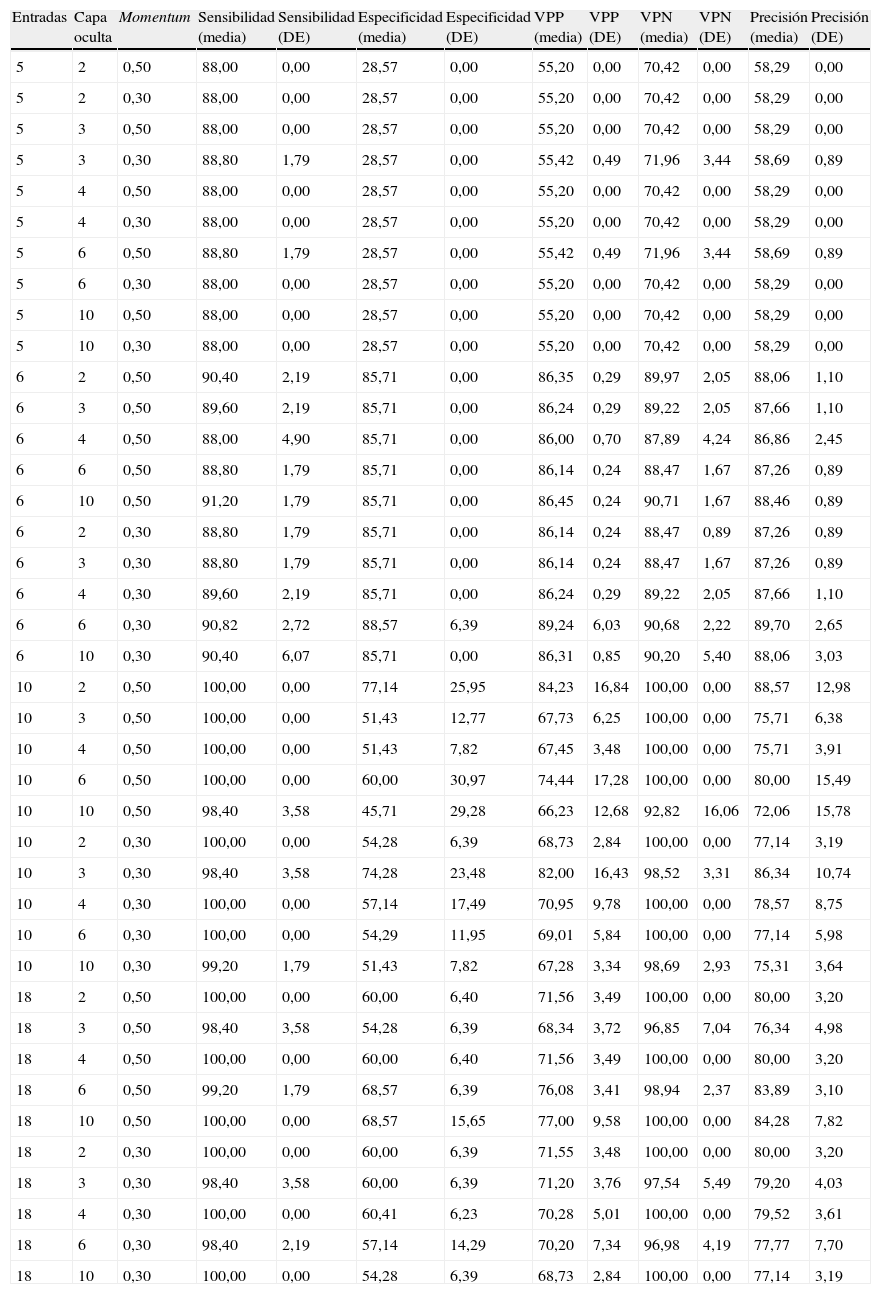
ResultadosSe diseñaron 40 redes neuronales, las cuales fueron entrenadas y probadas, cada una en 5 experimentos. Se obtuvieron los datos de sensibilidad, especificidad, precisión, así como valores predictivos positivo y negativo, los cuales se exponen en la tabla 1 con sus respectivos promedios y desviaciones estándar (DE).
Resultados de los diferentes experimentos de diseño de las redes neuronales
| Entradas | Capa oculta | Momentum | Sensibilidad (media) | Sensibilidad (DE) | Especificidad (media) | Especificidad (DE) | VPP (media) | VPP (DE) | VPN (media) | VPN (DE) | Precisión (media) | Precisión (DE) |
| 5 | 2 | 0,50 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 5 | 2 | 0,30 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 5 | 3 | 0,50 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 5 | 3 | 0,30 | 88,80 | 1,79 | 28,57 | 0,00 | 55,42 | 0,49 | 71,96 | 3,44 | 58,69 | 0,89 |
| 5 | 4 | 0,50 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 5 | 4 | 0,30 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 5 | 6 | 0,50 | 88,80 | 1,79 | 28,57 | 0,00 | 55,42 | 0,49 | 71,96 | 3,44 | 58,69 | 0,89 |
| 5 | 6 | 0,30 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 5 | 10 | 0,50 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 5 | 10 | 0,30 | 88,00 | 0,00 | 28,57 | 0,00 | 55,20 | 0,00 | 70,42 | 0,00 | 58,29 | 0,00 |
| 6 | 2 | 0,50 | 90,40 | 2,19 | 85,71 | 0,00 | 86,35 | 0,29 | 89,97 | 2,05 | 88,06 | 1,10 |
| 6 | 3 | 0,50 | 89,60 | 2,19 | 85,71 | 0,00 | 86,24 | 0,29 | 89,22 | 2,05 | 87,66 | 1,10 |
| 6 | 4 | 0,50 | 88,00 | 4,90 | 85,71 | 0,00 | 86,00 | 0,70 | 87,89 | 4,24 | 86,86 | 2,45 |
| 6 | 6 | 0,50 | 88,80 | 1,79 | 85,71 | 0,00 | 86,14 | 0,24 | 88,47 | 1,67 | 87,26 | 0,89 |
| 6 | 10 | 0,50 | 91,20 | 1,79 | 85,71 | 0,00 | 86,45 | 0,24 | 90,71 | 1,67 | 88,46 | 0,89 |
| 6 | 2 | 0,30 | 88,80 | 1,79 | 85,71 | 0,00 | 86,14 | 0,24 | 88,47 | 0,89 | 87,26 | 0,89 |
| 6 | 3 | 0,30 | 88,80 | 1,79 | 85,71 | 0,00 | 86,14 | 0,24 | 88,47 | 1,67 | 87,26 | 0,89 |
| 6 | 4 | 0,30 | 89,60 | 2,19 | 85,71 | 0,00 | 86,24 | 0,29 | 89,22 | 2,05 | 87,66 | 1,10 |
| 6 | 6 | 0,30 | 90,82 | 2,72 | 88,57 | 6,39 | 89,24 | 6,03 | 90,68 | 2,22 | 89,70 | 2,65 |
| 6 | 10 | 0,30 | 90,40 | 6,07 | 85,71 | 0,00 | 86,31 | 0,85 | 90,20 | 5,40 | 88,06 | 3,03 |
| 10 | 2 | 0,50 | 100,00 | 0,00 | 77,14 | 25,95 | 84,23 | 16,84 | 100,00 | 0,00 | 88,57 | 12,98 |
| 10 | 3 | 0,50 | 100,00 | 0,00 | 51,43 | 12,77 | 67,73 | 6,25 | 100,00 | 0,00 | 75,71 | 6,38 |
| 10 | 4 | 0,50 | 100,00 | 0,00 | 51,43 | 7,82 | 67,45 | 3,48 | 100,00 | 0,00 | 75,71 | 3,91 |
| 10 | 6 | 0,50 | 100,00 | 0,00 | 60,00 | 30,97 | 74,44 | 17,28 | 100,00 | 0,00 | 80,00 | 15,49 |
| 10 | 10 | 0,50 | 98,40 | 3,58 | 45,71 | 29,28 | 66,23 | 12,68 | 92,82 | 16,06 | 72,06 | 15,78 |
| 10 | 2 | 0,30 | 100,00 | 0,00 | 54,28 | 6,39 | 68,73 | 2,84 | 100,00 | 0,00 | 77,14 | 3,19 |
| 10 | 3 | 0,30 | 98,40 | 3,58 | 74,28 | 23,48 | 82,00 | 16,43 | 98,52 | 3,31 | 86,34 | 10,74 |
| 10 | 4 | 0,30 | 100,00 | 0,00 | 57,14 | 17,49 | 70,95 | 9,78 | 100,00 | 0,00 | 78,57 | 8,75 |
| 10 | 6 | 0,30 | 100,00 | 0,00 | 54,29 | 11,95 | 69,01 | 5,84 | 100,00 | 0,00 | 77,14 | 5,98 |
| 10 | 10 | 0,30 | 99,20 | 1,79 | 51,43 | 7,82 | 67,28 | 3,34 | 98,69 | 2,93 | 75,31 | 3,64 |
| 18 | 2 | 0,50 | 100,00 | 0,00 | 60,00 | 6,40 | 71,56 | 3,49 | 100,00 | 0,00 | 80,00 | 3,20 |
| 18 | 3 | 0,50 | 98,40 | 3,58 | 54,28 | 6,39 | 68,34 | 3,72 | 96,85 | 7,04 | 76,34 | 4,98 |
| 18 | 4 | 0,50 | 100,00 | 0,00 | 60,00 | 6,40 | 71,56 | 3,49 | 100,00 | 0,00 | 80,00 | 3,20 |
| 18 | 6 | 0,50 | 99,20 | 1,79 | 68,57 | 6,39 | 76,08 | 3,41 | 98,94 | 2,37 | 83,89 | 3,10 |
| 18 | 10 | 0,50 | 100,00 | 0,00 | 68,57 | 15,65 | 77,00 | 9,58 | 100,00 | 0,00 | 84,28 | 7,82 |
| 18 | 2 | 0,30 | 100,00 | 0,00 | 60,00 | 6,39 | 71,55 | 3,48 | 100,00 | 0,00 | 80,00 | 3,20 |
| 18 | 3 | 0,30 | 98,40 | 3,58 | 60,00 | 6,39 | 71,20 | 3,76 | 97,54 | 5,49 | 79,20 | 4,03 |
| 18 | 4 | 0,30 | 100,00 | 0,00 | 60,41 | 6,23 | 70,28 | 5,01 | 100,00 | 0,00 | 79,52 | 3,61 |
| 18 | 6 | 0,30 | 98,40 | 2,19 | 57,14 | 14,29 | 70,20 | 7,34 | 96,98 | 4,19 | 77,77 | 7,70 |
| 18 | 10 | 0,30 | 100,00 | 0,00 | 54,28 | 6,39 | 68,73 | 2,84 | 100,00 | 0,00 | 77,14 | 3,19 |
VPP: valor predictivo positivo; VPN: valor predictivo negativo.
Puede notarse escasa variación en el desempeño de cada red a través de cada uno de los experimentos de entrenamiento efectuado (pequeña desviación estándar). El modelo de 5 datos electrocardiográficos fue el que tuvo menor capacidad de clasificar el diagnóstico del infarto.
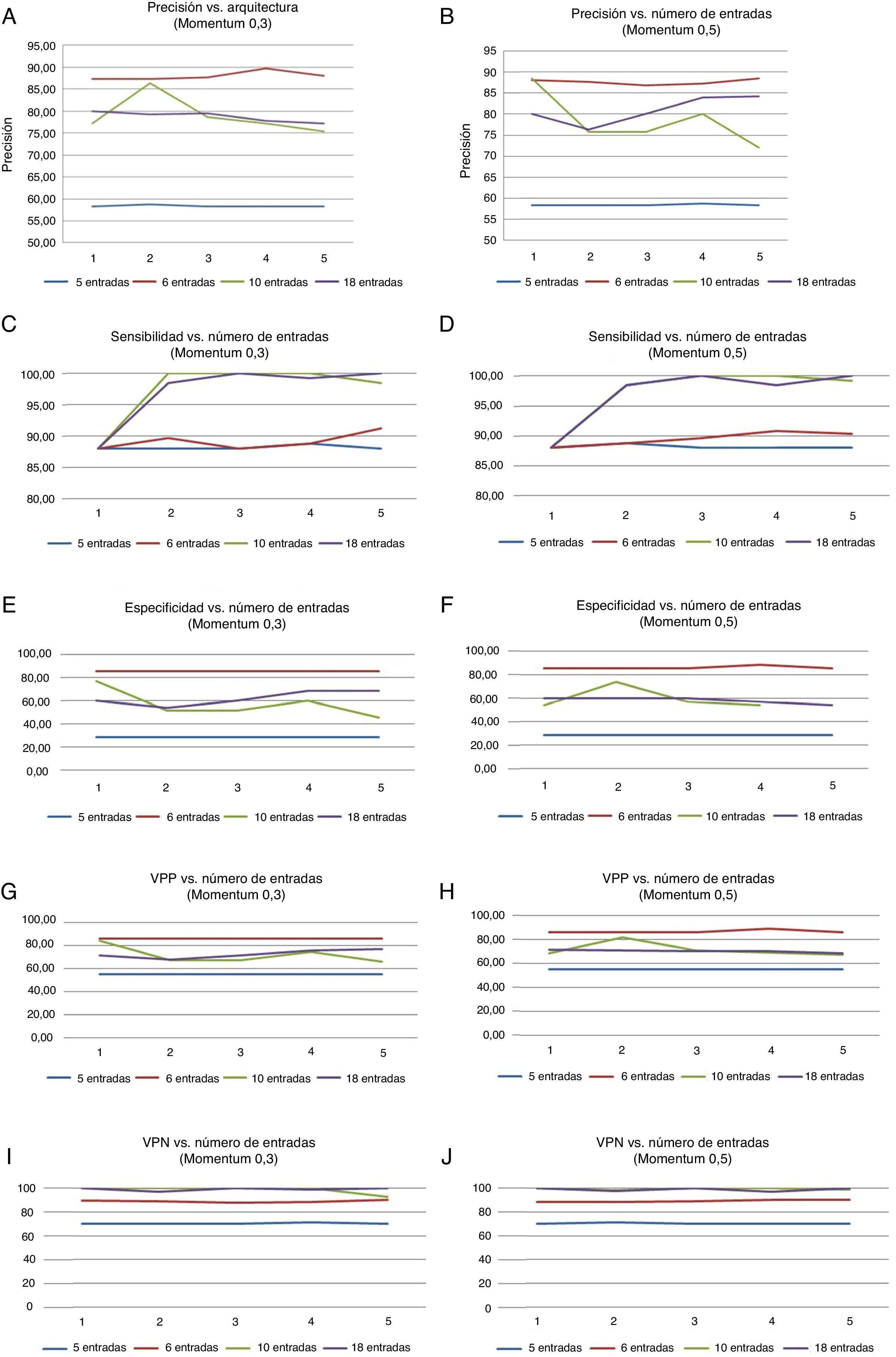
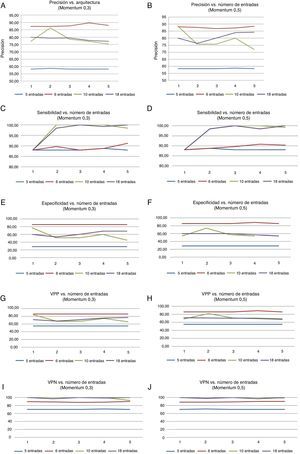
El modelo de 6 neuronas de entrada tuvo el mejor rendimiento diagnóstico, de manera consistente entre las diferentes arquitecturas exploradas. En la figura 2 se observa que con la adición de variables clínicas y antecedentes (10 y 18 variables de entrada) no se mejoró el desempeño global, aunque la red que obtuvo los mejores resultados en las pruebas fue la de 10 variables con 2 neuronas en la capa oculta y momentum de 0,5 (que tuvo 2 de 5 experimentos con el 100% de precisión).
Desempeño de las redes neuronales diseñadas de acuerdo con el número de entradas consideradas y el número de neuronas en la capa oculta.
VPP: valor predictivo positivo; VPN: valor predictivo negativo.
*En las abscisas se plasman el número de neuronas en la capa oculta así: 1) dos, 2) tres, 3) cuatro, 4) seis, y 5) diez neuronas.
En la mayor parte de los casos las redes tuvieron alta sensibilidad, con grados variables de especificidad. Los modelos con el número más grande de entradas tuvieron mejor desempeño al aumentar el número de neuronas en la capa oculta, aunque el número más alto de neuronas no aportó mejor capacidad de discriminación.
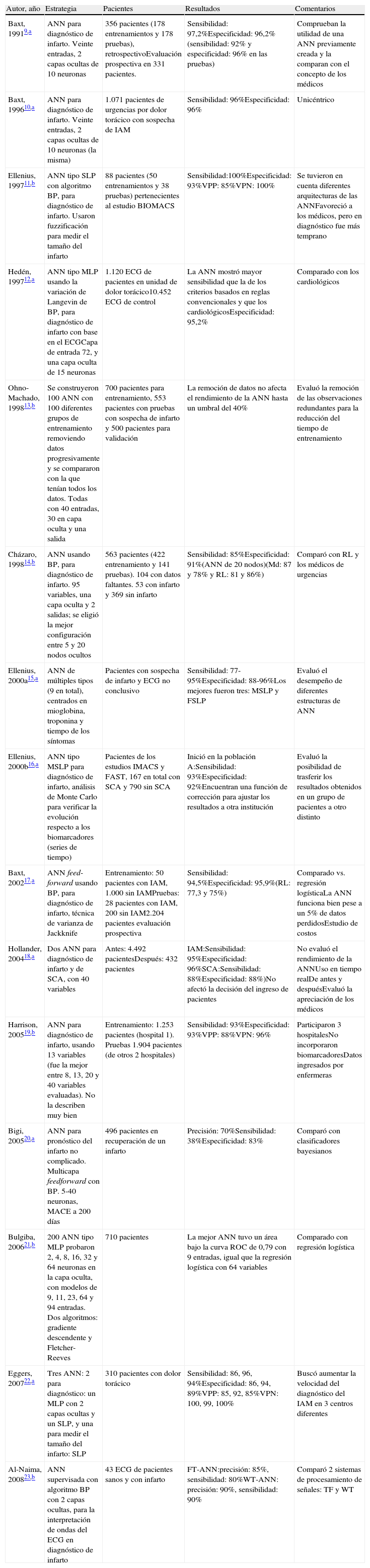
DiscusiónEl proceso de elaboración de una red neuronal es, en su mayoría, un trabajo de ensayo y error (según algunas apreciaciones «artesanal») e implica realizar el mayor número de pruebas con diferentes arquitecturas6. En la tabla 2 se resumen 15 artículos representativos relacionados con la evaluación de las redes neuronales en el diagnóstico del IAM; se observan diferentes maneras de abordar el problema, muchas basadas en el ECG y otras en datos clínicos y de laboratorio. En la mayoría de casos se obtuvieron arquitecturas muy similares, con una sola capa oculta y 2 posibles resultados de salida. En este estudio se presenta un conjunto de experimentos siguiendo lo aprendido en la revisión realizada, considerando distintos grupos de datos de entrada, solo desde el ECG hasta la totalidad de los componentes de la escala de Braunwald y sometiendo a variación el número de neuronas de la capa oculta y el momentum durante el entrenamiento.
Redes neuronales en el diagnóstico de infarto
| Autor, año | Estrategia | Pacientes | Resultados | Comentarios |
| Baxt, 19919,a | ANN para diagnóstico de infarto. Veinte entradas, 2 capas ocultas de 10 neuronas | 356 pacientes (178 entrenamientos y 178 pruebas), retrospectivoEvaluación prospectiva en 331 pacientes. | Sensibilidad: 97,2%Especificidad: 96,2%(sensibilidad: 92% y especificidad: 96% en las pruebas) | Comprueban la utilidad de una ANN previamente creada y la comparan con el concepto de los médicos |
| Baxt, 199610,a | ANN para diagnóstico de infarto. Veinte entradas, 2 capas ocultas de 10 neuronas (la misma) | 1.071 pacientes de urgencias por dolor torácico con sospecha de IAM | Sensibilidad: 96%Especificidad: 96% | Unicéntrico |
| Ellenius, 199711,b | ANN tipo SLP con algoritmo BP, para diagnóstico de infarto. Usaron fuzzificación para medir el tamaño del infarto | 88 pacientes (50 entrenamientos y 38 pruebas) pertenecientes al estudio BIOMACS | Sensibilidad:100%Especificidad: 93%VPP: 85%VPN: 100% | Se tuvieron en cuenta diferentes arquitecturas de las ANNFavoreció a los médicos, pero en diagnóstico fue más temprano |
| Hedén, 199712,a | ANN tipo MLP usando la variación de Langevin de BP, para diagnóstico de infarto con base en el ECGCapa de entrada 72, y una capa oculta de 15 neuronas | 1.120 ECG de pacientes en unidad de dolor torácico10.452 ECG de control | La ANN mostró mayor sensibilidad que la de los criterios basados en reglas convencionales y que los cardiológicosEspecificidad: 95,2% | Comparado con los cardiológicos |
| Ohno-Machado, 199813,b | Se construyeron 100 ANN con 100 diferentes grupos de entrenamiento removiendo datos progresivamente y se compararon con la que tenían todos los datos. Todas con 40 entradas, 30 en capa oculta y una salida | 700 pacientes para entrenamiento, 553 pacientes con pruebas con sospecha de infarto y 500 pacientes para validación | La remoción de datos no afecta el rendimiento de la ANN hasta un umbral del 40% | Evaluó la remoción de las observaciones redundantes para la reducción del tiempo de entrenamiento |
| Cházaro, 199814,b | ANN usando BP, para diagnóstico de infarto. 95 variables, una capa oculta y 2 salidas; se eligió la mejor configuración entre 5 y 20 nodos ocultos | 563 pacientes (422 entrenamiento y 141 pruebas). 104 con datos faltantes. 53 con infarto y 369 sin infarto | Sensibilidad: 85%Especificidad: 91%(ANN de 20 nodos)(Md: 87 y 78% y RL: 81 y 86%) | Comparó con RL y los médicos de urgencias |
| Ellenius, 2000a15,a | ANN de múltiples tipos (9 en total), centrados en mioglobina, troponina y tiempo de los síntomas | Pacientes con sospecha de infarto y ECG no conclusivo | Sensibilidad: 77-95%Especificidad: 88-96%Los mejores fueron tres: MSLP y FSLP | Evaluó el desempeño de diferentes estructuras de ANN |
| Ellenius, 2000b16,a | ANN tipo MSLP para diagnóstico de infarto, análisis de Monte Carlo para verificar la evolución respecto a los biomarcadores (series de tiempo) | Pacientes de los estudios IMACS y FAST, 167 en total con SCA y 790 sin SCA | Inició en la población A:Sensibilidad: 93%Especificidad: 92%Encuentran una función de corrección para ajustar los resultados a otra institución | Evaluó la posibilidad de trasferir los resultados obtenidos en un grupo de pacientes a otro distinto |
| Baxt, 200217.a | ANN feed-forward usando BP, para diagnóstico de infarto, técnica de varianza de Jackknife | Entrenamiento: 50 pacientes con IAM, 1.000 sin IAMPruebas: 28 pacientes con IAM, 200 sin IAM2.204 pacientes evaluación prospectiva | Sensibilidad: 94,5%Especificidad: 95,9%(RL: 77,3 y 75%) | Comparado vs. regresión logísticaLa ANN funciona bien pese a un 5% de datos perdidosEstudio de costos |
| Hollander, 200418,a | Dos ANN para diagnóstico de infarto y de SCA, con 40 variables | Antes: 4.492 pacientesDespués: 432 pacientes | IAM:Sensibilidad: 95%Especificidad: 96%SCA:Sensibilidad: 88%Especificidad: 88%)No afectó la decisión del ingreso de pacientes | No evaluó el rendimiento de la ANNUso en tiempo realDe antes y despuésEvaluó la apreciación de los médicos |
| Harrison, 200519,b | ANN para diagnóstico de infarto, usando 13 variables (fue la mejor entre 8, 13, 20 y 40 variables evaluadas). No la describen muy bien | Entrenamiento: 1.253 pacientes (hospital 1). Pruebas 1.904 pacientes (de otros 2 hospitales) | Sensibilidad: 93%Especificidad: 93%VPP: 88%VPN: 96% | Participaron 3 hospitalesNo incorporaron biomarcadoresDatos ingresados por enfermeras |
| Bigi, 200520,a | ANN para pronóstico del infarto no complicado. Multicapa feedforward con BP. 5-40 neuronas, MACE a 200 días | 496 pacientes en recuperación de un infarto | Precisión: 70%Sensibilidad: 38%Especificidad: 83% | Comparó con clasificadores bayesianos |
| Bulgiba, 200621,b | 200 ANN tipo MLP probaron 2, 4, 8, 16, 32 y 64 neuronas en la capa oculta, con modelos de 9, 11, 23, 64 y 94 entradas. Dos algoritmos: gradiente descendente y Fletcher-Reeves | 710 pacientes | La mejor ANN tuvo un área bajo la curva ROC de 0,79 con 9 entradas, igual que la regresión logística con 64 variables | Comparado con regresión logística |
| Eggers, 200722,a | Tres ANN: 2 para diagnóstico: un MLP con 2 capas ocultas y un SLP, y una para medir el tamaño del infarto: SLP | 310 pacientes con dolor torácico | Sensibilidad: 86, 96, 94%Especificidad: 86, 94, 89%VPP: 85, 92, 85%VPN: 100, 99, 100% | Buscó aumentar la velocidad del diagnóstico del IAM en 3 centros diferentes |
| Al-Naima, 200823,b | ANN supervisada con algoritmo BP con 2 capas ocultas, para la interpretación de ondas del ECG en diagnóstico de infarto | 43 ECG de pacientes sanos y con infarto | FT-ANN:precisión: 85%, sensibilidad: 80%WT-ANN: precisión: 90%, sensibilidad: 90% | Comparó 2 sistemas de procesamiento de señales: TF y WT |
ANN: red neuronal artificial; BP: back propagation; CV: cardiovascular; ECG: electrocardiograma; IAM: infarto agudo de miocardio; MACE: eventos cardiovasculares mayores; MLP: perceptrón de múltiples capas; MSLP: múltiples perceptrones de una sola capa; RL: regresión logística; SLP: perceptrón de una sola capa; TF: trasformada de Fourier; VPN: valor predictivo negativo; VPP: valor predictivo positivo; WT: trasformada de ondas discretas.
Los hallazgos del estudio demuestran que no es posible basarse únicamente en los datos del ECG para el diseño de una red neuronal para el diagnóstico del infarto. Si bien su especificidad es aceptable (cercana al 89%), se correlaciona con baja especificidad. Así mismo, se debe tener en cuenta que la escala de clasificación de la probabilidad de Braunwald no incluye todas las variaciones de hallazgos electrocardiográficos de los síndromes coronarios agudos e infarto (por ejemplo, el bloqueo de rama izquierdo nuevo o los criterios de Sgarbosa), con lo que se podría llegar a mejorar el rendimiento de una red neuronal que los incorpore. En todo caso, se sabe que un ECG normal no descarta infarto; entre el 1 y el 6% finalmente lo tiene25. Por otro lado, es frecuente que se encuentren alteraciones inespecíficas del segmento ST y de la onda T, que dificultan la toma de decisiones en este contexto. Algunos reportes indican que pueden diagnosticarse erróneamente solo con base en el ECG hasta en el 12% de los casos26.
La adición de troponina a los hallazgos electrocardiográficos incrementa la sensibilidad diagnóstica del infarto hasta en el 90%25; las redes neuronales entrenadas con estos criterios demostraron rendimientos superiores. La adición de criterios clínicos basados en edad, género, historia del dolor y antecedentes no mejoraron la sensibilidad ni la especificidad, si bien se encontró ganancia en el valor predictivo negativo.
Los resultados muestran que las variables de la escala de probabilidad de Braunwald para el diagnóstico del infarto tienen un rendimiento adecuado para la clasificación diagnóstica al utilizarse como valores de entrada de una red neuronal. Tras un amplio número de experimentos realizados se alcanzó una topología apropiada creando una red neuronal con una excelente precisión diagnóstica del infarto. Estos resultados deben confirmarse mediante un ensayo clínico, preferiblemente multicéntrico, que efectúe la validación cruzada de esta herramienta y dé pistas a cerca de su comportamiento en el momento de la valoración del paciente en urgencias. Es conveniente tener en cuenta que la red con mejor rendimiento se encontró en el modelo de 10 neuronas de entrada, que sería la escogida para dicho propósito.
El rendimiento diagnóstico de las redes neuronales desarrolladas fue similar al de las redes encontradas en la revisión bibliográfica. El grupo del doctor Baxt ha sido el que más ha evaluado esta técnica en el diagnóstico del infarto9,10,17,18; de hecho, fueron los primeros en publicar sus resultados en 1991: comenzaron con 20 neuronas de entrada con 2 capas ocultas cada una de 10 neuronas, hasta 40 neuronas de entrada en 2004; hasta el momento esta última ha sido la única empleada en tiempo real con un buen desempeño (sensibilidad y especificidad del 88%). Con la disminución del número de neuronas de entrada no se alteraba la precisión diagnóstica, como lo demuestran los trabajos de Harrison19 y Bulgiba21. Tampoco hubo diferencias entre las arquitecturas que tenían una o 2 capas ocultas, hecho conocido ya por los expertos en el tema.
Pese a la extensa cantidad de estudios que demuestran la capacidad para clasificar de forma acertada los IAM generados durante los últimos 20años, su uso no se ha extendido como se esperaba y, a excepción de las estrategias para la interpretación de las señales electrocardiográficas, existen muy pocos sistemas de soporte a las decisiones clínicas que estén en uso. Se ha propuesto que por tratarse de una caja negra, en la que se carece de una explicación de cómo se llega a tomar una decisión27, los médicos se resisten a seguir sus recomendaciones, independiente de su éxito real o potencial28.
Son posibles limitaciones de este trabajo el muestreo por conveniencia y la probabilidad de una falta de representación de otras entidades que se manifiesten con dolor torácico, lo que podría implicar un sesgo de selección. Se requiere la validación cruzada de los resultados y evaluar su funcionamiento en tiempo real. El número de ejemplos parece ser adecuado, ya que es posible lograr un entrenamiento apropiado de las redes neuronales si se logra que entre los ejemplos se encuentren los casos más representativos de la entidad por evaluar.
ConclusionesEs viable entrenar una red neuronal a partir de los parámetros de la escala de clasificación de probabilidad de Braunwald para el diagnóstico del IAM, con un desempeño tal que podría llegar a servir para el apoyo de la toma de decisiones de los médicos de urgencias que atienden pacientes que consultan por dolor torácico.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A las doctoras María Teresa Fontalvo y Carolina Araque por su ayuda en la fase de recolección de la información.