Comparar la eficacia del sulfato de magnesio con el clorhidrato de isoxuprina en la amenaza de parto pretérmino.
Materiales y métodosSe seleccionaron 82 embarazadas con edad gestacional entre 24 y 34 semanas y diagnóstico de amenaza de parto pretérmino para recibir sulfato de magnesio endovenoso (grupoA) o clorhidrato de isoxuprina endovenoso (grupoB). Se evaluaron el tiempo de cese de las contracciones y los efectos adversos maternos.
ResultadosSe logró una tocólisis efectiva en las primeras 24h en el 61.0% de las pacientes del grupoA y en el 61.0% de las pacientes del grupoB (p=ns). Después de 7días de tratamiento, el 36.6% de las pacientes del grupoA y el 36.6% de las pacientes en el grupoB aún permanecían sin contracciones (p=ns). Se logró un retraso del parto más allá de las 34 semanas en el 19.5% de las pacientes tratadas con sulfato de magnesio y en el 26.8% de las pacientes tratadas con clorhidrato de isoxuprina (p=ns). Las náuseas, temblores y vómitos fueron más frecuentes en el grupoA, mientras que los temblores y calorones fueron más frecuentes en las pacientes del grupoB (p=ns).
ConclusiónEl sulfato de magnesio es igual de efectivo que el clorhidrato de isoxuprina en la tocólisis del parto pretérmino.
To compare the efficacy of intravenous magnesium sulphate with isoxsuprine hydrochloride in the treatment of threatened pre-term labour.
Materials and methodsA total of 82 patients with a gestational age between 24 and 34 weeks and threatened pre-term labour were selected to receive intravenous magnesium sulphate (GroupA) or intravenous isoxsuprine hydrochloride (GroupB). An analysis was performed on the time of ceasing of uterine contractions and maternal adverse effects.
ResultsTocolysis was successful in the first 24hours in 61.0% of patients in GroupA and 61.0% in patients of GroupB (P=ns). After 7days of treatment, 36.6% of patients in GroupA and 36.6% of patients in GroupB still were without contractions (P=ns). A delay in delivery over 34weeks was obtained in 19.5% of patients treated with magnesium sulphate and 26.8% in patients treated with isoxsuprine hydrochloride (P=ns). Nausea, tremor, and vomiting were more frequent in GroupA, while tremors and sweating were more frequent in GroupB (P=ns).
ConclusionMagnesium sulphate is as effective as isoxsuprine hydrochloride for tocolysis in threatened pre-term labour.
El parto pretérmino y sus secuelas son un problema de salud pública global. A pesar de los avances para comprender la fisiología del parto y la medicina perinatal en general, la incidencia de parto pretérmino continúa al alza. El objetivo primario del tratamiento tocolítico es la reducción de la morbimortalidad neonatal al retrasar el parto, permitiendo la administración de corticosteroides y la referencia materna a un hospital con servicios neonatales avanzados1.
Los betamiméticos han sido recomendados como el tratamiento tocolítico estándar. Estos fármacos reducen el número de partos que ocurren en las 48h siguientes al inicio del tratamiento, comparado con el placebo2. Sin embargo, no se han asociado con una mejoría en la morbimortalidad neonatal y producen un número sustancial de efectos adversos en la madre3.
Los tocolíticos en general tienen una baja eficacia, no han demostrado que incrementan la posibilidad de la administración prenatal de corticosteroides, pueden causar efectos adversos maternos o fetales significativos y no disminuyen las complicaciones neonatales4-6. El uso de sulfato de magnesio presenta algunos riesgos, ya que se necesita de su administración endovenosa, tiene el potencial de producir sobremedicación y puede estar asociado con efectos neonatales adversos7. Es el tocolítico de primera línea más comúnmente utilizado en Norteamérica8, aunque no se ha demostrado que sea más efectivo que la solución salina sola y su uso ha sido motivo de controversia7,9. Cuando se comparan con los betamiméticos, el sulfato de magnesio parece ofrecer un mejor perfil de seguridad materna10.
El objetivo de la investigación fue comparar la efectividad tocolítica del sulfato de magnesio con el clorhidrato de isoxuprina en la amenaza de parto pretérmino.
Materiales y métodosSe incluyeron a todas las pacientes en edad gestacional entre 24 y 34 semanas y con diagnóstico de parto pretérmino, que se definirá como la presencia de contracciones uterinas regulares (6 o más por hora y con una duración de más de 30segundos), con o sin evidencia de dilatación y/o borramiento cervical y membranas íntegras. Se excluyeron las pacientes con gestaciones múltiples, con condiciones médicas que contraindiquen el uso de cualquiera de los medicamentos, presencia de infección intrauterina, alteraciones de la frecuencia cardíaca fetal, hemorragia anteparto o polihidramnios. El Comité de Ética del hospital aprobó el estudio y se obtuvo consentimiento por escrito de todas las pacientes.
Una vez que a la paciente se la diagnosticó de parto pretérmino se le realizó un electrocardiograma antes, a las 24h después del inicio del tratamiento y al momento de omitir el tratamiento. La presión arterial y la frecuencia cardíaca fueron monitorizadas al inicio del tratamiento y cada 15min durante las primeras 2h y luego cada 8h. El tiempo de gestación se basó en el momento del último ciclo menstrual, si los datos de esta determinación y las mediciones de ultrasonido más temprano presentaban una diferencia menor de 10días. Si la diferencia era mayor de 10días entre los dos cálculos, entonces la edad gestacional se estableció por las mediciones ecográficas.
Posterior a la obtención del consentimiento informado se les administró 500ml de solución salina al 0.9% y se practicó la asignación al azar. Para obtener una distribución igual del uso de los medicamentos en cada uno de los grupos se asignaron sobres sellados con una distribución al azar entre los diferentes grupos. A las pacientes tratadas con sulfato de magnesio (grupoA) se les administró por vía endovenosa una dosis carga de 4g en 30min, seguida de una infusión de mantenimiento de 2g/h para llegar a niveles terapéuticos en sangre de 5 a 8mg/dl. Una vez que cesaron las contracciones, la infusión se mantuvo a la mínima dosis efectiva por 12h y luego se retiró. De aparecer efectos adversos, fueron revertidos rápidamente con la infusión endovenosa de 1g de gluconato de calcio. La evaluación del tratamiento con sulfato de magnesio se realizó hasta el momento que se dio de alta a la paciente. Si las contracciones reaparecieron luego del uso del sulfato de magnesio, se comenzó el tratamiento con clorhidrato de isoxuprina y se excluyó a la paciente del estudio.
El clorhidrato de isoxuprina (grupoB) se preparó en una infusión de 4 ampollas (40mg) en una solución glucosada al 5%, y se inició con una dosis de carga de 200g/min por vía endovenosa. Tan pronto como se consiguió la tocólisis, el goteo de la infusión se disminuyó lo suficiente para mantener la tocólisis. La dosis máxima fue de 400g/min o dependiendo de la frecuencia cardiaca materna (máximo 130latidos/min).
La evaluación de la efectividad del tratamiento se realizó mediante la proporción de partos a las 24h y 7días del inicio del tratamiento y el número de partos antes de las 34 semanas. Los efectos adversos (taquicardia, enrojecimiento facial, cefalea, edema periférico, dolor torácico, náuseas, vómitos) de las pacientes fueron evaluados por interrogatorio a las pacientes 2h después del tratamiento y, posteriormente, en períodos de 24h.
Los resultados se presentaran en cuadros. Se utilizaron medidas absolutas y relativas. Las variables cuantitativas de los pacientes de ambos grupos se analizaron con la prueba t de Student para muestras no relacionadas y las variables cualitativas fueron analizadas con la prueba exacta de Fisher. Se consideró p<0.05 como estadísticamente significativa.
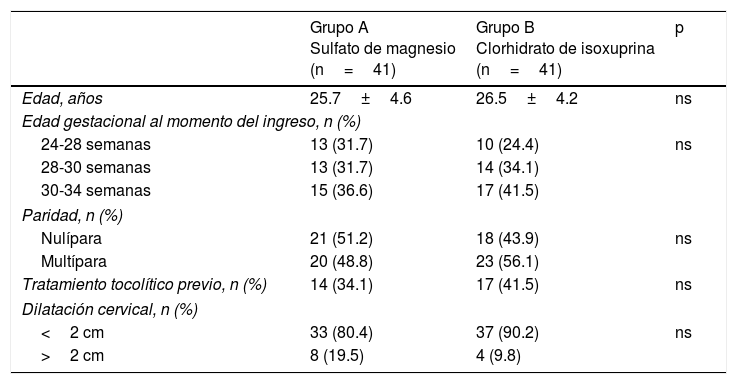
ResultadosSe seleccionó un total de 82 pacientes, las cuales se asignaron al azar para recibir sulfato de magnesio (grupoA; n=41) o clorhidrato de isoxuprina (grupoB; n=41). La duración promedio del tratamiento en el grupoA fue de 4.9±1.5 días, y en el grupoB fue de 5.6±2.1días (p=ns). El promedio de edad gestacional de las pacientes al momento del ingreso fue de 30.4±semanas en el grupoA y 32.4±2.4 semanas para el grupoB (p=ns). Las características maternas al momento del inicio del estudio se muestran en la tabla 1. No se encontraron diferencias con relación a la edad materna, la paridad, el tratamiento tocolítico previo y la dilatación cervical (p=ns)
Características maternas generales
| Grupo A Sulfato de magnesio (n=41) | Grupo B Clorhidrato de isoxuprina (n=41) | p | |
|---|---|---|---|
| Edad, años | 25.7±4.6 | 26.5±4.2 | ns |
| Edad gestacional al momento del ingreso, n (%) | |||
| 24-28 semanas | 13 (31.7) | 10 (24.4) | ns |
| 28-30 semanas | 13 (31.7) | 14 (34.1) | |
| 30-34 semanas | 15 (36.6) | 17 (41.5) | |
| Paridad, n (%) | |||
| Nulípara | 21 (51.2) | 18 (43.9) | ns |
| Multípara | 20 (48.8) | 23 (56.1) | |
| Tratamiento tocolítico previo, n (%) | 14 (34.1) | 17 (41.5) | ns |
| Dilatación cervical, n (%) | |||
| <2 cm | 33 (80.4) | 37 (90.2) | ns |
| >2 cm | 8 (19.5) | 4 (9.8) | |
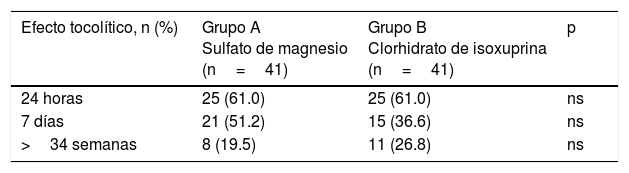
Los resultados del tratamiento tocolítico se muestran en la tabla 2. Se logró una tocólisis efectiva en las primeras 24h en el 61.0% de las pacientes tratadas con sulfato de magnesio y en el 61.0% de las pacientes del grupo tratado con clorhidrato de isoxuprina (p=ns). Después de 7días de tratamiento, el 51.2% de las pacientes del grupoA y el 36.6% de las pacientes del grupoB aún permanecían sin contracciones (p=ns). Se logró un retraso del parto más allá de las 34semanas en el 19.5% de las pacientes tratadas con sulfato de magnesio y en el 26.8% de las pacientes tratadas con clorhidrato de isoxuprina (p=ns).
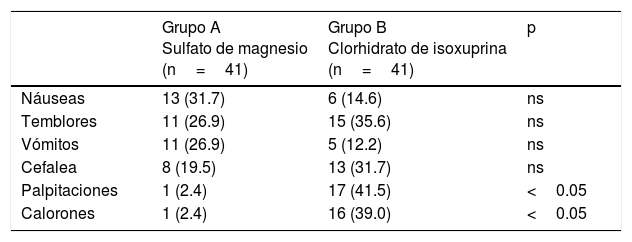
Las náuseas, los temblores y los vómitos fueron más frecuentes en el grupoA, mientras que los temblores y calorones fueron más frecuentes en las pacientes del grupoB (tabla 3), pero solo las palpitaciones y los calorones alcanzaron diferencias significativas entre ambos grupos de tratamiento (p<0.05). Sin embargo, no hubo necesidad de detener el tratamiento en ninguno de los grupos. Ninguna paciente refirió la presencia de edema periférico, dolor torácico, dolor precordial o disnea.
Efectos maternos asociados al tratamiento
| Grupo A Sulfato de magnesio (n=41) | Grupo B Clorhidrato de isoxuprina (n=41) | p | |
|---|---|---|---|
| Náuseas | 13 (31.7) | 6 (14.6) | ns |
| Temblores | 11 (26.9) | 15 (35.6) | ns |
| Vómitos | 11 (26.9) | 5 (12.2) | ns |
| Cefalea | 8 (19.5) | 13 (31.7) | ns |
| Palpitaciones | 1 (2.4) | 17 (41.5) | <0.05 |
| Calorones | 1 (2.4) | 16 (39.0) | <0.05 |
Los resultados de la investigación no demostraron diferencias significativas entre las pacientes tratadas con sulfato de magnesio comparado con las pacientes con clorhidrato de isoxuprina. Además, el sulfato de magnesio tiene una incidencia de efectos adversos similar a la del betamimético en estudio.
El sulfato de magnesio ha sido objeto de numerosos estudios clínicos para analizar su eficacia en el tratamiento del parto pretérmino. Estudios individuales han sido marcados por limitaciones en la capacidad de evaluar el impacto del tratamiento sobre las variables maternas y neonatales, la principal razón por la cual se intenta prolongar el embarazo10-12. A diferencia de los betamiméticos, la mayoría de los agentes tocolíticos no han sido probados comparados con un placebo o un grupo control, y el sulfato de magnesio no es la excepción a esta regla.
Diferentes investigadores han realizado la comparación de los efectos de sulfato de magnesio con una amplia variedad de agentes, incluyendo el alcohol, agentes betamiméticos, inhibidores de la ciclooxigenasa, bloqueadores de los canales de calcio y donadores de óxido nítrico11. Como otras drogas tocolíticas, la comparación de estudios individuales con relación al sulfato de magnesio se hace difícil debido a los diferentes criterios de inclusión (por ejemplo, criterios diagnósticos de parto pretérmino, edad gestacional, presencia o ausencia de membranas intactas), intervenciones farmacológicas concurrentes, al igual que reportes selectivos de los resultados de las investigaciones. Estos estudios han sido sujeto de varias revisiones y metaanálisis, los cuales suministran una descripción detallada de los diseños individuales y los resultados10,12.
Los agonistas betamiméticos, al unirse con los receptores beta2 en la membrana celular, activan la adenilatociclasa para incrementar la concentración intracelular de adenosinmonofosfato cíclica, produciendo una disminución de la disponibilidad de calcio libre intracelular para la actina y la miosina, llevando a la relajación del músculo liso uterino. Por otra parte, el sulfato de magnesio actúa sobre los canales de calcio dependientes del voltaje para bloquear competitivamente la entrada de calcio, llevando a una inhibición de la fosforilización de la cinasa de la cadena ligera de la miosina dependiente de calcio13.
Estudios en animales han demostrado que la actividad uterina es inhibida inicialmente por la infusión endovenosa de betamiméticos por 6h, pero la actividad regresa a los valores previos a la infusión a las 11-16h a pesar de la infusión continua14. Varios informes basados en experimentos in vitro también han demostrado que la exposición continua del miometrio a los agonistas betamiméticos produce una relajación inicial del miometrio seguido por una sensibilización y regreso de las contracciones miometriales15,16. Sin embargo, los resultados de la presente investigación demostraron que más del 50% de las pacientes que recibieron sulfato de magnesio permanecieron sin contracciones uterinas luego de 7días, comparado con el 36.6% de las pacientes del grupo de clorhidrato de isoxuprina, y aunque la diferencia no fue estadísticamente significativa, la observación clínica sugiere que las pacientes que reciben betamiméticos se desensibilizan y las contracciones reaparecen, lo cual no se observa en las pacientes que reciben sulfato de magnesio.
Los betamiméticos, en especial el clorhidrato de isoxuprina, son ampliamente empleados en el tratamiento de la amenaza de parto pretérmino y su uso disminuye la posibilidad de partos pretérmino durante su uso17. La estrecha ventana entre su eficacia terapéutica y los efectos adversos inaceptables o peligrosos (temblores, taquicardia, palpitaciones, hipotensión o edema pulmonar) limita el uso y la duración de estos fármacos. Esto podría ser una ventaja para el uso de otros tocolíticos, como el sulfato de magnesio.
Los resultados de la presente investigación son similares a los de investigaciones previas y con otros tipos de drogas tocolíticas. Existen investigaciones que han comparado el sulfato de magnesio con betamiméticos18-20, bloqueadores de los canales de calcio11,21,22 e inhibidores de la ciclooxigenasa23-26. Comparados con el sulfato de magnesio, los betamiméticos no se asociaron con una disminución en el número de partos a las 48h, 7días, partos pretérmino y bajo peso al nacer, a pesar de la aparente mejoría en la latencia global en dos estudios9,18. Los betamiméticos son susceptibles a la producción de taquifilaxia y a la reducción de la eficacia en el tiempo. Después de los primeros días de tratamiento, existe una disminución demostrable de la actividad de los receptores beta miometriales27.
La actualización de las revisiones sistemáticas de Cochrane con relación al sulfato de magnesio para la tocólisis en la amenaza de parto pretérmino fue publicada por Crowther et al.12. Se evaluaron datos publicados y no publicados de estudios en revistas arbitradas donde se incluyeron más de 2,000 embarazos. Los autores concluyeron que no existía evidencia, desde el punto de vista clínico, de ningún efecto tocolítico importante, ya que no se encontraron efectos sustanciales en la proporción de mujeres que presentaron partos en las 48h siguientes al inicio del tratamiento, tanto en forma general como en cualquier subgrupo de análisis.
En forma alternativa, en un estudio sobre la efectividad del parto pretérmino Tan et al.10 evaluaron estudios clínicos al azar, observacionales y retrospectivos. Con relación al magnesio como tratamiento de primera línea, este grupo determinó que no se encontraron diferencias significativas entre el sulfato de magnesio y el placebo, y con relación a las comparaciones entre las diferentes clases de tocolíticos describieron que los betamiméticos, los bloqueadores de los canales de calcio y el sulfato de magnesio casi doblaban la posibilidad de llegar hasta el término del embarazo con relación a los controles, con pequeñas diferencias potenciales de los efectos entre los grupos. Estos autores concluyen que en forma general la evidencia apoya que el tratamiento de primera línea con betamiméticos, bloqueadores de los canales de calcio y sulfato de magnesio ofrecen pequeñas mejorías en la prolongación del embarazo.
Los efectos adversos fueron similares entre los dos grupos, pero las pacientes del grupo tratado con clorhidrato de isoxuprina presentaron una incidencia significativamente mayor de palpitaciones y calorones. Se ha descrito que el uso de betamiméticos en bolo puede reducir los efectos adversos, pero esto no los elimina totalmente28. Como se mencionó previamente, durante los primeros días de tratamiento la paciente obstétrica puede adaptarse a la estimulación beta-adrenérgica al disminuir la actividad de los receptores, disminuyendo la posibilidad de la presencia de efectos adversos27. En esta investigación, en las pacientes tratadas con sulfato de magnesio no se observaron efectos maternos graves, como disnea o edema pulmonar, que han sido descritos en pacientes tratadas en otras investigaciones11.
ConclusiónSe concluye que el sulfato de magnesio es igual de efectivo que el clorhidrato de isoxuprina en la tocólisis del parto pretérmino.
AutoríaTodos los autores declaran que han realizado aportes a la idea, diseño del estudio, recolección de datos, análisis e interpretación de datos, revisión crítica del contenido intelectual y aprobación final del manuscrito que estamos enviando.
Responsabilidades éticasProtección de personasLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos del Hospital Central «Dr. Urquinaona» sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoLos autores certifican que no han recibido apoyos financieros, equipos, en personal de trabajo o en especie de personas, instituciones públicas y/o privadas para la realización del estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.