Hay diferentes motivos1 por los que el farmacéutico necesita interpretar un metaanálisis o, en ciertas ocasiones, realizarlo (tabla 1). Hace ahora cien años, Pearson diseñó una técnica para agrupar y combinar los resultados de estudios pequeños que no tenían suficiente potencia individualmente, pero que su unión metódica producía resultados adecuados.
Este problema se observa, en muchas ocasiones, en la investigación farmacéutica: los tamaños de las muestras analizadas son tan pequeños que no se puede inferir conclusión alguna de cada uno de ellos, o incluso, son contradictorios entre sí (tabla 1).
En otras ocasiones, el metaanálisis sirve para poner de manifiesto un hecho antes de haberse demostrado (como la efectividad de la estreptoquinasa en la reducción de la mortalidad postinfarto)2 o desterrar una tesis errónea obtenida de pobres evidencias (como la manifestada por Pauling acerca del beneficio de la vitamina C en la prevención de resfriados)3.
La realización de metaanálisis es muy habitual hoy en día: una sencilla búsqueda en MEDLINE con el término meta-analysis ofrece un gran número de ellos, y crece, además, cada año (tabla 2). Por eso, el farmacéutico debe tener cierta familiaridad con este tipo de estudios, con el objetivo de facilitar su comprensión.
Ahora bien, a pesar de las ventajas que tiene, la calidad de un metaanálisis depende de la de los estudios que lo integran: se ha evidenciado que los estudios de baja calidad metodológica presentan un resultado medio superior al ofrecido por los que están dotados de buena calidad4, lo que sobreestima el resultado final.
¿Qué estudios se recogen?
La primera cuestión se refiere a la inclusión de los estudios que conformarán el metaanálisis, porque de aquí se desprende un sesgo: se sabe que los estudios que presentan resultados positivos se publican con mayor probabilidad que los que los ofrecen de tipo negativo, de esta forma, habrá una desviación hacia la sobreestimación de resultado favorable al no poderse incluir los que manifiestan un resultado adverso.
Para obtener todos los publicados no se deberá acudir exclusivamente a la base de datos más habitual, MEDLINE, pues no los recoge en su totalidad5, por lo que se habrá buscado, al menos, en las bases citadas en este curso6.
Para intentar corregir este sesgo de inclusión, el metaanálisis debe incorporar un análisis final de sensibilidad, para estudiar cómo varía el resultado al modificar el número o tipo de estudio, o si se suprimen los valores extremos, o cuántos estudios harían falta para anular el resultado obtenido, pues se incrementa la validez de este resultado final si, a pesar de estos cambios, se mantiene su valor.
Otro importante factor que hay que observar es que los estudios combinados deben ser similares entre sí, y que sus resultados únicamente serán aplicables a un entorno similar al estudiado en ellos. Para evitar un sesgo por este motivo, se deberán expresar los criterios de su inclusión (p. ej., estudios aleatorizados, controlados, que tengan un resultado primario concreto, que estudien un perfil determinado de paciente, en cuanto a edad, estado de su patología, etc.) y exclusión (p. ej., que el paciente presente otras patologías adicionales, que las mediciones del resultado se hayan realizado a tiempos diferentes, que se hayan realizado en escenarios diferentes, como atención primaria y hospitalaria, etc.) de estudios que se combinarán en el metaanálisis.
¿Cómo se lee un metaanálisis?
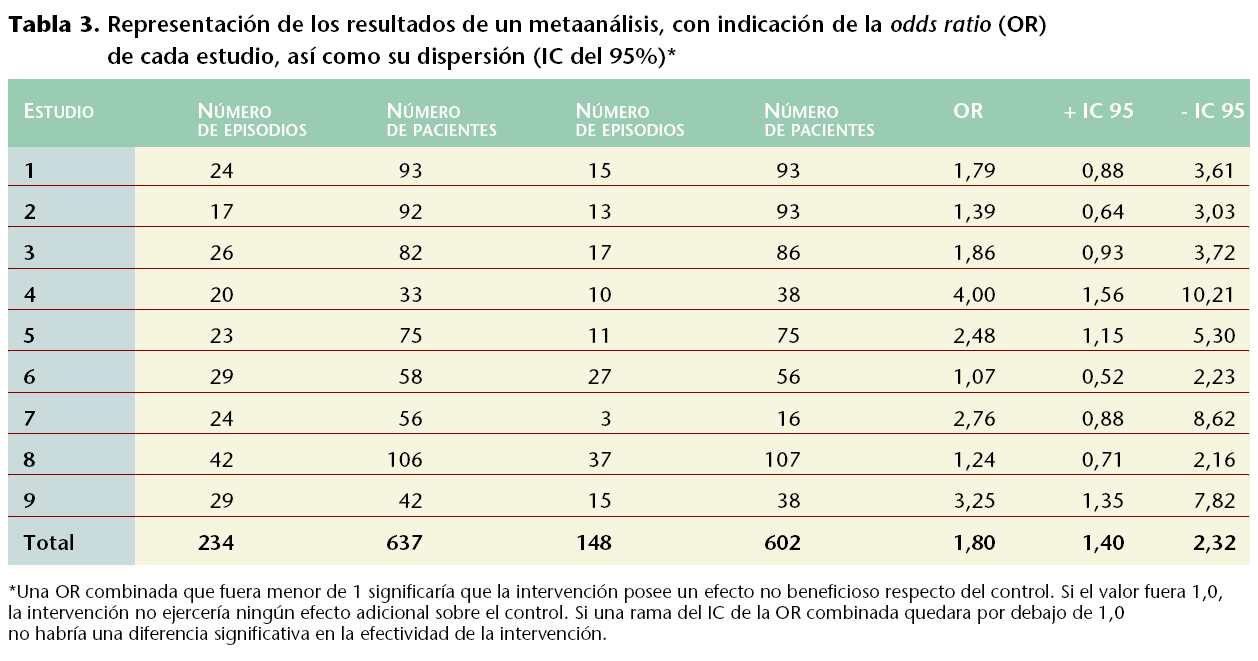
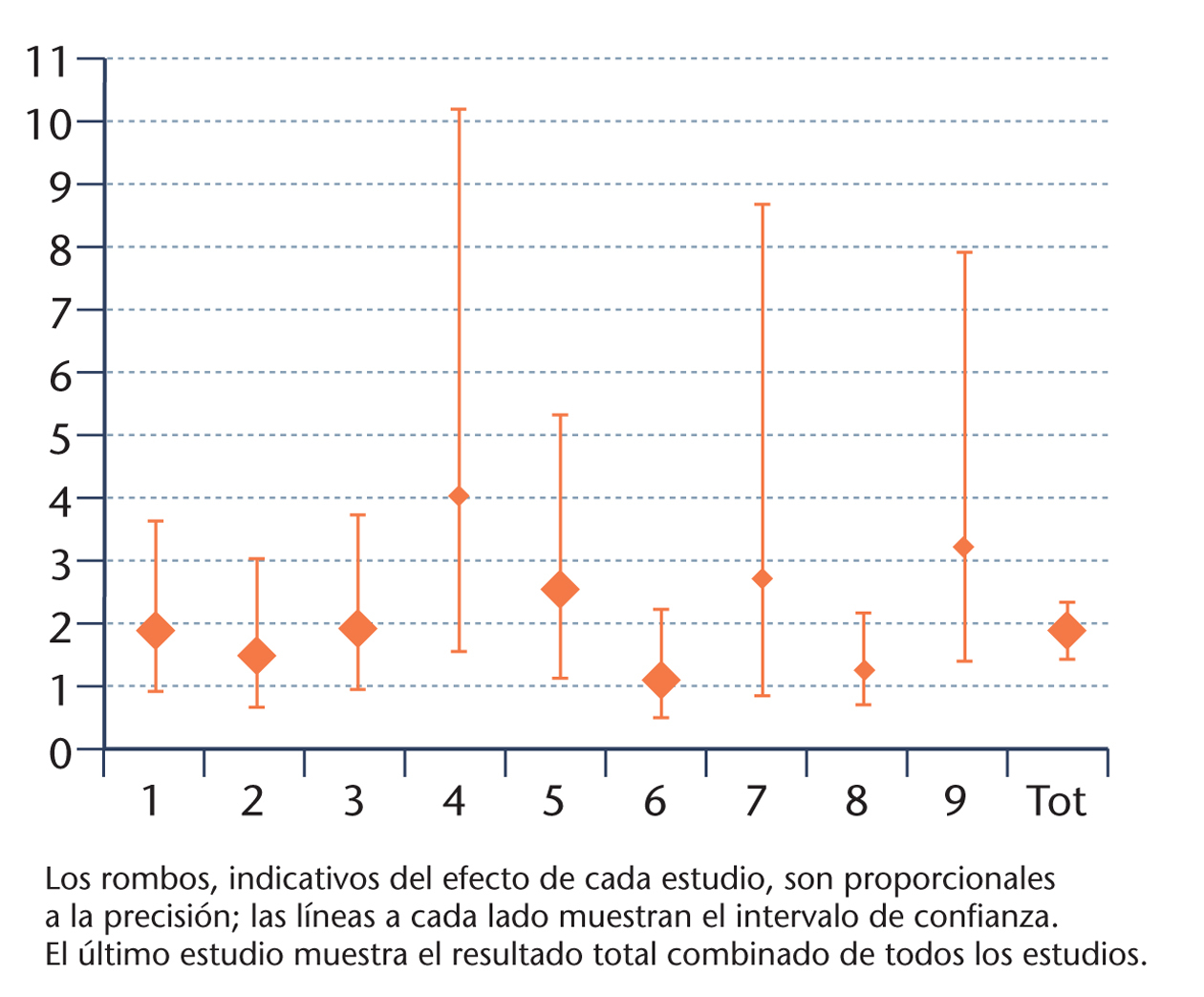
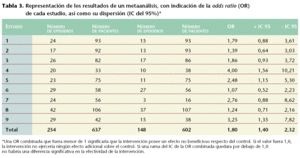
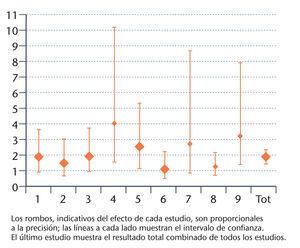
El grupo QUÓRUM7 definió un esquema de trabajo y presentación de este tipo de estudios. De este modo, los datos numéricos se presentan en una tabla con una fila para cada estudio (tabla 3), y a continuación se exponen gráficamente los resultados de cada estudio (fig. 1) mediante un símbolo de dimensión proporcional a la precisión del efecto, junto con una línea que lo atraviesa, que representa el intervalo de confianza (IC) del resultado individual. Los estudios se ordenan por tamaño de muestra, fecha, calidad, etc., y al final del gráfico se dibuja el valor global de la combinación de los estudios junto con su IC.
Fig. 1. Representación en gráfico de un metaanálisis.
En el ejemplo teórico desarrollado, la odds ratio (OR) combinada es superior a 1,0, lo que significa que la intervención tiene un efecto beneficioso. Además, su IC no incluye el 1, por lo que la diferencia es estadísticamente significativa.
Valoración de un metaanálisis
Hay ciertas listas de comprobación de la calidad de un metaanálisis, como la del grupo QUÓRUM, mediante las que podremos evaluar el que tengamos. Mediante estas listas se comprobará la calidad a través de la observación de si se han tenido en cuenta, para su elaboración, ciertos aspectos relevantes acerca de los estudios incluidos, como su homogeneidad, el análisis de los valores hallados, y el ámbito de las conclusiones (tabla 4).
PDF
Consultora científica