La esclerosis múltiple (EM) es una enfermedad crónica del sistema nervioso central que se caracteriza por la existencia de inflamación, desmielinización, gliosis y daño axonal. La introducción de dimetilfumarato y teriflunomida ha supuesto un aumento de las alternativas terapéuticas en la primera línea de tratamiento de la EM. El objetivo de este estudio fue evaluar el impacto económico de la incorporación de estas nuevas terapias orales en la Unidad de Referencia (CSUR) del Hospital Universitario Puerta de Hierro Majadahonda.
Material y métodosSe realizó un estudio observacional retrospectivo en la población de pacientes diagnosticados de EM, en tratamiento con fármacos modificadores de la enfermedad durante el año 2015, y su seguimiento se prolongó hasta obtener un seguimiento medio superior a un año de tratamiento. Los datos se recogieron de la historia clínica electrónica y del programa de dispensación de medicamentos a pacientes externos y ambulantes del Servicio de Farmacia.
ResultadosEvaluando el coste del cambio del tratamiento en 125 pacientes desde otros fármacos a dimetilfumarato o teriflunomida y comparando con el coste que habría supuesto el mantenimiento de los tratamientos previos, el ahorro total durante el periodo de observación fue de 169.107,31 €.
ConclusionesDimetilfumarato y teriflunomida, además de aportar nuevas alternativas terapéuticas, no solo no han supuesto un incremento sino, por el contrario, una disminución en los costes del tratamiento de la EM en nuestro hospital.
Multiple sclerosis (MS) is a chronic disease affecting the central nervous system and is characterised by inflammation, demyelination, gliosis, and axonal damage. The introduction of dimethyl fumarate and teriflunomide has led to an increase in the number of alternative first-line therapies for MS. The objective of this study was to evaluate the economic impact of the incorporation of new oral therapies at the reference unit (CSUR) at Hospital Universitario Puerta de Hierro Majadahonda.
Materials and methodsWe performed a retrospective observational study including patients diagnosed with MS, who underwent treatment with disease-modifying drugs in 2015 and were followed up for a minimum mean time of one year. Data were collected from patients’ electronic clinical histories and the pharmacy service's programme for dispensing drugs to outpatients.
ResultsEvaluating the cost of changing 125 patients’ treatment from other drugs to dimethyl fumarate and teriflunomide, and comparing this with the cost that would have resulted from maintaining their previous treatment, demonstrated a total saving of €169,107.31 over the study period.
ConclusionsIn addition to contributing new therapeutic alternatives, dimethyl fumarate and teriflunomide produced an economic saving in MS treatment at our hospital.
La esclerosis múltiple (EM) es una enfermedad crónica del sistema nervioso central que se caracteriza por la existencia de inflamación, desmielinización, gliosis y daño axonal, todo lo cual produce grados variables de lesión neurológica persistente. Suele comenzar en adultos jóvenes y es de 2 a 3 veces más común en mujeres. En el 90% de los pacientes produce, sobre todo en las etapas iniciales de la enfermedad, episodios de disfunción neurológica llamados brotes, que duran días o semanas y que suelen remitir parcial o totalmente. Una parte importante de estos pacientes desarrolla, a lo largo de su evolución, lo que se denominan formas secundariamente progresivas, en las que el deterioro neurológico progresa sin evidencia de brotes. Además, en torno a un 10% padece formas primariamente progresivas, caracterizadas por un deterioro neurológico progresivo sin brotes1.
Esta enfermedad tiene un alto impacto personal, social y sanitario por su frecuencia (en España la prevalencia se estima en 100-125 casos por cada 100.000 habitantes), su tendencia a producir discapacidad en el adulto joven, su repercusión laboral negativa, las necesidades de cuidados y los costes del tratamiento1.
En los últimos 20 años la Unión Europea ha aprobado sucesivamente 11 medicamentos para el tratamiento del curso de la enfermedad, unos para administración por vía parenteral y otros por vía oral. Los primeros comercializados fueron: interferón beta 1b (Betaferón®), interferón beta 1a intramuscular (Avonex®), interferón beta 1a subcutáneo (Rebif®), acetato de glatirámero (Copaxone®), mitoxantrona (Novantrone®), natalizumab (Tysabri®), fingolimod (Gilenya®) –el primero de los agentes orales–, y en 2014 se incorporaron los 4 últimos medicamentos: alemtuzumab (Lemtrada®), interferón beta 1a pegilado (Plegridy®) y 2 agentes orales más, dimetilfumarato (Tecfidera®) y teriflunomida (Aubagio®)1. De las terapias orales, son estos dos últimos los que se utilizan en primera línea.
Cada uno de estos medicamentos se aprobó sobre la base de los correspondientes ensayos clínicos y sus indicaciones están configuradas en función de la forma clínica de la enfermedad en la población sobre la que se realizó el ensayo1.
Dimetilfumarato y teriflunomida cuentan con la autorización como primera línea de tratamiento para iniciar la terapia en la forma recidivante remitente de la EM1–8. Su introducción ha supuesto tanto un aumento de las alternativas terapéuticas como una posibilidad de mejora en la calidad de vida de los pacientes en los que está indicado su empleo.
Al margen de estos aspectos, hay que considerar que es usual que la introducción de nuevos fármacos incremente los costes del tratamiento de la enfermedad correspondiente. En este sentido, el objetivo que persigue este estudio es evaluar el impacto económico que ha supuesto la incorporación de las nuevas terapias orales de primera línea en el tratamiento de la EM en la Unidad Centros, Servicios y Unidades de Referencia del Hospital Universitario Puerta de Hierro Majadahonda.
Material y métodosSe realizó un estudio observacional retrospectivo en la población de pacientes diagnosticados de EM, en tratamiento con fármacos modificadores de la enfermedad durante el año 2015, y su seguimiento se prolongó hasta obtener un seguimiento medio superior a un año de tratamiento.
Antes de iniciar el estudio se solicitó autorización al Comité Ético de Investigación con medicamentos del hospital, que aprobó el planteamiento desde el punto de vista metodológico y ético.
Los datos se recogieron de la historia clínica electrónica y del programa de dispensación de medicamentos a pacientes externos y ambulantes del Servicio de Farmacia. El tratamiento de la información se realizó de acuerdo con la legislación vigente sobre protección de datos de carácter personal (Ley Orgánica 15/1999, de 13 de diciembre, de protección de Datos de Carácter Personal). En la base de datos se incluyeron los datos clínicos de los pacientes anonimizados.
Las variables consideradas incluyeron: edad en el momento de realización del estudio, sexo, meses de seguimiento, principio activo utilizado en el tratamiento, modificaciones en el mismo durante el seguimiento y adherencia.
La adherencia terapéutica se midió mediante el control de la dispensación, según la fórmula: % adherencia = N.° de días de medicación dispensada/N.° de días entre las dispensaciones X 100. Se excluyeron los pacientes tratados con un mismo fármaco durante menos de 120 días consecutivos.
En aquellos pacientes en los que se cambió un tratamiento previo a dimetilfumarato o teriflunomida, se comparó el coste de estas terapias con el que hubiera supuesto el mantenimiento del fármaco anterior (precio neto × n.° de dispensaciones en el periodo de seguimiento). No se tuvieron en cuenta otros costes directos –asociados a la preparación y administración de los medicamentos en Hospital de Día, determinaciones bioquímicas, estudios de imagen, etc.–, ni costes indirectos e inaparentes –calidad de vida, capacidad productiva, etc.–, dado que en este estudio se ha valorado exclusivamente el impacto presupuestario que ha tenido la introducción de estos fármacos sobre la Farmacia del hospital.
Se realizó un análisis descriptivo de las variables para conocer las características generales de la población de estudio. Las variables cualitativas se presentaron con su distribución de frecuencias absolutas y porcentajes. Las variables cuantitativas se resumieron con su media y su desviación estándar. Se realizó un sumatorio del número de pacientes tratados con cada fármaco y del tiempo de tratamiento con cada uno de ellos. Se evaluó la asociación entre variables cualitativas con el test de χ2 con un nivel de significación de p<0,05. Los datos se analizaron mediante el programa ESTATA.
ResultadosDurante el periodo comprendido entre enero y diciembre de 2015, 501 pacientes diagnosticados de EM estaban en tratamiento con fármacos modificadores de la enfermedad.
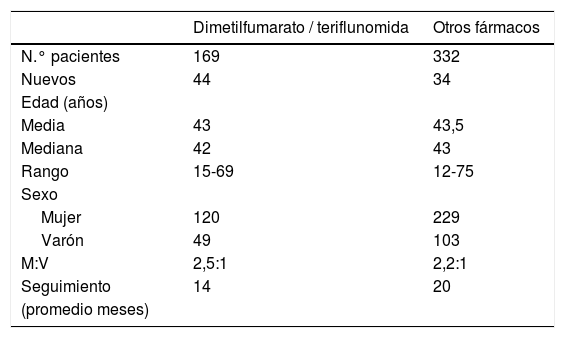
La edad media de estos pacientes fue de 43,2 años (mediana 43 años; rango 12-75 años). El sexo: mujer 349; varón 152; M:V = 2,3:1. Y el seguimiento promedio fue de 20 meses.
Durante dicho periodo, 169 de los pacientes diagnosticados de EM (34%) fueron tratados con los nuevos fármacos orales de primera línea, dimetilfumarato –113 pacientes– o teriflunomida –56 pacientes–: en 44 casos estos fármacos fueron la primera opción terapéutica (56% de los pacientes nuevos de ese año), mientras que en los restantes 125 sustituyeron a otro tratamiento (tabla 1).
Se registraron los cambios que fue preciso realizar en el tratamiento de los pacientes en el transcurso del seguimiento (tabla 2).
Cambios de tratamiento
| De dimetilfumarato a: | De otros fármacos a: | |||
| Teriflunomida | 4 | |||
| Fingolimod | 4 | Interferón Peg. | 38 | |
| Rebif 44® | 2 | Rituximab | 13 | |
| Natalizumab | 2 | Fingolimod | 6 | |
| A. glatirámero | 1 | Natalizumab | 5 | |
| Interferón peg. | 1 | Alemtuzumab | 3 | |
| De teriflunomida a: | Avonex® | 2 | ||
| Dimetilfumarato | 5 | A. Glatirámero | 1 | |
| Interferón peg. | 2 | Rebif 44® | 1 | |
| A. glatirámero | 1 | |||
| Rebif 22® | 1 | |||
| N.° de pacientes (porcentaje) | 23 (14%) | 69 (21%) | p<0,05 |
En negrita, valores con diferencia significativa.
De los 113 pacientes en tratamiento con dimetilfumarato, se cambió a otro fármaco en 14 (12,5%), y de los 56 en tratamiento con teriflunomida hubo cambios en 9 (16%). Considerados conjuntamente, los cambios se realizaron en 23 pacientes (14%), y estuvieron motivados por la aparición de efectos adversos o por la necesidad de utilizar un fármaco de segunda línea ante una mayor actividad de la enfermedad.
De los 332 pacientes que estaban en tratamiento con otros fármacos, estos se modificaron en 69 casos (21%) por los mismos motivos citados previamente.
La proporción de cambios de tratamiento entre los pacientes con dimetilfumarato y teriflunomida fue significativamente menor que en aquellos sometidos a otras terapias (p<0,05).
Adicionalmente, en la tabla 3 se recogen los porcentajes de adherencia al tratamiento con los diferentes fármacos: esta fue superior al 99% con los tratamientos orales –dimetilfumarato, teriflunomida y fingolimod–, cifra ligeramente superior a la obtenida con los fármacos inyectables, si bien las diferencias entre los grupos no fueron estadísticamente significativas.
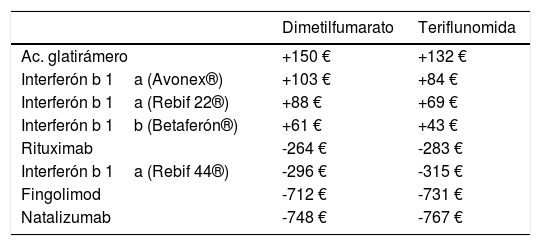
La diferencia de precio neto/dispensación entre los diferentes principios activos o productos se resume en la tabla 4. La dispensación con dimetilfumarato y teriflunomida tiene un coste mayor que con acetato de glatirámero, interferón beta 1a (Avonex® y Rebif 22®) e interferón beta 1b, pero ese coste es menor que con rituximab, interferón beta 1a (Rebif 44®), fingolimod y natalizumab.
Diferencias de precio neto/dispensación (€)
| Dimetilfumarato | Teriflunomida | |
|---|---|---|
| Ac. glatirámero | +150 € | +132 € |
| Interferón b 1a (Avonex®) | +103 € | +84 € |
| Interferón b 1a (Rebif 22®) | +88 € | +69 € |
| Interferón b 1b (Betaferón®) | +61 € | +43 € |
| Rituximab | -264 € | -283 € |
| Interferón b 1a (Rebif 44®) | -296 € | -315 € |
| Fingolimod | -712 € | -731 € |
| Natalizumab | -748 € | -767 € |
Dimetilfumarato/teriflunomida – restantes principios activos.
En la figura 1 se recoge el número de pacientes, el número de dispensaciones y el coste del tratamiento con dimetilfumarato y teriflunomida en el caso de los 125 pacientes que cambiaron desde otro tratamiento, y se compara con el coste que habría supuesto el mantenimiento de la terapia anterior. En conjunto, el ahorro total durante el periodo de seguimiento fue de 169.107,31€.
DiscusiónSe presenta un estudio retrospectivo en el que se pone de manifiesto que la utilización de los nuevos fármacos orales, dimetilfumarato y teriflunomida, ha supuesto una reducción en los costes del tratamiento de la EM, a diferencia de lo que suele ocurrir cuando se incorporan nuevas alternativas terapéuticas.
Estos fármacos se introdujeron en nuestro hospital en 2015. Se han utilizado como fármacos de primera línea, en pacientes de inicio y como alternativa a otros fármacos previamente utilizados por el paciente.
Entre las razones para la elección o sustitución de los fármacos se tienen en cuenta, además de las recomendaciones de prescripción de las guías internacionales1–5, las características individuales de cada paciente entre las que hay que destacar: edad de inicio de la enfermedad, marcadores de pronóstico clínicos, radiológicos y biológicos, sexo, deseo de embarazo, otras comorbilidades, antecedentes y/o presencia de neoplasias y efectos adversos producidos por otros fármacos.
Analizando la totalidad de cambios de tratamiento durante el seguimiento de nuestros pacientes, se observó que estos se produjeron en mayor número entre aquellos que estaban en tratamiento con fármacos diferentes de dimetilfumarato y teriflunomida. Entendemos que es debido, por una parte, a que los pacientes tratados con fármacos inyectables suelen tener más efectos adversos asociados con la administración a largo plazo y demandan otras alternativas, y por otra, a que los pacientes en segunda línea de tratamiento suelen presentar formas de la enfermedad más agresivas y, potencialmente, más susceptibles de precisar cambios.
También se analizó la adherencia terapéutica: definida como el grado en el que el comportamiento del paciente se corresponde con las recomendaciones de su médico, es crucial para obtener el máximo beneficio de un tratamiento9,10. La tasa de adherencia se define como el porcentaje de la dosis prescrita que realmente toma el paciente en un tiempo determinado, y se puede medir por métodos directos e indirectos.
Entre estos últimos está el control de la dispensación, que ha sido el utilizado en este estudio: valora la concordancia de tiempos entre la pauta prescrita y la recogida de medicación, si bien esto no significa que el paciente se administre el tratamiento tal y como se le ha prescrito. Sin embargo, sus resultados se consideran razonablemente objetivos en sistemas que utilizan registros médicos electrónicos y dispensación exclusivamente hospitalaria de los fármacos analizados9, como es nuestro caso.
Las tasas de adherencia entre nuestros pacientes fueron más elevadas en las terapias orales, de primera y segunda línea, que en las inyectables, si bien las diferencias entre los grupos no fueron estadísticamente significativas.
También han sido más elevadas que las publicadas por The Global Adherence Project10. Las diferencias con este estudio podrían radicar en que tanto nuestra población de pacientes como el tiempo de seguimiento han sido menores, si bien consideramos que el sistema coordinado que existe entre la Unidad de Neuroinmunología y el Servicio de Farmacia de nuestro hospital ha podido desempeñar un papel relevante en este sentido: tras cada prescripción por parte de la Unidad de Neuroinmunología, donde se realiza la educación y seguimiento periódico del paciente, el Servicio de Farmacia mantiene una primera entrevista de información sobre el tratamiento y un seguimiento en cada dispensación, estableciéndose un sistema de alerta informática al neurólogo si el paciente no recoge el tratamiento cuando le corresponde. Cuando esto sucede, se entra en contacto con él para averiguar cuál es el problema, tratar de solventarlo y lograr así la mayor adherencia posible en cada caso.
Con respecto a los costes, aunque la diferencia de dimetilfumarato y teriflunomida es mayor con respecto a fingolimod y natalizumab, el número de pacientes que cambiaron de interferón b 1a (Rebif 44®) a los fármacos orales de primera línea, así como algunos cambios indicados desde una segunda línea a dimetilfumarato, han constituido la principal fuente de ahorro que, en nuestro estudio, supera los 169.000€ en 20 meses. A esa cifra habría que añadir el coste que habría supuesto el cambio a fármacos de segunda línea (fingolimod, natalizumab), hecho que se ha podido retrasar y/o disminuir gracias a la disponibilidad de estos nuevos tratamientos.
A pesar de que el precio neto de los nuevos fármacos orales es algo superior a otras terapias de primera línea ya establecidas, este estudio demuestra que la introducción de nuevas alternativas terapéuticas no siempre va asociada a incrementos en los costes.
Dimetilfumarato y teriflunomida, además de aportar alternativas terapéuticas y de ofrecer al paciente, en muchos casos, una mejora en su calidad de vida, en nuestra experiencia han supuesto no ya un incremento sino, por el contrario, una disminución en los costes del tratamiento de la esclerosis múltiple.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.