La hiperglucemia en la diabetes tipo 2 se produce por un defecto combinado en la sensibilidad a la insulina y en la secreción de insulina debido a una progresiva disfunción de las células beta pancreáticas.
El tratamiento inicial de los pacientes con diabetes mellitus (DM) tipo 2 e hiperglucemia moderada debe consistir en la modificación del estilo de vida (dieta y ejercicio físico) que mejora la resistencia a la insulina y secundariamente la capacidad secretora pancreática. Sin embargo, este tratamiento es poco efectivo en muchos pacientes, por lo que se plantea aplicar medidas farmacológicas. Hoy día existe especial preocupación por las cifras de glucemia postprandial, que hasta ahora no estaban tan vigiladas, por la relación que existe entre cifras altas a las dos horas de las comidas y las complicaciones macrovasculares asociadas a la diabetes.
Existen diferentes tipos de antidiabéticos orales según su mecanismo de acción:
1) Inhibidores de la enzima alfa-glucosilasa. Interfieren en la absorción intestinal de hidratos de carbono, disminuyendo la hiperglucemia postprandial al inhibir de forma competitiva la acción de las alfa-glucosilasas intestinales. En este grupo se encuentran la acarbosa y el miglitol, siendo este último una de las novedades en el tratamiento farmacológico de la diabetes tipo 2.
2) Insulín secretores. Los principales son: a) sulfonilureas: 1.a generación (clorpropamida), 2.a generación (glibenclamida, glipizida, glicazida) y 3.a generación (glimepirida), y b) glinidas: nueva generación de insulín secretores, los cuales imitan la secreción fisiológica de la insulina. Existen dos tipos: la repaglinida y la nateglinida.
3) Insulín sensibilizadores. Los principales son:
a) Biguanidas.Son los hipoglucemiantes más anti-guos, aunque muchos se han retirado por el riesgo de acidosis láctica que presentaban. En la actualidad la biguanida comercializada es la metformina. Mejora la sensibilidad a la insulina, inhibe la neoglucogénesis hepática y favorece la captación de glucosa por el tejido adiposo y muscular. Impide ligeramente la absorción de glucosa en el intestino, con lo que los pacientes no engordan o incluso adelgazan de 1 a 5 kilos aproximadamente. No produce hipoglucemias y mejoran el perfil lipídico.
b) Glitazonas. Son un grupo de fármacos descubiertos en la década de los ochenta, cuya estructura química y mecanismo de acción es diferente a otros hipoglucemiantes.
Nuevos inhibidores de la alfa-glucosilasa: el miglitol
Como la acarbosa, interfiere en la absorción intestinal de los hidratos de carbono y disminuye la hiperglucemia postprandial al inhibir de forma competitiva la acción de las alfa-glucosidasas intestinales que desdoblan los oligosacáridos y polisacáridos. Los hidratos de carbono no digeridos son metabolizados por bacterias intestinales en el colon, con formación de ácidos grasos y diversos gases que explican los efectos secundarios frecuentes de estos fármacos (meteorismo, flatulencia, diarreas, etc.).
Sin embargo, se diferencian por su estructura química y características farmacológicas: la acarbosa, introducida hace unos años en el mercado, es un tetrasacárido no absorbible de origen microbiano. El miglitol es un derivado de la desoxinojirimicina, estructuralmente similar a los monosacáridos, que se absorbe en más del 60%, utilizando el mismo transportador intestinal que la glucosa, hecho que no ocurre con la acarbosa. Después de absorberse no se metaboliza y se elimina rápidamente por vía renal. El miglitol es más potente que la acarbosa y es efectivo a dosis relativamente bajas, especialmente en ancianos, lo que parece asociarse a un menor número de efectos adversos.
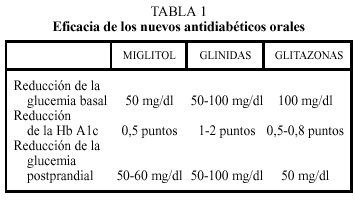
El efecto fundamental es sobre la hiperglucemia postprandial, que disminuye alrededor de 50-60 mg/dl, lo que se refleja en una disminución de la hemoglobina glucada (HbA1c), que disminuye en torno a 0,5 puntos. La hiperglucemia basal también disminuye de forma moderada (50 mg/dl). Los efectos son más importantes si existe hiperglucemia moderada (menor de 200 mg/dl), y si la dieta contiene de forma mayoritaria hidratos de carbono de absorción lenta (tabla 1).
A diferencia de las sulfonilureas, estos fármacos no producen un aumento de la insulinemia ni un aumento ponderal. Su acción predominante sobre la hiperglucemia postprandial puede hacerlos especialmente indicados en fases muy iniciales de la DM tipo 2. Por sí solos no producen hipoglucemia, sólo asociados a sulfonilureas o insulina; en caso de hipoglucemia se debe tratar con glucosa pura (no con sacarosa). Además, aunque las sulfonilureas reducen más los niveles de HbA1c, el miglitol ofrece mayor o similar reducción de los niveles de glucemia postprandial. Pueden combinarse con otros antidiabéticos orales o con insulina en pacientes mal controlados a pesar de la dieta y el tratamiento.
Los efectos adversos asociados al miglitol, como ya hemos adelantado, son generalmente alteraciones gastrointestinales como flatulencia, diarrea o dolor abdominal. La intensidad se relaciona con la dosis y se acentúa por el consumo de hidratos de carbono simples, edulcorantes, legumbres y algunas verduras (coles). Suelen aparecer al principio del tratamiento, disminuyendo con el tiempo y desapareciendo con la retirada del fármaco o con un ajuste de dosis.
El miglitol no tiene efectos significativos sobre el riñón, aparato respiratorio, sistema cardiovascular o sobre los parámetros hematológicos. No precisa ajuste de dosis en pacientes ancianos, en insuficiencia hepática ni en insuficiencia renal leve y moderada. En estos tipos de pacientes es donde estaría más indicado. No producen aumento de peso y se ha observado una disminución del nivel de triglicéridos.
Estaría contraindicado en casos de hipersensibilidad al miglitol y en enfermedades intestinales crónicas. No se aconseja su uso en menores de 18 años, en embarazadas ni en la lactancia.
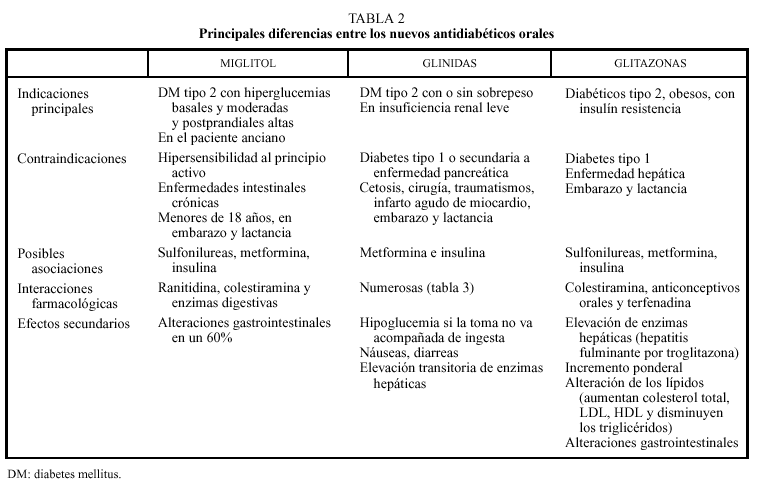
Reducen su efecto la ranitidina y enzimas digestivas. Se presenta en comprimidos de 50 y 100 mg. Se recomienda empezar por 25-50 mg en la comida e ir subiendo semanalmente de 50 en 50 mg hasta llegar a la dosis efectiva de 100 mg en desayuno, comida y cena (300 mg/día). Se debe administrar al inicio de la comida y sin masticar (tabla 2).
Nuevos insulín secretores. Las glinidas
Estimulan la secreción de insulina a partir de las células beta del páncreas, cerrando los canales de potasio sensibles a la adenosina trifosfato (ATP) (igual mecanismo que las sulfonilureas, pero se unen en lugares diferentes). Los canales de potasio (ATP dependientes) se localizan también en células cardíacas, pero las glinidas tienen selectividad por los canales de las células pancreáticas y no por el tejido cardiovascular (a diferencia de las sulfonilureas, que no tienen esta selectividad, pudiendo tener efectos adversos cardiovasculares).
El bloqueo de los canales de potasio despolariza la célula, abriendo canales de calcio, y este aumento del flujo de calcio al interior de la célula induce la secreción de insulina.
Restablecen el perfil fisiológico de la secreción de insulina, provocando la liberación rápida de la insulina almacenada en la célula beta.
Farmacológicamente la repaglinida y la nateglinida son diferentes. La repaglinida es un derivado del ácido carbamoylmethilbenzoico y la nateglinida es un derivado de la D-fenilalanina. Ambos son los primeros reguladores prandiales de la glucosa. La repaglinida ha sido ya comercializada en España y pronto lo hará la nateglinida. Ambas facilitan una liberación rápida de insulina postprandial de las células beta del páncreas, seguida de un descenso veloz de la glucemia. Después de su administración oral es rápidamente absorbida y eliminada. La repaglinida alcanza su Cmáx a la hora de su administración. Se metaboliza en el hígado y se elimina fundamentalmente por vía biliar, por lo que puede ser utilizada en pacientes con insuficiencia renal leve (creatinina menor a 2 mg/dl). A diferencia de las sulfonilureas, producen menos hipoglucemias y controlan las hiperglucemias postpandriales, que contribuyen a aumentar el nivel de hemoglobina glucosilada, el cual es un indicador del nivel de glucemia total.
Se reduce la glucemia en ayunas entre 50 y 100 mg/dl y la glucemia postprandial 50 a 100 mg/dl. Disminuye los niveles de hemoglobina glucosilada de 1 a 2 puntos. Se han realizado estudios en los que la repaglinida y nateglinida han mostrado efecto similar a la glibenclamida en cuanto a disminución de niveles totales de glucosa, aunque fueron superiores a la glibenclamida en la disminución de glucosa postprandial. En cuanto a los estudios en el tratamiento coadyuvante con metformina, se ha comprobado que los niveles de glucosa disminuyen más que con los fármacos administrados por separado.
Se pueden administrar en alérgicos a las sulfonilureas y no se deben dar en casos de diabetes tipo 1 o secundaria, si existe cetosis, cirugía, traumatismos, infarto agudo de miocardio, enfermedades intercurrentes graves, embarazo y lactancia.
El tratamiento se debe iniciar con 0,5 mg de repaglinida quince o treinta minutos antes de cada comida principal (tres veces al día); si el paciente ya tomaba hipoglucemiantes orales empezar con 1 mg (excepto si era metformina). Al cabo de una o dos semanas ajustar la dosis según glucemias. La dosis máxima total diaria no debe exceder los 16 mg. Se presenta en comprimidos de 0,5, 1 y 2 mg. Con respecto a la nateglinida, tendremos que esperar que se comercialice, pero las dosis terapéuticas se situarán entre los 30 y los 120 mg antes de cada comida.
Está indicada en diabetes tipo 2, cuya hiperglucemia no se controla con dieta, ejercicio y disminución de peso o en los tratados con metformina como tratamiento coadyuvante.
Pueden producir como efectos secundarios hipoglucemias leves, trastornos gastrointestinales (diarrea en un 7%), exantema cutáneo, trastornos visuales transitorios, cefalea, ligera elevación de enzimas hepáticas (que no suele requerir la suspensión del tratamiento). En los ensayos clínicos se ha visto una mejor tolerancia con menor incidencia de hipoglucemia respecto a sulfonilureas, así como un mejor perfil de efectos cardiovasculares.
El efecto hipoglucémico de la repaglinida se potencia al administrarse conjuntamente con salicilatos, inhibidores de la monoaminooxidasa, antiinflamatorios no esteroideos, inhibidores de la enzima convertidora de angiotensina, alcohol, ketoconazol, miconazol, eritromicina, sulfonamidas y betabloqueantes, y disminuye con diuréticos tiazídicos, corticoides, anticonceptivos orales, hormona tiroidea y simpaticomiméticos (tablas 1, 2 y 3).
Nuevos insulín sensibilizadores. Las glitazonas o tiazolidinedionas
Son un grupo de fármacos descubiertos en la década de los ochenta, cuya estructura química y mecanismo de acción es diferente a otros hipoglucemiantes. Su mecanismo de acción fundamental es el de mejorar la sensibilidad a la insulina, sobre todo en tejido adiposo, hígado y músculo, a través de la activación específica del receptor gamma de activación de la proliferación del peroxisoma (PPAR-g). La activación de este sistema determina la expresión de proteínas específicas que regulan el metabolismo lipídico y de los hidratos de carbono y provoca un aumento de la acción de la insulina a nivel celular, mejorando la acción de la glucosa. Se metabolizan por vía hepática y tienen eliminación biliar.
Mejoran la glucemia basal un 20% en individuos moderadamente diabéticos y una disminución de la HbA1c de 0,5 a 0,8 puntos. Disminuyen la glucemia basal unos 100 mg/dl y la postpandrial unos 50 mg/dl. Simultáneamente, mejoran los otros componentes del síndrome metabólico, como la tensión arterial, la dislipidemia y la hiperinsulinemia. Estos efectos también se observan en individuos no diabéticos con el síndrome metabólico X. No producen hipoglucemia. Poseen, además, efecto sinérgico con sulfonilureas, metformina o insulina.
Pueden interaccionar con la colesteramina, los anticonceptivos orales y la terfenadina. No produce intolerancia digestiva ni hepática. Se indican en pacientes obesos con insulinorresistencia tanto en monoterapia como en asociación con sulfonilureas, metformina o insulina (pueden disminuir adicionalmente la HbA1c de 0,9 a 1,8 puntos). Su efectividad es menor que las sulfonilureas y que la metformina, con lo que no las sustituyen como fármacos de primera línea.
Los principales problemas son el aumento de peso con el que se asocian, que puede representar un 3% al inicio del tratamiento, y que la mejoría del control glucémico no es espectacular. De las glitazonas estudiadas, la troglitazona, que se comercializó en diversos países, produjo varios casos de fallo hepático grave. La rosiglitazona y la pioglitazona ya han sido aprobadas por la Food and Drug Administration (FDA) en América y pronto se comercializarán en España. Se ha observado un aumento de las enzimas hepáticas (alamina aminotransferasa [ALT] tres veces superior a lo normal) en el 1% de los pacientes, por lo que la FDA recomienda hacer determinaciones de enzimas hepáticas y bilirrubina antes de comenzar el tratamiento, mensualmente los primeros 6 meses, cada 2 meses hasta el año y posteriormente de forma
periódica. Puede producirse un aumento del colesterol total y LDL del 10%-15%, de HDL del 5%-10% y una reducción de triglicéridos del 15%-30%. Otros efectos secundarios son diarrea, vómitos, náuseas, flatulencia y alteraciones hematológicas leves.
El tratamiento se iniciaría con un comprimido al día en la comida y aumentar hasta dos comprimidos en dos tomas (tablas 1 y 2).
Bibliografía recomendada
American Diabetes Association. The pharmacological treatment of hiperglycemia in NIDDM. Diabetes Care 1995; 18:1.510-1.518.
Evans AJ, Krentz AJ. Recent developments and emerging therapies for type 2 diabetes mellitus. Drugs 1999; 2:75-94.
Hatorp V, Thomsen MS. Drug interaction studies with repaglinide: repaglinide on digoxine or theophyline pharmacokinetics and cimetidine on repaglinide pharmacokinetics. J Clin Pharmacol 2000; 40: 184-192.
Hu S, Wang S, Dunning BE. Tissue selectivity of antidiabetic agent nateglinide: study on cardiovascular and beta-cell K (ATP) channels. J Pharmacol Exp Ther 1999; 291:1.372-1.379.
Jovanovic L, Dailey G, Huang WC, Strang P, Goldsteing B. Repaglinidein type 2 diabetes: a 24-week, fixed-dose efficacy and safety study. J Clin Pharmacol 2000; 40:49-57.
Keilson L, Mather S, Walter YH, Subramanian S, McLeod JF. Synergistic effects of nateglinide and meal administration on insulin secretion in patients with type 2 diabetes mellitus. J Clin Endocrinol Metab 2000; 85:1.081-1.086.
Marbury TC, Ruckle JL, Hatorp V, Andersen MP, Nielsen KK, Huang WC, et al. Pharmacokinetics of repaglinide in subjects with renal impairment. Clin Pharmacol Ther 2000; 67:7-15.
Mooradian AD, Thurman JE. Drug therapy of postpandrial hyperglycaemia. Drugs 1999; 57:19-29.
Moses R. Repaglinide in combination therapy in type 2 diabetes. Diabetes Metab 1999; 25 (suppl 7):26-27.
Mozersky RP. Pharmacologic management of diabetes mellitus. J Am Osteopath Assoc 1999; 99 (suppl 12):15-19.
Scott LJ, Spencer CM. Miglitol: a review of its therapeutic potential in type 2 diabetes mellitus. Drugs 2000; 59:521-524.
Verges B. The impact of regulation of postprandial glucose in practice. Diabetes Metab 1999; 25 (suppl 7):22-25.