La enfermedad cardiovascular secundaria a aterosclerosis es la principal causa de morbilidad y mortalidad en el mundo. La estratificación del riesgo cardiovascular ha demostrado ser una aproximación insuficiente para detectar aquellos sujetos que van a padecer un evento cardiovascular por lo que desde hace años se buscan otros marcadores que ayuden a estratificar cada individuo con mayor precisión, la ecografía vascular en dos dimensiones es un excelente método para la evaluación de riesgo vascular.
Cardiovascular disease secondary to atherosclerosis is the main cause of morbidity and mortality in the world. Cardiovascular risk stratification has proven to be an insufficient approach to detect those subjects who are going to suffer a cardiovascular event, which is why for years other markers have been sought to help stratify each individual with greater precision. Two-dimensional vascular ultrasound is a excellent method for vascular risk assessment.
La enfermedad cardiovascular (ECV) secundaria a la aterosclerosis sigue siendo la principal causa de morbilidad y mortalidad en el mundo. Este proceso se desarrolla progresivamente y de forma silente desde los primeros años de vida y se distribuye a lo largo de todo el árbol arterial acelerándose con la presencia de determinados factores de riesgo cardiovascular (FRCV)1,2. La estratificación del riesgo cardiovascular (RCV) de un individuo basado en el efecto de estos FRCV (sexo, edad, presión arterial, dislipidemia, presencia de diabetes o historia de tabaquismo) han demostrado ser una aproximación insuficiente para detectar con suficiente sensibilidad y especificidad aquellos sujetos que van a padecer un evento cardiovascular (ECV) en forma de cardiopatía isquémica, enfermedad cerebrovascular o enfermedad arteria periférica. Según estas guías, uno de cada cinco varones, y casi la mitad de las mujeres que sufren ECV, no tendrían indicación para iniciar tratamiento hipolipemiante en prevención primaria por lo que desde hace años se buscan otros marcadores que ayuden a estratificar el RCV de cada individuo con mayor precisión3.
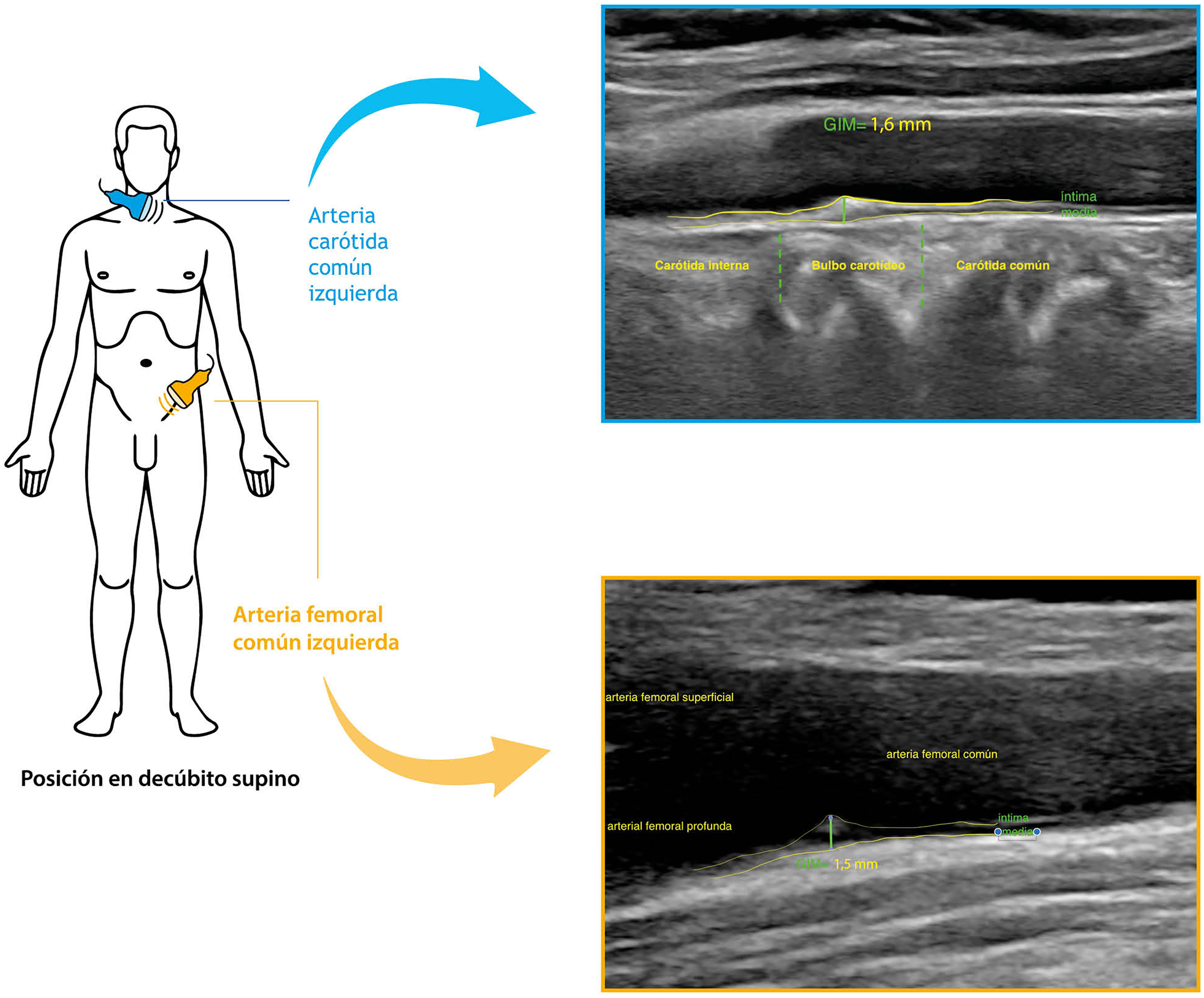
La ecografía vascular como método de detección de arteriosclerosis subclínicaEl desarrollo tecnológico asociado a las ciencias biomédicas ha permitido observar la evolución natural de las lesiones arterioscleróticas de forma no invasiva1,2. La ecografía vascular en dos dimensiones (ECOV-2D) permite observar y cuantificar lesiones desde fases iniciales, mediante el grosor de la pared arterial (GIM), definido como la distancia entre la capa íntima, en la interfase entre la luz arterial y el inicio de la pared arterial y el final de la capa media, en el límite entre las capas media y adventicia (fig. 1). El aumento del GIM de la arteria carótida se ha relacionado de forma directa con la incidencia de ECV en estudios poblacionales1,2, ya en el año 2006 se estableció por consenso la definición de lesión avanzada o placa de ateroma en arteria carótida, aquella con un GIM≥1,5mm o con un engrosamiento> 50% respecto a los segmentos adyacentes1,4. La presencia de placa de ateroma en arteria carótida ha demostrado tener una asociación robusta e independiente con la incidencia de ECV en la población general de mediana edad5,6, al ser su aparición más precoz en las poblaciones con mayor RCV, tales como en sujetos con dislipidemias primarias7, diabetes8 o con un único FRCV de larga evolución como el tabaquismo9. Recientemente, tanto la Sociedad Europea de Cardiología como la de Aterosclerosis han reconocido la presencia de placa en la pared de arteria carótida mediante ECOV-2D como una lesión ateroesclerótica avanzada que obligaría a reclasificar el RCV de un determinado individuo10.
La evaluación de la arteria femoral mediante ECOV-2D ha sido igualmente accesible para la exploracion, incluida en la valoracion de aterosclerosis subclinica hasta años recientes. La presencia de placa en esta localización se ha demostrado más frecuente y precoz que en la arteria carótida, especialmente en varones fumadores5,7–9, además de tener una asociación mayor con FRCV y con el calcio coronario que las placas en la arteria carótida8,9. Estudios prospectivos han demostrado el valor aditivo en la predicción de ECV de la detección conjunta de aterosclerosis en territorio carotídeo y femoral5,9.
¿Cómo se hace?Protocolo de exploración: equipo, posición del paciente y sistemática de la técnicaLas ecografías de arterias carótidas y femorales se realizan preferentemente con un ecógrafo que disponga de una sonda lineal de alta frecuencia (≥ 7MHz) que permita obtener imágenes de calidad aceptable con una profundidad del campo de entre 3 y 4cm, aplicándose una ganancia media de 60 dB1, si bien incluso dispositivos portátiles han demostrado capacidad para la detección de placas en la pared arterial.
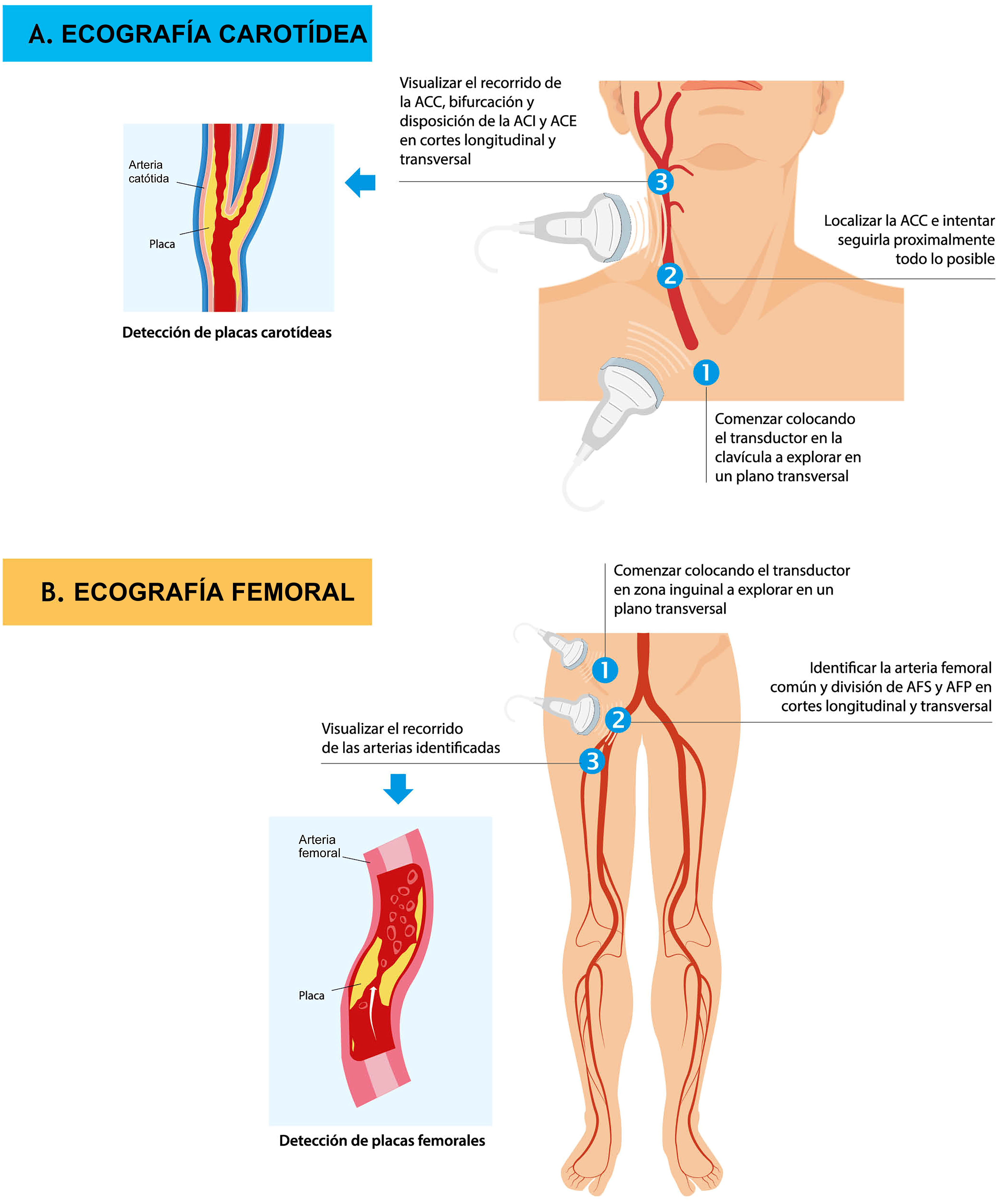
Ecografía de arteria carótida: para obtener la imagen debemos colocar al paciente en decúbito supino, con el cuello extendido y con una inclinación de 45° en dirección contraria al área explorada. El profesional que realiza la prueba se coloca a la cabecera del paciente, bien de frente o por detrás del mismo. Se inicia la exploración con un barrido transversal en modo B, desde la base del cuello justo por encima de la clavícula en dirección ascendente hasta llegar a la mandíbula, localizando la arteria carótida en el centro de la pantalla (fig. 2). Debemos mantener en todo momento el transductor perpendicular al plano de la piel y con el marcador de la sonda mirando a la izquierda. Este barrido permite una primera evaluación de la presencia de placas, algunas no detectadas en la proyección longitudinal por estar situadas en una zona de la pared no perpendicular a la proyección utilizada. Posteriormente, tras girar el transductor 90° en sentido horario, se visualiza el mismo segmento arterial en proyección longitudinal. En esta proyección podremos conseguir una imagen de ambas paredes de la arteria, aunque en general se obtienen imágenes más nítidas de la pared posterior de todo el trayecto de la arteria carótida común (ACC) y el inicio de sus ramas principales, que nos permitan una cuantificación rápida del GIM (fig. 1).
El primer segmento arterial que se visualiza en el barrido transversal corresponde al final de la ACC que se distingue por tener un calibre regular y por localizarse justo antes de que este aumente el calibre de la arteria, conocido como bulbo carotídeo (BC). Este segmento se delimita entre el final de la ACC y la ramificación en arteria carotídea externa y arteria carotídea interna. El BC es visible en la inmensa mayoría de los pacientes y es donde con más frecuencia se detectan placas de ateroma (fig. 1) por lo que, salvo en casos de dificultad anatómica, nunca debería quedar sin explorar1,4,5. Para localizar las ramas de la arteria carótida podemos valernos de su localización, estando la arteria carótida interna con más frecuencia en un plano superior y medial en la proyección transversal, mientras que la arteria carótida externa se localiza en el plano inferior y lateral.
Ecografía de arteria femoral: la arteria femoral se encuentra en una posición medial respecto a la vena, inmediatamente debajo del ligamento inguinal y por encima del plano muscular del músculo iliopsoas. La vena tiene un diámetro mayor y se deja colapsar con una moderada compresión, mientras que la arteria pone de manifiesto su característica pulsátil durante la compresión.
Para realizar la exploración debemos colocar al paciente en decúbito supino descubriendo la zona inguinal con el explorador situado lateralmente al paciente. El examen se realiza en dos pasos: el primero, una vez localizada la arteria por palpación, con el transductor perpendicular al plano de la piel y con el marcador de la sonda mirando a la derecha, es realizar un barrido transversal desde la zona inguinal en dirección caudal identificando el segmento distal de la arteria femoral común (AFC) y su bifurcación en la arteria femoral superficial y profunda (fig. 2). Una vez realizado el barrido transversal, giramos la sonda 90°, con la punta del transductor en dirección caudal, de modo que podemos ver la proyección longitudinal del segmento distal de la AFC seguido de su bifurcación, que da lugar a las arteria femoral superficial y profunda. El objetivo es obtener una imagen de la arteria lo más horizontal posible de la pared posterior del segmento más distal de la AFC y el inicio de la bifurcación, ya que en esta localización también se detectan placas de ateroma con mayor frecuencia que el resto de segmentos explorados de la arteria femoral.
Tanto en la arteria carótida como femoral, en caso de encontrarnos con una lesión compleja la ecografía, no es el mejor procedimiento para su caracterización, y deberían valorarse otras exploraciones de imagen que quedan fuera de los objetivos de este artículo.
¿A quién se aconseja realizar?La exploración mediante ECOV-2D para la detección de placas de ateroma en arteria carótida y femoral tiene sentido solo en aquellos sujetos en prevención primaria de ECV. El screening de estas lesiones estará indicado en aquellos en los que sea probable su detección y en los que la presencia de placas supondrá una intensificación del tratamiento preventivo, farmacológico y del estilo de vida. El efecto de dichos tratamientos sobre estas lesiones es algo que discute la comunidad científica hoy en día y está fuera del objetivo de este protocolo. Además no ha de desestimarse el valor disuasorio de su visualización para la cumplimentación del tratamiento farmacológico por parte del paciente1–3.
Los datos observacionales obtenidos en estudios y la necesidad de mejorar la estratificación del RCV aconsejan realizar la ECOV-2D de la arteria carótida y femoral en los siguientes grupos:
- 1.
Personas mayores de 45 años con riesgo intermedio1,6,9.
- 2.
Personas que presenten un factor de riesgo extremo (p. ej., hipercolesterolemia primaria) que puede modificar sustancialmente su RCV8.
- 3.
Personas con diabetes, especialmente al inicio del diagnóstico o sin otros marcadores de RCV8.
- 4.
Sujetos clasificados como de alto RCV (no de muy alto RCV) sin ECV clínica6,10.
- 5.
Personas con dudas para iniciar tratamiento en prevención primaria5,6.
La detección de placas en arterias de mediano calibre ha demostrado ser un método de imagen inocuo que mejora la estratificación del RCV. Esta exploración, por su poder, su alto valor predictivo, bajo coste e inocuidad podría implementarse en la valoración inicial del RCV de todos los pacientes en nuestra práctica clínica habitual.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.