La electrocoagulación con argón plasma (EAP) es una técnica segura y efectiva, ampliamente utilizada para el tratamiento de lesiones vasculares a nivel gastrointestinal, pudiendo considerarse como técnica de elección en el manejo de estas1.
La enfermedad de Rendu-Osler-Weber es una afección caracterizada por la aparición de malformaciones arteriovenosas en piel, mucosas y diversos órganos, presentando típicamente sangrados a nivel gastrointestinal. La EAP ha demostrado ser una técnica eficaz en el tratamiento de estos pacientes2,3.
Está descrito que el contacto de la sonda con la mucosa o el alto flujo de argón puede llegar a producir un escape de gas a través de la pared gastrointestinal o incluso, en algunos casos, puede llegar a producir una perforación de víscera hueca4.
La presencia de neumoperitoneo tras la EAP puede ser asintomática y deberse al paso de gas a través de la pared gastrointestinal, pudiendo ser de elección en muchos casos el tratamiento conservador5,6.
Presentamos un caso de neumoperitoneo masivo tras EAP tratado mediante manejo conservador con imágenes demostrativas.
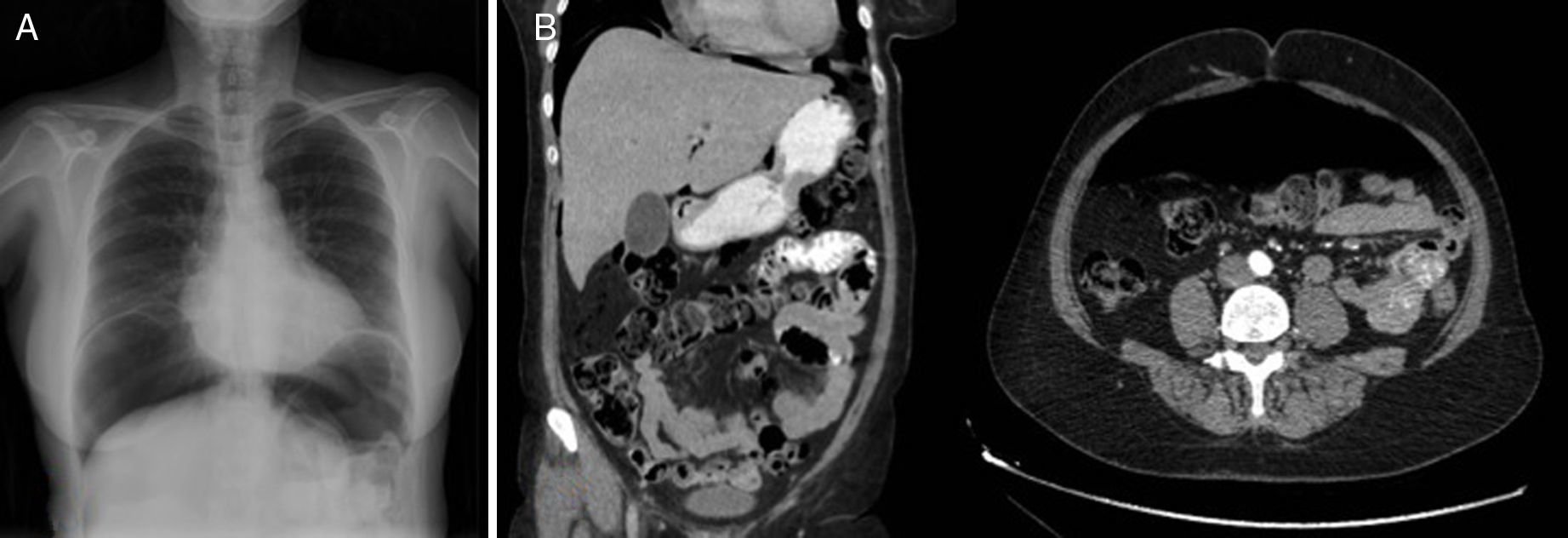
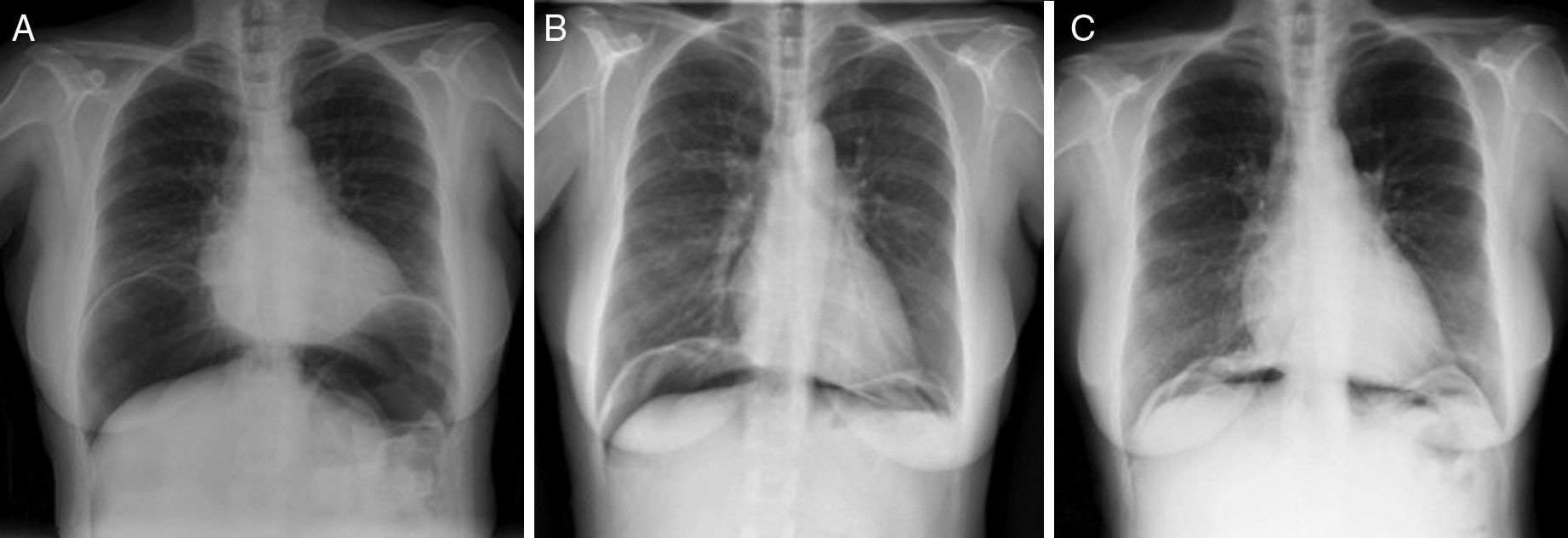
Se trata de una mujer de 57 años, en tratamiento con EAP (Argon ERBE APC-300) por angiodisplasias gástricas y duodenales, secundarias a enfermedad de Rendu-Osler-Weber. Tras una sesión acude a urgencias por distensión abdominal y dolor epigástrico de 12h de evolución. Presenta un abdomen distendido, levemente doloroso, sin signos de irritación peritoneal. En la radiografía torácica presenta neumoperitoneo masivo (fig. 1). En la TC con triple contraste se evidencia abundante neumoperitoneo sin líquido libre, no identificando zona de dehiscencia y sin objetivar extravasación de contraste oral hidrosoluble (fig. 1). Durante su estancia en urgencias se realizan analíticas seriadas sin elevación de reactantes de fase aguda, permaneciendo la paciente asintomática. Ante los hallazgos clínico-analítico-radiológicos se decide observación y manejo mediante tratamiento conservador con dieta absoluta, sonda nasogástrica y ertapenem 1g iv/24h. Fue dada de alta a los 6 días sin presentar complicación alguna durante el ingreso. Tras el alta, se hizo un seguimiento clínico-radiológico, que evidenció una reducción gradual del volumen de aire intraabdominal (fig. 2).
A) Radiografía de tórax AP en la que se observa un neumoperitoneo masivo. B) Cortes coronal y sagital de la TC en la que se aprecia abundante neumoperitoneo sin observarse presencia de contraste oral extraluminal. No se observa líquido libre intraperitoneal ni colecciones organizadas.
En la literatura, son pocos los casos descritos de neumoperitoneo masivo tras EAP, 3 en el manejo de pólipos en colon y 2 en el tratamiento de angiodisplasias. En 3 de estos pacientes se realizó un tratamiento conservador sin complicaciones, mientras que en los otros 2 se llevó a cabo una laparotomía exploradora inicialmente sin objetivarse perforación alguna5-7. Probablemente se producen muchos más casos de neumoperitoneo tras EAP de los que se describen. Si se realizaran radiografías abdominales sistemáticas tras cada tratamiento, nos encontraríamos con un número elevado de casos de neumoperitoneo asintomáticos6.
Ante el hallazgo de neumoperitoneo tras EAP no se debe considerar automáticamente que nos encontramos ante la presencia de una perforación de víscera hueca, si no que puede estar causado por el paso de gas a través de la pared gastrointestinal5,6. Resulta imprescindible identificar aquellos pacientes que presentan una perforación de víscera hueca y que requerirán una intervención quirúrgica urgente, y diferenciarlos de aquellos con un acúmulo de aire intraabdominal que simula una perforación, pero que realmente está causado por el paso del gas a través de la pared gastrointestinal, en los que puede plantearse un manejo conservador5,6. Se considera que en estos últimos el tratamiento conservador podría ser de elección, reservando la cirugía urgente para aquellos pacientes con signos de irritación peritoneal o hallazgos clínicos-analíticos de sepsis6. En series como la de Kwan et al. o Manner et al. no se han descrito casos de perforación de víscera hueca asociada a la EAP, sin embargo, Grund et al. describen una tasa del 0,31% de perforaciones accidentales1,4,7.
La TC es considerada la técnica diagnóstica de elección ante la sospecha de perforación de víscera hueca8–10. Como principales signos de perforación destacan la identificación de un defecto en la pared intestinal y la presencia de gas o contraste oral extraluminal8. El tiempo transcurrido desde la perforación hasta la realización de la TC no condiciona su precisión diagnóstica9. La extravasación de contraste oral es un signo directo de perforación con una alta especificidad, pero muy baja sensibilidad. Su ausencia no excluye la presencia de perforación8,10.
El gas argón se reabsorbe lentamente, por lo que la persistencia a largo plazo de aire a nivel intraabdominal no debe considerarse como un signo de alarma. El tratamiento conservador de estos pacientes puede mantenerse con seguridad siempre y cuando el paciente permanezca asintomático, sin peritonismo y se observe una disminución progresiva del volumen de aire intraabdominal6,7. Según la literatura se describe una reducción del volumen de aire intraabdominal al mes y una desaparición completa a los 3 meses de seguimiento5. En el caso de nuestra paciente, 15 días después se apreciaba una marcada disminución del aire intraabdominal, habiendo prácticamente desaparecido al mes.
En conclusión, en los casos de neumoperitoneo tras EAP resulta imprescindible distinguir entre el causado por el paso de gas a través de la pared gastrointestinal y el secundario a una perforación de víscera hueca. Como en el caso presentado, ante un paciente escasamente sintomático, sin signos de irritación peritoneal ni datos de sepsis y sin hallazgos radiológicos concluyentes, el tratamiento de elección consistirá en un manejo conservador, sin riesgo de desarrollar complicaciones.
Este caso clínico fue presentado como póster en la XXIII Reunión Anual de la Asociación de Cirujanos del Norte, Laredo, 6 de mayo de 2016.