La enfermedad aterosclerótica de la aorta ascendente es una circunstancia vinculada al desarrollo de eventos neurológicos en el postoperatorio de cirugía de revascularización miocárdica (CRM). La utilización de una técnica sin circulación extracorpórea (CEC) y con puentes compuestos y/o in situ que eviten la manipulación de la aorta (no touch) disminuiría este riesgo.
ObjetivoEl objetivo de nuestro trabajo fue evaluar la evolución de seis pacientes sometidos a CRM sin CEC con técnica no touch.
Material y métodosEntre 2005–2007, 229 pacientes fueron sometidos a CRM sin CEC. En seis casos, por calcificación de la aorta se realizó el procedimiento con técnica no touch. La arteria mamaria interna izquierda (AMII) se utilizó para revascularizar la descendente anterior y la mamaria interna derecha (AMID) como injerto libre en y sobre la Amii para revascularizar la circunfleja. La vena safena fue anastomosada con el pedículo remanente de la AMID y se utilizó para realizar un puente a la coronaria derecha en cinco casos y a la arteria diagonal en el restante. se realizó seguimiento angiográfico a 6 meses y clínico a 15 meses.
ResultadosEn el postoperatorio ningún paciente presentó eventos neurológicos, todos fueron dados de alta, y en el seguimiento se encuentran asintomáticos y no han requerido reintervenciones. Por angiografía todos los puentes permanecen permeables.
ConclusiónEsta variante quirúrgica de la CRM sin CEC con técnica no touch parece ser una opción eficaz para pacientes con enfermedad coronaria y calcificación de la aorta.
Atherosclerosis of the ascending aorta is a risk factor for the development of neurological events in the postoperative period after coronary artery bypass graft. The use of an off pump technique with composite and/or in situ bypass avoi ding manipulation of the aorta («no touch») might reduce the said risk.
ObjectiveThe objective of the study was to evaluate the outcome of 6 patients who underwent off pump surgical myocardial revascularization with the «no touch» technique.
Material and methodsBetween 2005-2007, 229 patients underwent off pump revascularization. The «no touch» technique was used in 6 cases due to calcification of the aorta. The left internal mammary artery (LIMA) was used to revascularize the left anterior descending artery and the internal right mammary artery (RIMA) was used for the circumflex artery. the saphenous vein was anastomosed with the remaining pedicle of the RIMA, and was used for bypass grafting to the posterior descending artery in 5 cases and to the remaining diagonal artery. Follow up angiograms were performed at 6 months.
ResultsNo patient developed neurological events during the post-op period. All the patients were discharged, and at 15-month follow-up they are all asymptomatic, and have not required any further intervention. All grafts are patent.
ConclusionOff-pump revascularization with the «no touch» technique appears to be an effective surgical option for patients with coronary artery disease and calcification of the aorta.
La cirugía de revascularización miocárdica convencional (CRMcc) posee un beneficio conocido y ampliamente aceptado sobre el tratamiento médico en cuanto a mejoría de la sobrevida y sintomatología1. Este procedimiento, sin embargo, se asocia a un riesgo de mortali dad que varía de un 2-5% y no está exento de complicaciones tales como: requerimiento de transfusiones (50–90%), fibrilación auricular (30%), trastornos neurocognitivos (50–75%) y accidente cerebrovascular (2%)2–5. Las implicancias adversas de la CRMcc han sido atribuidas al circuito de CEC, al paro cardíaco cardiopléjico y a la manipulación de la aorta6; por lo tanto, una alternativa terapéutica como la CRM sin CEC (CRMsc) ha ganado popularidad en los últimos años. Los múltiples beneficios clínicos y económicos de la CRMsc comparada con la CRMcc7,8 en la actualidad siguen siendo fuente de debate, como lo muestran Cheng, et al.9 en su reciente metaanálisis, en el cual concluyen que la CRMsc, por un lado, no reduce significativamente la mortalidad ni la in cidencia de accidente cerebrovascular, infarto de miocardio o disfunción renal; sin embargo, a 30 días, se apre cia una tendencia clínica favorable atenuando la recurrencia de fibrilación auricular, requerimiento de inotrópicos y transfusiones sanguíneas, sin aumentar el riesgo para el paciente y reduciendo la utilización de recursos socioeconómicos.
Durante el procedimiento, la elección de los tipos de conductos (arteriales vs venosos), así como también de su configuración y sitio de inserción proximal es un tema que se encuentra en permanente investigación y desarrollo a fin de mejorar los resultados de la técnica más uti lizada para tratar la enfermedad coronaria de múltiples vasos. A largo plazo, los puentes con vena safena han demostrado tener baja tasa de permeabilidad y han fallado en mejorar la morbimortalidad10. Por el contrario, desde hace más de dos décadas se ha estado utilizando la arteria mamaria interna izquierda (AMII), la cual ha demostrado tener excelentes resultados clínicos y superior tasa de permeabilidad11–13. Recientemente se ha demostrado, con un seguimiento a 20 años, que los beneficios de la utilización de la AMI se pueden potenciar realizando con dicha arteria múltiples puentes a los distintos sistemas coronarios (descendente anterior, circunfleja y coronaria derecha)13.
Para aumentar la disponibilidad de conductos se utilizan otras arterias tales como: mamaria derecha (AMID), ra dial (AR) y gastroepiploica (GE) asociadas o no a puentes venosos; esto ha permitido implementar una técnica de revascularización con puentes compuestos y secuenciales, con lo cual se puede realizar mayor número de anastomosis distales evitando las anastomosis proximales en la aorta14,15. La enfermedad aterosclerótica significativa de la aorta ascendente es uno de los principales factores de riesgo para el desarrollo de eventos adversos neurológicos en el postoperatorio, por lo tanto, la modificación de la estrategia quirúrgica evitando la manipulación de la aorta mediante la implementación de la técnica no touch descrita por Mills y Everson16 podría ser de vital importancia en pacientes de alto riesgo, como son aquellos con enfermedad coronaria asociada a: enfermedad carotídea, enfermedad de aorta abdominal significativa, lesión de tronco de coronaria izquierda o irregularidades de la pared de la aorta ascendente.
Si bien en la actualidad existen escasas comunicaciones acerca de la utilización en forma conjunta de CRMsc con técnica no touch y con el empleo de puentes compuestos, in situ o secuenciales17–19, el objetivo de este trabajo es presentar nuestra experiencia con una asociación de CRMsc y técnica no touch, en la cual se utilizó un sitio alternativo para la realización de la anastomosis venosa proximal.
Material y métodosPacientesDurante el periodo comprendido entre julio de 2005 y agosto de 2007, 229 pacientes fueron sometidos a CRMsc en la Fundación Favaloro Hospital Universitario (Buenos Aires, Argentina).
El grupo evaluado recibió un promedio de 3,2±0,7 puentes/paciente. La RM fue realizada con conductos arteriales y venosos en todos los casos; en un 20% de ellos se utilizaron más de dos anastomosis distales arteriales/paciente. En 223 pacientes los conductos venosos se utilizaron como puentes aortocoronarios, mientras que en los seis pacientes restantes se constató calcificación grave de la aorta ascendente, por lo que se decidió realizar la CRM con puentes arteriales y venosos compuestos y secuenciales con técnica no touch. En estos seis casos se utilizaron ambas arterias mamarias como conductos arteriales y la vena safena como conducto venoso. La anastomosis venosa proximal se realizó en el pedículo in situ de la AMID. La RM no fue arterial pura porque los pacientes presentaban malos lechos a nivel de la arteria coronaria derecha y, como es bien conocido, la mala calidad y/o las obstrucciones moderadas del vaso nativo son factores predictivos de baja tasa de permeabilidad del puente arterial a medio plazo.
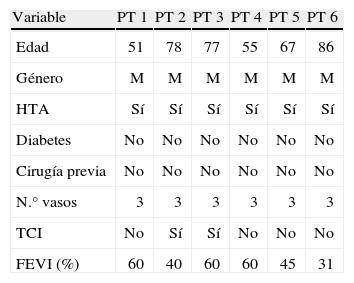
Las características basales de la población pueden observarse en la tabla I. Los seis pacientes pertenecían al género masculino y la media de edad de los mismos fue de 69±13,8 años. Se constató enfermedad coronaria difusa con lesiones graves de los tres vasos epicárdicos en todos los pacientes, y sólo en dos se asoció lesión grave de tronco de coronaria izquierda. En tres pacientes la función sistólica del ventrículo izquierdo se constató como conservada, en dos moderada, y sólo un paciente presentó deterioro importante de la misma. Del total de procedimientos quirúrgicos tres se realizaron en forma electiva y tres en condiciones de urgencia.
Características Basales de la Población
| Variable | PT 1 | PT 2 | PT 3 | PT 4 | PT 5 | PT 6 |
| Edad | 51 | 78 | 77 | 55 | 67 | 86 |
| Género | M | M | M | M | M | M |
| HTA | Sí | Sí | Sí | Sí | Sí | Sí |
| Diabetes | No | No | No | No | No | No |
| Cirugía previa | No | No | No | No | No | No |
| N.° vasos | 3 | 3 | 3 | 3 | 3 | 3 |
| TCI | No | Sí | Sí | No | No | No |
| FEVI (%) | 60 | 40 | 60 | 60 | 45 | 31 |
HTA: hipertensión arterial; TCI: lesión de tronco de coronaria izquierda; FEVI: fracción de eyección ventricular izquierda.
La evaluación preoperatoria de los pacientes que van a ser sometidos a CRM no incluye ningún método diagnóstico que constate rutinariamente la presencia de enfermedad aterosclerótica grave de la aorta ascendente; por este motivo, es durante el acto quirúrgico que debe realizarse dicho diagnóstico a fin de tomar las dedebidas precauciones para minimizar el riesgo de embolia. La evaluación radiológica y angiográfica preoperatoria permitió sospechar la presencia de enfermedad de la aorta ascendente en tres pacientes de la serie, y en los tres restantes la palpación intraoperatoria y la ecografía epiaórtica (sonda de 7,5 MHz [5500 Hewlett-Packard, Seattle, WA, USA]) confirmaron la presencia de calcificaciones.
Técnica anestésica y técnica quirúrgicaLa premedicación anestésica se realizó con loracepam la noche anterior al procedimiento. La inducción con midazolam 0,07–0,1 mg/kg, citrato de fentanilo 5–7μg/kg y bromuro de pancuronio 0,1mg/kg. Para el mantenimiento se utilizó una técnica anestésica combinada con fármacos inhalatorios (isofluorano) y endovenosos (propofol, fentanilo). Para obtener un adecuado monitoreo clínico y hemodinámico de los pacientes, en todos los casos se colocaron al menos un acceso venoso central y un acceso arterial radial. En los pacientes que presentaban deterioro apreciable de la función sistólica del ventrículo izquierdo (FSVI) se colocó un catéter de Swan-Ganz. También se controlaron en forma permanente el trazado electrocardiográfico, la oximetría de pulso y el ritmo urinario.
El abordaje quirúrgico fue a través de esternotomía mediana en los seis pacientes. Se disecaron ambas AMI pediculizadas y la vena safena interna. Se administró heparina en dosis de 2mg/kg unos minutos antes de la oclusión coronaria. Como estabilizador se utilizó el modelo Octopus® (Medtronic Inc, Minneapolis, USA) y las derivaciones intracoronarias fueron Clearview® (Medtronic Inc, Minneapolis, USA). El corazón fue movilizado y posicionado para alcanzar la revascularización de los territorios de las arterias coronaria derecha y circunfleja mediante el posicionador Starfish® (Medtronic Inc, Minneapolis, USA). Para las anastomosis con mamaria se utilizó polipropileno 8/0 y para las anastomosis con vena safena polipropileno 7/0.
En los seis pacientes la AMII se utilizó para revascularizar la arteria descendente anterior y la AMID como injerto libre con anastomosis proximal terminolateral (en Y) en la AMII para revascularizar la arteria circunfleja. La vena safena interna fue anastomosada en forma terminoterminal con el pedículo remanente de la AMID con sutura continua de polipropileno 8/0; el extremo distal de este puente se destinó en cinco casos a la rama descendente posterior (de la arteria coronaria derecha), y en el caso restante se revascularizó la primera rama diagonal. Una vez finalizado el procedimiento se revirtió la heparinización con protamina.
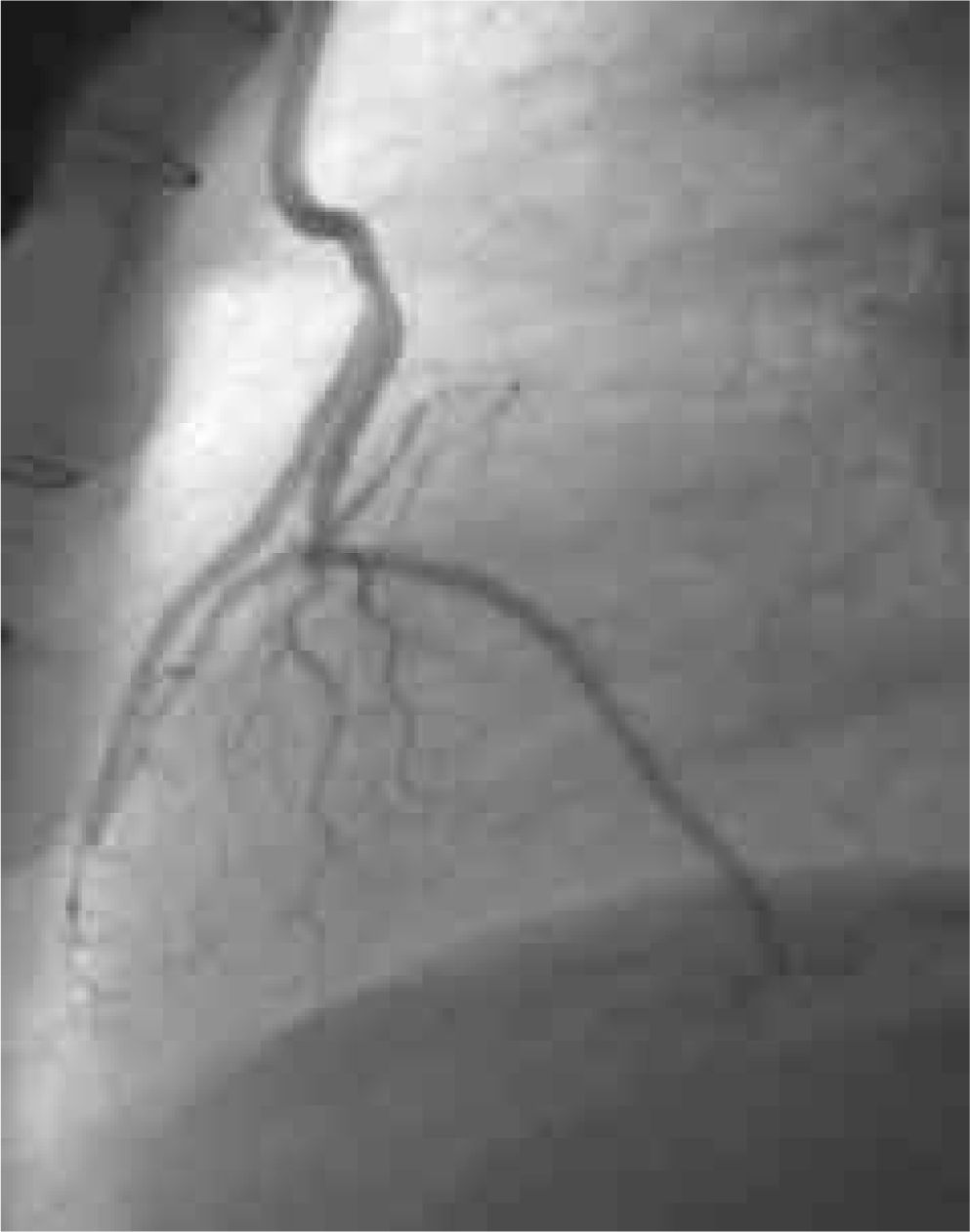
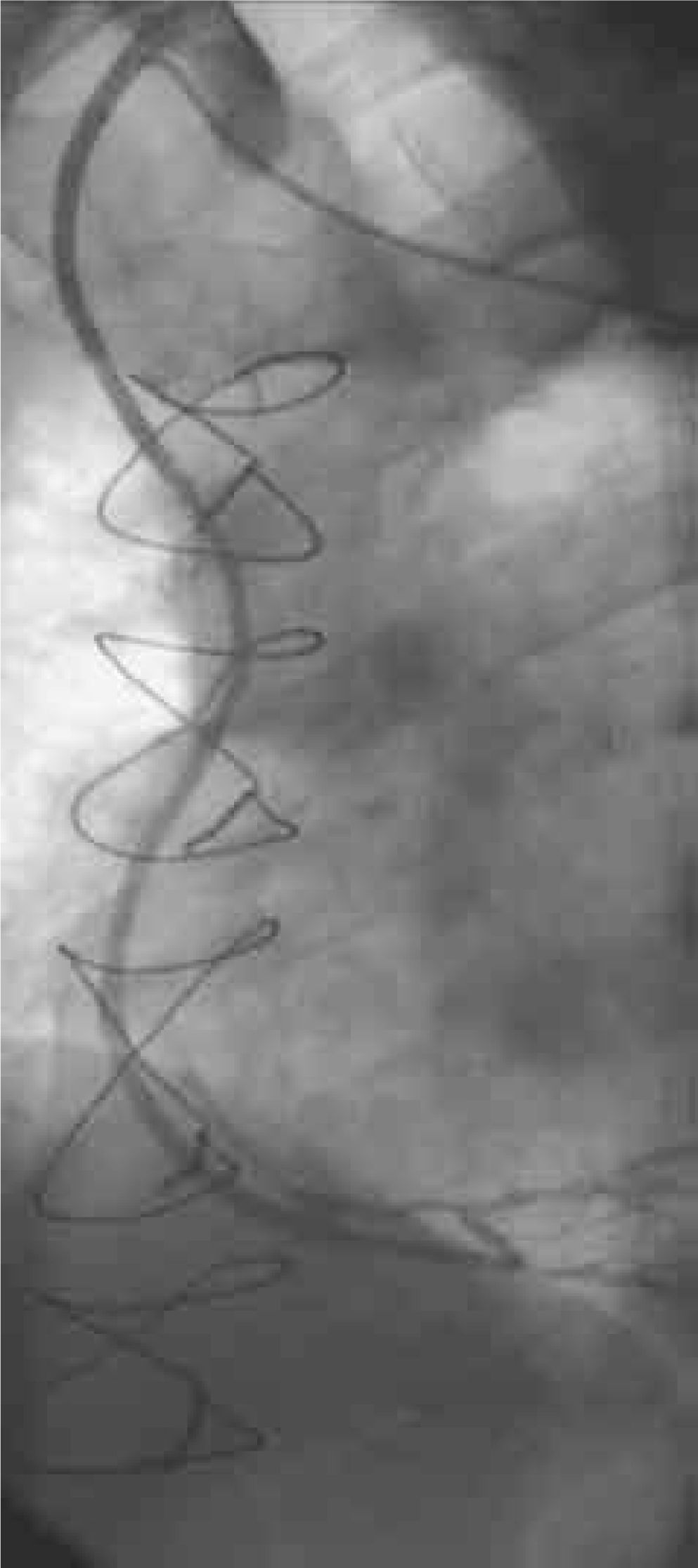
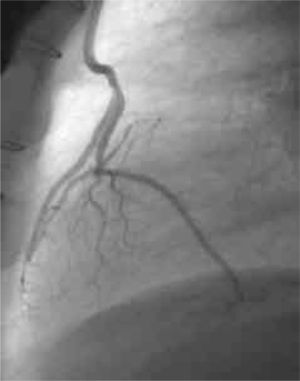
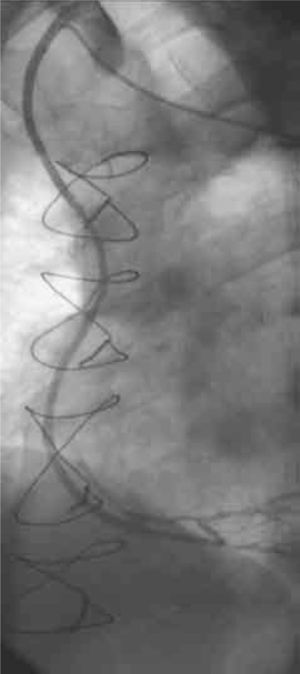
Permeabilidad de los injertosLos seis pacientes se evaluaron a 6 meses de la intervención mediante angiografías de control, constatándose la permeabilidad de todos los injertos realizados (Figs. 1 y 2).
En el postoperatorio inmediato, tres pacientes requirieron en forma transitoria bajas dosis de inotrópicos, y de ellos uno solo, que presentaba deterioro grave de la función sistólica del ventrículo izquierdo en el preoperatorio, necesitó balón de contrapulsación intraaórtico. En un caso se llegó al diagnóstico de infarto perioperatorio, el cual se definió por un aumento de la CKMB superior a 100 UI/l. Ningún paciente se reoperó por sangrado aumentado y no se observaron en la evolución eventos neu rológicos adversos. En un paciente con comorbilidades de causa no cardiovascular la asistencia respira toria mecánica fue prolongada (superior a 24h), así como el tiempo de internación. La estadía promedio en el área de cuidados intensivos fue de 2 días (1–3), mientras que el tiempo total de internación alcanzó un pro medio de 7 días (5–46). Todos los pacientes fueron dados de alta.
El seguimiento fue clínico y angiográfico. A 6 meses del procedimiento se realizaron estudios angiográficos de control (Fig. 1) en todos los casos, constatándose en ellos la permeabilidad de todos los injertos realizados. A 15 meses (6–31) los pacientes intervenidos quirúrgicamente se encuentran asintomáticos, libres de eventos cardiovasculares, y no han requerido nuevos procedimientos de revascularización miocárdica quirúrgica ni percutánea.
DiscusiónEn la actualidad, la CRMcc basada en la utilización de la AMII por los beneficios en resultados clínicos y morbimortalidad que este conducto ha demostrado a largo plazo20,21 asociada a uno o más puentes venosos es la técnica quirúrgica considerada de referencia. Si bien es conocida su superioridad sobre los procedimientos percutáneos, aún existen dudas sobre los resultados a largo plazo en cuanto a permeabilidad de los conductos venosos, lo cual es de suma importancia, fundamentalmente, en pacientes jóvenes y con enfermedad coronaria de múl tiples vasos. Por este motivo, se han publicado numerosos artículos que instan al uso rutinario de la AMII por los beneficios en resultados clínicos y morbimortalidad que este conducto ha demostrado a largo plazo20,21. Con el objetivo de extender los efectos alentadores y fa vorables de la utilización de la AMII, en los últimos años ha ganado popularidad la utilización de otros conductos arteriales (AMID, AR, GE, epigástrica inferior) asociados a la AMII22,23. La elección del mejor conducto arterial para usar junto con la AMII sigue siendo en la actualidad un tema de debate.
En nuestro trabajo la revascularización no fue arterial completa, ya que en las angiografías preoperatorias se observaba que la arteria coronaria derecha presentaba malos lechos. La calidad del vaso a revascularizar es uno de los principales factores que disminuye la permeabilidad a largo plazo de un conducto arterial, transformando su resultado en similar al de una vena. Recientemente, Ferrari, et al.24 han publicado que el conducto de elección para revascularizar la coronaria derecha sigue siendo la vena safena, ya que a la fecha no existen beneficios demostrados al utilizar conductos arteriales en esta posición. Por otro lado, tres de los seis procedimientos quirúrgicos incluidos en este trabajo fueron de urgencia, y en estos casos se prefirió no utilizar exclusivamente arterias con el fin de disminuir el tiempo de procuración de los conductos.
En nuestra serie de seis pacientes la evaluación radiológica y angiográfica preoperatoria permitió sospechar la presencia de enfermedad de la aorta ascendente en tres pacientes, y en los tres restantes la palpación intraoperatoria y la ecografía epiaórtica confirmaron la presencia de calcificaciones. El diagnóstico de calcificación de la aorta ascendente realizado durante el procedimiento quirúrgico permitió cambiar la técnica de revascularización a implementar por una variante de la CRMsc con puentes compuestos e in situ utilizando, como se describió previamente, el pedículo remanente de la AMID como sitio alternativo para la anastomosis venosa proximal anteriormente descrita, en la cual se evita la manipulación de la aorta durante la realización de las anastomosis proximales. Esta opción, como ya se ha mencionado en otras comunicaciones24, ha permitido disminuir la incidencia de eventos adversos neurológicos en el postoperatorio y no aumenta los costos. Un mayor gasto económico sí puede ser observado con la utilización de dispositivos de sutura automática de la vena safena sobre la aorta, alternativa que también puede realizarse sin oclusión aórtica y que tendría, por lo tanto, efectos favorables sobre los resultados neurológicos. Como contrapartida, esta variante de CRMsc es una técnica laboriosa que requiere paciencia y meticulosidad por parte del cirujano.
Por todo lo dicho previamente, la revascularización sin CEC con técnica no touch de los seis pacientes fue combinada con conductos arteriales y venosos, eligiendo para realizar la anastomosis proximal de la vena safena el pedículo remanente de la arteria mamaria interna derecha, un sitio alternativo y poco explorado hasta el momento. En nuestra serie, el escaso número de pacientes y el corto tiempo de seguimiento son dos limitaciones que no permiten arrojar resultados concluyentes, por lo que se requiere aumentar el número de pacientes, compararlos con pacientes sometidos a CRM con manipulación de la aorta ascendente y establecer un seguimiento a largo plazo para explorar la relevancia de la utilización de esta alternativa quirúrgica.
ConclusiónPodemos concluir que esta variante quirúrgica de la cirugía de revascularización miocárdica sin CEC con técnica no touch utilizando un sitio alternativo para la realización de la anastomosis venosa proximal parece ser una opción eficaz para pacientes con enfermedad coronaria y calcificación de la aorta ascendente.