La primera infección del tracto urinario puede ser un marcador de una anomalía del tracto urinario, principalmente de reflujo vésico-ureteral. El objetivo de este trabajo fue determinar la asociación entre microorganismos de la familia Enterobacteriaceae con la presencia y grado de reflujo vésico-ureteral en pacientes neonatales quienes debutaron con infección del tracto urinario.
MétodosSe realizó un estudio retrospectivo, observacional y analítico de recién nacidos con infección del tracto urinario, quienes ingresaron en el Servicio de Neonatología del Hospital Pediátrico Universitario “Juan Manuel Márquez”, La Habana, Cuba, desde 1992 hasta 2013, y en quienes el microorganismo causal era de la familia Enterobacteriaceae. Se realizaron estudios por imagen y se analizó la asociación entre la presencia y grado de reflujo vésico-ureteral con el microorganismo causal de la infección del tracto urinario.
ResultadosSe estudiaron 450 recién nacidos. Los aislamientos bacterianos en los urocultivos correspondieron a E. coli en 316 casos (70.2%). La prevalencia de reflujo vésico-ureteral resultó del 18.2%. Se comprobó que el microorganismo causal —otras bacterias diferentes a E. coli correspondientes a la familia Enterobacteriaceae— se asoció significativamente con el riesgo (OR 2.02; p < 0.01) y el grado de reflujo vésico-ureteral (para los de más alto grado, p < 0.01).
ConclusionesE. coli es el agente causal más frecuente de la infección del tracto urinario neonatal. Sin embargo, existe una asociación entre la presencia de un microorganismo de la familia Enterobacteriaceae diferente a E. coli y el reflujo vésico-ureteral, principalmente los de mayor grado.
The first urinary tract infection can be a marker of a urinary tract anomaly, mainly vesicoureteral reflux. The aim of this work was to determine the association between isolated enterobacteria with the presence and grade of vesicoureteral reflux in neonatal patients with their first urinary tract infection.
MethodsA retrospective, observational and analytic study of newborns, who were admitted to the Neonatal Department, University Pediatric Hospital “Juan Manuel Márquez,” in Havana, Cuba, from 1992 to 2013 was conducted. The causal microorganism of urinary tract infection was from the Enterobacteriaceae family. They were evaluated by radio imaging. The association between the presence and grade of vesicoureteral reflux with the causal microorganism of the urinary tract infection was analyzed.
ResultsNewborn infants with urinary tract infection (450) were studied. Bacterial isolations in the urine cultures corresponded to E. coli in 316 cases (70.2%). The prevalence of vesicoureteral reflux was 18.2%. The presence of bacteria corresponding to the Enterobacteriaceae family (other than E. coli) had significant risk association with vesicoureteral reflux (OR: 2.02; p < 0.01) and vesicoureteral reflux classification (for higher grades, p < 0.01).
ConclusionsE. coli is the most frequent causal microorganism in neonatal urinary tract infection. However, an association between the isolation of a microorganism of the Enterobacteriaceae family different to E. coli with the presence of vesicoureteral reflux and mainly with higher grades of vesicoureteral reflux exists.
La infección del tracto urinario (ITU) es la infección bacteriana más frecuente que involucra este aparato en el primer año de vida1. Los microorganismos causales mayormente involucrados en esta infección son aquellos propios de la flora bacteriana del colon, predominando E. coli; sin embargo, también son comunes otros microorganismos de la familia Enterobacteriaceae2–5. Se reconoce que para poder producir ITU alta, la vía canalicular ascendente es la principal. E. coli posee una serie de características, como factores de virulencia (fimbrias P, adhesinas MR),6–10 que le confieren propiedades para poder adherirse al uroepitelio, ascender y provocar pielonefritis.
Cuando un niño debuta temprano en la vida con ITU, en muchos casos se demuestra la presencia de una anomalía del tracto urinario (ATU), principalmente reflujo vésico-ureteral (RVU), con reportes entre el 14-39.2% para este tipo de anomalía2,11–14. Estudios previos en pacientes con ITU han señalado una asociación significativa para la presencia de RVU cuando esta infección es causada por microorganismos diferentes a E. coli. Estos microorganismos engloban una diversidad de agentes de diferentes familias2,13,15–19, aunque no se considera el grado del RVU, por lo que resulta relevante para la práctica clínica poder establecer asociaciones entre estos aspectos. El objetivo de este trabajo fue determinar la asociación entre microorganismos de la familia Enterobacteriaceae con la presencia y grado de RVU en pacientes neonatales quienes debutaron con ITU. Hasta donde se conoce, este es el primer reporte en Latinoamérica que se enfoca en una población particular: recién nacidos (RN).
2MétodosSe realizó un estudio de tipo retrospectivo, observacional y analítico de RN provenientes de la comunidad con la primera ITU alta por criterios clínicos. Los pacientes ingresaron en el Servicio de Neonatología del Hospital Pediátrico Universitario “Juan Manuel Márquez” desde febrero de 1992 hasta mayo del 2013. Se registraron en una base de datos sobre ITU de una línea de investigación propia del Servicio Neonatal. Solamente se incluyeron aquellos pacientes cuyo microorganismo causal fuera de la familia Enterobacteriaceae y a quienes se realizaron estudios de ultrasonido (US) renal y uretrocistografía miccional (UCGM). Se excluyeron los que no reunieron estas condiciones, por lo que la población de estudio fue de 450 RN. La investigación fue aprobada por el Comité de Ética y Consejo Científico del hospital.
Las variables de estudio fueron sexo, edad cronológica, edad gestacional, peso al nacer, método de recolección de orina, edad a la UCGM, microorganismo causal, presencia de RVU (primario o secundario a otra ATU) y grado de RVU.
Se realizó un US renal durante los primeros 3 días del diagnóstico de ITU para detectar anomalías estructurales del tracto urinario y dilataciones pielocaliciales. La realización de la UCGM fue después de comprobada la remisión de la ITU. Se utilizó la técnica estándar, con llenado completo de la vejiga y toma de vistas en fase de llenado y de micción espontánea. El grado de RVU se basó en la clasificación del Comité Internacional para Estudio del RVU20; en el caso de pacientes con RVU bilateral, se consideró el de mayor grado presente.
La ITU se diagnosticó por la presencia de manifestaciones clínicas y exámenes de laboratorio compatibles con esta afección (fiebre, piuria > 10,000/ml en orina no centrifugada y algún reactante de fase aguda positivo, como velocidad de sedimentación globular ≥ 20mm/h, proteína C reactiva cualitativa positiva, conteo global de leucocitos sanguíneos < 5 o ≥ 15 x 109/l), además del crecimiento de un único microorganismo en orina en cualquier cantidad de unidades formadoras de colonias (UFC)/ml en muestras tomadas por punción vesical suprapúbica (PVS), o > 10 000UFC/ml cuando fue por cateterismo vesical, o > 100 000UFC/ml si se obtuvo por las otros métodos de recolección de orina. Para los métodos de PVS y cateterismo, solamente se requirió una muestra de orina; para las otras técnicas, fue imprescindible contar con dos muestras de orina obtenidas en momentos diferentes y que tuvieran el mismo microorganismo.
Para el análisis estadístico, se calcularon frecuencias absolutas y relativas, así como medidas de resumen (media y mediana) y de dispersión (desviación estándar, cuartiles y rango). Para el análisis de asociación de la presencia de RVU con el microorganismo causal de ITU, se estimó el valor puntual de la razón de momios (OR) con su intervalo de confianza (IC) al 95%; para exposiciones a variables categóricas, por tablas 2 x 2, como también tablas 2 x n en la asociación para los distintos grados de RVU. El nivel de significación asumido para el valor de p fue < 0.05. Todos los análisis se computaron usando el programa estadístico SPSS, versión 12.0 y el programa Epidat versión 3.1.
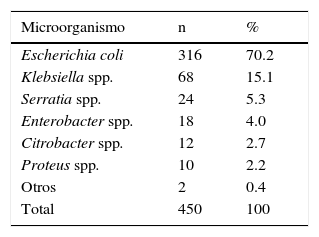
3ResultadosUn total de 450 RN con diagnóstico de ITU reunieron los criterios de inclusión para esta investigación. La media y desviación estándar de los pacientes para edad, peso al nacer y edad gestacional fueron de 16 ± 7.1 días, 3458 ± 496g (rango de 2010 a 5100g) y 39 ± 1.4 semanas (rango de 32 a 43 semanas), respectivamente. De estos, solamente 16 RN (3.5%) fueron pretérmino, 412 RN de sexo masculino (91.5%) y ninguno estaba circuncidado. La recolección de orina para el diagnóstico de la ITU se realizó por PVS en 431 pacientes (95.8%). Los aislamientos bacterianos en los urocultivos correspondieron a E. coli en 316 pacientes (70.2%) (tabla 1). Klebsiella sp. fue el agente causal que le siguió en frecuencia, con 68 RN (15.1%).
Microorganismos causales de la familia Enterobacteriaceae en pacientes con infección del tracto urinario en el periodo neonatal
| Microorganismo | n | % |
|---|---|---|
| Escherichia coli | 316 | 70.2 |
| Klebsiella spp. | 68 | 15.1 |
| Serratia spp. | 24 | 5.3 |
| Enterobacter spp. | 18 | 4.0 |
| Citrobacter spp. | 12 | 2.7 |
| Proteus spp. | 10 | 2.2 |
| Otros | 2 | 0.4 |
| Total | 450 | 100 |
A todos los RN incluidos en el estudio se les había realizado un US renal dentro de los primeros 3 días del diagnóstico, así como una UCGM después de la remisión. Durante este estudio de imagen, la mediana para la edad fue de 4 meses, con el primer y el tercer intercuartil para la mediana de 3 y 6 meses, respectivamente.
Se observaron diferentes tipos de RVU en 82 pacientes (18.2%; IC 95% 14.5-22.6), predominando el RVU primario sobre el secundario (15.8% y 2.4% de los pacientes con ITU, respectivamente) (tabla 2).
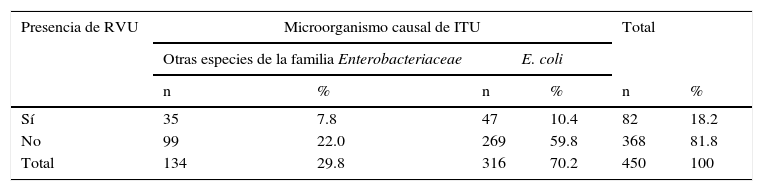
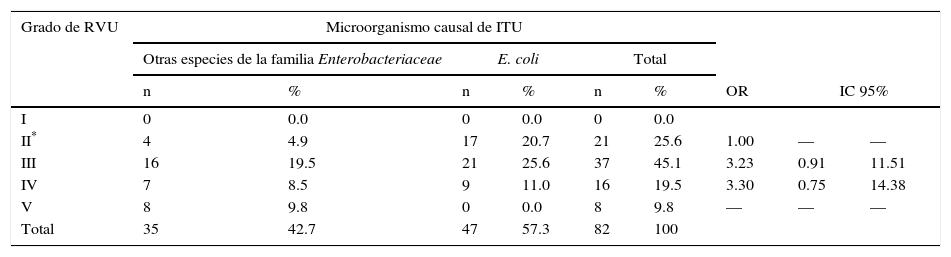
Se comparó la presencia de RVU con el microorganismo causal. Para ello, se formaron dos grupos: el primer grupo correspondió a aquellos casos en los que se aislaron otras especies correspondientes a la familia Enterobacteriaceae; el segundo grupo correspondió a los casos en los que se identificó E. coli (tabla 3). Se comprobó que la presencia de RVU presenta una asociación de riesgo estadísticamente significativa con el microorganismo causal otras bacterias de la familia Enterobacteriaceae diferentes a E. coli (OR 2.02; p < 0.01). Los pacientes se distribuyeron según el grado de RVU y en relación con el microorganismo causal (tabla 4). La comparación de RVU grado III con respecto al grado II denota un OR de 3.23, mientras que para el grado IV con respecto al grado II resultó un OR de 3.30. No se pudo calcular el OR entre grado V con el II, ya que hubo en una casilla cero casos; no obstante, la prueba de homogeneidad entre niveles en conjunto reveló una asociación significativa entre ambas variables (p < 0.01), demostrando que el microorganismo causal otras bacterias de la familia Enterobacteriaceae diferentes a E. coli se asocia con un mayor grado de RVU.
Presencia de RVU respecto a microorganismo causal en pacientes con ITU en el periodo neonatal
| Presencia de RVU | Microorganismo causal de ITU | Total | ||||
|---|---|---|---|---|---|---|
| Otras especies de la familia Enterobacteriaceae | E. coli | |||||
| n | % | n | % | n | % | |
| Sí | 35 | 7.8 | 47 | 10.4 | 82 | 18.2 |
| No | 99 | 22.0 | 269 | 59.8 | 368 | 81.8 |
| Total | 134 | 29.8 | 316 | 70.2 | 450 | 100 |
RVU: reflujo vésico-ureteral; ITU: infección del tracto urinario.
OR 2.02 (IC 95% 1.23-3.31), p < 0.01.
Grado de RVU con respecto al microorganismo causal en pacientes con ITU en el periodo neonatal
| Grado de RVU | Microorganismo causal de ITU | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Otras especies de la familia Enterobacteriaceae | E. coli | Total | |||||||
| n | % | n | % | n | % | OR | IC 95% | ||
| I | 0 | 0.0 | 0 | 0.0 | 0 | 0.0 | |||
| II* | 4 | 4.9 | 17 | 20.7 | 21 | 25.6 | 1.00 | — | — |
| III | 16 | 19.5 | 21 | 25.6 | 37 | 45.1 | 3.23 | 0.91 | 11.51 |
| IV | 7 | 8.5 | 9 | 11.0 | 16 | 19.5 | 3.30 | 0.75 | 14.38 |
| V | 8 | 9.8 | 0 | 0.0 | 8 | 9.8 | — | — | — |
| Total | 35 | 42.7 | 47 | 57.3 | 82 | 100 | |||
RVU: reflujo vésico-ureteral; ITU: infección del tracto urinario.
Los resultados observados demostraron que al contrastar el tipo de microorganismo causal de la ITU con el RVU existe una asociación estadísticamente significativa entre ambas variables: cuando se aísla un microorganismo de la familia Enterobacteriaceae diferente a E. coli, es muy probable que el paciente sea portador de RVU, principalmente de un grado mayor.
La población estudiada tiene la característica de ser preponderantemente RN de término y buen peso al nacer, quienes adquirieron la ITU en la comunidad después de egresar de las respectivas maternidades donde nacieron. Solamente 16 casos resultaron ser RN pretérmino que, aunque son más susceptibles a las infecciones, tienen poca representatividad en esta población de estudio. Otra característica de la población es que, en este periodo de la vida, la ITU afecta fundamentalmente a RN de sexo masculino, y es ocasionada predominantemente por E. coli, lo cual ha sido ampliamente descrito en la literatura universal2–5.
Cuando ocurre el debut de una ITU en etapas tempranas de la vida, debe considerarse la probabilidad de que exista, de manera subyacente, una ATU. Sin considerar la hidronefrosis transitoria e idiopática, las tasas de prevalencia de RVU oscilan entre el 14-39.2%2,11–14; en este estudio, la tasa observada se encontró dentro de este rango (24.2%). La anomalía más prevalente entre los pacientes resultó ser el RVU primario, lo cual también concuerda con los rangos de prevalencia que se reportan internacionalmente, como ya se mencionó, aunque la mayor parte de los estudios realizados reportan tasas de menos del 24%3,21,22.
La mayoría de las investigaciones han englobado bajo el término de “agentes no E. coli” a microorganismos tanto de la propia familia Enterobacteriaceae, como a los pertenecientes a los géneros Streptococcus, Enterococcus, así como otras bacterias correspondientes a bacilos no fermentadores13,15,17,18,23,24. Este espectro de microorganismos es muy disímil, por lo que resultó interesante explorar si la asociación del microorganismo aislado en urocultivos con la presencia de RVU ocurre igualmente en pacientes neonatales con ITU causada específicamente por microorganismos de la familia Enterobacteriaceae, contrastando la E. coli con otros agentes causales de la misma familia.
Se comprobó una asociación de riesgo significativa entre la presencia de RVU con el aislamiento en urocultivos de otras Enterobacteriaceae diferentes a E. coli en neonatos con ITU aunque, tanto para los afectados por RVU como para los que tuvieron ITU sin anomalías evidentes, E. coli fue el microorganismo causal más frecuentemente aislado. Este hallazgo ha sido reportado previamente en la literatura médica internacional, pero es la primera vez que se observa y se reporta en el contexto latinoamericano. Cleper y colaboradores16 compararon el aislamiento de E. coli con Klebsiella spp. en un estudio con RN afectados por ITU, en el que demostraron que el RVU se diagnosticó cuatro veces más en los pacientes con ITU causada por Klebsiella spp. que en aquellos en quienes se aisló E. coli. Al estudiar retrospectivamente 62 RN con la primera ITU, Kanellopoulos y colaboradores encontraron que los RN con RVU fueron estadísticamente más afectados por bacterias Gram negativas distintas a E. coli que aquellos sin esta anomalía, en quienes E. coli fue la bacteria predominante (p = 0.0008). Sin embargo, esta asociación no fue significativa para la presencia de otras ATU diferentes a RVU. Los autores describieron que las bacterias diferentes a E. coli aisladas en nueve neonatos con RVU fueron K. pneumoniae (seis casos) y Proteus (tres casos)2.
Así mismo, se demostró que entre diferentes cepas de E. coli que provocan ITU en niños, aquellos aislamientos de E. coli sin factores de virulencia se relacionaron significativamente con la presencia de alguna ATU. En este sentido, un estudio reportó que cepas de E. coli sin el factor de virulencia papGII fueron más frecuentes entre los pacientes con ATU en comparación con los que tuvieron un tracto urinario normal (25% vs. 5%, p = 0.043); también fue más común el aislamiento de cepas del grupo filogenético A no virulento (58% vs. 10%, p = 0.0003) en dichos pacientes con ATU19. Otro estudio obtuvo resultados similares, donde cepas de E. coli negativas al factor pap fueron de mayor incidencia en el grupo de niños portadores de RVU que en los que no tenían RVU (42.8% vs. 15.6%, p = 0.031). Sin embargo, no se observaron diferencias significativas entre el grupo de pacientes con RVU, o sin esta anomalía, para otros factores de virulencia tales como el antígeno O y la producción de hemolisinas y colisina25.
En contraste con los resultados anteriores, Marcus y colaboradores26, quienes incluyeron 158 niños de varias edades con ITU (mediana de edad 4 meses), verificaron que el microorganismo causal de la ITU, representado por patógenos diferentes a E. coli, se relacionó de manera significativa con la presencia de alguna ATU subyacente en el niño. Sin embargo, cuando se especificó el análisis con la presencia de RVU en particular, no se observó una relación estadísticamente significativa, aunque los microorganismos distintos a E. coli eran los que mayormente causaron la ITU en aquellos pacientes portadores de RVU.
Las fimbrias P, principalmente, y otras adhesinas, son factores de virulencia de superficie de E. coli uropatógena. Por ello, la presencia de estas se encuentra típicamente asociada con la pielonefritis no obstructiva6–10. Se ha señalado que las fimbrias tipo 1 desempeñan un rol principal en la cistitis; sin embargo, resultados más recientes han encontrado que las fimbrias P y tipo 1 actúan sinérgicamente para facilitar la colonización, y enfrentar así los obstáculos como el flujo urinario. De esta manera, también juegan un rol en la infección del riñón27. Otros microorganismos diferentes a E. coli, o la misma E. coli —cepas que no exhiben los factores de adherencia mencionados—, al no tener estos factores de virulencia, necesitan la presencia de determinadas anomalías para poder llegar a producir una ITU alta en comparación con E. coli uropatógena que puede afectar a niños con tracto urinario normal. Este razonamiento se sustenta en el trabajo de de Man y colaboradores,28 quienes estudiaron 241 niños con su primera ITU evaluados por imagen, así como la determinación de adhesinas en cepas de E. coli. Encontraron que las secuelas cicatrizales renales se identificaron la mayoría de niños en quienes se aislaron bacterias adhesinas negativo (RR = 8.3; IC 95% 3.3-20.4, p < 0.001); sin embargo, los niños infectados por E. coli adhesinas negativo tuvieron con mayor frecuencia RVU en la evaluación por imagen.
Klebsiella, Proteus y Enterobacter, aunque comparten características con la E. coli y se clasifican en la familia Enterobacteriaceae, no necesariamente poseen factores de virulencia que faciliten el ascenso por el tracto urinario. No obstante, se ha señalado que Proteus mirabilis se encuentra dotado de factores de virulencia, como adhesinas, que facilitan la colonización del tracto urinario29.
En el 2007 se dieron a conocer las Guías del Instituto Nacional para la Excelencia Clínica (NICE, por sus siglas en inglés) para el diagnóstico y manejo de la ITU en niños30. En estas guías, se mencionan las características de una ITU atípica. La Academia Americana de Pediatría, en el 2011, emitió las “Guías para el diagnóstico y manejo de la ITU inicial en lactantes y niños febriles de 2 a 24 meses de edad”’31. Una de las recomendaciones para realizar una UCGM después de la primera ITU es la calificación de ser atípica. De esta manera, el hecho, entre otros, de aislar un microorganismo diferente a E. coli como agente causal de la ITU, ya determina esta calificación. En la literatura internacional no se aborda específicamente al RN. Estas mismas Guías de la Academia Americana de Pediatría solamente plantean sus recomendaciones a partir de los 2 meses de edad. Resulta obvio que estos lineamientos también compatibilizan para neonatos que debutan con ITU. De hecho, esta investigación refuerza uno de los aspectos que determinan la calificación de ITU atípica: cuando se halla un microorganismo causal diferente a E. coli (por su comprobada asociación con la presencia de RVU).
Un hallazgo novedoso es que se comprobó la mayor probabilidad de una ITU causada por un microorganismo de la familia Enterobacteriaceae diferente a E. coli con un mayor grado de RVU. A la fecha, esto solo se ha podido confirmar en la literatura con el trabajo de Shaikh y colaboradores,32 quienes determinaron, en 769 niños de diferentes edades con ITU, que los pacientes con RVU de grados 3-4 tuvieron mayor predisposición a ser infectados por microorganismos no E. coli.
Esta investigación tiene como limitación los aspectos propios y asociados con un estudio de diseño retrospectivo. Por otra parte, no se pudieron determinar los factores de riesgo de las cepas aisladas, particularmente adhesinas u otros factores, que pudieran arrojar más luz en la asociación comprobada de la presencia de ATU con el tipo de microorganismo causal de la ITU. Como fortaleza del estudio se considera que se trata de una serie de pacientes neonatales numerosa, con características muy similares y control estrecho. Además, mientras duró la investigación, se mantuvieron las mismas técnicas de diagnóstico microbiológico, así como de manejo clínico de los pacientes.
Se concluye que E. coli es el agente causal más frecuente de la ITU neonatal. Sin embargo, existe una asociación entre aislamiento de un microorganismo de la familia Enterobacteriaceae diferente a E. coli con la presencia de RVU, y principalmente con mayores grados de RVU. Ante esta circunstancia, se debe tratar de verificar la presencia de un RVU subyacente.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciamientoLos gastos de la investigación fueron asumidos por los propios autores.
Conflicto de interesesLos autores declaran que no existen conflictos de interés con el contenido del artículo ni beneficios particulares, salvo el hecho de tener la oportunidad de difundir nuevos conocimientos científicos a través de la publicación de estos resultados.
A los médicos y enfermeras del Servicio de Neonatología, así como a los médicos y técnicos del Laboratorio de Microbiología y Radioimaginología de Hospital Pediátrico Universitario “Juan M. Márquez”.