Las fístulas arteriovenosas (FAV) autólogas son los mejores accesos vasculares para hemodiálisis debido a su durabilidad y a su bajo porcentaje de complicaciones.
ObjetivoDeterminar la utilidad de la flujometría intraoperatoria como valor pronóstico en la permeabilidad precoz prehemodiálisis de las FAV nativas.
Pacientes y métodoSe ha realizado la medición de flujos intraoperatorios (FIO) mediante flujómetro (Medi-Stim mod. Butterfly Flowmeter, Noruega) en 204 FAV nativas, 106 radiocefálicas (FAV RC) (52 %) y 98 humerocefálicas (FAV HC) (48 %). Se registraron para su análisis otras variables, como el sexo, la edad, la presencia de diabetes o hipertensión arterial. Se ha valorado la funcionalidad de la FAV dentro del primer mes, considerándose permeables aquellas que presentaban soplo y/o thrill.
ResultadosPermeabilidad precoz global de 94,1 % (192), FAV RC 90,6 % (96) y FAV HC 98 % (96). Curva COR del FIO diastólico FAV RC: área bajo la curva 73,1 % (intervalo de confianza 95 %, límites: 0,58–0,89). Para un valor de 60 ml/min: sensibilidad 81 %, especificidad 60 %.
ConclusionesEl flujo diastólico determinado mediante flujometría intraoperatoria muestra una buena correlación con el pronóstico inicial de las FAV.
Autogenous arteriovenous fistula (AVF) are the best vascular access for haemodialysis due to its durability and low complication rates.
ObjectiveThe purpose of this study is to determine the usefulness of intra-operative blood flow measurement as a prognostic value with respect to pre-haemodialysis patency of the AVF.
Patients and methodsIntra-operative blood flow (IOF) was measured by ultrasonic transit time flowmetry (Medi-Stim mod. Butterfly Flowmeter, Norway) in 204 AVFs, 106 radiocephalic (RCAVFs) (52 %) and 98 brachiocephalic (BCAVFs) (48 %). Demographic variables such as sex, age, presence of diabetes or arterial hypertension were analysed. The functionality of the AVF during the first month was evaluated, considering as patent those having an audible bruit and/or palpable thrill.
ResultsEarly patency AVFs 94.1 % (192), RCAVFs 90.6 % (96) and BCAVFs 98 % (96). ROC analysis of the diastolic IOF of RCAVF: area under the curve 73.1 % (95 % confidence interval: 0.58–0.89). For a value of 60 ml/min: sensitivity 81 %, specificity 60 %.
ConclusionsDiastolic intra-operative blood flow measurement shows a good correlation with the initial outcome of AVF.
El número de pacientes con insuficiencia renal crónica (IRC) en diálisis está continuamente en aumento, debido sobre todo al mayor número de pacientes diabéticos y a la entrada de personas mayores de 60 años en programas de hemodiálisis (HD). Se estima que en España cerca de 45.000 pacientes (1.000 pacientes por cada 1.000.000 de población) están siendo tratados mediante tratamiento sustitutivo renal1.
Desde que Brescia et al2 describieron en 1966 la técnica para la realización de fístulas arteriovenosas (FAV), se generalizó el uso de FAV autólogas para HD. Distintas guías clínicas de Nefrología incluyen en sus recomendaciones la realización de forma preferente de accesos vasculares autólogos, de modo que en las guías K/DOQI recomiendan incrementar la prevalencia de FAV autólogas hasta alcanzar el 65 % del total3.
En varios trabajos publicados se describe la baja permeabilidad primaria en FAV autólogas, alcanzando en alguno de ellos el fracaso en el 49 % en FAV radiocefálicas (FAV RC) y el 57 % en FAV humerocefálicas (FAV HC), a los 6 meses4. Debido a esta alta tasa de fracaso inicial, múltiples estudios se han encaminado hacia la búsqueda de factores que influyan en el fallo precoz de las FAV. Así, se han analizado factores demográficos 56, factores anatómicos valorados por eco-doppler7–10, y factores postoperatorios que predispongan al fracaso precoz11.
La valoración intraoperatoria de la funcionalidad de las FAV se apoya únicamente en determinaciones subjetivas por parte del cirujano, que valora parámetros como la pulsatilidad arterial, el apropiado tamaño de la vena arterializada, la presencia de thrill y de soplo en el trayecto venoso, de modo que en el momento actual no existen técnicas objetivas para valorar el correcto funcionamiento de los accesos vasculares nativos para HD.
La flujometría intraoperatoria ha sido utilizada en la cirugía de revascularización miocárdica como método objetivo para verificar el correcto funcionamiento de los puentes coronarios. Esta técnica ha sido descrita y validada en múltiples artículos12–14.
El objetivo de este trabajo es valorar la utilidad de la flujometría intraoperatoria como factor predictor de permeabilidad precoz previa a HD de las FAV autólogas.
Pacientes y métodoDesde enero de 2006 hasta junio de 2007 se realizó un estudio prospectivo en nuestro centro sobre la permeabilidad en 204 FAV autólogas realizadas de forma consecutiva en 194 pacientes y su relación con el flujo intraoperatorio. La localización de FAV autóloga a realizar se determinó mediante exploración física valorando la continuidad y la accesibilidad del trayecto venoso, la pulsatilidad arterial y la prueba de Allen. También se realizó estudio eco-doppler preoperatorio siguiendo las recomendaciones de las guías K/DOQI3; se desestimaron las venas con diámetro interno menor de 2,5 mm o que presentasen oclusiones en su trayecto, y las arterias menores de 2 mm o con calcificación importante de sus paredes.
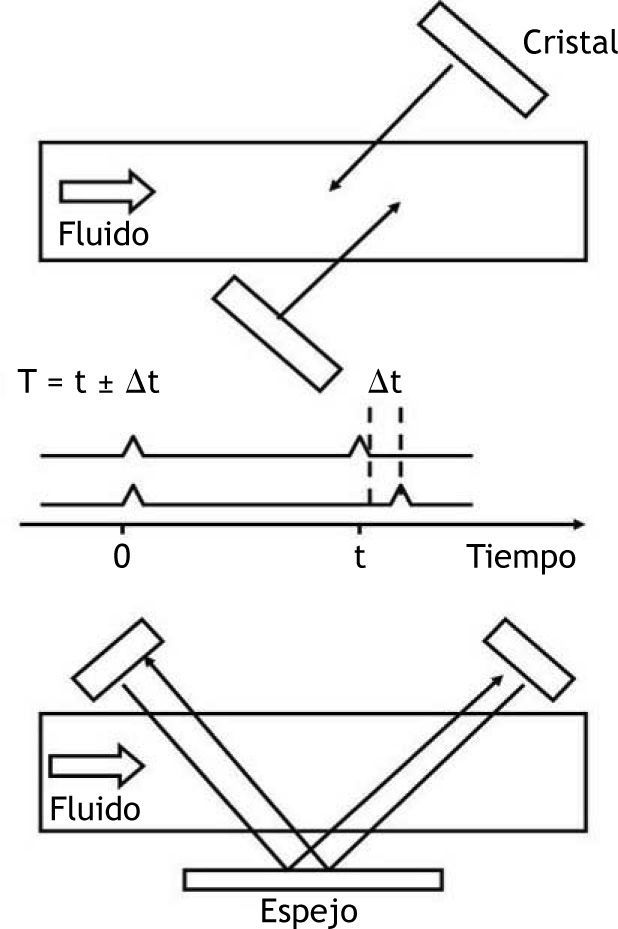
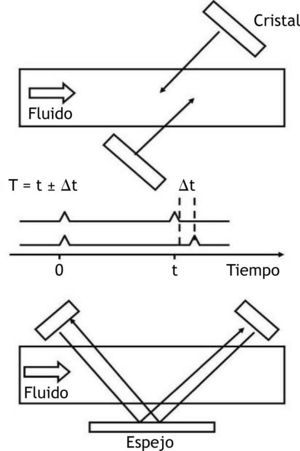
Las FAV se realizaron mediante anastomosis arteriovenosa terminolateral o laterolateral con ligadura distal de la vena cefálica exclusivamente. Al finalizar la anastomosis se realizó medición del flujo intraoperatorio (FIO) utilizando la técnica de medición de flujo por tiempo de tránsito (MFTT)15. Este método se basa en que el ultrasonido viajando en contra de la corriente sanguínea tarda más tiempo que el ultrasonido que viaja en el sentido de la misma corriente. El sensor contiene dos transductores que se localizan en un lado del vaso y un reflector que se localiza en el lado opuesto. Esto induce un doble paso de ultrasonido a través del vaso sanguíneo (fig. 1). La diferencia en el tiempo de tránsito depende del volumen de flujo de sangre (Q = ∫ t2 − t1).
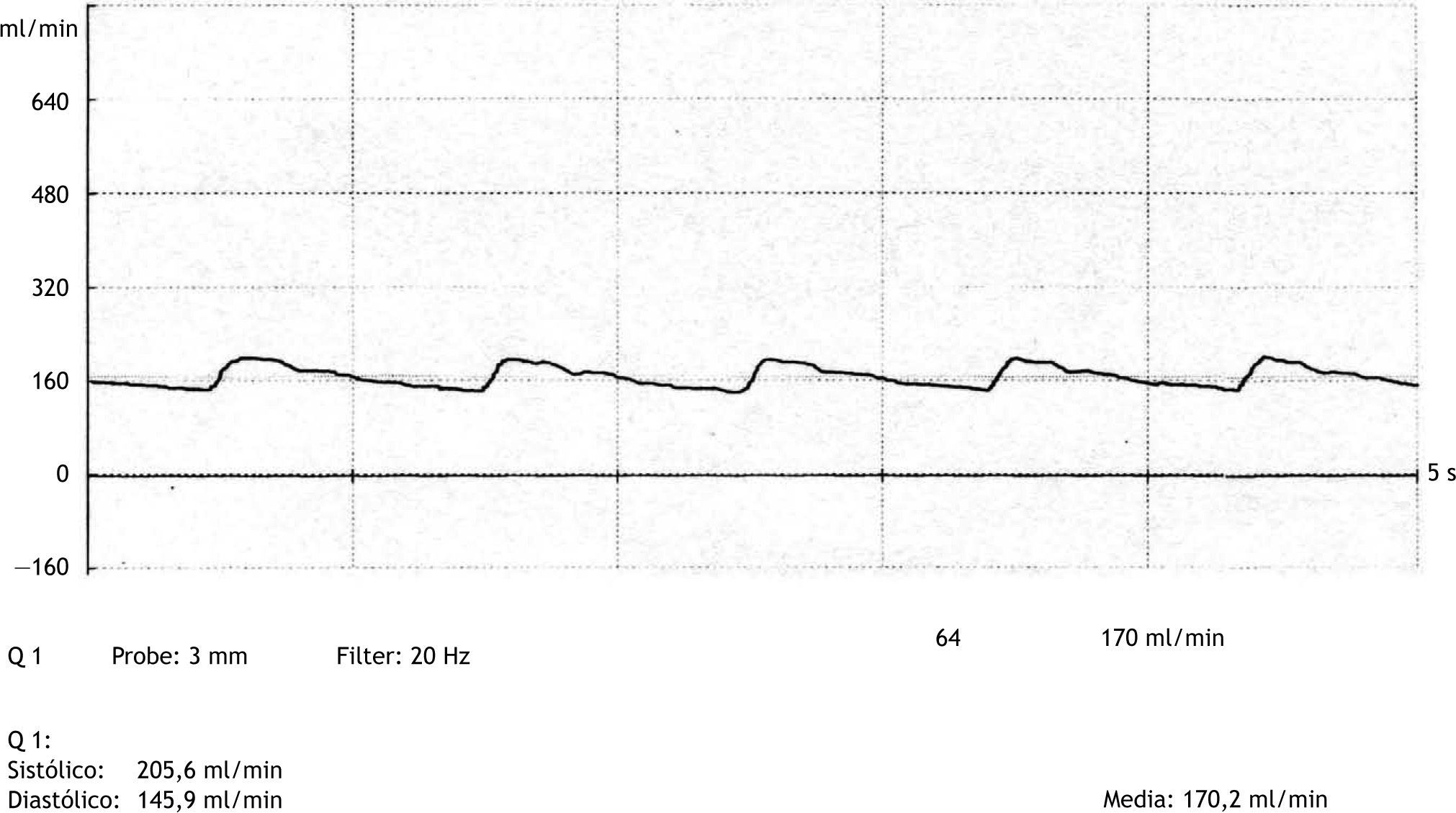
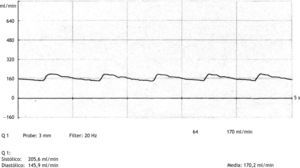
En nuestro trabajo, la medición del FIO se realizó mediante flujómetro (Medi-Stim mod. Butterfly Flowmeter, Noruega): se colocó el sensor rodeando la vena arterializada a los 5 minutos de finalizada la anastomosis, ajustando el tamaño del sensor al diámetro de la vena y situándolo a 1 cm de la anastomosis, obteniéndose el valor del flujo de forma directa y en tiempo real. La medida del flujo intraoperatorio se realiza una vez estabilizada la onda y los valores de flujo. El tiempo requerido para la realización de la prueba es inferior a un minuto. Se registraron en papel, para su posterior análisis, la gráfica de flujo obtenida y los valores del flujo medio, sistólico y diastólico en ml/min (fig. 2).
Se evaluó la permeabilidad de las FAV al mes de la intervención, considerando permeables las FAV que presentaban thrill palpable o soplo sistodiastólico a la auscultación. También se registraron variables demográficas como la edad, el sexo y los diámetros de vena y arteria empleados según el marcaje ecográfico preoperatorio. Las variables clínicas estudiadas fueron la presencia de diabetes mellitus (DM) e hipertensión arterial (HTA).
Se realizó estudio estadístico de las variables demográficas y clínicas recogidas y los valores de flujo intraoperatorio en relación con la permeabilidad al mes determinada mediante exploración física. Los valores de la flujometría se estudiaron con el valor medio ± el error estándar. Se analizaron las variables mediante las pruebas de Chi cuadrado, exacta de Fisher y t de Student. Se consideró el valor de p < 0,05 estadísticamente significativo. Se realizaron curvas COR para aquellas variables de FIO que obtuvieron diferencias significativas en cuanto a permeabilidad de las FAV. El programa informático estadístico utilizado fue el SPSS 14.0.
ResultadosLa distribución topográfica de las 204 FAV una vez realizado el estudio preoperatorio fue 106 FAV RC y 98 FAV HC.
El diámetro medio de la vena utilizada fue de 2,9 ± 0,8 mm (2,5-4,2) en FAV RC y de 4,4 ± 1,4 mm (2,3-6,6) en FAV HC. El tamaño de la arteria utilizada en FAV RC fue 2,6 ± 0,5 mm (2–3,8) y en FAV HC el diámetro medio fue 4,3 ± 1,1 mm (2,8-7,2).
La distribución demográfica de la población fue: 146 varones (71,6 %) y 58 mujeres (28,4 %), con una edad media de 62 años (rango 18–87), siendo 104 (50,9 %) mayores de 5 años. Entre las características clínicas de la muestra destacaba la presencia de DM en 54 pacientes (26,5 %) e HTA en 118 (57,8 %).
De las 204 FAV realizadas, se mantuvieron permeables al mes 192 (94,1 %): 96 FAV RC (90,6 %) y 96 FAV HC (98 %).
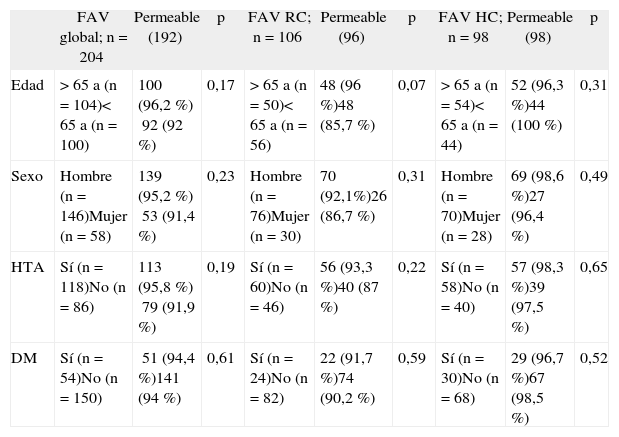
El análisis de los datos demográficos mostró que la permeabilidad no presentaba asociación estadísticamente significativa con respecto al sexo, la edad, ni con los factores clínicos asociados. Tampoco se observaron diferencias significativas cuando se valoraron estos factores en las FAV RC y FAV HC de forma independiente (tabla 1).
Resultados demográficos y clínicos
| FAV global; n = 204 | Permeable (192) | p | FAV RC; n = 106 | Permeable (96) | p | FAV HC; n = 98 | Permeable (98) | p | |
| Edad | > 65 a (n = 104)< 65 a (n = 100) | 100 (96,2 %)92 (92 %) | 0,17 | > 65 a (n = 50)< 65 a (n = 56) | 48 (96 %)48 (85,7 %) | 0,07 | > 65 a (n = 54)< 65 a (n = 44) | 52 (96,3 %)44 (100 %) | 0,31 |
| Sexo | Hombre (n = 146)Mujer (n = 58) | 139 (95,2 %)53 (91,4 %) | 0,23 | Hombre (n = 76)Mujer (n = 30) | 70 (92,1%)26 (86,7 %) | 0,31 | Hombre (n = 70)Mujer (n = 28) | 69 (98,6 %)27 (96,4 %) | 0,49 |
| HTA | Sí (n = 118)No (n = 86) | 113 (95,8 %)79 (91,9 %) | 0,19 | Sí (n = 60)No (n = 46) | 56 (93,3 %)40 (87 %) | 0,22 | Sí (n = 58)No (n = 40) | 57 (98,3 %)39 (97,5 %) | 0,65 |
| DM | Sí (n = 54)No (n = 150) | 51 (94,4 %)141 (94 %) | 0,61 | Sí (n = 24)No (n = 82) | 22 (91,7 %)74 (90,2 %) | 0,59 | Sí (n = 30)No (n = 68) | 29 (96,7 %)67 (98,5 %) | 0,52 |
a: años; DM: diabetes mellitus; FAV: fístula arteriovenosa; FAV HC: fístula arteriovenosa humerocefálica; FAV RC: fístula arteriovenosa radiocefálica; HTA: hipertensión arterial.
Es de destacar que fue en el grupo de menores de 65 años donde se produjo un mayor número de fracasos (8) y todos ellos fueron FAV RC, lo que supone el 80 % de las FAV RC ocluidas, por lo que la permeabilidad de las FAV RC en este grupo fue del 85,7 %.
Los resultados de la flujometría intraoperatoria en FAV RC y en FAV HC y la permeabilidad se describen en las tablas 2 y 3. Todos los valores de FIO (medio, sistólico y diastólico) fueron mayores en FAV permeables frente a ocluidas tanto en FAV RC como en FAV HC, aunque únicamente el flujo diastólico en FAV RC (140 ± 9,5 frente a 75 ± 16,7) alcanzó significación estadística (p = 0,04) respecto a la permeabilidad precoz.
Resultados de la flujometría intraoperatoria en fístulas arteriovenosas radiocefálicas
| FAV RC; n = 106 | Permeable (96) | Ocluida (10) | p |
| Flujo medio | 180 ± 11,9 (607–23) | 150 ± 40,2 (367–42) | 0,4 |
| Flujo sistólico | 235 ± 15,2 (827–45) | 192 ± 52,4 (480–56) | 0,4 |
| Flujo diastólico | 140 ± 9,5 (531–10) | 75 ± 16,7 (163–10) | 0,04 |
Valores de flujo en ml/min. FAV RC: fístula arteriovenosa radiocefálica.
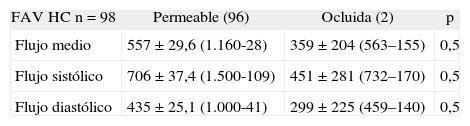
Resultados de la flujometría intraoperatoria en fístulas arteriovenosas humerocefálicas
| FAV HC n = 98 | Permeable (96) | Ocluida (2) | p |
| Flujo medio | 557 ± 29,6 (1.160-28) | 359 ± 204 (563–155) | 0,5 |
| Flujo sistólico | 706 ± 37,4 (1.500-109) | 451 ± 281 (732–170) | 0,5 |
| Flujo diastólico | 435 ± 25,1 (1.000-41) | 299 ± 225 (459–140) | 0,5 |
Valores de flujo en ml/min. FAV RC: fístula arteriovenosa radiocefálica.
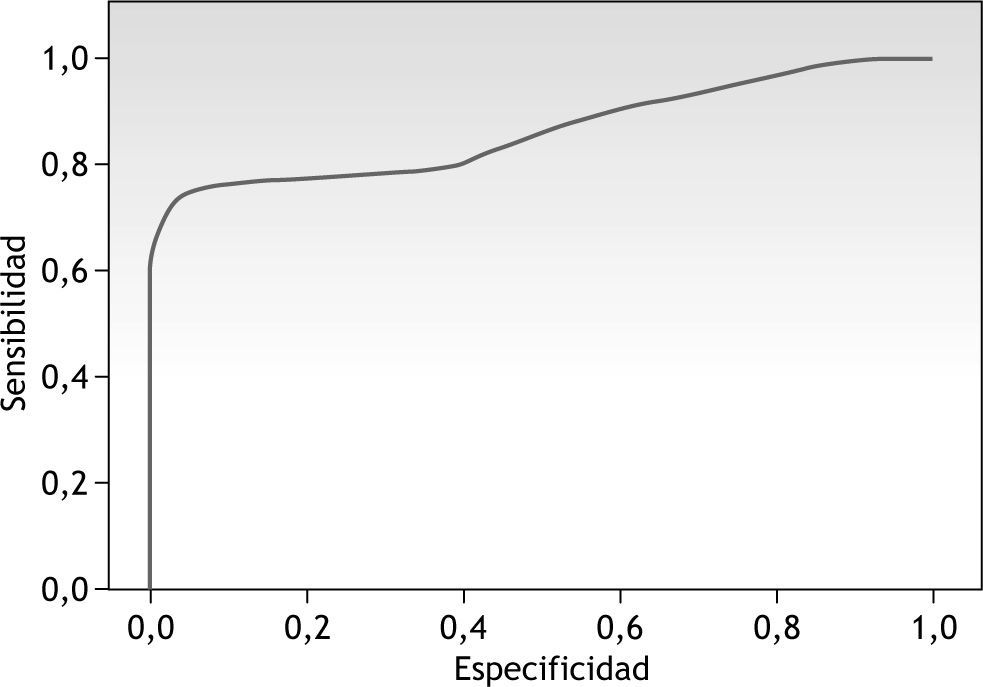
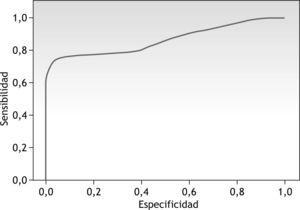
Dada esta diferencia significativa, se realizó una curva COR para el FIO diastólico en las FAV RC. Esta curva queda expuesta en la figura 3 y muestra un área bajo la curva del 73,1 % (nivel de confianza 95 %: 0,58-0,89). Se valoraron diferentes puntos de corte, determinando que para un FIO diastólico igual o superior a 60 ml/min se obtuvo una sensibilidad del 81 %, alcanzando una especificidad del 60 % en cuanto a la permeabilidad precoz de la FAV RC.
DiscusiónLos buenos resultados en cuanto a permeabilidad precoz global que se obtienen en este estudio estimamos que son debidos a una buena selección del lugar de realización de las FAV mediante la exploración física y el eco-doppler, siguiendo los criterios de las guías K/DOQI.
En contra de lo que refiere la literatura, no hemos encontrado diferencias en cuanto a permeabilidad según la edad o el sexo de los pacientes5, ni entre los pacientes diabéticos y los no diabéticos6.
La flujometría intraoperatoria es una técnica contrastada para la evaluación de by pass en cirugía cardiaca y vascular12–15. Es una prueba técnicamente sencilla, cuantitativa, que no precisa adiestramiento específico del operador ni presenta diferencias interoperador. Permite la medición directa e inmediata sin precisar cálculos de ajuste por la modificación del valor del flujo en función de la forma o del diámetro del vaso ni por el grado de inclinación del sensor.
Johnson et al16 fueron los primeros en documentar el uso de la flujometría intraoperatoria en accesos vasculares. Determinaron que FAV RC con flujos menores de 170 ml/min tenían una probabilidad de fracaso superior al 50 %.
Won et al17 encontraron que FAV RC con flujos menores de 160 ml/min debían ser vigiladas durante su maduración y flujos menores de 70 ml/min obligaban a realizar una nueva FAV. Tampoco ellos encontraron asociación entre la edad, el sexo ni la diabetes y el fracaso precoz de las FAV RC.
Publicaciones más recientes, como la de Lin et al18 y la de Berman et al19, también muestran la utilidad de la flujometría intraoperatoria como valor pronóstico en la permeabilidad precoz de FAV autólogas. Lin et al determinaron como valor de referencia de FIO los 200 ml/min en FAV RC. Berman et al hallaron diferencias significativas en el FIO máximo entre las FAV funcionantes y las no útiles. En su análisis mediante las curvas ROC encontraron el valor de 140 ml/min para FAV RC y 308 ml/min para FAV HC como predictores de la maduración de las FAV.
En 2009 Saucy et al20 mostraron el valor de la flujometría intraoperatoria como prueba predictiva del fallo primario de FAV RC previo a HD. El seguimiento se realizó mediante la estimación del flujo con dúplex a la semana y a las 4 semanas. Obtuvieron como valor de referencia un flujo intraoperatorio menor de 120 ml/min para el fracaso precoz.
En los anteriores artículos, salvo el último mencionado de Saucy, solo se utilizó la exploración física para la selección del tipo de FAV. Pensamos que el uso de dúplex preoperatorio para la elección de la FAV autóloga proporciona información anatómica y funcional determinante en los casos con exploración dudosa, bien por el diámetro arterial o venoso, bien por la existencia de fibrosis debida a las habituales venopunciones previas en los pacientes en IRC terminal, o bien en pacientes obesos donde no se palpa la continuidad de los trayectos venosos.
Nuestros resultados obtenidos en los valores de flujo diastólico medio en FAV RC (FIO medio 180 ± 11,9) son coincidentes con los descritos por los anteriores autores en las publicaciones mencionadas. Sin embargo, ellos no distinguen entre FIO medio y FIO sistólico o diastólico. Consideramos que la permeabilidad de las FAV está en mayor medida relacionada con bajas resistencias periféricas y, por lo tanto, el valor del FIO diastólico determina el pronóstico de las FAV. El FIO diastólico elevado, superior a 140 ml/min, se asocia a mayor permeabilidad precoz en FAV RC. Los valores menores de 60 ml/min determinan un mal pronóstico inicial y debería considerarse la revisión de la FAV en el mismo acto quirúrgico.
En nuestra serie las FAV HC ocluidas, únicamente dos, presentaron un error estándar muy elevado en todos los valores de flujo, por lo que creemos que con un mayor tamaño muestral encontraríamos una significación estadística y un valor de corte pronóstico. De cualquier modo, valores elevados del FIO en FAV HC orientan hacia la óptima permeabilidad precoz de la FAV.
Como limitaciones del estudio, encontramos que los resultados precisan corroborarse con un mayor número de casos para determinar la utilidad en el caso de FAV HC, y que es preciso asociar la flujometría intraoperatoria a la funcionalidad de las FAV tras el comienzo de la HD.
ConclusionesEncontramos que la edad, el sexo y la presencia de DM no han sido determinantes en la permeabilidad precoz de las FAV autólogas.
La flujometría intraoperatoria es una prueba sencilla, rápida, cuantitativa, directa e inmediata y el flujo diastólico intraoperatorio muestra una buena correlación con el pronóstico de las FAV, siendo una herramienta útil en la toma de decisiones quirúrgicas durante la intervención para conseguir una mayor eficiencia de las FAV autólogas RC para HD.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Trabajo presentado como Comunicación Oral en el 54.° Congreso Nacional de Angiología y Cirugía Vascular (Barcelona, mayo de 2008).