La asociación de opioides potentes a dosis bajas puede producir un efecto sinérgico antinociceptivo. Esto en combinación con analgésicos menores como el paracetamol puede potenciar el efecto antiálgico a la vez que se minimizan los efectos adversos.
Caso clínicoVarón de 47 años con cáncer de páncreas y metástasis hepáticas que presenta, como síntoma principal, dolor refractario en hipocondrio derecho, y que encuentra respuesta analgésica con asociación de opioides de tercer escalón.
La retirada del paracetamol ocasiona un empeoramiento claro del dolor.
ConclusionesEn este caso únicamente se consiguió alivio sintomático con la asociación de opioides (fentanilo/oxicodona) y paracetamol, con escasos-nulos efectos secundarios, utilizando dosis recomendadas en Cuidados Paliativos.
The combination of strong low-dose opioids can produce a synergistic antinociceptive effect. In combination with minor analgesics, such as paracetamol it may strengthen the analgesic effect as well as minimising adverse events.
Clinical CaseA 47 year-old male diagnosed with pancreatic cancer and hepatic metastases presenting as primary symptom, with refractory pain in right hypochondrium, and an analgesic response found with a combination of third-level opioids. Removal of paracetamol caused a clear worsening of pain.
DiscussionSymptomatic relief was only achieved with a combination of opioids (fentanyl/ oxycodone) and paracetamol, with few/no adverse events by using recommended Palliative Care doses.
Existen estudios experimentales a favor de la asociación de opioides para mejorar la analgesia1. La coadministración de dosis bajas de opioides puede producir un marcado efecto sinérgico antinociceptivo con reducción de efectos adversos sobre el sistema nervioso central2.
El objetivo de dichos estudios fue evaluar el resultado de añadir un segundo opioide a dosis bajas en pacientes con pobre respuesta a dosis altas de analgésicos.
Por otro lado, existe una significativa variabilidad de los opioides en la inducción de la endocitosis de los receptores de opiáceos. Esta es una propiedad funcional independiente, clínicamente importante, que distingue a los analgésicos como es el caso del fentanilo y que puede tener funciones de protección en la reducción del desarrollo de tolerancia.
El efecto agonista y la endocitosis del receptor tienen efectos opuestos en la señalización mediada por receptor, y el resultado final es la función de ambos procesos (RAVE). Por lo tanto, una combinación de opiáceos con características distintas pueden mutuamente alterar sus RAVES, reduciendo así el potencial de desarrollo de la tolerancia. Si nos referimos al fentanilo, al unirse a receptores μ, producen mayor internalización del receptor, pero no por eso generan mayor tolerancia3.
Si hacemos referencia al grupo de los analgésicos menores, además del grupo de los antiinflamatorios no esteroideos (AINE), se encuentra el de los paraaminofenoles, entre ellos el paracetamol, es atípico porque carece de acción antiinflamatoria e inhibe pobremente a la ciclooxigenasa, principalmente en el sistema nervioso central. Es conveniente recordar, que en la escalera analgésica de la Organización Mundial de la Salud (OMS), pertenece al primer escalón, correspondiente al grupo de los no opioides para el tratamiento del dolor leve y asociado tanto con opioides débiles como potentes para el tratamiento del dolor moderado y severo en el escalón intermedio y superior4.
Una estrategia prometedora sería la de usar combinaciones de dosis bajas de opioides con fármacos no opioides, AINE y otros como pueden ser, el paracetamol o acetaminofén y el metamizol. Así se minimizarían los efectos adversos propios de las dosis altas de los compuestos individuales a la vez que se potencian los efectos analgésicos5–7.
Nuestro caso es un ejemplo de lo anteriormente expuesto, el control de dolor difícil, se benefició finalmente con la asociación de opioides y fármacos no opioides como el paracetamol.
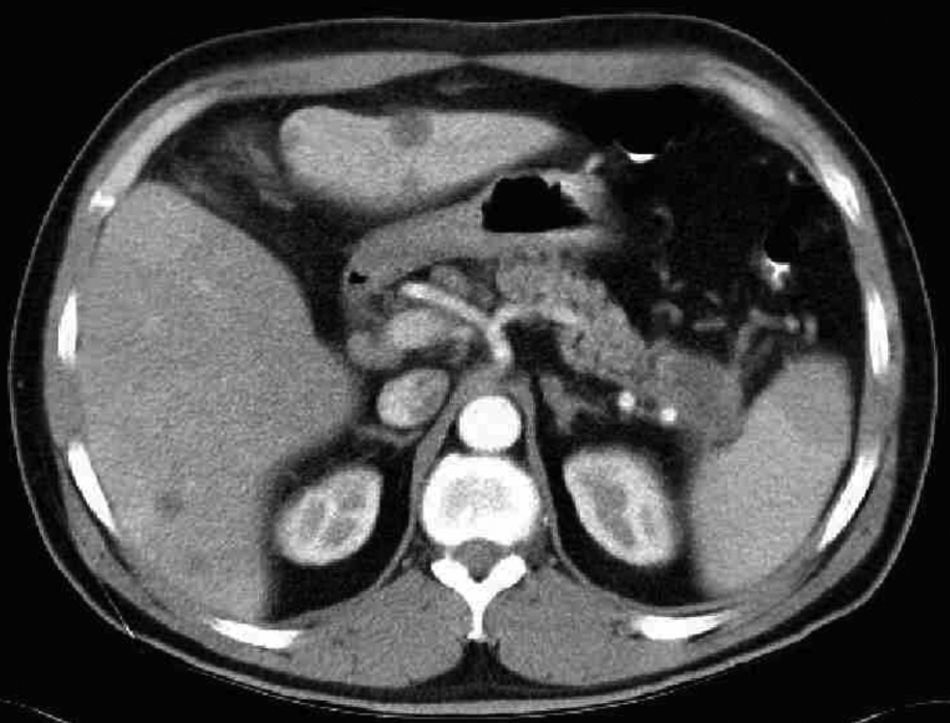
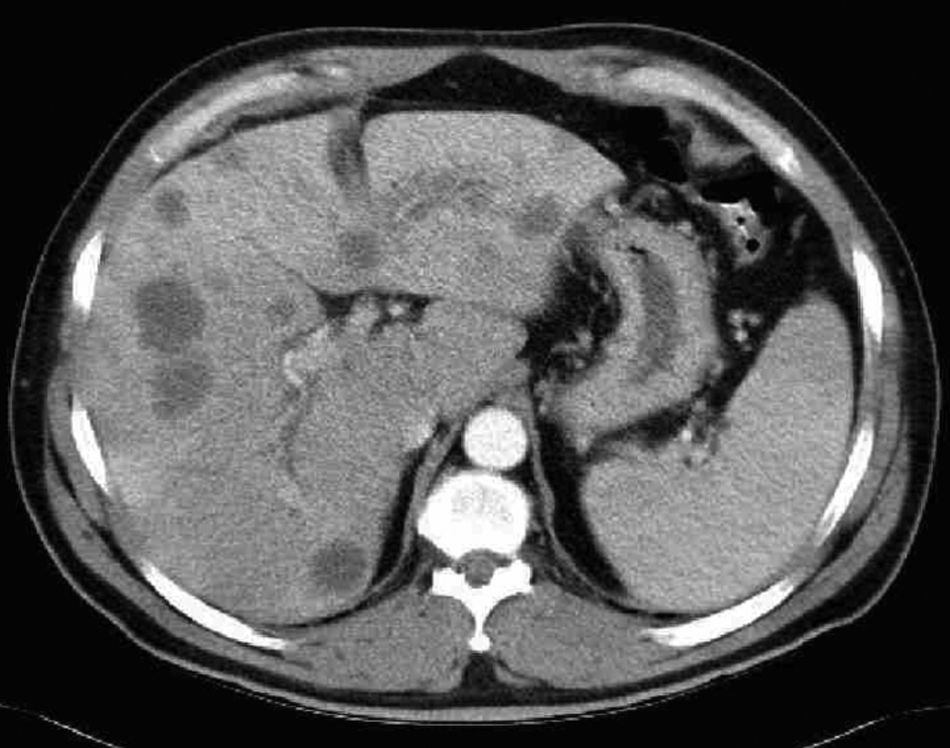
Caso clínicoPaciente varón de 47 años de edad, sin alergias medicamentosas conocidas, fumador activo de 1 paq/día y con antecedentes personales de hipertensión arterial, que inició cuadro de epigastralgia y dolor en hipocondrio derecho con aparición progresiva de ictericia, coluria y acolia, motivo por el que acudió a urgencias. Se realizó estudio analítico, objetivándose: Bilirrubina Total (BT) 5, 69, Bilirrubina Directa (BD) 4,87, Transaminasa Glutamicooxalacética (GOT) 167, Transaminasa Glutamicopirúvica (GPT) 269, Fosfatasa Alcalina (FA) 787, Gama Glutamil Transpeptidasa (GGT) 1.447 y Lactato Deshidrogenasa (LDH) 307. La ecografía abdominal mostró hígado aumentado de tamaño con múltiples Lesiones Ocupantes de Espacio (LOES) sólidas en ambos lóbulos y nódulo en hilio esplénico de 4cm, por lo que se indicó ingreso hospitalario para estudio. La serología para hepatitis B y C fue negativa y los marcadores tumorales, alfa-fetoproteina 2, Antígeno carcinoembrionario (CEA) 233, Ca 19,9 402. La esofagogastroduodenoscopia presentó heterotopia gástrica en esófago cervical y en colonoscopia, con mala preparación, no se identificaron lesiones groseras. TAC Abdominal múltiples LOES hepáticas bilaterales sugerentes de metástasis y nódulo hipodenso en cola pancreática de unos 33mm compatible con tumor del mismo (figs. 1 and 2).
Se realizó biopsia hepática, diagnosticándose en octubre de 2007 de infiltración por adenocarcinoma bien diferenciado, tubular y desmoplásico, compatible con metástasis de origen pancreato-biliar (cola de páncreas). Se presentó en comité de tumores donde, dado lo avanzado del proceso, el único tratamiento que se valoró fue la quimioterapia paliativa en caso de que la hiperbilirrubinemia mejorara, cosa que no ocurrió.
Realizamos una primera valoración durante el ingreso en planta de Medicina Interna tanto a nivel psicosocial como físico. El paciente conocía la realidad de su situación, Ellershaw (Grado de información del paciente y familia) al inicio del proceso grado 2 y familia 3, en la recta final del proceso, paciente y familia 4. Vivía con esposa y 2 hijas. Estaba presente la conspiración de silencio entre matrimonio e hijas y pese a disponer de gran apoyo sociofamiliar, presentó grandes dificultades para afrontar la enfermedad con intenso miedo a la muerte.
Encontramos los problemas que se exponen a continuación:
- 1.
Fase de negación.
- 2.
Dolor hipocondrio derecho con irradiación a tórax continuo y un EVA 7-8/10.
- 3.
Crisis HTA que coinciden con crisis de dolor de EVA 10.
- 4.
Nicturia.
- 5.
Prurito generalizado.
En la exploración destacaba PPS 90, ictericia de piel y mucosas con abdomen blando y depresible, doloroso en epigastrio y ambos hipocondrios especialmente el derecho. Hepatomegalia de 1-2 traveses de dedo. Polo inferior del bazo palpable. Peristaltismo presente. Resto de la exploración sin hallazgos significativos.
El paciente recibía como tratamiento hospitalario, Fentanilo transdérmico 25μg/hora cada 72h, morfina comprimidos de liberación normal 10 mgr si dolor (precisaba 6-7 /24h), paracetamol 1g/8h, enalapril 20mg/24h, atenolol 25mg /12h, amlodipino 5mg/24h, torasemida 5mg/24h, prednisona 30mg/24h, clorazepato dipotásico 5mg/8h, omeprazol 20mg/12h; de rescate, si precisaba metoclopramida, lactitol y dexclorfeniramina, que no tomaba.
Dados los síntomas, ajustamos inicialmente el tratamiento aumentando las dosis de fentanilo trandérmico progresivamente hasta 75 junto a morfina viales unidosis de 10mg/4h en caso de persistencia del dolor. Pasadas 72 horas y dada la escasa mejoría obtenida con los aumentos de dosis se decidió rotar a morfina comprimidos de liberación retardada 100/12h con dosis de rescate 20mg/ 4h vía oral además de Cloruro mórfico 10mg subcutáneo (sc) si lo precisaba. El dolor se controló de forma temporal, EVA 2-3/10, durante apenas 7 días precisando aumento de dosis de morfina y rescates por lo que se decidió rotar a oxicodona a pesar de lo cual el dolor continuaba, EVA 7/10, requiriendo aumentos de dosis de oxicodona de hasta 120mg/12h 4 días después, dejando como rescate 20mg sc. de morfina y controlando el dolor de forma parcial. Tras dos semanas, sufrió nueva descompensación importante con aumento de dolor, EVA 10/10 y decidimos añadir fentanilo 50μg/hora cada 72 horas a oxicodona de liberación retardada 120/12. Mantuvimos como rescate la morfina sc. a dosis de 20mg que sí estaba siendo efectiva.
Con este tratamiento el dolor mejoró considerablemente, EVA 2/10, si bien reaparecía por las mañanas en forma de dolor irruptivo de final de dosis de la oxicodona, lo que se solucionó ajustando la dosis de Oxycodona a 80mg/8h. Estando el paciente controlado con este tratamiento se retiró el paracetamol con objeto de reducir medicación, lo que ocasionó una nueva reagudización del dolor que cesó al reincorporar nuevamente dicho analgésico.
El tratamiento definitivo fue: Oxycodona 80mg/8h, Fentanilo 50/72h, Paracetamol 1 gr/8h, Prednisona 50/24h por la mañana, Rifampicina 300 en desayuno.
Pasados 49 días el paciente falleció tras haber sido sedado por delirium, secundario a su afectación hepática, pasó estas últimas 7 semanas libre de dolor, usando solo de manera esporádica el rescate de morfina sc. con buena respuesta al mismo.
DiscusiónAunque la administración conjunta de opioides en la práctica clínica no se recomienda de manera general, ante un dolor difícil la coadministración de fentanilo y oxicodona a dosis mas bajas puede disminuir los secundarismos y mejorar al mismo tiempo la analgesia de manera considerable, mas allá del efecto obtenido por un solo opioide utilizado a dosis mayores. Se comprobó una disminución del índice de progresividad de opioides (OEI) tras añadir un segundo opioide independientemente de la combinación de fármacos utilizados.
La rápida escalada de los opioides, debido al aumento de la intensidad del dolor o al desarrollo de tolerancia, es un factor pronóstico negativo para la aparición de efectos adversos8, ya que puede limitar la capacidad de respuesta de opiáceos9, sin embargo, en estos estudios, el dolor intenso mejoró de forma significativa y esto no se tradujo en aumento de secundarismos10.
En 2004, Mercadante et al. realizaron un estudio de 20 pacientes oncológicos con dolor difícil y seguimiento durante 30 días tras asociar fentanilo y oxicodona midiendo la intensidad del dolor por EVA, siendo el valor inicial medio de 7,28. La dosis media de oxicodona fue de 59,5mg diarios (máximo de 100mg).
En 13 pacientes se redujo el EVA a los 30 días 2,12 puntos de media, la asociación potenció el efecto analgésico. Esto evita una rápida escalada que puede presentar manifestaciones clínicas de excitabilidad neuronal, como es el fenómeno de hiperalgesia.
En el paciente que nos ocupa, el problema principal fue controlar el dolor, pese a distintas alternativas terapéuticas, no se obtuvo resultado satisfactorio. Ocasionalmente manifestó mejoría parcial durante un breve periodo de tiempo, con posteriores descompensaciones de carácter severo por lo que optamos por dicha asociación (fentanilo y oxicodona) asociados a un analgésico menor como el paracetamol, que resultó ser imprescindible para el control del dolor, sin obtener más efectos secundarios que los esperados con monoterapia.
Es de destacar que la retirada del paracetamol una vez controlado el dolor, ocasionó una nueva reagudización del mismo, que se controló de manera clara tras reintroducirlo, evidenciando que la combinación del analgésico menor con los opioides optimizaron el tratamiento. Finalmente, el paciente falleció con buen control sintomático y sin síntomas tóxicos atribuibles al tratamiento.