Las mutaciones en el genoma de SARS-CoV-2 pueden afectar al gen que codifica el antígeno espicular (S), que interactúa con el receptor específico de la célula huésped, seleccionando variantes mutantes con alteraciones en su capacidad infectiva, potencial patógeno y resistencia a los anticuerpos neutralizantes. En la nomenclatura de las variantes se utiliza una forma «coloquial» que suele hacer referencia al país o lugar de detección, un código de la base de datos «Pangolín» y uno de la página «Nextstrain». Entre las nuevas variantes que se han ido propagando se incluyen la Británica B.1.1.7 (20I/501Y.V1), la Sudafricana B.1.351 (20H/501.V2), la Brasileña P.1 (20J/501Y.V3), las Californianas B.1.427 y B.1.429 (20C/S:452R) y la más reciente, la India B.1.617 (VUI-21APR-01).
El método de referencia para la identificación de las variantes es la secuenciación del genoma completo. Sin embargo, ya se han desarrollado técnicas de PCR (reacción en cadena de la polimerasa por sus siglas en inglés Polymerase Chain Reaction) en tiempo real para la detección de mutaciones específicas que pueden facilitar su identificación presuntiva.
El impacto de estas variantes en los programas globales de vacunación ha suscitado inquietud. En general se piensa que, dado que la respuesta evocada por la vacuna frente al antígeno S se dirige a la totalidad de la proteína y las mutaciones sólo afectan a regiones concretas, el efecto de escape a los anticuerpos vacunales será sólo limitado. Entre las estrategias futuras propuestas para la inmunoprotección se ha sugerido el incremento del número de dosis, la alternancia vacunal y el desarrollo de vacunas específicas frente a diferentes variantes.
Mutations in the SARS-CoV-2 genome can affect the gene encoding the Spike (S) antigen, which interacts with the host cell specific receptor, selecting mutant variants with changes in their infective capacity, pathogenic potential and resistance to neutralizing antibodies. The nomenclature to design the variants uses a colloquial form referred to the country or place of detection, a code from the “Pangolin” database and one from the “Nextstrain” page. New variants that have spread include the British B.1.1.7 (20I/501Y.V1), the South African B.1.351 (20H/501.V2), the Brazilian P.1 (20J/501Y.V3), the Californians B.1.427 B.1.429 (20C/S:452R) and the most recent, the Indian B.1.617 (VUI-21APR-01).
The gold standard for the identification of the variants is whole genome sequencing. However, real-time PCR techniques have already been developed for the detection of specific mutations that can facilitate their presumptive identification.
The impact of these variants on global vaccination programs has raised concern. It is generally thought that, since the response evoked by the vaccine against the S antigen is directed at the entire protein and the mutations only affect specific regions, the escape effect of the vaccine antibodies will be limited. Among the future strategies proposed for immuno-protection, the increase in the number of doses, the alternation of vaccines and the development of specific vaccines against different variants has been suggested.
Aunque el genoma de SARS-CoV-2 parece relativamente estable, este tipo de virus ARN de cadena simple acumula una tasa de mutaciones estimada en torno a 10−6-10−4 por ciclo replicativo. Estas mutaciones pueden afectar a la interacción antígeno espicular (S) con el receptor específico de la célula huésped (la enzima convertidora de la angiotensina 2 [ACE2]), alterando la susceptibilidad a la respuesta inmune, la agresividad de la infección y/o la capacidad de transmisión del virus. De esta manera, algunas mutaciones pueden otorgar ventajas evolutivas que favorezcan la selección de determinados linajes o variantes1.
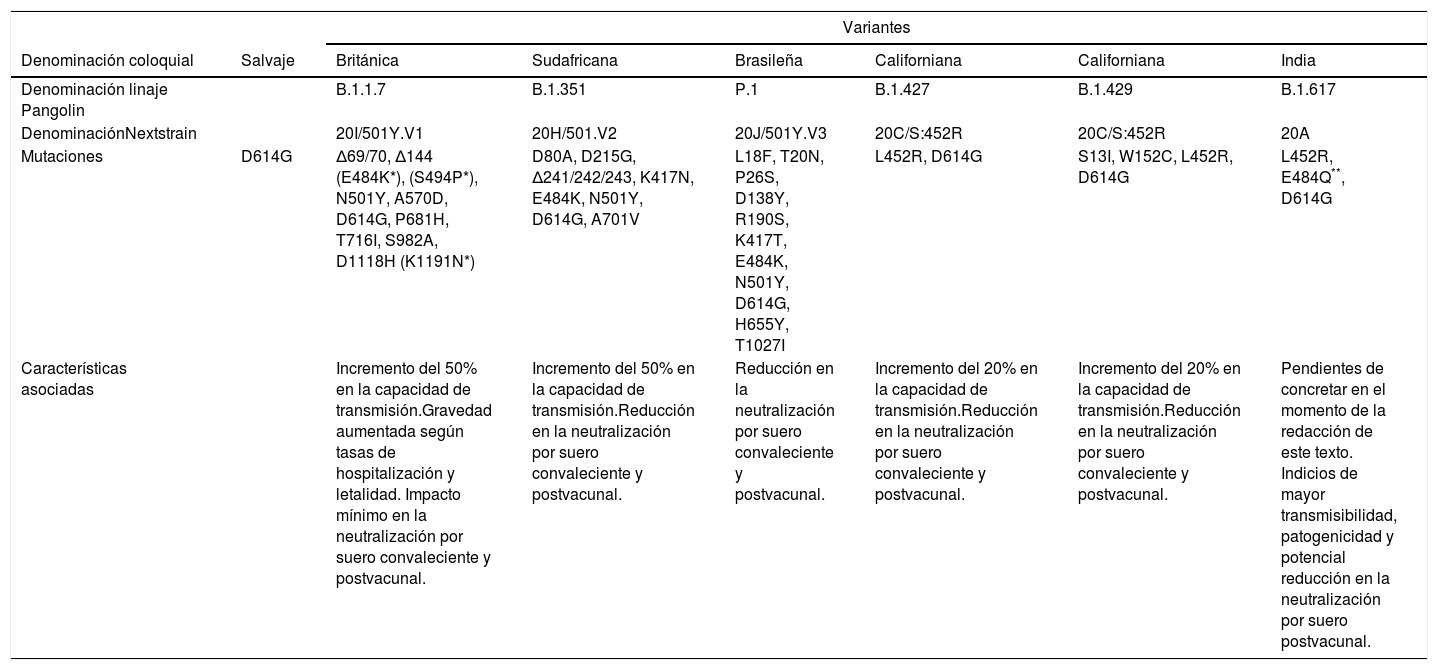
Las variantes pueden aparecer por deleciones genéticas (caracterizadas por la pérdida de una porción de la secuencia de ácidos nucleicos), por mutaciones sinónimas (también conocidas como silenciosas o sin sentido, que no ocasionan cambios en la síntesis de aminoácidos) o por mutaciones no sinónimas (asociadas con un cambio en la codificación de aminoácidos). Estas últimas son las más relevantes desde un punto de vista funcional. Ciertas mutaciones denominadas «de escape» se expanden subsecuentemente bajo una presión inmunológica selectiva que limita, pero no elimina, la replicación2. En los últimos meses han surgido diferentes variantes que co-circulan en todo el mundo y es previsible que en un futuro puedan continuar apareciendo otras nuevas. La tabla 1 resume las principales variantes de SARS-COV-2 actualmente circulantes.
Principales variantes de SARS-COV-2 actualmente circulantes7
| Variantes | |||||||
|---|---|---|---|---|---|---|---|
| Denominación coloquial | Salvaje | Británica | Sudafricana | Brasileña | Californiana | Californiana | India |
| Denominación linaje Pangolin | B.1.1.7 | B.1.351 | P.1 | B.1.427 | B.1.429 | B.1.617 | |
| DenominaciónNextstrain | 20I/501Y.V1 | 20H/501.V2 | 20J/501Y.V3 | 20C/S:452R | 20C/S:452R | 20A | |
| Mutaciones | D614G | Δ69/70, Δ144 (E484K*), (S494P*), N501Y, A570D, D614G, P681H, T716I, S982A, D1118H (K1191N*) | D80A, D215G, Δ241/242/243, K417N, E484K, N501Y, D614G, A701V | L18F, T20N, P26S, D138Y, R190S, K417T, E484K, N501Y, D614G, H655Y, T1027I | L452R, D614G | S13I, W152C, L452R, D614G | L452R, E484Q**, D614G |
| Características asociadas | Incremento del 50% en la capacidad de transmisión.Gravedad aumentada según tasas de hospitalización y letalidad. Impacto mínimo en la neutralización por suero convaleciente y postvacunal. | Incremento del 50% en la capacidad de transmisión.Reducción en la neutralización por suero convaleciente y postvacunal. | Reducción en la neutralización por suero convaleciente y postvacunal. | Incremento del 20% en la capacidad de transmisión.Reducción en la neutralización por suero convaleciente y postvacunal. | Incremento del 20% en la capacidad de transmisión.Reducción en la neutralización por suero convaleciente y postvacunal. | Pendientes de concretar en el momento de la redacción de este texto. Indicios de mayor transmisibilidad, patogenicidad y potencial reducción en la neutralización por suero postvacunal. | |
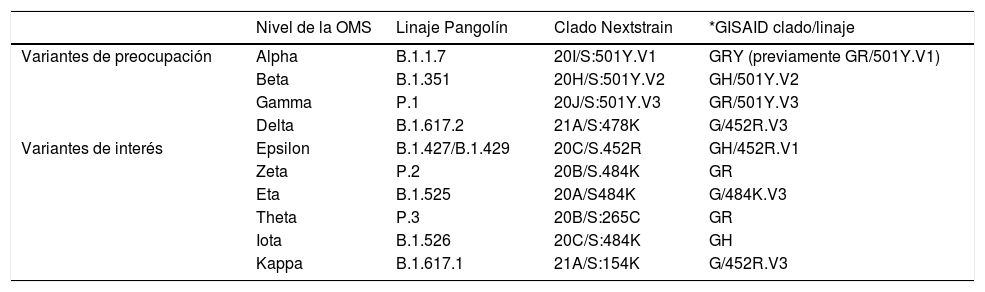
Pese a que habitualmente, tras la aparición de mutaciones, los términos cepa y variante se emplean como sinónimos, en sentido puro deberían considerar la inducción o no de cambios en el comportamiento del virus3. Sin embargo, en este texto estos términos se usarán indistintamente. En la nomenclatura de las diferentes variantes de SARS-CoV-2 que han ido surgiendo paulatinamente se utiliza una forma «coloquial» que suele hacer referencia al país o lugar de detección (cepa Británica), un código de la base de datos Pangolín4 (B.1.1.7), y uno basado en la página Nextstrain5 (20I/501Y.V1). Este sistema múltiple, con frecuencia puede generar confusiones. Con el ánimo de facilitar la información, muy recientemente la Organización Mundial de la Salud (OMS) ha adoptado un sistema más simple sustentado en el uso de letras del alfabeto griego para denominar a las diversas variantes6. En la tabla 2 se muestra la nueva nomenclatura de designación de distintas variantes.
Nomenclatura de la OMS, propuesta para la designación de variantes de preocupación y variantes de interés
| Nivel de la OMS | Linaje Pangolín | Clado Nextstrain | *GISAID clado/linaje | |
|---|---|---|---|---|
| Variantes de preocupación | Alpha | B.1.1.7 | 20I/S:501Y.V1 | GRY (previamente GR/501Y.V1) |
| Beta | B.1.351 | 20H/S:501Y.V2 | GH/501Y.V2 | |
| Gamma | P.1 | 20J/S:501Y.V3 | GR/501Y.V3 | |
| Delta | B.1.617.2 | 21A/S:478K | G/452R.V3 | |
| Variantes de interés | Epsilon | B.1.427/B.1.429 | 20C/S.452R | GH/452R.V1 |
| Zeta | P.2 | 20B/S.484K | GR | |
| Eta | B.1.525 | 20A/S484K | G/484K.V3 | |
| Theta | P.3 | 20B/S:265C | GR | |
| Iota | B.1.526 | 20C/S:484K | GH | |
| Kappa | B.1.617.1 | 21A/S:154K | G/452R.V3 |
Las distintas mutaciones asociadas con cambios en los aminoácidos se denominan con una clave alfa-numérica que indica, en primer lugar, el código de una letra mayúscula del aminoácido que ha sido sustituido, un número que hace referencia a la posición del cambio y finalmente la letra mayúscula correspondiente al código del nuevo aminoácido. Así, por ejemplo, la mutación N501Y indica que el aminoácido asparagina (N) ha sido sustituido por una tirosina (Y) en la posición 501.
Clasificación de las variantes de SARS-CoV-2Las distintas variantes de SARS-CoV-2 se han clasificado según su grado de importancia7:
Variantes de interés (VOI) son las que se han asociado con cambios que afectan al receptor de unión celular del virus, con una reducción de la capacidad neutralizante de los anticuerpos generados por la infección natural o la vacunación, disminución de la eficacia de los tratamientos, potencial impacto diagnóstico o previsión de un incremento en la transmisibilidad y/o gravedad de la infección, con agrupación de casos y brotes, pero con una prevalencia limitada en otros países. Ejemplos de variantes de interés son B.1.525 (20A/S:484K) B.1.526 (20C/S:484K), B.1.526.1 (20C), B.1.617 (20A), B.1.617.1 (20A/S:154K), B.1.617.2 (20A/S:478K), B.1.617.3 (20A) y P.2 (20J)7.
Variantes de preocupación (VOC) incluyen aquellas en las que existe evidencia de un aumento de la transmisibilidad, gravedad, disminución de la capacidad neutralizante de los anticuerpos naturales o generados tras la vacunación, reducción de la efectividad del tratamiento o fallos en los test de diagnóstico. Ejemplos de variantes de preocupación son la británica B.1.1.7 (20I/501Y.V1), la sudafricana B.1.351 (20H/501.V2), la brasileña P.1 (20J/501Y.V3), la californiana B.1.427 (20C/S:452R) y la californiana B.1.429 (20C/S:452R)7.
Variantes de alta importancia (VOHC) incluirían aquellas para las que exista una clara evidencia de que las medidas preventivas y terapéuticas muestren una eficacia significativamente menor que las conocidas para las variantes previamente circulantes. Afortunadamente, por el momento, no se conocen variantes de SARS-CoV-2 que se acojan a esta categoría7.
El Centro Europeo para la Prevención y el Control de las Enfermedades (ECDC, por sus siglas en inglés) considera una categoría adicional, denominada variantes bajo vigilancia, para aquellas con propiedades similares a las de las variantes de preocupación, pero para las que la evidencia científica sólo es preliminar8.
Cepa salvajeLa cepa original que inició la pandemia de COVID-19 en 2020 portaba la mutación 484E. Esta mutación se localiza en el epítope de la región dominante que codifica la proteína S9. Entre enero y febrero de 2020 emergió una variante de SARS-CoV-2 con una sustitución D614G en el gen codificante de la proteína S10. La cepa original tenía el precursor 614D11. Esta mutación D614G en la cepa salvaje favoreció su adaptabilidad para impulsar la pandemia12. Durante un periodo de varios meses la cepa mutante D614G remplazó a la inicialmente detectada en China y en junio de 2020 ya se hizo dominante. Esta cepa, comparada con la precursora, mostró un incremento de infectividad y transmisibilidad. Sin embargo, no se asoció con mayor gravedad, ni con pérdida de rendimiento de los test de diagnóstico de laboratorio, ni disminución de la capacidad neutralizante de los anticuerpos, ni menor efectividad terapéutica10.
Variante británicaLa denominada variante británica B.1.1.7 (20I/501Y.V1) se detectó a finales de 2020 en el Reino Unido y rápidamente se ha extendido por numerosos países13, suplantando en muchas ocasiones a la cepa salvaje original. Acumula más de 20 mutaciones, sin considerar las que no se asocian a cambios de aminoácidos, casi la mitad afectan a regiones codificantes del antígeno S (principal diana de los anticuerpos neutralizantes)14. Esta variante mantiene la mutación D614G y muestra, además, la mutación N501Y que parece incrementar la interacción de la proteína S con el receptor ACE215 ya que afecta al dominio de unión al receptor (RBD)16. Además, presenta la deleción 69/7010,16. Esta deleción puede disminuir la sensibilidad diagnóstica de ciertos test de PCR que tienen como diana al gen codificante del antígeno S. Sin embargo, dado que la mayoría de las técnicas de PCR combinan múltiples dianas, este hecho puede no ser muy problemático. Estos cambios moleculares parecen carecer de repercusión sobre el rendimiento de los test antigénicos rápidos10. Esta variante se ha relacionado con mayor transmisibilidad y gravedad. Aunque puede ser cuestionable la severidad clínica aumentada por esta y otras variantes10,17, el incremento de letalidad informado por esta cepa es de 4,1 muertes por 1.000 casos detectados (con relación a la de las cepas previamente circulantes estimada en 2,5 por 1.000 casos)18 y muestra una relativa resistencia a la neutralización por anticuerpos monoclonales frente al antígeno S. Sin embargo, no es más resistente al plasma de individuos expuestos a la infección natural o tras la vacunación19.
Variante sudafricanaEn diciembre de 2020 se informó en Sudáfrica la variante B.1.351 (20H/501.V2)2,13,15, que quizá pudo aparecer algunos meses antes. Esta variante, emergió independientemente de B.1.1.7.16 y alberga varias mutaciones no sinónimas y una deleción que inciden mayoritariamente en la proteína S14. Combina las mutaciones D614G y N501Y15 con las mutaciones K417N, E484K20. A diferencia de la cepa británica, no porta la deleción 69/7016. La mutación N501Y de la variante sudafricana, aunque está también presente en la variante británica, parece ser filogenéticamente distinta10. Existen dudas sobre si se relaciona con mayor gravedad o peor pronóstico10. En comparación con la cepa salvaje parece ser marcadamente más resistente a la neutralización por suero de sujetos convalecientes o vacunados19,21,22.
Variante brasileñaLa variante brasileña P.1 (B.1.1.28.1, 20J/501Y.V3)13 se detectó en Japón a partir de viajeros procedentes de Brasil16. Contiene varias mutaciones, incluyendo tres que afectan a la proteína S14,16. La mutación E484K, compartida tanto por la variante brasileña como la sudafricana23, ha desencadenado alarma por su posible vínculo con cierta capacidad de evasión de la respuesta inmune14. Ambas variantes se han relacionado con mayor transmisibilidad y mayor tasa de reinfección13,14. Las otras dos mutaciones de esta variante que afectan a la proteína S son la K417T y la N501Y16. Una forma de distinguir la variante sudafricana de la brasileña es que esta última carece de la mutación K417N.
Variante B.1.1.7 con mutación E484KLa detección de la mutación E484K en secuencias B1.1.7. ha generado también preocupación por una posible pérdida de eficacia vacunal, debida a su combinación con el resto de las mutaciones de la variante británica14.
Variante californianaOtras variantes emergentes incluyen la cepa B.1.429 (20C/S:452R)15,24,25 y la B.1.427 (20C/S:452R)24 diseminadas en California. La variante B.1.429 que posee, entre otras, las mutaciones L452R, D614G y W152C7,25, se ha extendido rápidamente por Estados Unidos y otros países, y es menos susceptible a la neutralización por el suero de sujetos convalecientes o vacunados21. Estas variantes se han clasificado como de preocupación por los CDC (Centros para el Control y la Prevención de Enfermedades)7, mientras que la OMS las considera sólo como variantes de interés6.
Variante indiaMás recientemente han suscitado gran alarma las noticias relacionadas con la aparición y difusión en India de la nueva variante B.1.617 26, también conocida como VUI (Variant Under Investigation)-21APR-01 27,28 y 20A según «Nextstrain»7. Por el momento se considera una variante de interés7. Esta cepa se ha denominado, en ciertos medios de comunicación, como «doble mutante» porque aúna las mutaciones L452R de la cepa de California con la mutación E484Q. Este término de «doble mutante» carece de sentido si se tiene en cuenta que las otras variantes de SARS-CoV-2 también reúnen simultáneamente varias mutaciones a la vez. Otros linajes relacionados son B.1.617.1 (20A/S:154K), B.1.617.2 (20A/S:478K) y B.1.617.3 (20A). Estos tres linajes presentan en común la mutación L452R. Las variantes B.1.617.1 y B.1.617.3 (ambas consideradas como de interés tanto por los CDC como por el ECDC)7,8 presentan al igual que B.1.617 también la mutación E484Q7. La variante B.1.617.2, aunque sigue clasificada como de interés por los CDC7, ha sido recientemente considerada por el ECDC una variante de preocupación8.
Se piensa que las mutaciones en la proteína S, que incrementan la transmisibilidad del virus, podrían favorecer el reemplazo de las cepas salvajes precursoras por las nuevas variantes ya circulantes y por eventuales futuras mutantes29.
Variantes y vacunaciónEl impacto de estas variantes en los programas globales de vacunación ha suscitado inquietud y se considera prioritario desarrollar marcadores que correlacionen vacuna y protección24. Como se ha comentado, se ha planteado que las nuevas variantes podrían escapar más fácilmente a la respuesta inmune. En general, se considera que, dado que la respuesta evocada por la vacuna frente al antígeno S se dirige a la totalidad de la proteína y las mutaciones sólo afectan a regiones concretas, no parece que las nuevas variantes puedan evadir totalmente la acción generada tras la vacunación3. En este sentido son alentadores los resultados de la inmunización en Israel, donde la variante británica es mayoritaria30. Asimismo, ciertos ensayos preliminares han mostrado una aceptable respuesta neutralizante inducida por la vacunación frente a diferentes variantes28,31,32. Entre las principales vacunas frente a SARS-CoV-2 se encuentran las de ARN mensajero (mRNA-1273; Moderna y BNT162b2; Pfizer), las vectoriales (ChAdOx1; AstraZeneca y Ad26.COV2.S; Janssen) y la de subunidades proteicas NVX-CoV2373 (Novavax)33. Las vacunas de ARN mensajero (mRNA-1273; Moderna y BNT162b2; Pfizer) parecen mostrar una eficacia sólo ligeramente inferior sobre la variante británica. Sin embargo, su capacidad de neutralización sí que está significativamente reducida frente a las variantes sudafricana y en menor medida frente a la brasileña (dado el alto título de anticuerpos generado para esta última variante, el descenso en actividad neutralizante parece condicionar una menor repercusión que para la sudafricana)33. Recientemente se ha sugerido que, aunque la variante india B.1.617.1 es también más resistente a la neutralización, las vacunas de ARN mensajero de Moderna y Pfizer muy posiblemente conserven su capacidad de protección frente a ella34. La vacuna vectorial ChAdOx1 (AstraZeneca), aunque puede mostrar una pérdida limitada de actividad frente a la variante británica, mantiene una efectividad admisible para ella. Sin embargo, la eficacia de esta vacuna para la sudafricana parece haberse visto mermada de manera muy importante, cuestionado su uso en ciertos países con alta prevalencia de infección por esta variante33. Esta vacuna vectorial, pese a producir una respuesta de anticuerpos con una capacidad reducida de neutralización frente a la variante india B.1.617.1, parece mantener una eficacia que limita la gravedad y la mortalidad de la infección35. La vacuna vectorial Ad26.COV2.S (Janssen) muestra una eficacia inferior al 60% para la protección de la enfermedad moderada/grave causada por la cepa sudafricana33. La vacuna de subunidades proteicas NVX-CoV2373 (Novavax) presenta una eficacia superior al 80% frente a la variante británica pero inferior al 50% para la sudafricana33. El comportamiento de las variantes californianas respecto a las vacunas puede ser muy similar al de la variante británica33.
Existen datos que sugieren que más allá de la respuesta inmune humoral, la respuesta celular es capaz de reconocer a las nuevas variantes de SARS-CoV-236. De esta forma las vacunas podrían dar lugar, además de la producción de anticuerpos específicos, a una inducción de una respuesta celular (células T helper y T citotóxicas-killer)33. La respuesta inmune T-dependiente frente a la proteína S de SARS-CoV-2 se caracteriza por niveles elevados de interferón gamma (IFN-ɣ) que puede ser detectados mediante los ensayos de liberación de interferón-gamma (IGRA)37. Estos ensayos pueden representar un complemento para determinar el inmunostatus en la actual pandemia38.
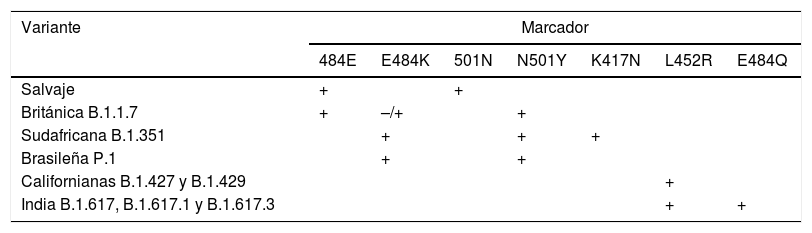
Diagnóstico de variantesAl margen de las importantes repercusiones clínico-epidemiológicas que puedan generar, una consecuencia secundaria de la aparición de las cepas mutantes radica en la pérdida de rendimiento de determinados test de diagnóstico in vitro39. Los métodos de secuenciación del genoma completo son las técnicas de referencia para la identificación de las variantes de SARS-CoV-240. Sin embargo, recientemente se han desarrollado para este propósito procedimientos alternativos, más simples y rápidos, basados en técnicas de PCR en tiempo real para la detección de mutaciones específicas41. Ciertas combinaciones de marcadores mutantes permiten diferenciar las principales variantes. La combinación 484E y 501N identifica a la cepa salvaje. La combinación 484E y 501Y identifica a la británica. La presencia concomitante de 484K y 501Y se da en las variantes brasileña y sudafricana, pero esta última también porta la mutación 417N. Las variantes californianas contienen la mutación L452R. Las nuevas variantes indias B.1.617, B.1.617.1 y B.1.617.3 reúnen esta última mutación junto con la E484Q. La tabla 3 muestra los marcadores de las mutaciones que permiten distinguir entre las variantes más importantes.
Marcadores de las mutaciones que permiten distinguir entre las principales variantes actualmente circulantes
| Variante | Marcador | ||||||
|---|---|---|---|---|---|---|---|
| 484E | E484K | 501N | N501Y | K417N | L452R | E484Q | |
| Salvaje | + | + | |||||
| Británica B.1.1.7 | + | –/+ | + | ||||
| Sudafricana B.1.351 | + | + | + | ||||
| Brasileña P.1 | + | + | |||||
| Californianas B.1.427 y B.1.429 | + | ||||||
| India B.1.617, B.1.617.1 y B.1.617.3 | + | + | |||||
La vacunación masiva que se ha comenzado a aplicar en los últimos meses puede significar el inicio del fin de la actual pandemia de COVID-19. Sin embargo, es previsible que en un futuro próximo continúen apareciendo nuevas variantes del virus. Esto hace necesaria una monitorización de las mutaciones que puedan producirse, para adecuar así las pertinentes medidas de Salud Pública10. Las potenciales nuevas cepas que puedan surgir pueden conllevar cambios respecto a su capacidad infectiva, evolución clínica, pronóstico y efectividad vacunal. En concreto, en el peor de los casos, se debe estar alerta ante la eventual y temida posibilidad de emergencia de variantes de alta importancia (no identificadas en el presente). Por el momento, permanecen vigentes las medidas preventivas estándar destinadas a reducir la transmisión, basadas en limitar los contactos interpersonales y mantener las distancias sociales de seguridad42. Ciertas vacunas conservan su eficacia protectora frente a nuevas variantes y, de esta forma, su empleo extensivo puede resultar altamente exitoso40.
A fin de evitar la posibilidad de selección de variantes de escape vacunal, se recomienda emplear preparados que ya con una dosis generen niveles elevados de anticuerpos con una alta actividad de neutralización y, para aquellas vacunas que requieren dos dosis, no prolongar demasiado el intervalo entre la primera y la segunda33. Entre las estrategias futuras propuestas para la inmunoprotección se ha sugerido: el incremento del número de dosis, la alternancia vacunal y el desarrollo de vacunas monovalentes y polivalentes frente a diferentes variantes43.
FinanciaciónLos autores declaran que no han recibido financiación para la realización de este estudio.
Conflicto de interésLos autores declaran no tener ningún conflicto de intereses.