El manejo de los defectos óseos completos secundarios a una infección periprotésica a nivel de la cadera y/o rodilla continúa siendo un auténtico reto quirúrgico.
Material y métodosPresentamos una modificación técnica para la realización de un espaciador femoral biarticulado con un enclavado femoral, sin necesidad de abordar la tibia proximal, ya sea para obtener la fijación del espaciador o la articulación del mismo.
ResultadosSe han intervenido 3 pacientes mediante esta técnica, no existiendo ninguna complicación intraoperatoria, resolviéndose la infección y mejorando la función previa en todos ellos, volviendo a deambular con diferentes ayudas.
ConclusionesEsta modificación técnica es una alternativa en aquellos casos donde es preciso resecar el fémur completo pero no es necesario abordar la tibia.
The management of complete bone defects in hip and knee periprosthetic infection is still a real surgical challenge.
Material and methodsWe present a technical modification for performing a biarticular total femoral spacer with a femoral nail without the need to approach the proximal tibia.
ResultsThree patients were operated with this technique. There was no intraoperative complication. The infection was resolved in all patients operated at final follow-up. All patients improved their previous functional situation and could walk with different aids.
ConclusionsThis technical modification is an alternative for cases where it is necessary to resect the complete femur, but it is not necessary to approach the tibia.
La infección periprotésica es una de las complicaciones más devastadoras en cirugía protésica. El recambio en dos tiempos sigue siendo el «patrón oro» para el tratamiento de la infección periprotésica1-3. A pesar del aumento de popularidad del recambio en un tiempo, debido principalmente a un teórico menor coste, duración, mejores resultados funcionales con menor morbimortalidad y similares tasas de curación4, la cirugía en dos tiempos sigue presentando mejores tasas de curación en situaciones especiales. Estas situaciones incluyen pacientes multiintervenidos, microorganismos resistentes, infecciones polimicrobianas o cuando existen defectos óseos voluminosos que requieren implantes tumorales o aloinjertos masivos5, cada vez más frecuentes en la práctica diaria.
En casos donde el defecto femoral, una vez retirado el implante, se considera masivo, resulta especialmente compleja la implantación de un espaciador articulado. Esto es debido a que la incidencia de complicaciones habitualmente observadas con el uso de espaciadores (luxación, fractura periimplante y rotura del propio espaciador) aumenta considerablemente cuando existe este tipo de defectos óseos, siendo un auténtico reto quirúrgico en defectos femorales completos6.
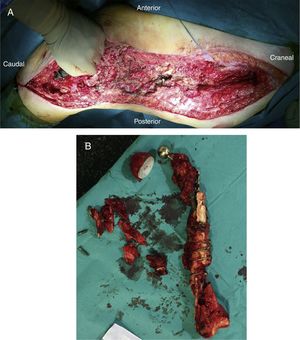
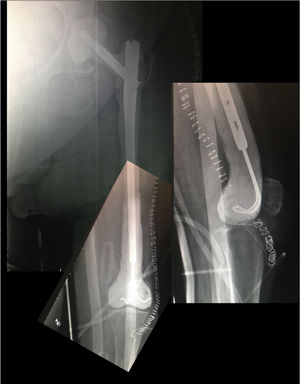
Actualmente existen diferentes técnicas quirúrgicas para la realización de un espaciador de fémur completo, teniendo todas en común la necesidad de sacrificar la articulación de la rodilla. Para ello, de manera general, utilizan un enclavado intramedular para fijar el espaciador a nivel del tercio medio de la tibia, y diferentes «implantes» para realizar la reconstrucción el fémur proximal7-10. Nosotros describimos previamente una nueva técnica para la realización de un espaciador femoral biarticulado10, evitando el sacrificio de la articulación de la rodilla. Para ello se realiza, a nivel de la rodilla, una articulación tipo ball and socket, según la técnica descrita por MacAvoy y Ries11. No obstante, la utilización de esta técnica implica el fresado inicial de la superficie proximal de la tibia, lo que puede conllevar la aparición de un defecto óseo en el segundo tiempo quirúrgico. Para evitar esta pérdida ósea y sus consecuencias asociadas, presentamos una modificación de la técnica original, realizando de manera manual una articulación del fémur distal que articula con la tibia proximal, manteniendo ambos meniscos hasta el segundo tiempo (fig. 1).
Técnica quirúrgicaPreparación y abordajeLa intervención se lleva a cabo bajo anestesia general en decúbito lateral, permitiendo el acceso a la cadera y la rodilla. Es importante, a la hora de preparar el campo quirúrgico, dejar libre la región inguinal como posible acceso vascular, por si fuera necesario durante la intervención. A nivel proximal se realiza una vía de abordaje posterolateral, siendo esta la utilizada de rutina por los autores, efectuando además una extensión distal por la cara lateral del muslo hasta convertirse en un abordaje anterolateral a nivel de la rodilla. Tras la disección superficial, se realiza una apertura fascial entre la fascia lata y el glúteo mayor a nivel proximal, disecando las fibras musculares de este último a nivel proximal y de la cintilla iliotibial a nivel distal llegando al plano óseo. Posteriormente se realiza una artrotomía en L incluyendo «en bloque» cápsula y rotadores, movilizando estos tejidos hacia posterior para la protección de las estructuras nerviosas.
Tras completar el abordaje, se comprueba macroscópicamente el aspecto del trocánter mayor, para decidir si se respeta parte de este, o se sacrifica completamente. En caso de respetarlo, se realiza una osteotomía deslizante paralela al eje longitudinal del fémur, dejando una pastilla ósea de trocánter mayor, tratando de mantener las inserciones musculares del glúteo medio y vasto lateral. Si no es posible conservar dicha pastilla, se lleva a cabo una disección subperióstica liberando dichas estructura musculares. Posteriormente se continúa con la disección distal, desplazando el vasto lateral hacia anterior con la ayuda de 2 retractores tipo Hohmann, siendo especialmente cuidadoso con la hemostasia a nivel de la línea áspera.
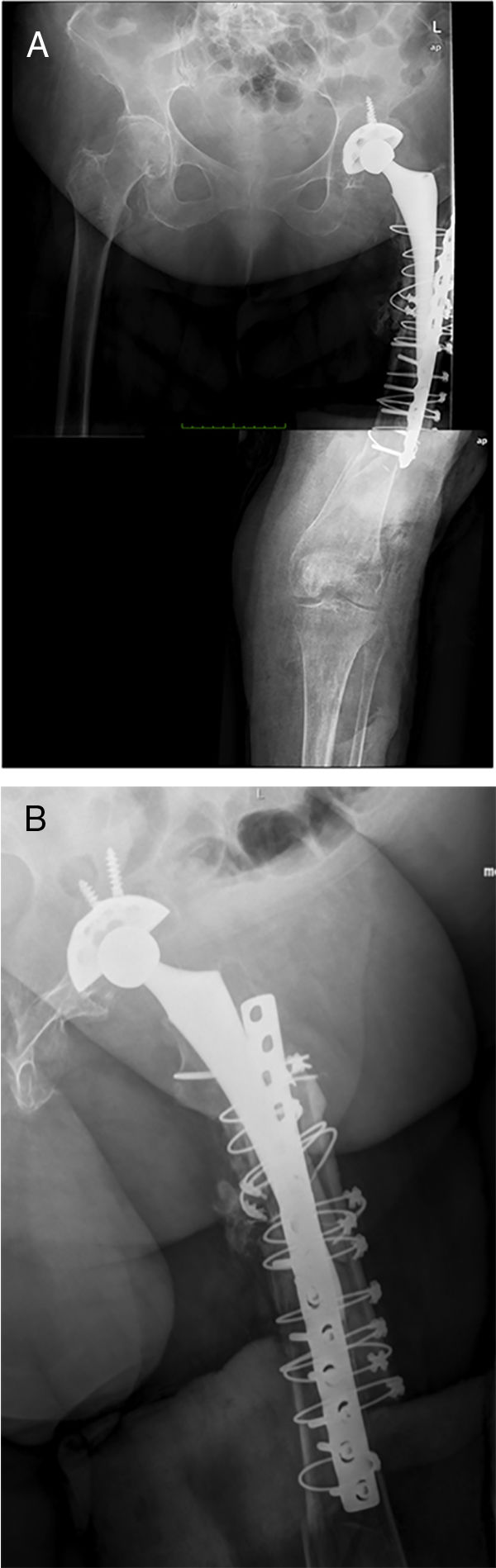
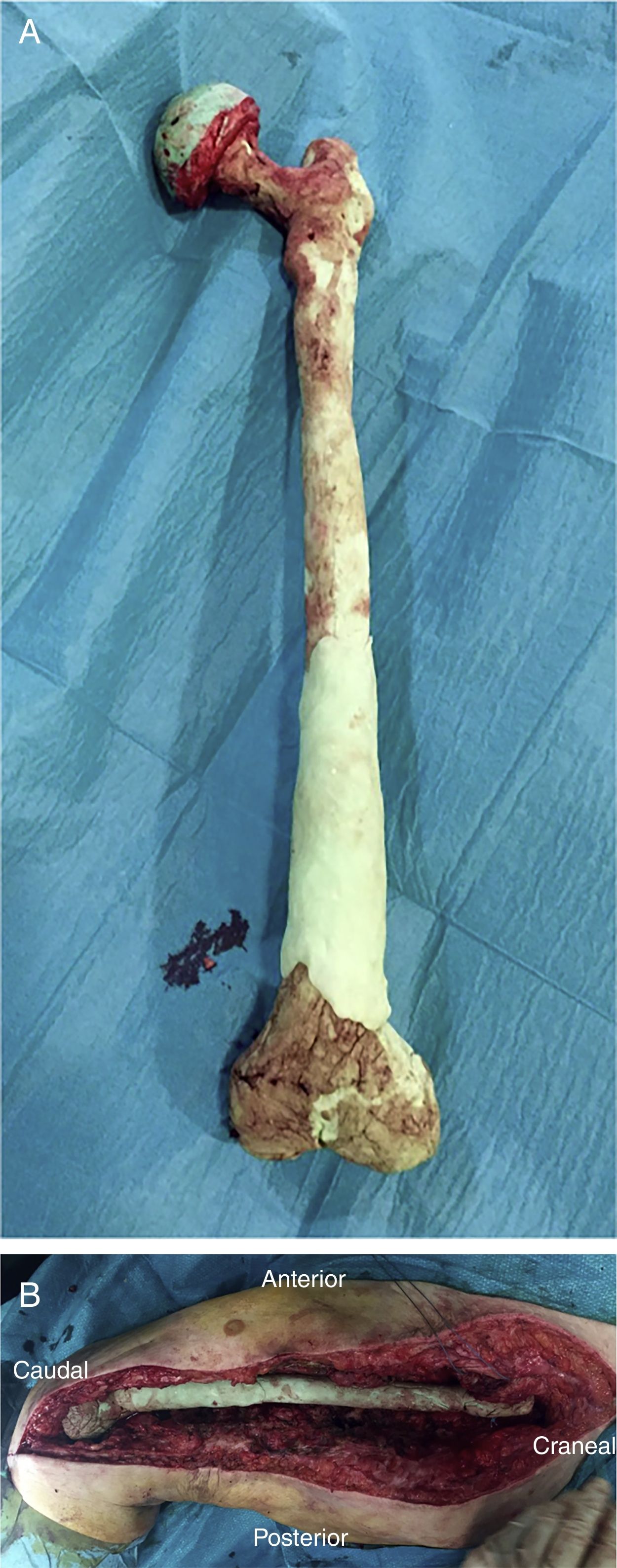
Tras la liberación de toda la cara posterolateral del fémur, se prosigue con la disección medial, dependiendo de la situación del propio fémur. En caso de encontrarse fracturado (fig. 1), se realizará la disección desde la zona media de este, elevándose con una pinza tipo Verbrugge ambos fragmentos, disecando desde el foco de la fractura hacia proximal o distal, y teniendo especial cuidado de separar de manera roma las estructuras mediales para alejarse lo máximo posible de los vasos. A nivel distal, previa liberación del epicóndilo lateral, se realiza un movimiento de rotación interna del fragmento óseo, liberándose ambos cruzados en la escotadura y, por último, el ligamento colateral medial a nivel del epicóndilo medial, tratando de respetar ambos meniscos.
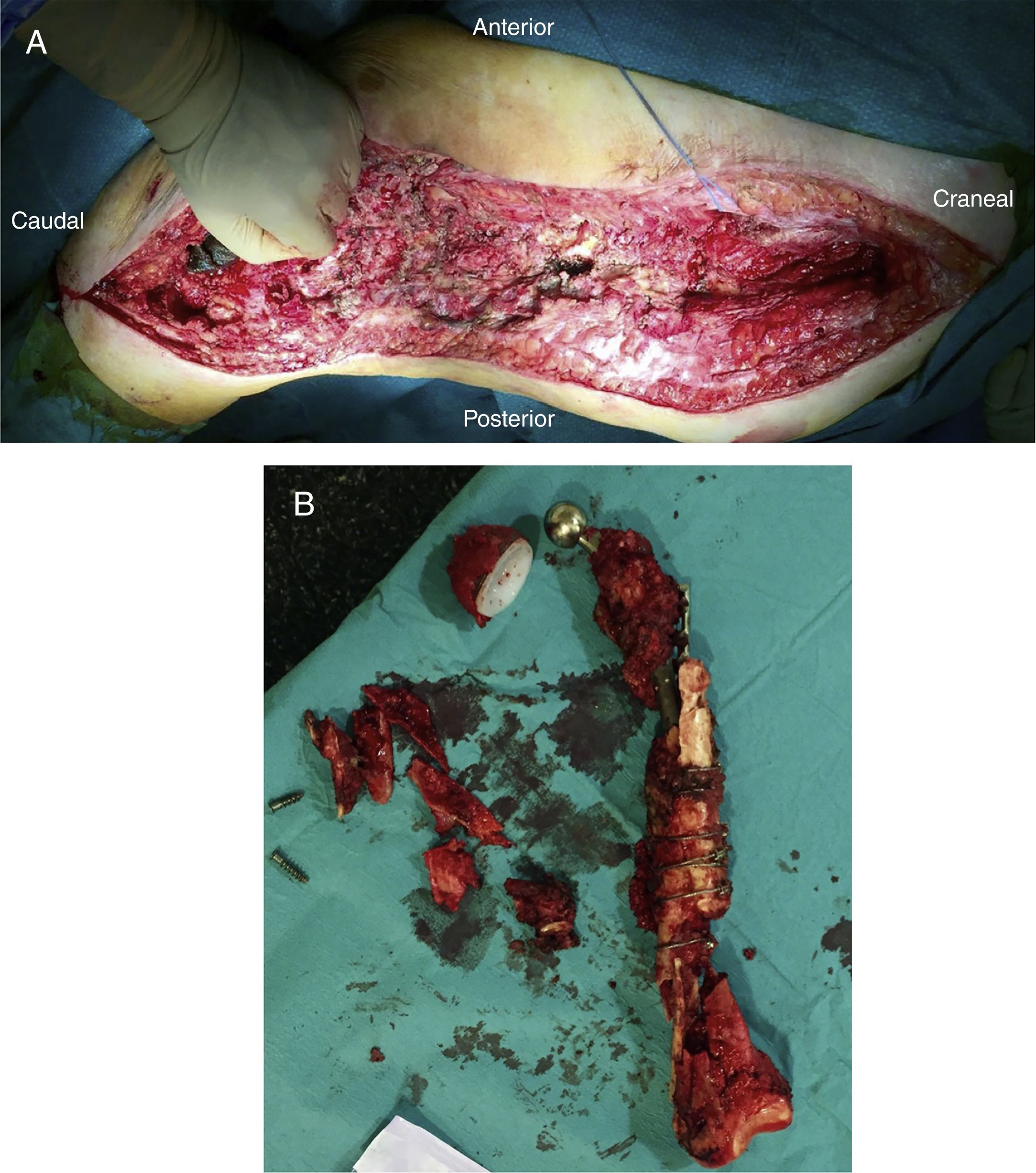
Una vez efectuada la extracción del fémur, se obtienen 6 muestras para su análisis microbiológico, a las que se suma el implante explantado según protocolo (fig. 2A). Posteriormente se procede con un desbridamiento amplio de todos los tejidos necróticos, hasta obtener un lecho sangrante (fig. 2B), teniendo especial cuidado en la zona medial a nivel proximal y la zona posteromedial a nivel distal para no lesionar las estructuras vasculares (fig. 2).
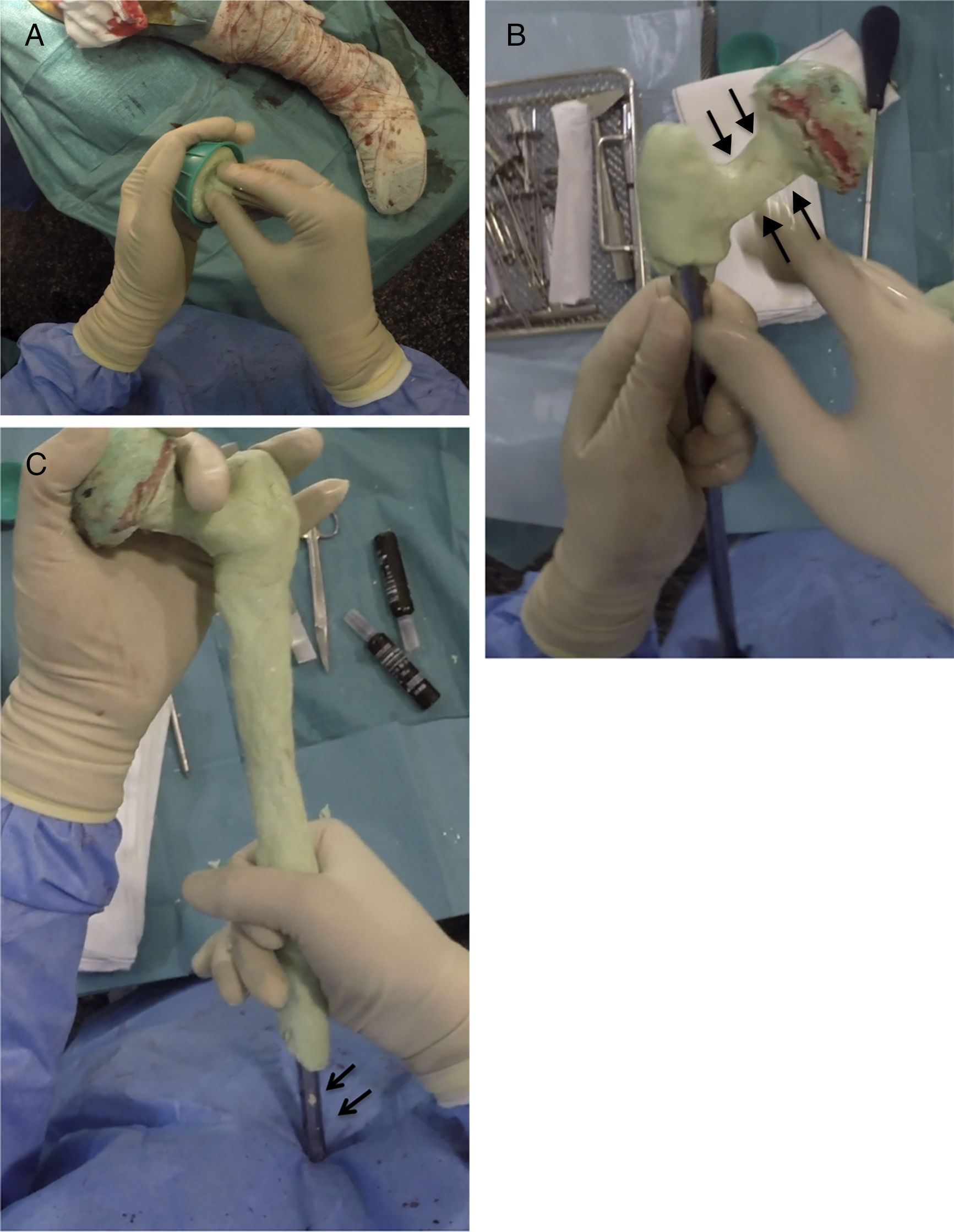
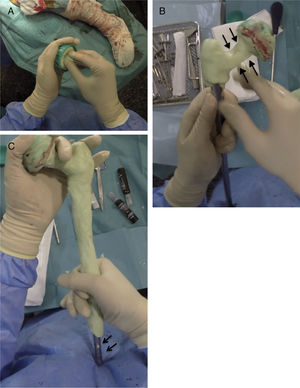
Realización del espaciadorPreviamente a la cirugía es necesario realizar una radiografía calibrada del fémur completo, para decidir la longitud del implante a usar en la reconstrucción. Para realizar el esqueleto del espaciador, se utiliza un enclavado cefalomedular al menos 6cm menor que la longitud del fémur previamente medida. El tornillo cefálico utilizado suele ser de 75-85mm de longitud en función del offset necesario, siendo importante que el tornillo no sobresalga en la cara lateral del clavo para evitar complicaciones a la hora del cierre. Una vez montado el clavo, se realiza la cabeza femoral de este, utilizando para ello como molde la pera de una jeringa de lavado (fig. 3A). Es importante intentar conseguir la mejor relación cabeza/cuello posible y cubrir completamente la zona proximal y media del clavo con cemento con antibióticos que dependerán del microorganismo causante de la infección (fig. 3B). Es importante dejar la zona distal del clavo sin cubrir en este paso para evitar la entrada de cemento en el interior del canal del clavo (fig. 3C).
Secuencia de la realización de la parte proximal y cuerpo espaciador. A) Realización de la cabeza femoral con jeringa de lavado y tornillo cefálico enclavado cefalomedular. B) Realización del cuello de la zona proximal. Nótese la relación cabeza/cuello favorable (flechas). C) Cobertura del cuerpo espaciador, dejando la zona distal libre (flechas).
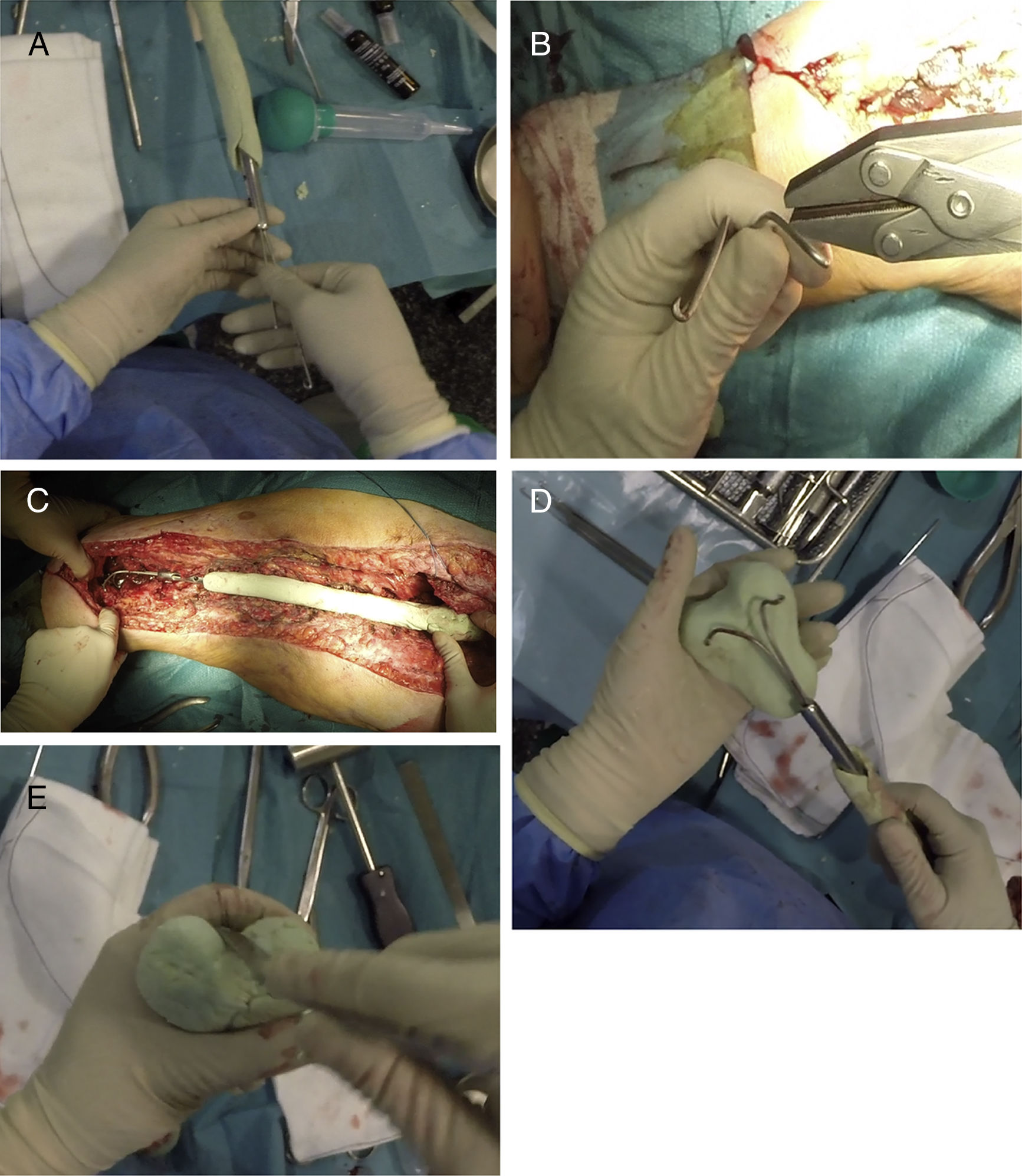
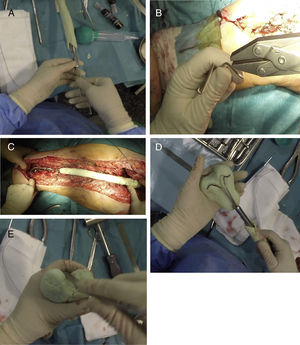
Una vez finalizada la parte proximal y media del espaciador, se utilizan 2 clavos tipo Rush de pequeño diámetro, que se doblarán según se aprecia en la figura 4A, introduciéndolos en el interior del clavo, dejando la zona distal de estos divergentes (fig. 4B). Antes de cubrir estos clavos con cemento, es necesario presentar el espaciador en el lecho quirúrgico para comprobar la adecuada longitud de este (fig. 4C). Una vez seguros de la correcta longitud del espaciador, se cubren dichos clavos con más cemento con antibiótico, procurando imitar la anatomía del fémur distal, poniendo especial énfasis en la forma de los cóndilos posteriores (tamaño y offset) y en la tróclea femoral (fig. 4D y E). También es importante poner especial atención a la anteversión de dichos cóndilos, siendo recomendable la realización de estos colocando el cuello femoral a 20-30° respecto a la mesa de trabajo. En este momento se pueden llevar a cabo perforaciones en las caras laterales del fémur para tratar de reanclar las estructuras colaterales, aunque en la experiencia de los autores, este gesto es innecesario.
Secuencia de la realización de la zona distal del espaciador. A) Introducción de clavos de Rush dentro del clavo femoral. B) Curvatura de los clavos para servir como esqueleto de la articulación distal. C) Presentación previa de la realización de la zona distal para llevar a cabo el ajuste «fino» de la longitud del espaciador. D) Cobertura de los clavos de Rush con cemento con antibiótico tratando de obtener la forma de un fémur distal. E) Remate final de la zona distal, poniendo especial énfasis en la tróclea y los cóndilos femorales.
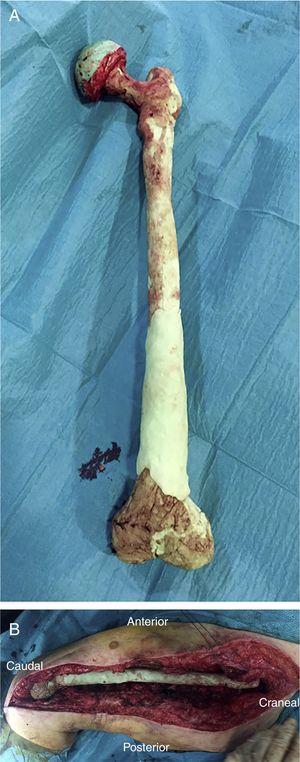
Tras la realización del espaciador (fig. 5A) se reduce este en el lecho quirúrgico, primero a nivel distal haciendo coincidir ambos cóndilos con ambos meniscos y posteriormente a nivel proximal (fig. 5B). Tras comprobar la estabilidad de los componentes y la posibilidad de obtener 90° de flexión en ambas articulaciones se realiza un cierre por planos, como en cualquier abordaje de cadera/rodilla.
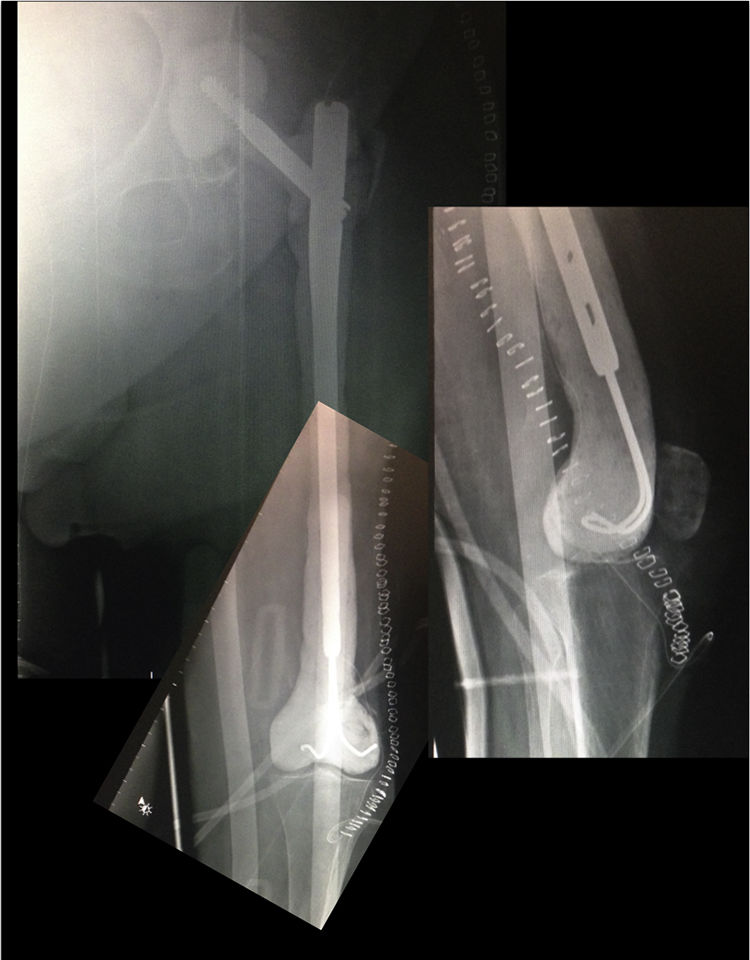
PostoperatorioA las 24h se efectúa un control radiográfico (fig. 6), comprobando que el espaciador se encuentra posicionado correctamente, y se permite al paciente sentarse, insistiendo en la realización pasiva y activa de ejercicios de flexo-extensión de la rodilla y cadera. La carga parcial es permitida, siendo necesaria la utilización de una ortesis a nivel de la rodilla para controlar la posible inestabilidad residual, no siendo necesaria a nivel de la cadera.
ResultadosMediante esta técnica se han intervenido 3 pacientes con un seguimiento mínimo de un año tras el segundo tiempo. La edad media de los pacientes fue de 81 años (75-89), y todas eran mujeres. Todos los pacientes presentaban una elevada morbilidad, como muestra el elevado índice de Charlson (5 en 2 pacientes, y 6 en uno) y el grado de la valoración anestésica preoperatoria ASA (2 pacientes ASA III, y un paciente ASA II). El número medio de cirugías previas fue de 5,3 (2-11), siendo la indicación quirúrgica la presencia de una infección periprotésica sobre un vástago largo en 2 casos, y una fractura periprotésica sobre un paciente con tratamiento supresor crónico en una infección periprotésica previa. Todos los pacientes presentaban defectos femorales tipo IV que justifican la utilización de esta técnica, siendo el defecto acetabular asociado según la clasificación de Praposky de tipo IIB, IIIA y IIIB. Un solo paciente era capaz de deambular con andador previamente, utilizando el resto silla de ruedas de manera continua (tabla 1).
Datos demográficos
| Paciente | Edad | Sexo | Implante previo | Pérdida ósea femoral | Pérdida ósea acetabular | N.o cirugías previas | Años tras última cirugía | ASA | Índice Charlson | Capacidad de deambulación |
|---|---|---|---|---|---|---|---|---|---|---|
| Caso 1 | 89 | F | Vástago cónico+placa periprotésica+cotilo hemisférico | IV | IIB | 3 | 5 | III | 6 | No |
| Caso 2 | 79 | F | Vástago cónico+placa periprotésica+cotilo roscado intrapélvico | IV | IIIA | 2 | 18 | III | 5 | No |
| Caso 3 | 75 | F | Vástago Wagner+cup-cage | IV | IIIB | 11 | 4 | II | 5 | Sí (andador) |
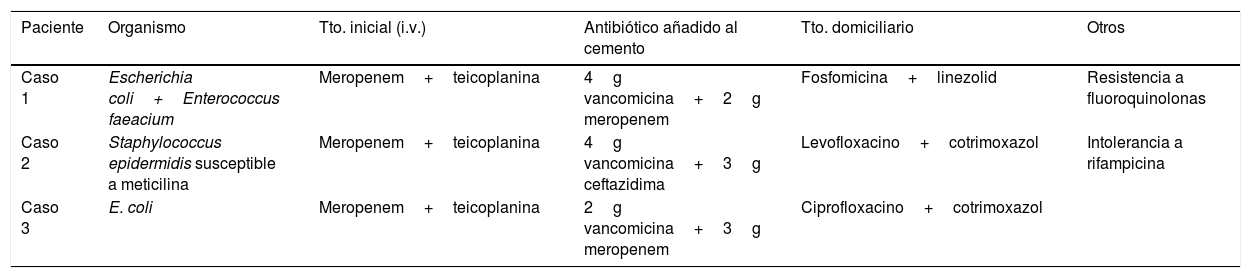
En todos los pacientes se realizó una aspiración preoperatoria, obteniéndose en 2 casos cultivos positivos para Escherichia coli y en el tercer caso un Staphylococcus epidermidis. En 2 casos se añadió en el cemento 4g de vancomicina+2g de meropenem; y en el tercero, 4g vancomicina+2g de ceftazidima. El antibiótico oral utilizado entre el primer y el segundo tiempo queda reflejado en la tabla 2.
Patógenos y antibióticos utilizados en función del organismo identificado
| Paciente | Organismo | Tto. inicial (i.v.) | Antibiótico añadido al cemento | Tto. domiciliario | Otros |
|---|---|---|---|---|---|
| Caso 1 | Escherichia coli+Enterococcus faeacium | Meropenem+teicoplanina | 4g vancomicina+2g meropenem | Fosfomicina+linezolid | Resistencia a fluoroquinolonas |
| Caso 2 | Staphylococcus epidermidis susceptible a meticilina | Meropenem+teicoplanina | 4g vancomicina+3g ceftazidima | Levofloxacino+cotrimoxazol | Intolerancia a rifampicina |
| Caso 3 | E. coli | Meropenem+teicoplanina | 2g vancomicina+3g meropenem | Ciprofloxacino+cotrimoxazol |
Ningún paciente presentó complicación intraquirúgica alguna, obteniendo todos la capacidad de sedestación en la primera semana de evolución. No hubo ninguna fractura ni luxación del espaciador.
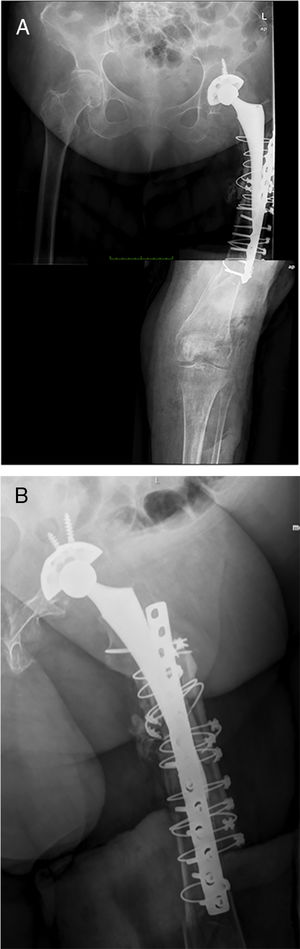
En todos los pacientes se resolvió la infección, definiéndose como tal la obtención de cultivos negativos en el segundo tiempo así como ausencia de clínica al final del seguimiento (mínimo un año). En todos los pacientes se realizó el segundo tiempo mediante la implantación de un fémur total Mega C® (Waldemar LINK GmbH, Hamburgo, Alemania) con diferentes sistemas de reconstrucción acetabular, usándose en todos los pacientes cotilos constreñidos. En ningún paciente fue necesaria la utilización de espaciadores a nivel tibial al no existir ningún defecto óseo a ese nivel.
Al año de la intervención todos los pacientes se encontraban libres de infección, siendo capaces de deambular con ayuda de andador (2 pacientes) y con una muleta (un paciente), estando todos satisfechos con la intervención.
DiscusiónMientras el número de prótesis primarias, de revisión e infecciones periprotésicas incrementa continuamente, el número de revisiones en dos tiempos también aumenta12. Múltiples estudios han demostrado la utilidad del uso de un espaciador articulado en el tratamiento de la infección periprotésica, con mejores tasas de erradicación de la infección, facilitando la reimplantación de la prótesis definitiva y mejorando los resultados funcionales de los pacientes13-16. En pacientes con mínima pérdida ósea, los espaciadores comerciales resultan útiles17,18. No obstante, la presencia de bacterias resistentes a múltiples antibióticos o fracturas periprotésicas hacen inadecuados estos espaciadores, especialmente en pacientes con defectos óseos severos y pobre calidad ósea secundaria a múltiples cirugías, siendo necesario realizar los espaciadores de manera manual según diferentes técnicas publicadas11,19-21.
A pesar de las teóricas ventajas del uso del espaciador, existen múltiples complicaciones inherentes al propio espaciador, como son la luxación, la fractura periespaciador y la propia fractura del espaciador13,19,20,22. Hay diferentes factores que favorecen estas complicaciones. En primer lugar, la baja relación cabeza-cuello de los espaciadores comerciales, como de la mayoría de los realizados manualmente, es un factor de riesgo para la luxación de este. Un segundo factor asociado al fallo de los espaciadores es el insuficiente anclaje en el canal intramedular, especialmente en defectos óseos masivos. Leuning et al.22 observaron un anclaje de 22±33mm en espaciadores fracasados debido a fracturas (periprotésicas y del propio implante) frente a un anclaje de 57±41mm en el grupo de espaciadores sin fracturas asociadas. El uso de espaciadores en defectos masivos acrecienta el riesgo de aparición de estas complicaciones6,23.
Existen múltiples técnicas descritas para la realización de espaciadores en defectos óseos masivos, utilizando diferentes estructuras como «esqueleto» del espaciador. No obstante, cuando el defecto afecta al fémur completo7-10, solo existen 4 artículos publicados que muestren cómo realizar un espaciador de fémur completo, siendo común a todos la utilización de una fijación intramedular a nivel tibial mediante el uso de un clavo como «esqueleto» del espaciador, sacrificando la articulación de la rodilla entre ambos tiempos y utilizando un vástago femoral cementado o un espaciador tipo Prostalac a nivel proximal para realizar la parte proximal del espaciador. Solo Canham et al.7 y Sanz-Ruiz et al.10 han mostrado una alternativa a la fijación tibial, mediante la creación de un espaciador biarticulado. Canham et al.7 utilizaron 2 espaciadores comerciales, uno de cadera y otro de rodilla, que conectaban mediante la utilización de 3 clavos de Harrington reforzados con cemento. A diferencia de la técnica de Canham, la utilización de un clavo cefalomedular como esqueleto del espaciador permite, además de elegir el diámetro de la cabeza femoral más adecuado, poder determinar el offset necesario para mantener una adecuada tensión de las estructuras periarticulares a nivel de la cadera, maximizando la estabilidad del propio espaciador. A nivel distal, la realización de una articulación tipo ball and socket aumenta la estabilidad en ausencia de ligamentos, como diferentes series previamente han mostrado. A las ventajas antes descritas hay que añadir la solidez del propio espaciador, siendo más resistente a posibles fracasos. Esto queda patente en que en todos los pacientes intervenidos con esta técnica se les permitió mantener la bipedestación con ayuda de una rodillera. En último lugar, es importante recalcar que el coste de la realización de un espaciador con un enclavado cefalomedular y 2 clavos de Rush es sensiblemente inferior a la técnica descrita por Canham, donde la utilización de 2 espaciadores comerciales (Prostalac+espaciador comercial de rodilla) eleva de manera considerable el coste de dicho espaciador. Esto es especialmente importante, teniendo en cuenta que en estos pacientes será necesario implantar en un segundo tiempo implantes tumorales de fémur completo, con costes generalmente muy elevados.
En resumen, en este artículo se presentan las ventajas y posibles inconvenientes de una modificación técnica en la articulación distal del espaciador biarticulado previamente publicado10. Esta modificación permite respetar el hueso tibial en pacientes en los que, debido a la causa de la cirugía, no resulte necesaria su resección. En todos los pacientes intervenidos mediante dicha modificación, se llevó a cabo el mismo protocolo posquirúrgico que en los pacientes con la técnica convencional (ball and socket), no existiendo ningún episodio de luxación del espaciador, aunque en todos los pacientes fue necesaria la utilización de una ortesis estabilizadora para la bipedestación. En nuestra opinión, la posibilidad de evitar el fresado a nivel tibial disminuye la agresividad de la propia cirugía, disminuyendo el dolor postoperatorio a nivel de la rodilla y evitando completamente la presencia de defectos óseos metafisarios a nivel de la rodilla en el segundo tiempo quirúrgico. La ausencia de defectos óseos tibiales en el segundo tiempo disminuye el tiempo quirúrgico en dicho proceso, dado que evita la necesidad de reconstrucción de dichos defectos, así como la necesidad del uso de sistemas de reconstrucción complejos, como conos, vainas, etc., con el consiguiente ahorro económico.
El presente artículo no está exento de limitaciones. La primera de ellas es el bajo número de pacientes intervenidos con dicha técnica, lo que hace prácticamente imposible la extracción de conclusiones clínicas. No obstante, dado que solo existen 6 casos publicados de espaciadores de fémur distal, pensamos que el bajo tamaño no es una limitación para la aplicación de esta técnica quirúrgica para situaciones excepcionales como es la presencia de un defecto femoral masivo en el contexto de una infección periprotésica. La segunda de ellas es el corto periodo de seguimiento de los pacientes presentados (mínimo un año). No obstante, no es el objetivo del presente manuscrito el seguimiento de dichos pacientes, sino presentar la seguridad de una modificación de una técnica quirúrgica previamente descrita y sus teóricas ventajas respecto a la previa, no debiendo existir diferencias en el control de la infección respecto a la técnica original.
ConclusiónLa modificación de la articulación distal en un espaciador biarticulado resulta útil para el tratamiento de los defectos femorales totales en el contexto de una infección periprotésica cuando no es necesario resecar hueso tibial, disminuyendo el defecto óseo existente en el segundo tiempo. No obstante, dichas afirmaciones deben tomarse con cautela dado el bajo número de pacientes intervenidos con dicha técnica.
Nivel de evidenciaNivel de evidencia V.
FinanciaciónNo se ha recibido ninguna fuente de financiación.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de intereses en relación con el artículo presentado.