El trastorno bipolar y la demencia son entidades clínicas de gran repercusión y calado dentro de la comunidad psiquiátrica internacional. La demencia es una de las patologías más incapacitantes a nivel cognitivo, funcional, social y económico, y representa una de las principales enfermedades que más preocupación causan a la población mayor de 60años. El objetivo consistió en explorar la posible existencia de una correlación entre el trastorno bipolar y la demencia, con el fin de conocer si el trastorno bipolar es un factor de riesgo predisponente para el desarrollo posterior de demencia en la vejez.
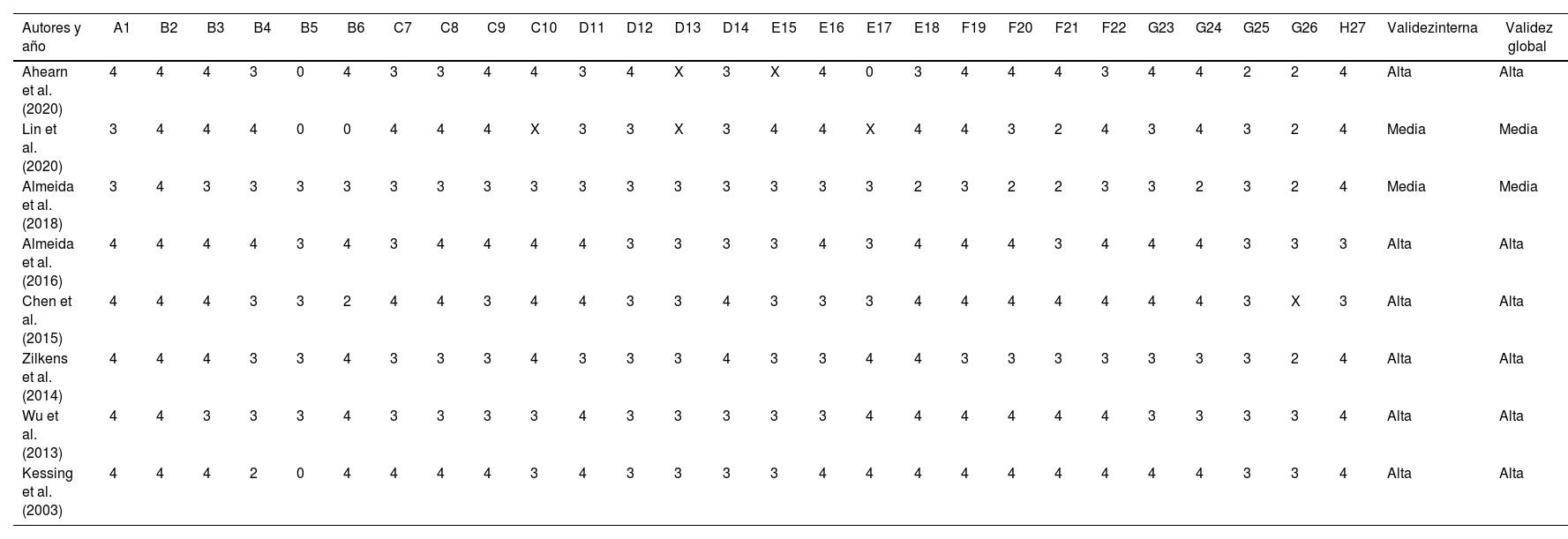
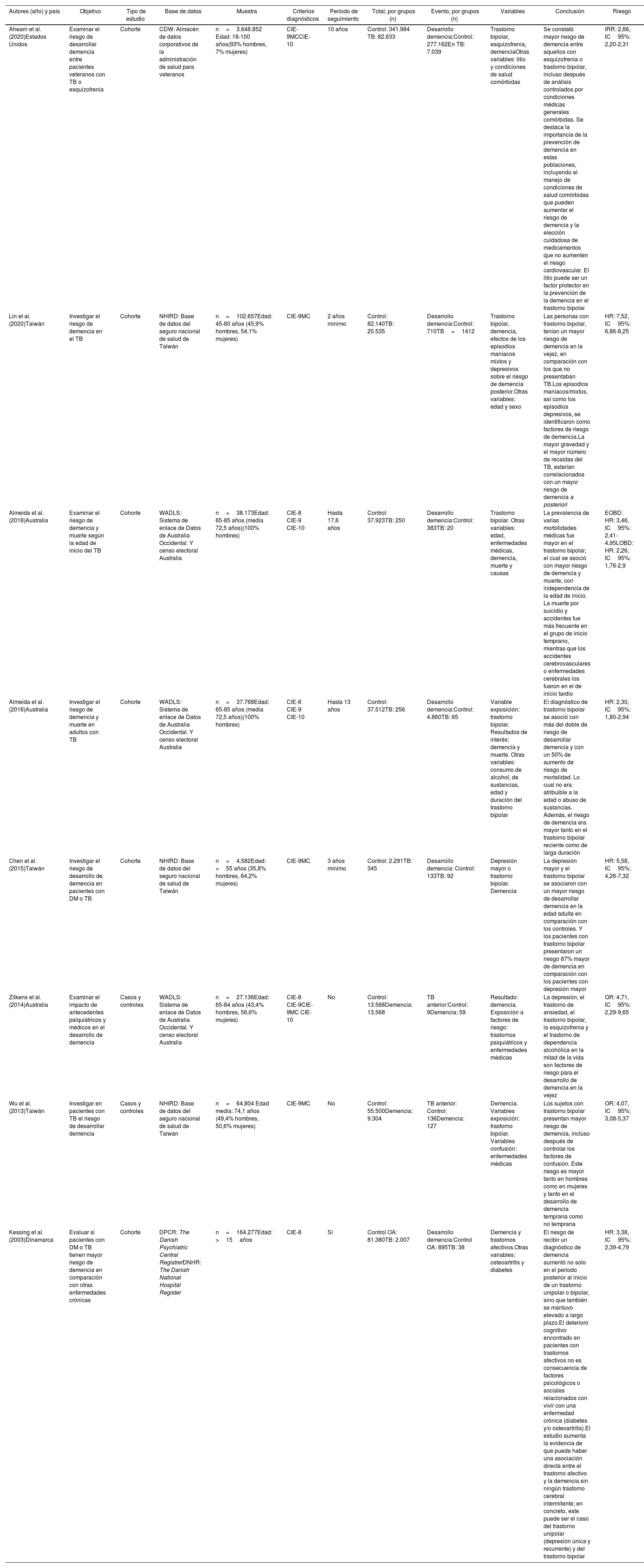
DesarrolloSe llevó a cabo una búsqueda en las bases de datos PubMed, PsycInfo y Web of Science. Se acotó la búsqueda a artículos publicados entre los años 2000 y 2020. Se obtuvieron 1.708 artículos. Se eliminaron aquellos repetidos y no relacionados con el tema, quedando un total de 8 artículos que cumplían con los criterios de selección. Esta revisión sistemática se llevó a cabo de acuerdo con los criterios de la declaración PRISMA.
ConclusionesSe encontró que el trastorno bipolar está asociado con una mayor probabilidad de presentar demencia en el futuro, siendo este resultado consistente en todos los estudios. Además, se halló que es un factor de riesgo de demencia independientemente de si el trastorno bipolar es de inicio temprano o tardío, que supone un riesgo mayor de demencia que la depresión y que implica un aumento del riesgo de mortalidad.
Bipolar disorder and dementia are clinical entities of great impact and depth within the international psychiatric community, dementia being one of the most disabling pathologies at a cognitive, functional, social and economic level, representing one of the main diseases that most concern. It affects the population over 60years of age. The objective was to explore the possible existence of a correlation between bipolar disorder and dementia, in order to know if bipolar disorder is a predisposing risk factor for the later development of dementia in old age.
DevelopmentA search was carried out in the PubMed, PsycInfo and Web of Science databases. The search was limited to articles published between the years 2000 and 2020. 1708 articles were obtained. Those repeated and unrelated to the topic were eliminated, leaving a total of 8 articles that met the selection criteria. This systematic review was carried out according to the criteria of the PRISMA statement.
ConclusionsBipolar disorder was found to be associated with a higher probability of presenting dementia in the future, this result being consistent in all studies. In addition, it was found to be a risk factor for dementia regardless of whether the bipolar disorder is early or late onset, to carry a higher risk of dementia than depression, and to carry an increased risk of mortality.