Introducción
El compromiso ético que tenemos los profesionales sanitarios de ofrecer a los pacientes una atención de suficiente calidad, junto con la concepción actual del sistema sanitario como empresa de servicios y la necesidad de contener el gasto sanitario, han generado un creciente interés por la evaluación y mejora continua de la calidad de la asistencia sanitaria en todas sus dimensiones, introduciendo poco a poco en nuestras organizaciones sanitarias el concepto de gestión por procesos en el camino hacia la excelencia.
Gestionar la calidad en un servicio de cirugía requiere la participación decidida de sus máximos responsables, junto con una formación adecuada de los profesionales del equipo y una selección cuidadosa de los procesos clave, con el fin de analizarlos, simplificarlos y establecer los indicadores precisos para controlar su calidad. Los sistemas de información son herramientas imprescindibles para la correcta gestión de los procesos1.
Nuestras organizaciones sanitarias se caracterizan por la presencia de una gran variabilidad en la práctica clínica. Esto se relaciona, por una parte, con la falta de evidencia científica sobre algunas actividades asistenciales, pero también con la ausencia de información suficiente sobre los propios procesos que se desarrollan en la institución y con los estilos de práctica de los profesionales. Esta variabilidad no deseable conlleva falta de eficiencia, peores resultados clínicos e insatisfacción de los pacientes2. Por todo ello se han buscado diferentes formas de sistematizar los procesos mediante protocolos, guías de práctica clínica y vías clínicas (VC).
Las VC son planes asistenciales diseñados específicamente para un proceso clínico de evolución predecible. Definen la secuencia de duración y las responsabilidades de las actividades de los médicos, enfermería y otros profesionales que actúan en el proceso. Se han de sustentar en la evidencia científica y deben ser consensuadas por los profesionales implicados en el proceso. Facilitan la sistematización del proceso y la evaluación de los resultados mediante el análisis periódico de los indicadores y su comparación con los estándares previamente fijados3.
El desarrollo y la implantación de una VC obtienen los mejores resultados cuando se aplican sobre un proceso prevalente, con variabilidad conocida y en el que se hayan identificado determinadas áreas susceptibles de mejora en relación con su manejo clínico. El diseño de una VC se ve facilitado si previamente se obtiene información sobre las distintas dimensiones de la calidad (calidad científico-técnica, efectividad clínica, eficiencia y calidad percibidas) del proceso que se desea gestionar ya que, además, aporta una valiosa información para definir los objetivos que se pretende conseguir e identificar los indicadores y estándares adecuados.
El desarrollo en nuestra unidad de una metodología para la gestión de procesos nos ha permitido mejorar de manera progresiva los más representativos mediante el análisis de distintas dimensiones de la calidad y el desarrollo de VC como instrumentos de mejora.
Siguiendo esta línea de trabajo, presentamos la sistemática seguida para la gestión del proceso "Tratamiento quirúrgico del cáncer gástrico" tras haberlo evaluado bajo la perspectiva de las distintas dimensiones de la calidad (calidad científico-técnica, efectividad clínica, eficiencia y calidad percibida) y haber diseñado un plan de mejora mediante el desarrollo de una VC. La disponibilidad en nuestro hospital de un Registro de tumores4 y de un Protocolo para el diagnóstico y tratamiento del cáncer gástrico5 ha permitido disponer de información adicional que ha servido como referencia para el análisis del proceso y el propio diseño de la VC.
Aunque la incidencia de carcinoma gástrico está disminuyendo de forma evidente en todos los países del mundo (ha descendido de 32,5 a 15,5 por 100.000 varones y de 17,6 a 7,0 por 100.000 mujeres en España de 1960 a 2003)6,7, continúa siendo un problema de salud importante debido a la mortalidad que conlleva, a la complejidad de su tratamiento quirúrgico y a la ausencia de otras terapias verdaderamente efectivas. La localización anatómica de los carcinomas gástricos también se ha visto modificada durante los últimos años8, con una disminución de la frecuencia de los tumores de localización distal y un aumento de los más próximos al esófago, lo que conlleva una mayor dificultad en la técnica quirúrgica. En Estados Unidos y en nuestro ámbito geográfico, el diagnóstico de la enfermedad suele ser tardío. El porcentaje de gastrectomías con intención curativa no excede del 50% y, de ellas, la supervivencia a los 5 años se sitúa entre el 30 y el 40% de los casos9-15. Tanto la complejidad del tratamiento quirúrgico del carcinoma gástrico como la variabilidad clínica y la morbimortalidad, junto con su elevado consumo de recursos, convierten al cáncer gástrico en un proceso clave dentro de nuestro servicio de cirugía.
Material y método
Se constituyó un grupo de trabajo formado por 2 cirujanos, 2 miembros de enfermería y el coordinador de calidad del hospital. Tras una etapa de formación en calidad se estableció un calendario de reuniones periódicas para el desarrollo del proyecto, y se nombró, finalmente, un coordinador del proceso.
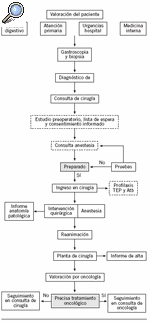
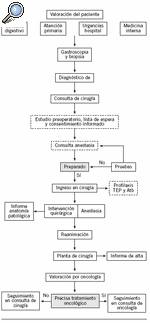
Se analizó la prevalencia del proceso "carcinoma gástrico" en nuestro hospital mediante la información aportada por el Registro de tumores del hospital4. Se definió el inicio del proceso como el momento del diagnóstico endoscópico con toma de biopsias y el final del proceso como la citación del paciente para la primera revisión en la consulta. El proceso se representó gráficamente mediante el diagrama de flujo (fig. 1).
Figura 1. Diagrama de flujo. Proceso de carcinoma gástrico.
Para obtener información sobre el proceso se realizó un estudio descriptivo, de tipo transversal y observacional, con carácter retrospectivo. Se revisaron las historias clínicas de pacientes intervenidos por adenocarcinoma gástrico en el Servicio de Cirugía General "A" del Hospital 12 de Octubre durante el período 1998-2000. Los criterios de inclusión y exclusión fueron los siguientes:
1. Criterios de inclusión:
Pacientes diagnosticados de carcinoma gástrico mediante gastroscopia y toma de biopsia.
Riesgo anestésico ASA <_ III.
Intervención quirúrgica programada.
2. Criterios de exclusión:
Tumoraciones gástricas con diagnóstico diferente de adenocarcinoma.
Adenocarcinomas gástricos que afecten además al tercio distal de esófago.
Indicación de cirugía urgente.
Cirugía paliativa sin gastrectomía.
Presencia de algún proceso concomitante cuya resolución se efectúe en el mismo acto quirúrgico.
Se excluyeron los carcinomas que afectaban al tercio distal de esófago por considerarlos una entidad distinta que requiere una técnica quirúrgica y un manejo clínico diferentes. Asimismo, se excluyó a los pacientes considerados de riesgo elevado (ASA > III), a los que presentaban neoplasias múltiples y a los enfermos que recibieron una cirugía urgente, ya que suponen un manejo clínico y un consumo de recursos muy diferente.
En el análisis retrospectivo se revisaron las historias clínicas para obtener la siguiente información sobre el proceso:
Características clínicas de los pacientes.
Calidad científico-técnica.
Efectividad clínica.
Consumo de recursos.
Puntos fuertes y áreas susceptibles de mejora.
Indicadores y estándares de calidad.
Al tratarse de un estudio retrospectivo, el análisis de la documentación clínica presentaba algunas limitaciones en relación con la evolución posquirúrgica. Para mejorar la información sobre la evolución clínica de los pacientes se actualizaron los datos mediante citación en la consulta o encuesta telefónica. Las variables estudiadas se eligieron por consenso de los miembros del grupo de mejora y se analizaron en una base de datos Access de Microsoft. Se realizó un estudio estadístico descriptivo mediante el paquete estadístico SPSS versión 11.0. A la vista de estos datos, el grupo de mejora seleccionó los puntos fuertes del proceso y los que eran susceptibles de mejora.
El desarrollo final de la VC se sustentó en la información obtenida del propio proceso, junto con una revisión específica sobre los indicadores de proceso y el resultado del tratamiento quirúrgico del cáncer gástrico. Dicha revisión se realizó a través de MEDLINE (1990-2005) y se utilizaron las palabras clave: "gastric cancer", "indicators", "preoperative evaluation". Con esta información se diseñaron los documentos de la VC: matriz temporal, documentos de verificación médica y de enfermería, hoja de variaciones, indicadores y estándares de calidad y documentos de información al paciente. La encuesta de satisfacción utilizada ha sido la Servqhos®16. Se han desarrollado reuniones periódicas del grupo de trabajo para efectuar el seguimiento periódico del proceso.
Resultados
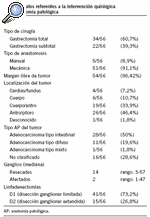
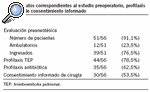
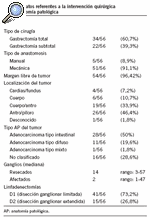
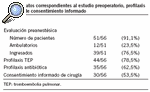
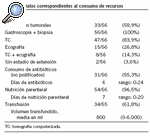
Se revisaron 56 historias clínicas correspondientes a pacientes intervenidos por adenocarcinoma gástrico de forma programada durante los años 1998-2000, y se consideraron los criterios de inclusión. En las tablas 1 y 2 se muestran las variables relacionadas con las características de los pacientes y de los tumores. Las variables referentes a la calidad científico-técnica se encuentran en las tablas 2 y 3. La mediana de edad fue de 74 años, con un 59% de varones y un 41% de mujeres. Se realizó gastrectomía total en el 60,7% y subtotal en el 39,3%. Se efectuó una disección ganglionar limitada (linfadenectomía D1) en el 73,2% de los pacientes y una disección ganglionar extendida (linfadenectomía D2) en el 26,8%. En la tabla 3 se expresan los datos sobre la valoración anestésica, que se realizó en el 91,1% de los pacientes (en el 23,5% de forma ambulatoria); el intervalo entre diagnóstico y tratamiento fue de 27 días (rango, 2-135 días). Se realizó profilaxis tromboembólica en el 78,5% de los pacientes y antibiótica en el 62,5%; se obtuvo consentimiento informado en el 53,5%. No se realizó tomografía computarizada (TC) abdominal en el 16,8% de los pacientes y se utilizó nutrición parenteral de forma no justificada en el 72% de los casos.
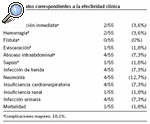
Los datos referentes a los tiempos intermedios del proceso se encuentran en la tabla 4, donde se observa que la mediana de estancia global fue de 21 días, con una estancia preoperatoria de 9 días. El consumo de recursos se muestra en la tabla 5; se observa que el 96,5% de los pacientes recibiaron nutrición parenteral total, se pautaron antibióticos sin causa justificada en el 55,3% y fueron transfundidos el 61,8% de los pacientes. En la tabla 6 se recogen los datos sobre la efectividad clínica y se comprueba la presencia de complicaciones mayores (reintervención inmediata, hemorragia, fístula, evisceración, absceso intraabdominal, sepsis) en el 18,15% de los casos. Dos pacientes fueron reintervenidos de forma inmediata como consecuencia de una hemorragia postoperatoria con repercusión hemodinámica, uno de ellos falleció en el período postoperatorio. La tasa de muertes durante el ingreso fue del 1,8%.
Tras revisar los resultados obtenidos y contrastarlos con la bibliografía (morbimortalidad9-15, uso de nutrición parenteral17-19, ganglios aislados17,20,21), el grupo de mejora seleccionó, mediante consenso, los puntos fuertes del proceso y los susceptibles de mejora:
1. Puntos fuertes del proceso:
Intervalo de tiempo correcto entre diagnóstico e intervención quirúrgica (27 días).
Baja tasa de complicaciones mayores.
Baja tasa de mortalidad tras la cirugía.
2. Áreas susceptibles de mejora:
Valoración preanestésica del paciente de forma ambulatoria.
Estancia media hospitalaria. Preferentemente a expensas de la estancia preoperatoria.
Consentimiento informado de cirugía.
Cumplimiento del protocolo de carcinoma gástrico en lo referente a: a) profilaxis tromboembólica y antibiótica; b) administración de nutrición parenteral; c) administración de antibióticos, y d) realización de TC abdominal preoperatoria.
Identificación de mayor número de ganglios.
Adecuación del número de pacientes transfundidos.
Conocimiento de la opinión de los pacientes y familiares mediante una encuesta de satisfacción.
Con toda esta información, el grupo de trabajo se propuso como objetivo final una estancia global de 12 días.
Se diseñaron los distintos documentos de la VC:
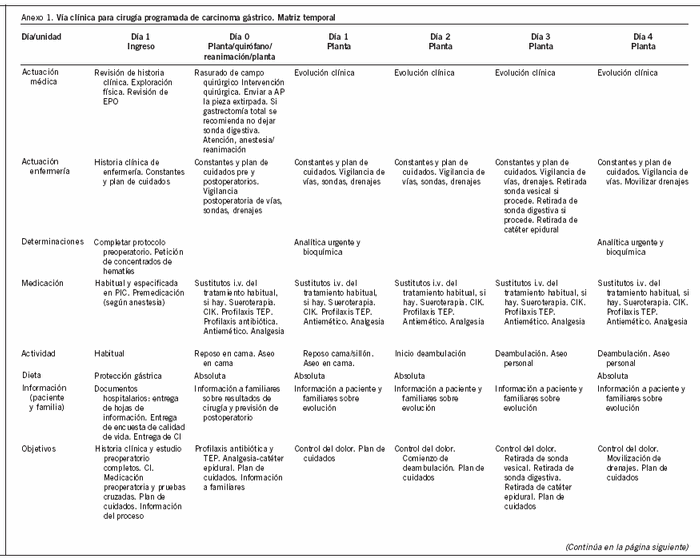
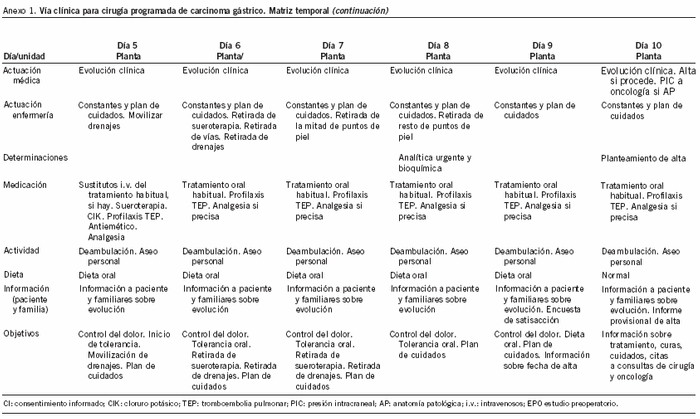
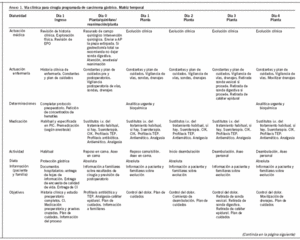
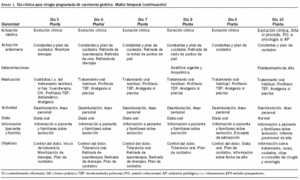
1. Matriz temporal (anexo 1).
2. Documento de verificación médica (anexos 2 y 3).
El primer apartado consta de una tabla en la que se recogen datos acerca de:
Características del paciente (edad, sexo, riesgo anestésico ASA, alergias).
Comorbilidad y medicación habitual.
Tipo de tumor.
Cirujano.
Pruebas diagnósticas y de extensión realizadas.
El segundo apartado deriva de la matriz temporal y representa en una tabla la secuencia temporal de la evolución del paciente. En la cabecera de las columnas se indica el día evolutivo del período postoperatorio que corresponde al paciente. Cada columna consta de 4 filas. La primera fila corresponde a cada una de las actuaciones médicas que han de realizarse, y cada una de ellas va precedida por una casilla en blanco que se debe marcar con una "X" para su verificación. La segunda fila se refiere a la medicación que corresponde a cada día, y cada día evolutivo está precedido por unas casillas en blanco para su verificación. La tercera fila corresponde a la dieta. La cuarta fila corresponde a las constantes biológicas del paciente y a los comentarios de evolución.
3. Documento de verificación de enfermería (anexo 4). Deriva de la matriz temporal. Se trata de una tabla en la que se recogen las distintas actividades correspondientes al personal de enfermería. Consta de casillas en blanco, casillas sombreadas y casillas en blanco con asterisco. Las casillas en blanco se deben marcar con una "X" para su verificación, las casillas sombreadas significan actividad no planificada y las casillas con asterisco deben ser marcadas sólo en casos determinados (pero su cumplimentación no supone variación).
4. Hoja de variaciones: recoge las variaciones producidas sobre lo planificado en la matriz temporal. Para su correcta cumplimentación es necesario anotar la fecha de la variación, la causa y la solución adoptada. Se indica una codificación (para facilitar el posterior análisis de los datos según la variación se deba a condiciones del paciente, aspectos propios del proceso o aspectos institucionales).
5. Documento de indicadores de resultados (anexo 5). En él se definen los indicadores de calidad propuestos por consenso por el grupo de mejora, para evaluar los resultados de la VC según los estándares que se indican (también definidos por consenso).
6. Otros documentos de la vía:
Encuesta de satisfacción.
Documentos de información al paciente.
Condiciones que debe presentar el paciente para ser dado de alta.
Pautas clínicas del protocolo de cáncer gástrico.
Protocolo de profilaxis antibiótica.
Protocolo de profilaxis tromboembólica.
Discusión
Es un hecho constatado y sin explicación científica convincente la disminución de la incidencia del carcinoma gástrico en todos los países del mundo6,7. Sin embargo, se continúa atendiendo un número importante de casos anuales. Según los datos del último Registro de tumores de nuestro hospital4 (2001), el carcinoma gástrico ocupa el segundo lugar en frecuencia de los tumores digestivos, con 123 nuevos casos/año, y el décimo lugar con respecto al resto de tumores (3,8%) lo que, unido a la repercusión que entraña la técnica quirúrgica sobre la salud de los pacientes y la variabilidad clínica de su plan de cuidados, confiere al proceso "tratamiento quirúrgico del cáncer gástrico" en nuestro centro hospitalario las condiciones deseables para establecer un plan de mejora. En este caso concreto se ha considerado importante desarrollar una VC como herramienta para facilitar este objetivo. La VC se ha elaborado a partir de la información obtenida del análisis previo del proceso, lo que nos ha permitido conocer sus puntos fuertes y las áreas susceptibles de mejora, así como establecer los indicadores y estándares precisos para permitir la evaluación de nuestros resultados.
Siguiendo la trayectoria de otros procesos gestionados anteriormente en nuestro servicio de cirugía22, se consensuaron unos criterios de inclusión y exclusión que permitieron definir un proceso quirúrgico en el que se ha minimizado la influencia de condiciones ajenas al propio proceso, y por esta razón se excluyó a los pacientes con riesgo anestésico elevado (ASA > III), los sometidos a cirugía urgente, la resolución de procesos quirúrgicos concomitantes, etc.
La evaluación de los resultados se realizó mediante consenso de los miembros del grupo de mejora tras consultar el estado actual del tema. La tasa de mortalidad perioperatoria obtenida (1,8%) se consideró adecuada, dado que en la bibliografía se aceptan cifras de hasta el 5-10%9-15 y, además, se comprueba que las complicaciones de nuestros pacientes se encuentran dentro de los límites publicados. Por otra parte se verificó un grave incumplimiento (46,5%) del consentimiento informado, por lo que en la VC se ha establecido un estándar del 100%, ya que su cumplimentación supone un precepto legal obligatorio. La estancia media hospitalaria (21 días) se ha considerado demasiado prolongada; su causa fundamental fue la presencia de una estancia preoperatoria muy prolongada (9 días) relacionada con la falta de estudio preanestésico ambulatorio. Por todo ello, en la VC se ha establecido que el ingreso hospitalario se realice 24 h antes de la intervención quirúrgica, y para su cumplimiento se ha fijado un estándar >= 80%, y que el porcentaje de pacientes visitados en la consulta ambulatoria de anestesiología sea >= 80% (hay que tener en cuenta que algunos pacientes son trasladados de otros servicios). En lo que se refiere a los protocolos de profilaxis antibiótica y de la enfermedad tromboembólica23,24 vigentes en nuestro hospital, su grado de cumplimiento en el análisis previo del proceso fue inferior al deseable (62,5 y 78,5%, respectivamente), por lo que se ha establecido un estándar para ambos >= 90%. Tras haber revisado el protocolo del tratamiento del cáncer gástrico de nuestro hospital5, se observó en el análisis previo del proceso una utilización excesiva de la nutrición parenteral total17-19 en los pacientes gastrectomizados (96,4%), de forma innecesaria en el 72% de los casos, por lo que se han restringido sus indicaciones a pacientes con mal estado nutricional y se ha fijado un estándar de utilización < 20%. Asimismo, se ha comprobado una ausencia de TC abdominal en el 16,8%, y ésta es una exploración precisa para el estudio de extensión de la enfermedad. El número de ganglios aislados (mediana, 14) se ha considerado demasiado bajo, ya que debería ser >= 2017,20,21, por lo que se estableció un indicador específico y un estándar >= 80%. En lo referente al grado de infección de herida quirúrgica y de mortalidad perioperatoria, no se encontraron cifras demasiado elevadas en la revisión previa del proceso pero, dado que son indicadores típicos de efectividad clínica, se han incluido.
Desde nuestro punto de vista resulta importante evaluar el número de pacientes que, cumpliendo los criterios establecidos para entrar en la VC, se incluyen realmente en ella, así como el porcentaje de pacientes que, tras haber entrado en la VC continúan en ella hasta el final, aunque presenten algunas variaciones. Con el objetivo de evaluar ambos parámetros se ha establecido para ellos un estándar >= 85%. En experiencias anteriores hemos comprobado que, tras evaluar las VC de procesos quirúrgicos complejos, hay un pequeño porcentaje de pacientes que abandona la VC por presentar un curso clínico muy diferente del previamente establecido y que es importante vigilar porque suelen presentar complicaciones postoperatorias importantes25. En la revisión previa del proceso comprobamos que la sonda nasogástrica para descompresión digestiva se utilizó en todos los pacientes gastrectomizados. Sin embargo, tras revisar la bibliografía26,27 se decidió considerar su uso inadecuado cuando se realiza gastrectomía total.
Finalmente, un aspecto de suma importancia pero que no se tuvo en cuenta con anterioridad es el de la calidad percibida por los pacientes y familiares; con vistas a subsanar este aspecto se ha incorporado a la VC una encuesta de satisfacción que se entrega a los pacientes durante los últimos 2 días del ingreso hospitalario.
El hecho de haber tomado como base para el diseño de la VC la información obtenida tras el análisis del proceso y el consenso de los profesionales nos ha permitido elaborar un plan de cuidados con unos indicadores adaptados a la realidad de la unidad quirúrgica para la que va dirigido, lo que según la experiencia adquirida tras la gestión de anteriores procesos ha facilitado la implantación de la VC y minimizará la aparición de posibles resistencias al cambio.