La enfermedad digestiva es una de las comorbilidades más frecuentes en niños con parálisis cerebral infantil (PCI). Nuestro objetivo es analizar el estado nutricional de los pacientes con PCI, la prevalencia de disfagia según la afectación motriz (GMFCS) y su repercusión en la calidad de vida.
Material y métodosEstudio descriptivo transversal y abierto en pacientes con PCI seguidos en un hospital terciario de la Comunidad de Madrid mediante una entrevista estructurada y la clasificación de la disfagia según la escala Eating and Drinking Ability Classification System (EDACS). Recogimos datos demográficos y antropométricos y relacionamos el nivel de disfagia con el nivel funcional según el Gross Motor Function Classification System (GMFCS).
ResultadosLa muestra incluyó 44 pacientes (65,9% varones), con una edad media de 9,34±5 años y un IMC de 18,5±4,9. El 43% tenía limitaciones en seguridad y/o eficiencia (EDACS>II). El porcentaje de pacientes afectados fue mayor cuanto más extensa desde el punto de vista topográfico fue la PCI (tetraparesia 60%), más variada la semiología clínica (87% en formas mixtas) y peor el nivel funcional (100% en GMFCS V). La repercusión nutricional aumentó con puntuaciones más altas en EDACS y GMFCS.
ConclusionesPresentamos el primer estudio sobre la utilidad de la escala EDACS en una muestra representativa de niños y adolescentes españoles con PCI. Los resultados deben hacernos reflexionar sobre la importancia del cribado de disfagia en estos pacientes, independientemente del grado de afectación motriz y la necesidad de una intervención precoz para evitar sus principales consecuencias: desnutrición (hipocrecimiento, déficit de micronutrientes, osteopenia, etc.), microaspiraciones o infecciones de repetición que empeoran el estado neurológico.
Digestive disorders are one of the most common comorbidities among children with cerebral palsy (CP). The aim of this study is to examine the nutritional status of patients with CP, the prevalence of dysphagia by degree of motor impairment, and the impact of digestive disorders on quality of life.
Material and methodsWe conducted a descriptive, cross-sectional, open-label study of outpatients with CP from a tertiary hospital in the Region of Madrid using a structured interview, classifying dysphagia using the Eating and Drinking Ability Classification System (EDACS). We gathered demographical and anthropometric data, and analysed the correlation between severity of dysphagia and functional status as measured with the Gross Motor Function Classification System (GMFCS).
ResultsOur sample included 44 patients (65.9% boys), with a mean (standard deviation) age of 9.34 (5) years and a mean BMI of 18.5 (4.9). Forty-three percent presented safety and efficiency limitations (EDACS level>II). Safety and efficiency limitations were associated with more extensive motor involvement (60% had tetraparesis), more varied clinical manifestations (87% had mixed forms) and poorer functional capacity (100% on GMFCS V). The impact on nutritional status increased with higher EDACS and GMFCS scores.
ConclusionsThis is the first study into the usefulness of the EDACS scale in a representative sample of Spanish children and adolescents with CP. Our findings underscore the importance of screening for dysphagia in these patients, regardless of the level of motor impairment, and the need for early treatment to prevent the potential consequences: malnutrition (impaired growth, micronutrient deficiencies, osteopaenia, etc.), microaspiration, or recurrent infections that may worsen patients’ neurological status.
La parálisis cerebral infantil (PCI) es la causa más frecuente de discapacidad en la infancia en los países desarrollados. Tiene una prevalencia que oscila entre 1,5-3 por cada 1.000 recién nacidos vivos, sin embargo, el desarrollo de protocolos de seguimiento, de unidades de cuidados paliativos y los avances en los cuidados médicos han conseguido prolongar la esperanza de vida de los pacientes y aumentar de forma global su prevalencia1,2.
La PCI engloba un grupo heterogéneo de síndromes que implican una disfunción motora persistente que afecta al tono muscular, el movimiento y la postura, debida a una lesión en el cerebro en desarrollo3. Aunque por definición es un trastorno no progresivo, su expresión clínica varía con la edad del paciente y la aparición de diversas comorbilidades que pueden condicionar su calidad de vida incluso más que los trastornos neurológicos4.
La comorbilidad digestiva es la más frecuente tras los trastornos neurológicos asociados. Prácticamente todos los pacientes con PCI presentarán síntomas gastrointestinales y/o alteración del estado nutricional en algún momento de su vida5,6.
Hasta un 30-40% de los pacientes tienen dificultades para la alimentación secundarias a disfagia, vómitos y regurgitaciones o retraso del vaciamiento gástrico. Si a estos problemas le sumamos la dependencia de otra persona para la ingesta, las dificultades para expresarse (hambre, saciedad, etc.), la posible alteración en la postura y el equilibrio del tronco (dificulta la ingesta) y el incremento de las pérdidas o de las necesidades calóricas, la consecuencia directa es el riesgo de ingesta insuficiente y, consecuentemente, un mayor riesgo de malnutrición7–10.
Por todo ello, es importante conocer las posibles complicaciones digestivas en este grupo de pacientes y anticiparse a su repercusión sobre el estado nutricional y de salud, pues la malnutrición puede contribuir al deterioro neurológico.
El objetivo del estudio es analizar la prevalencia de dificultades para la deglución en niños y adolescentes con PCI según el grado de afectación motriz y otras comorbilidades.
Material y métodosEstudio descriptivo, transversal y abierto, para valorar la prevalencia y el grado de dificultades para la deglución, así como el estado nutricional según el grado de afectación motriz de niños y adolescentes con PCI seguidos en la consulta externa de neurología infantil de un hospital terciario de la Comunidad de Madrid entre 2016-2017, según el siguiente protocolo de valoración durante la visita en consulta, en la que se recogieron los siguientes datos:
- a.
Datos demográficos: edad, sexo, tipo de PCI clasificada desde el punto de vista topográfico (tetraplejia, hemiplejia, diplejia, etc.), del trastorno motor predominante (espástica, discinética, atáxica, hipotónica, mixta, etc.)11 y según el grado de afectación funcional mediante la escala Gross Motor Function Classification System (GMFCS). Esta última diferencia 5 niveles según el estado de afectación motriz:
- -
Nivel I: sin limitaciones (andar, correr, subir escaleras, etc.). Escasa coordinación.
- -
Nivel II: limitación en la marcha en terreno irregular o larga distancia. Precisa apoyo en escaleras. Dificultad para correr y saltar.
- -
Nivel III: camina con bastón o muletas. Silla de ruedas para larga distancia.
- -
Nivel IV: andador en casa. Silla de ruedas manejada por otro en el resto de las circunstancias.
- -
Nivel V: dependencia completa para moverse.
- b.
Anamnesis dirigida para detectar posibles alteraciones relacionadas con la alimentación: ingesta (cantidad y texturas de los alimentos que consume), uso de vías complementarias de alimentación (sonda nasogástrica, gastrostomía, etc.) y la dependencia o no de cuidadores para el proceso de la alimentación.
- c.
Despistaje de disfagia: mediante preguntas clave (red flags) dirigidas a detectar signos de alarma de la misma y que nos permitan clasificarlos posteriormente2. Las principales preguntas fueron:
- 1.
¿La comida es estresante para el niño o los cuidadores?
- 2.
¿Tarda más de 40min en comer?
- 3.
¿Tiene preferencia por algún tipo de textura?
- 4.
¿Tiene infecciones respiratorias de repetición?
- 5.
¿Durante la ingesta presenta cambios en la coloración (rubefacción o cianosis), accesos de tos o náuseas, sialorrea y/o congestión conjuntival?
- d.
Clasificación del grado de disfagia según la escala Eating and Drinking Ability Classification System (EDACS). La EDACS es una escala que describe las capacidades funcionales para comer y beber de los niños con parálisis cerebral. Se basa en características claves relacionadas con la «seguridad» (aspiración y ahogo) y la «eficiencia» (cantidad de comida perdida y el tiempo para comer), y valora la capacidad de los pacientes para la realización de diversos procesos relacionados con la alimentación12,13:
- -
Función neuromotora: capacidad para morder, masticar y deglutir.
- -
Manejo de las diferentes texturas de alimentos y fluidos.
- -
Respiración: identificación del riesgo de microaspiraciones, aspiraciones o asfixia.
Según estas características, establece 5 niveles:
- -
Nivel I: come y bebe de manera eficiente y segura.
- -
Nivel II: come y bebe de manera segura, pero con limitaciones en la eficiencia.
- -
Nivel III: come y bebe con limitaciones en la eficiencia y la seguridad.
- -
Nivel IV: limitaciones significativas en la seguridad.
- -
Nivel V: incapaz de comer o beber de forma segura. Considerar soporte nutricional por sonda.
El EDACS está validado y dispone de una versión traducida al castellano, que se puede descargar gratuitamente en: www.edacs.org
- e.
Valoración somatométrica: fue realizada en consulta siempre por el mismo facultativo. Se determinó el peso, la talla y el índice de masa corporal (IMC) utilizando para ello una báscula electrónica de columna SECA 799, con tallímetro SECA 220. En los pacientes no ambulantes e incapaces para la bipedestación, el peso se obtuvo mediante doble pesada (peso de la madre y el niño, menos el peso de la madre), y la estimación de la talla, mediante la aplicación de la siguiente fórmula14:
Longitud (cm)=3,26×longitud de la tibia (cm)+30,8.
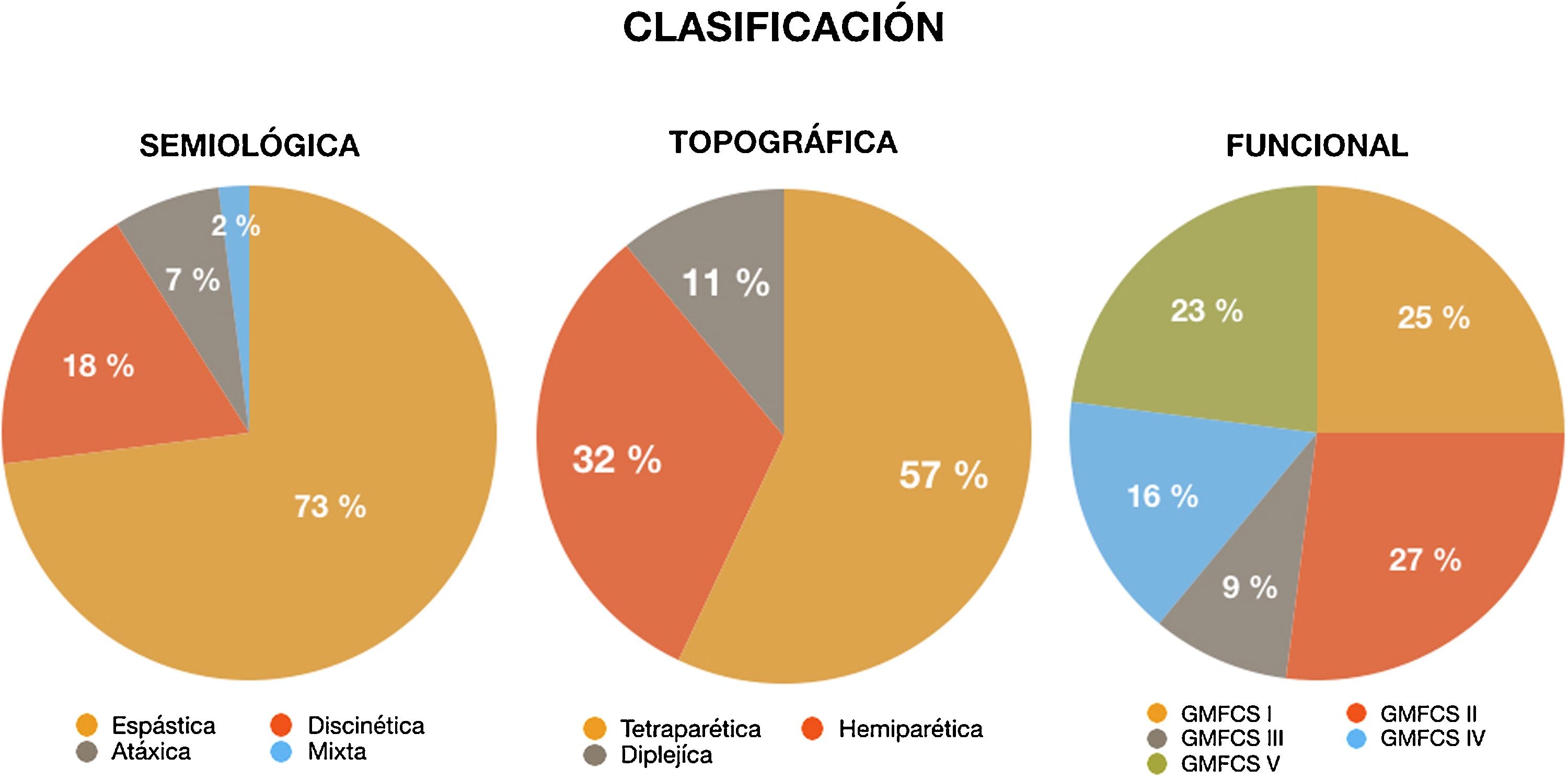
ResultadosIncluimos un total de 44 pacientes, el 65,9% varones, con edades comprendidas entre los 3 y los 21 años, con una edad media de 9,34±5 años. Desde el punto de vista topográfico, la tetraparesia fue el subtipo de PCI más frecuente (57%), seguida de la hemipléjica (32%) y la dipléjica (11%). Teniendo en cuenta el trastorno del movimiento, la mayoría de los pacientes tenían espasticidad, como trastorno único (73%) o en el contexto de una PCI mixta (18%).
Según la escala GMFCS, la mitad de la muestra estaba incluida en los 2 primeros niveles. El resto se repartió de la siguiente manera: un 9% estaría dentro del nivel iii del GMFCS, el 16% en el nivel iv y el 23% en el v.
En la figura 1 se detallan gráficamente los porcentajes de los distintos tipos de PCI según los diferentes criterios de clasificación.
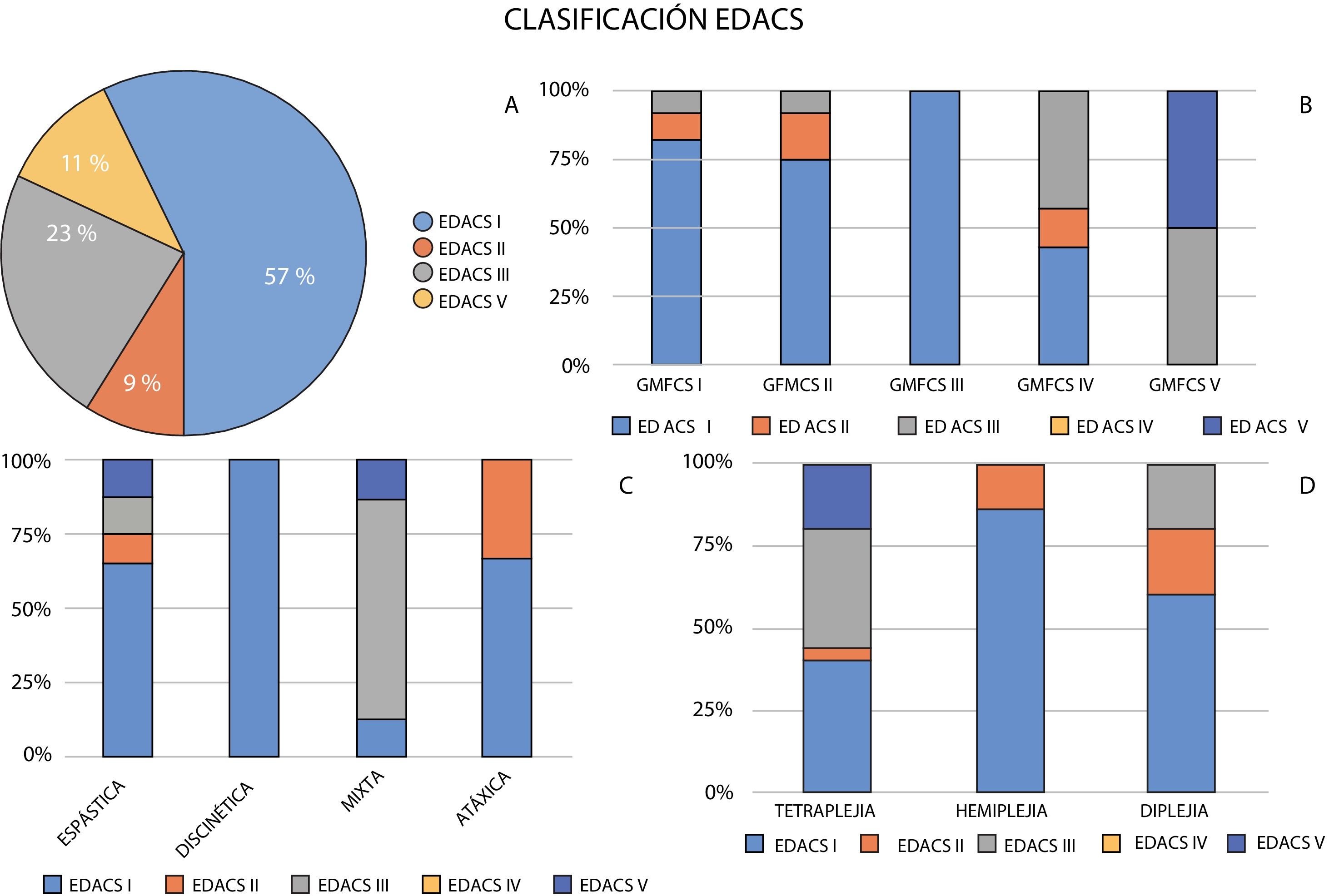
Respecto a los signos de alarma de disfagia y según la entrevista clínica, el 57% de los pacientes incluidos comían y bebían de manera segura y eficiente y fueron incluidos como EDACS I. En el resto encontramos alguna alteración. El 9% comía y bebía de manera segura pero poco eficiente (EDACS II), en el 23% existían signos de alarma en cuanto a la seguridad, y la alimentación era poco eficiente (EDAC III), y el resto era incapaz de comer y/o beber de forma segura y tenía algún dispositivo para el soporte nutricional (sonda nasogástrica o gastrostomía), siendo incluidos como EDACS V (11%).
Teniendo en cuenta las características topográficas de la PCI, el porcentaje de pacientes con dificultades para beber o comer fue mayor cuanto más extensa era la afectación motriz.
En el caso de los pacientes con tetraparesia, el 40% tenía un nivel EDACS I, el 4%, un EDACS II, el 36%, un EDACS III y el 20%, un EDACS V. En el grupo de pacientes con diplejia, el 60% podía clasificarse como EDACS I, el 20% estaba en el nivel ii de EDACS y el 20%, en EDACS III. En el caso de los hemipléjicos, el 86% comía y bebía de manera segura y eficiente (EDACS I) y solo el 14% tenía alguna pequeña limitación respecto a la eficiencia, que los situaba en el nivel ii de la escala EDACS.
Teniendo en cuenta la semiología motora predominante, el grupo de pacientes con diversos trastornos del movimiento, clasificados como PCI mixta, presentaron mayores dificultades para la alimentación (75% EDACS III y 12,5% EDACS V), seguidos de los espásticos (12,5% EDACS III y 12,5% EDACS V). En el resto de los grupos, prácticamente ningún paciente presentaba dificultades para comer ni beber de forma segura y eficaz.
En la figura 2 se detalla la distribución del nivel EDACS de los pacientes según el tipo de PCI.
Distribución del grado de disfagia según la escala Eating and Drinking Ability Classification System (EDACS) y su relación con el tipo de parálisis cerebral según el trastorno del movimiento predominante, la distribución topográfica y el grado funcional Gross Motor Function Classification System (GMFCS).
Al analizar las dificultades en la alimentación con el grado de disfunción motriz según el GMFCS, encontramos una cierta relación entre los distintos niveles de ambas escalas. El porcentaje de pacientes con importantes dificultades para la alimentación, es decir, un nivel EDACS más alto, fue mayor cuanto más afectación funcional tenían según el GMFCS. Así, mientras que la mayoría de los pacientes por debajo del nivel iii del GMFCS podían comer y beber de manera segura (EDACS I), el 100% de los pacientes con un nivel v del GMFCS tenían dificultades (EDACS mayor o igual a iii). El 50% tenía problemas respecto a la seguridad o una limitada eficiencia para la alimentación (EDACS III), y el resto era incapaz de comer o beber de manera segura (EDACS V). Los porcentajes para cada uno de los niveles EDACS según el nivel de GMFCS se detallan en la figura 2.
Desde el punto de vista somatométrico y según el índice de Quetelet, la mayoría de los pacientes eran delgados. El IMC medio fue de 17,63±4,84kg/m2, siendo este menor cuanto mayor fue el nivel EDACS y el grado de afectación motriz según el GMFCS. El 40% de los pacientes con EDACS I, el 100% de los EDACS II, el 50% de los EDACS III y el 80% de los EDACS V tenían un IMC por debajo de 18,5.
DiscusiónLa PCI es la causa más frecuente de discapacidad en la infancia en los países desarrollados, observando en los últimos años un aumento de la prevalencia, posiblemente relacionada con la mejora de los cuidados y tratamientos médicos, los protocolos de seguimiento y los cuidados paliativos de los pacientes con mayor afectación, aumentando de forma global la expectativa de vida de los pacientes.
El trastorno para la deglución es una de las comorbilidades más frecuentemente asociadas a estos pacientes. La lesión neurológica produce una alteración de la función neuromuscular que, de forma directa o indirecta, puede causar disfunción motora a nivel oral, discinesia faringoesofágica y/o dismotilidad intestinal. Todo ello puede condicionar dificultades para la apertura bucal, la incoordinación para la succión y el proceso de masticación-deglución, el reflujo gastroesofágico, etc., que impiden que el niño pueda comer y beber de una forma adecuada.
De forma similar a lo descrito en la literatura, el 43% de los pacientes incluidos en el estudio presentaron, en mayor o menor medida, limitaciones en la seguridad y/o eficiencia para comer y beber13. Estas dificultades estuvieron presentes en todas las formas de PCI, independientemente de la clasificación utilizada, salvo en los pacientes incluidos como discinéticos, según el trastorno motor predominante.
Como esperábamos, el porcentaje de pacientes afectados (EDACS>II) fue mayor cuanto más extensa fue la afectación (60% de los pacientes con tetraparesia), y más variada la semiología clínica del trastorno del movimiento, encontrando dificultades hasta en el 87% de las formas mixtas.
Aunque la aparición de signos clínicos indicativos de disfagia orofaríngea fue más frecuente y más grave cuanto mayor era el nivel de afectación funcional según el GMFCS (100% en GMFCS V), al igual que en otras series publicadas, la dificultad para comer y beber estuvo presente prácticamente en todos los niveles de GMFCS2,14,15.
El 18% de los pacientes con GMFCS I y hasta el 25% de aquellos con GMFCS II presentaron niveles ii y iii en la escala EDACS, porcentajes nada despreciables si tenemos en cuenta sus posibles consecuencias: mayor riesgo de ingesta insuficiente y malnutrición.
La malnutrición se presenta de forma global en el 40-90% de los pacientes con PCI. Puede acompañarse de hipocrecimiento, déficit de micronutrientes y osteopenia, y empeorar el pronóstico neurológico de estos niños.
En nuestro estudio, el estado nutricional de los pacientes según el IMC fue peor cuanto mayor era el nivel de EDACS y mayor grado de afectación motriz tenían según el GMFCS. Sin embargo, como sucedió con los signos de alarma de disfagia, aunque el porcentaje de pacientes con IMC por debajo de 18,5kg/m2 fue directamente proporcional al nivel EDACS (100% en GMFCS V), encontramos pacientes delgados en todos los niveles (el 40% de los pacientes con EDACS I, el 100% de los EDACS II, el 50% de los EDACS III y el 80% de los EDACS IV).
A pesar del reducido tamaño muestral, consideramos que nuestra serie podría considerarse homogénea y representativa de la práctica clínica habitual, ya que los pacientes incluidos pertenecen a una población similar respecto a la sintomatología y las disfunciones producidas por la enfermedad. Por tanto, consideramos que los resultados tienen cierta relevancia clínica y deben hacernos reflexionar sobre la importancia de realizar una anamnesis y exploración física minuciosa, dirigida al despistaje de dichos trastornos en todos los pacientes con PCI, independientemente de su grado de afectación motriz.
Su detección nos permitiría una intervención precoz de la función afectada y prevenir o tratar las principales comorbilidades asociadas (desnutrición, microaspiraciones, infecciones de repetición, etc.) que empeoran el estado neurológico6,7,15–18.
Debemos incorporar a nuestra anamnesis preguntas relacionadas con la capacidad para morder, masticar y deglutir; para manejar diferentes texturas de alimentos y fluidos, y signos de alarma indirectos relacionados con disfagia (cambios en la respiración durante la ingesta, voz ronca o historia de neumonías de repetición), que nos permitan identificar el riesgo de microaspiración o asfixia y derivar al paciente al especialista correspondiente que confirme nuestra sospecha con los estudios complementarios pertinentes, principalmente videofluoroscopia (permite una visualización dinámica de la fase orofaríngea) o endoscopia flexible19,20.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.