El electroencefalograma (EEG) es una exploración útil en unidades de críticos, sobre todo en alteraciones de consciencia en apariencia inexplicables. La encefalitis herpética (EH) es una enfermedad grave, con varios factores pronósticos relacionados, quizás el principal el tiempo transcurrido hasta la instauración del tratamiento antiviral1. Otro factor no desdeñable lo constituye la irrupción de crisis comiciales; aparecen en un porcentaje significativo de afectados2 y se responsabilizan de una cascada de fenómenos fisiopatológicos que parecen ser potenciadores de daño cerebral3,4. Carrera et al.5 apreciaron que hasta un tercio de los pacientes con infección del sistema nervioso central sometidos a monitorización electroencefalográfica continua (M-EEG-C) presentaron crisis y, de ellas, casi la mitad sin semiología clínica; además, establecieron la presencia de actividad ictal en ausencia de cambios clínicos y el patrón de descargas epileptiformes lateralizadas periódicas (PLED) como variables independientes de mal pronóstico.
Describimos una paciente con EH complicada por la progresión agresiva y la alteración de consciencia profunda de origen epiléptico. Resaltamos la aportación que puede suponer la realización de EEG seriados, periódicos y frecuentes, en el seguimiento, manejo y muy probablemente en el pronóstico de estos enfermos.
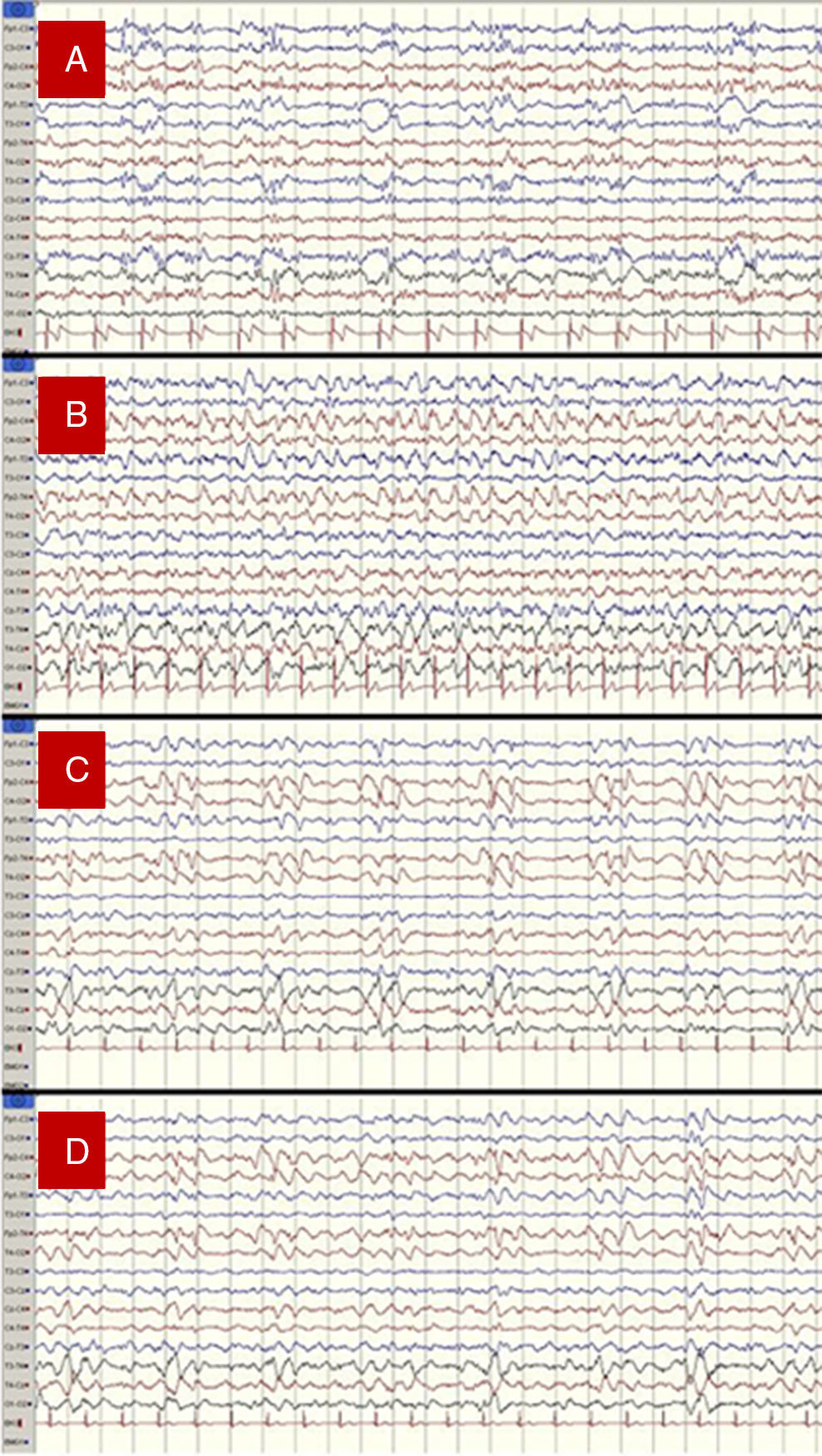
Mujer de 56años, sin antecedentes de interés, que presentó fiebre al levantarse, progresiva desorientación y disminución de la fluencia verbal. En su hospital se realizó TC craneal y análisis de LCR, siendo todo normal; ingresó bajo tratamiento empírico con aztreonam, sin mejoría significativa. Al tercer día se trasladó a nuestro centro (de referencia) evidenciándose estado estuporoso, déficit sensitivo-motor en hemicuerpo derecho y reflejo cutaneoplantar ipsilateral indiferente. La TC craneal continuó siendo normal, aunque una nueva punción lumbar mostró un LCR patológico (96 células/mm3 [75% linfocitos], 76mg/dl de proteínas y 52mg/dl de glucosa [glucemia de 137mg/dl]). Se instauró aciclovir y pusimos en marcha nuestra sistemática en estos casos de seguimiento con EEG (al menos 2 registros y en alguna ocasión 3 cada 24h). Se detectó en el primero un patrón de PLED que sugirió EH. Los EEG posteriores documentaron la progresión rápida y grave del proceso, así como determinadas complicaciones añadidas (fig. 1):
- 1.
1.er día de ingreso: PLED hemisféricos izquierdos con predominio en áreas temporales. Se inició tratamiento con levetiracetam.
- 2.
3.er día de ingreso: crisis epilépticas no convulsivas (CENC) que por su persistencia definieron una situación de estatus epiléptico no convulsivo (EENC) generalizado, con mayor expresividad en el hemisferio derecho. Se administró propofol intravenoso con la consecuente inducción de un patrón de brote-supresión, y se reforzó la medicación antiepiléptica con fenitoína.
- 3.
4.° día de ingreso: PLED hemisféricos derechos. No se evidenciaron episodios críticos.
- 4.
6.° día de ingreso: PLED hemisféricos derechos y actividad epiléptica fluctuante sobreañadida de características críticas e importante persistencia, con algunos episodios prolongados en el tiempo, todo ello más llamativo en ese hemisferio. Se añadió lacosamida.
A)1.er día de ingreso: PLED izquierdos con predominio en áreas temporales. B)3.er día de ingreso: estatus epiléptico generalizado aunque asimétrico de predominio derecho. C)4.° día de ingreso: PLED hemisféricos derechos. D)6.° día de ingreso: PLED derechos con sobreimposición de actividad epiléptica crítica en ese hemisferio.
Se intuyó la evolución tórpida mediante el seguimiento EEG, que se confirmó con una nueva TC, mostrando hipodensidad parcheada temporal y frontobasal bilateral de predominio izquierdo (fig. 2A). Se añadieron medidas antiedema, así como corticoterapia, lo que provocó cierta mejoría. Al cabo de una semana se trasladó a la planta de hospitalización del servicio de neurología. Tras 21días la paciente presentaba inatención, apatía, preferencia oculocefálica a la izquierda, heminegligencia derecha, signos de liberación frontal, disfasia global, hemianopsia homónima derecha y leve hemiparesia derecha. En nuevos controles de EEG la actividad epiléptica disminuyó considerablemente. Pocos días después la PCR confirmó la EH por VHS-1, y la RM definió la extensión de la lesión estructural (fig. 2B y C).
En una unidad de neurocríticos hasta una tercera parte de ingresados sometidos a M-EEG-C presentan CENC, el 75% de ellos en forma de EENC6, e independientemente de los antecedentes incluso el 8% de pacientes en estado de coma tienen CENC7. Dado el alto porcentaje de sujetos que no presentan manifestaciones de naturaleza epiléptica, es esencial mantener la sospecha y la utilización del EEG en su reconocimiento3. En este sentido numerosos estudios enfatizan en cómo la actividad ictal, sobre todo en caso de EENC, tiene efectos deletéreos y, por tanto, conlleva mal pronóstico8,9. Se deduce de todo lo comentado que la utilización del EEG, sobre todo en modalidad de M-EEG-C, es una herramienta de alto valor en la identificación de CENC y EENC10,11, de otro modo no detectables. Además posibilita el tratamiento temprano de esta complicación y, por lógica, un mejor pronóstico resultado de la minimización de secuelas cognitivo-conductuales, frecuentes en EENC3.
Es un tema de gran controversia decidir qué pacientes monitorizar y durante cuánto tiempo; desde 2012 existen guías que recomiendan la M-EEG-C al menos durante 48h si el paciente está en estado de coma12, porque alrededor del 80% de crisis acontecían en las primeras 24h y hasta el 87% si la monitorización se extendía a 48h según un estudio previo4. Sin embargo, en la actualidad no existen directrices claras que aborden los diferentes aspectos metodológicos de la M-EEG-C13.
La realización frecuente de EEG convencionales de corta duración en ningún caso sustituye la rentabilidad de la M-EEG-C14 pero es un recurso aceptable si no hay posibilidad de un registro prolongado15, como ocurre en nuestro centro. Así, hemos implementado una sistemática en nuestros pacientes críticos con patología neurológica aguda, en especial estatus epiléptico, llevando a cabo una rutina exploratoria consistente en la obtención de registro EEG sin vídeo, con un electroencefalografista in situ que establece el tipo de relación clínico-eléctrica y emite un informe inmediatamente. La frecuencia es 2-3 veces al día: a primera hora (8-9h) y a última de la jornada ordinaria de la mañana (14-15h), así como de la tarde (19-20h), y en fin de semana cada 24h (o si se precisa antes) en forma de «alerta» o guardia localizada con desplazamiento del médico neurofisiólogo. La duración de los registros ronda los 30min15, o algo más si lo estimamos oportuno en base a las condiciones del paciente. Así, a la espera de poder implantar en nuestro centro la M-EEG-C para pacientes neurocríticos, tenemos la impresión de que esta metodología consigue un buen rendimiento, mejor que estudios aislados diarios o cada 48h, aunque un amplio estudio prospectivo, que estamos realizando en la actualidad, es imperativo para determinar este aspecto.
Mediante la utilización de esta herramienta conseguimos apoyar de forma temprana el diagnóstico y detectar tempranamente las crisis, con mayor importancia si se presentan en forma de EENC, algo que pensamos tuvo implicaciones en el manejo terapéutico y en el pronóstico de nuestra paciente.
FinanciaciónLos autores no hemos recibido financiación para la realización de este artículo.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.
Este trabajo no ha sido presentado en la Reunión Anual de la SEN ni en otras reuniones/congresos.




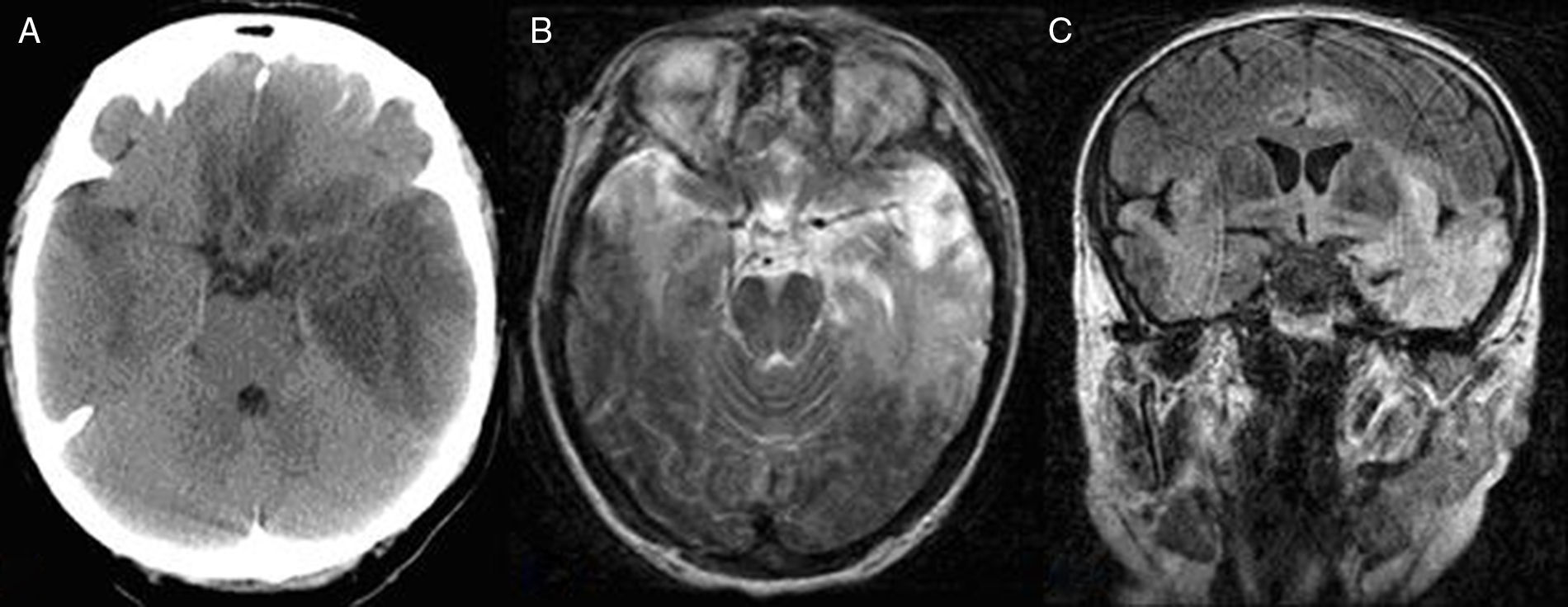
![Afectación temporal, frontal basal, insular y cingular, de forma bilateral asimétrica con predominio izquierdo en imágenes de TC (A) y RM (corte axial potenciado en T2 [B] y coronal FLAIR [C]). Afectación temporal, frontal basal, insular y cingular, de forma bilateral asimétrica con predominio izquierdo en imágenes de TC (A) y RM (corte axial potenciado en T2 [B] y coronal FLAIR [C]).](https://static.elsevier.es/multimedia/02134853/0000003200000003/v1_201703191224/S0213485315000997/v1_201703191224/es/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)


