Actualizar las recomendaciones de la Sociedad Española de Neurología para la prevención de ictus, tanto primaria como secundaria, en pacientes con hipertensión arterial.
DesarrolloSe han planteado diferentes preguntas para identificar cuestiones prácticas para el manejo de la presión arterial (PA) en prevención de ictus, analizando cuál debe ser el objetivo de control de la presión arterial y cuáles son los fármacos más adecuados en prevención primaria, cuándo iniciar el tratamiento antihipertensivo después de un ictus, cuáles son las cifras que debemos alcanzar y qué fármacos son los más adecuados en prevención secundaria de ictus. Se ha realizado una revisión sistemática en Pubmed analizando los principales ensayos clínicos para dar respuesta a estas preguntas y se han elaborado unas recomendaciones.
ConclusionesEn prevención primaria se recomienda iniciar tratamiento antihipertensivo con cifras de PA>140/90mmHg, con un objetivo de control de PA<130/80mmHg. En prevención secundaria de ictus se recomienda iniciar tratamiento antihipertensivo pasada la fase aguda (primeras 24h) con un objetivo de control de PA<130/80mmHg, siendo preferible el empleo de ARA-II o diuréticos solos o en combinación con IECA.
To update the recommendations of the Spanish Society of Neurology on primary and secondary stroke prevention in patients with arterial hypertension.
DevelopmentWe proposed several questions to identify practical issues for the management of blood pressure (BP) in stroke prevention, analysing the objectives of blood pressure control, which drugs are most appropriate in primary prevention, when antihypertensive treatment should be started after a stroke, what levels we should aim to achieve, and which drugs are most appropriate in secondary stroke prevention. We conducted a systematic review of the PubMed database and analysed the main clinical trials to address these questions and establish a series of recommendations.
ConclusionsIn primary stroke prevention, antihypertensive treatment should be started in patients with BP levels >140/90mmHg, with a target BP of <130/80mmHg. In secondary stroke prevention, we recommend starting antihypertensive treatment after the acute phase (first 24hours), with a target BP of <130/80mmHg. The use of angiotensin-II receptor antagonists or diuretics alone or in combination with angiotensin-converting enzyme inhibitors is preferable.
La hipertensión arterial es el factor de riesgo modificable de ictus más prevalente y uno de los que más contribuyen al desarrollo de estas enfermedades. Además, se asocia a ictus más graves y con peor pronóstico. El control de la presión arterial disminuye el riesgo de ictus en prevención primaria, pero también disminuye el riesgo de recurrencia tras haber sufrido un ictus. En este capítulo revisaremos el efecto que ejerce la presión arterial sobre el riesgo de ictus y cuáles son los objetivos de control en prevención tanto primaria como secundaria.
MétodosSe han planteado diferentes preguntas que identifiquen cuestiones prácticas en el manejo de la presión arterial en la prevención del ictus. Se ha analizado: 1)cuál debe ser el objetivo de control de la presión arterial en prevención primaria; 2)cuáles son los fármacos más adecuados en prevención primaria; 3)cuándo iniciar el tratamiento antihipertensivo después de un ictus; 4)cuáles son las cifras de presión arterial que debemos alcanzar en la prevención secundaria, y 5)qué fármacos son los más adecuados en prevención secundaria de ictus. Se ha realizado una revisión sistemática en Pubmed analizando los principales ensayos clínicos y metaanálisis para dar respuesta a estas preguntas y se han elaborado unas recomendaciones. Para la recomendación de cuándo iniciar el tratamiento antihipertensivo hemos excluido aquellos trabajos en los que se estudia la intervención sobre la presión arterial en pacientes que reciben terapias de reperfusión, por considerarlo dentro del tratamiento agudo del ictus.
Los niveles de evidencia se han clasificado como nivel de evidenciaA (evidencia de alta calidad procedente de más de un ensayo clínico aleatorizado, metaanálisis de alta calidad, o uno o más ensayos clínicos aleatorizados corroborados por estudios de registro de alta calidad); nivel de evidenciaB (evidencia de calidad moderada procedente de uno o más ensayos clínicos aleatorizados, o de uno o más estudios no aleatorizados, observacionales o registros de alta calidad, metaanálisis de ensayos clínicos de moderada calidad, o metaanálisis de estudios no aleatorizados); nivel de evidenciaC (datos limitados cuando los datos proceden de estudios observacionales o registros con limitaciones metodológicas en su diseño o ejecución). Se consideraron los siguientes grados de recomendación: claseI: fuerte recomendación (beneficio muy superior al riesgo); claseIIa: recomendación moderada (beneficio superior al riesgo); claseIIb: recomendación débil; claseIII: no beneficio cuando el beneficio es equivalente al riesgo1.
Manejo de la presión arterial en prevención primariaLa definición de hipertensión arterial ha ido cambiando a lo largo de los años, debido a que se ha ido conociendo más a fondo el efecto de la presión arterial sobre el riesgo vascular. Mientras que en los años cincuenta del pasado siglo se consideraba hipertensión arterial cifras de PAS >180mmHg y de PAD >100mmHg, en la actualidad se consideran cifras más bajas. Hoy en día se considera que la presión arterial es normal cuando la PAS está por debajo de 120mmHg y la PAD por debajo de 80mmHg. Hablamos de hipertensión arterial cuando las cifras de presión arterial superan los 130/80mmHg, considerando un estadio1 las cifras de PAS entre 130-139mmHg o de PAD entre 80-89mmHg y un estadio2 las cifras de PAS ≥140mmHg o PAD ≥90mmHg. Las cifras de PAS entre 120-129mmHg son consideradas como elevadas2.
Existe una relación directa entre las cifras de presión arterial y el riesgo vascular. Un estudio observacional que incluyó a un millón de individuos mostró que por cada 20mmHg de incremento de la PAS o 10mmHg la PAD se duplica el riesgo de mortalidad por ictus o enfermedad coronaria a partir de cifras de presión arterial de 115/75mmHg3. También está ampliamente demostrado que el control de la presión arterial disminuye el riesgo de enfermedades vasculares. En un metaanálisis del año 2016 en el que se incluyeron más de 600.000 pacientes se demostró que por cada 10mmHg que se disminuyese las cifras de PAS se conseguía disminuir un 20% (RR: 0,80, IC95%: 0,77-0,83) el riesgo de eventos vasculares graves (infarto agudo de miocardio, muerte vascular, revascularización coronaria, ictus e insuficiencia cardíaca), un 17% el riesgo de cardiopatía isquémica (RR: 0,83; IC95%: 0,78-0,88), un 27% el riesgo de ictus isquémico (RR: 0,73; IC95%: 0,68-0,77) y un 13% la mortalidad por cualquier causa (RR: 0,87; IC95%: 0,84-0,91)4.
Sabemos que el control adecuado de la presión arterial disminuye el riesgo de ictus y otras enfermedades vasculares, pero es importante saber cuáles son las cifras de presión arterial que debemos alcanzar en prevención primaria y si existe algún fármaco que ejerza un mayor efecto en la disminución del riesgo de ictus.
¿Cuál es el objetivo de control de la presión arterial en prevención primaria?Existen diferentes estudios que han demostrado que el control de la presión arterial en pacientes con hipertensión reduce el riesgo de sufrir un ictus y otras enfermedades vasculares. En el año 2014 se publicó un metaanálisis basado en datos individuales de pacientes incluidos en ensayos clínicos que evaluaban diferentes fármacos antihipertensivos frente a placebo o estrategias intensivas de control de la presión arterial frente a otras más conservadoras. El objetivo principal consistía en analizar el riesgo de eventos vasculares definidos como ictus, infarto agudo de miocardio, insuficiencia cardíaca o mortalidad vascular5. Se analizaron 11 ensayos clínicos que incluyeron a 67.475 individuos con riesgo vascular estratificados en 4 grupos en función del riesgo estimado a 5años de sufrir un evento vascular: grupo1 (<11%), grupo2 (11-15%), grupo3 (15-21%), grupo4 (>21%). El control de la presión arterial consiguió una disminución del riesgo relativo de eventos vasculares en todos los grupos de intervención (un 18% en el grupo1, un 15% en el grupo2, un 13% en el grupo3 y un 15% en el grupo4).
A pesar de que se sabe que el control de la presión arterial ejerce un efecto positivo en la disminución del riesgo vascular, existen controversias en cuanto a cuál debe ser el objetivo de control de la presión arterial en prevención primaria. El estudio Systolic Hypertension in the Elderly Program (SHEP) fue realizado para investigar el efecto del control de la presión arterial en la disminución del riesgo de ictus en prevención primaria en pacientes con PAS >160mmHg6. Se comparó el uso de un diurético (clortalidona) con placebo durante un seguimiento de 4,5años. El empleo del diurético se asoció a una disminución de la PAS hasta cifras de 143mmHg, mientras que el grupo placebo alcanzó cifras de 155mmHg. Este efecto se tradujo en una disminución del 36% del riesgo relativo de ictus en el grupo de tratamiento. Por otro lado, también se observó una disminución del 27% del riesgo relativo de infarto agudo de miocardio y del 13% de la mortalidad por cualquier causa. Otro estudio mostró que en pacientes mayores de 80años que presentaban una PAS superior a 160mmHg el control de presión arterial por debajo de 150/80mmHg mediante indapamida, con o sin perindopril, conseguía reducir el riesgo relativo de ictus un 30%, la mortalidad por ictus un 39% y un 21% la mortalidad por cualquier causa en comparación con el placebo7.
En un metaanálisis del año 2011 se investigó cuáles deberían ser las cifras de presión arterial a partir de las cuales debemos iniciar tratamiento antihipertensivo8. Se incluyeron 22 ensayos clínicos con 201.566 participantes y se analizó el efecto del control de la presión arterial en diferentes grupos en función de la PAS basal: <140, 140-159, 160-179 y ≥180mmHg. En todos los grupos se consiguió disminuir el riesgo relativo de enfermedades vasculares: un 15% en el grupo de PAS <140mmHg, un 18% en el grupo de PAS 140-159mmHg, un 20% en el grupo de PAS 160-179mmHg y un 35% en el grupo de PAS ≥180mmHg. La reducción del riesgo no fue significativamente diferente entre los grupos predefinidos de PAS basal (p=0,17), ni usando otros puntos de corte de PAS y/o PAD. Tampoco se observó una diferencia significativa en la reducción del riesgo entre los diferentes grupos por cada mmHg de reducción obtenida de la PAS o la PAD, indicando que en todos los grupos se observa un beneficio similar.
El estudio The Action to Control Cardiovascular Risk in Diabetes (ACCORD) blood pressure trial (ACCORD-BP) investigó el efecto del control intensivo de la presión arterial (objetivo de PAS <120mmHg) comparado con el control estándar (PAS <140mmHg), en pacientes con diabetes9. En este caso no se encontraron diferencias entre ambos grupos en cuanto al objetivo principal de combinación de infarto de miocardio, ictus o mortalidad de causa vascular (HR: 0,88; IC95%: 0,73-1,06; p=0,20) ni de mortalidad (HR: 1,07; IC95%: 0,85-1,35; p=0,55). Lo que sí se observó es que en los pacientes con control intensivo de la presión arterial se consiguió disminuir un 41% el riesgo relativo de sufrir un ictus (HR: 0,59; IC95%: 0,39-0,89; p=0,01).
El estudio The Systolic Blood Pressure Intervention Trial (SPRINT) también analizó si el control intensivo de la presión arterial conseguía disminuir el riesgo de enfermedades vasculares, pero en este caso se excluyeron los pacientes con diabetes10. Este estudio incluyó 9.361 personas con un riesgo vascular elevado que no habían sufrido un ictus y con cifras de PAS por encima de 130mmHg. Se aleatorizaron a 2grupos: tratamiento intensivo (control de PAS <120mmHg) o tratamiento estándar (control de PAS <140mmHg). La variable principal del estudio fue la combinación de infarto agudo de miocardio, síndrome coronario, ictus, insuficiencia cardíaca o mortalidad por causa vascular. Se alcanzó la variable principal del estudio en el 1,65% de las personas en el grupo intensivo y en el 2,19% en el grupo estándar, lo que supone una disminución del 25% con tratamiento intensivo (HR: 0,75; IC95%: 0,64-0,89; p<0,001). En el grupo de tratamiento intensivo también se demostró una disminución del 27% en la mortalidad (HR: 0,73; IC95%: 0,60-0,90, p=0,003). En el subgrupo de individuos mayores de 75años se observó una disminución del 35% en la variable principal del estudio y del 33% en la mortalidad en el grupo de control intensivo11.
En el año 2016 se publicó un metaanálisis que recogía 16 ensayos clínicos que incluyeron 52.235 sujetos, que analizaban el efecto del control intensivo de la presión arterial sobre el riesgo vascular12. De forma global, el control intensivo de la presión arterial consiguió reducir el riesgo relativo de ictus un 29%, de cardiopatía isquémica un 20% y de mortalidad vascular un 21%. Sin embargo, los diferentes estudios consideraban distintos objetivos de control de presión arterial, por lo que se realizó un análisis estratificando el efecto en función del objetivo de PAS alcanzado. Se comparó el control de PAS <130 vs. ≥130mmHg, entre 130-139 vs. ≥140mmHg y entre 140-149 y ≥150mmHg. En todos los grupos el tratamiento intensivo consiguió una disminución del riesgo de ictus, cardiopatía isquémica y mortalidad vascular, y si bien no se observó una diferencia en la reducción del riesgo relativo de ictus entre los diferentes grupos de presión arterial objetivo, sí se observó que la reducción absoluta de riesgo era menor en el grupo de control <130 vs. ≥130mmHg, sugiriendo que los pacientes con PAS inicial más baja presentaban un riesgo vascular menor.
Recomendaciones:
- 1.
Se recomienda iniciar tratamiento antihipertensivo en prevención primaria de ictus en pacientes con cifras de presión arterial superiores a 140/90mmHg (recomendación claseI, nivel de evidenciaA).
- 2.
En pacientes con hipertensión arterial está indicado alcanzar cifras de presión arterial <130/80mmHg (recomendación claseI, nivel de evidenciaA).
Se han estudiado diferentes fármacos antihipertensivos en la prevención de eventos vasculares, como diuréticos, betabloqueantes, inhibidores de la enzima convertidora de angiotensina (IECA), antagonistas del receptor de angiotensina (ARA-II) o antagonistas del calcio. Los resultados de los principales ensayos clínicos se recogen en un metaanálisis de 2018 que compara los diferentes antihipertensivos en prevención primaria13. De forma global, no se encontraron diferencias estadísticamente significativas entre los diferentes fármacos antihipertensivos en cuando a la prevención de infarto agudo de miocardio o muerte de causa vascular. Únicamente se observó una tendencia a una mayor mortalidad vascular cuando se usaban betabloqueantes comparado con los diuréticos tiazídicos (OR: 1,20; IC95%: 0,98-1,40) y los antagonistas del calcio (OR: 1,2; IC95%: 0,98-1,40). Analizando específicamente el riesgo de ictus, se encontró que los betabloqueantes conferían un aumento del 30% del riesgo relativo de ictus comparado con los diuréticos tiazídicos (OR: 1,30; IC95%: 1,1-1,6) y de un 40% (OR: 1,4, IC95%: 1,1-1,7) comparado con los antagonistas del calcio. No se encontraron diferencias entre los IECA y los ARA-II y el resto de los fármacos antihipertensivos.
Recientemente se ha publicado un estudio que analiza el momento en el que debe tomarse la medicación antihipertensiva14. Incluyeron 19.084 pacientes con hipertensión arterial que fueron aleatorizados a tomar el tratamiento antihipertensivo al acostarse o al levantarse por la mañana. Como objetivo principal analizaron el riesgo vascular definido como mortalidad vascular, infarto agudo de miocardio, revascularización coronaria, insuficiencia cardíaca o ictus. Los pacientes que tomaban el tratamiento al acostarse presentaron un 45% menos de riesgo vascular (OR: 0,55; IC95%: 0,50-0,61). Analizando específicamente la enfermedad cerebrovascular, la toma de medicación nocturna redujo un 49% el riesgo relativo de ictus (OR: 0,51; IC95%: 0,41-0,63).
Recomendaciones:
- 1.
No está claro cuál es el fármaco más adecuado para el control de la hipertensión arterial en prevención primaria de ictus. Como tratamiento de inicio es razonable utilizar diuréticos tiazídicos y antagonistas del calcio en lugar de betabloqueantes (recomendación claseI, nivel de evidenciaA).
- 2.
La toma nocturna de la medicación antihipertensiva puede ser útil en la reducción del riesgo de ictus y otras enfermedades vasculares (recomendación claseIIa, nivel de evidenciaB).
En la mayoría de los pacientes se produce una elevación de la presión arterial durante la fase aguda del ictus15, con una disminución progresiva en los días siguientes hasta alcanzar los niveles basales16. En estudios observacionales se ha evidenciado que las cifras de presión arterial durante la fase aguda del ictus ejercen un efecto en U, y tanto valores extremos tanto altos como bajos de presión arterial se asocian a un peor pronóstico funcional, con mayor porcentaje de deterioro neurológico precoz, recurrencia de ictus y mortalidad17,18. Este efecto puede explicarse por el hecho de que las cifras elevadas de presión arterial incrementan el riesgo de edema y transformación hemorrágica19 y las cifras bajas pueden disminuir la perfusión cerebral en la región isquémica20. También puede deberse a un aumento de la respuesta inflamatoria que se asocia a un peor pronóstico, que se observa en los pacientes con cifras elevadas de presión arterial durante la fase aguda del ictus que no tenían diagnóstico previo de hipertensión arterial21.
En base a estos hallazgos nos preguntamos cuándo se debe iniciar el tratamiento antihipertensivo tras un ictus, cuáles son las cifras que debemos alcanzar en prevención secundaria de ictus y si existe algún fármaco más adecuado para el control de la presión arterial tras un ictus.
¿Cuándo se debe iniciar el tratamiento antihipertensivo después de un ictus?Fuera del manejo de la presión arterial en el contexto de terapias de reperfusión, los datos de los que disponemos para contestar a esta pregunta proceden en su mayor parte de estudios en los se evalúa el efecto del tratamiento antihipertensivo durante las primeras 72h del ictus (tabla 1), si bien en algunos de estos estudios la población objetivo estudiada incluye también pacientes con ictus hemorrágico y un muy pequeño porcentaje de pacientes que recibieron tratamiento trombolítico.
Resumen de los principales estudios que valoran el inicio temprano del tratamiento antihipertensivo
| Nombre del estudio y cita | Año | Número de pacientes | Tiempo límite para inclusión, horas | Tiempo desde inicio de los síntomas, horas (media) | % tPA | Intervención | Resultados |
|---|---|---|---|---|---|---|---|
| VENUS23 | 2001 | 454 (261 ictus isquémicos) | < 6 | ND | ND | Nimodipino vs. placebo 10 días | ERm > 3 a los 3 mesesGlobal: RR: 1,2 (IC95%: 0,9-1,6)Isquémico: RR: 1,4 (IC95%: 1-2,1) |
| ACCESS26 | 2003 | 339 ictus isquémicos | < 36 | 30 (media) | ND | Candesartán vs. placebo 7 días | IB a los 3 meses: no diferencias.Estudio parado de forma prematura por más eventos vasculares y mortalidad a los 12 meses en el grupo placebo.OR: 0,48 (IC95%: 0,25-0,90) |
| ProFESS29 | 2009 | 1.360 ictus isquémicos | < 72 | 58 (media) | ND | Telmisartán vs. placebo 90 días | ERm al día 30: No diferencias en análisis ordinal (OR: 1,03; IC95% 0,84-1,26) o dicotómico (OR: 1; IC95%: 0,77-1,29) |
| CHHIPS28 | 2009 | 176 (99 ictus isquémicos) | < 36 | ND | 0 | Labetalol o lisinopril vs. placebo 2 semanas | ERm > 3 a las 2 semanasRR: 1,03; IC95%: 0,8-1,33Mortalidad día 90 reducida en el grupo de tratamiento (HR: 0,4; IC95%: 0,2-1) |
| COSSACS30 | 2010 | 763 (454 isquémicos) | < 48 | ND | 0 | Continuar vs. interrumpir medicación antihipertensiva durante 2 semanas | ERm > 3 a las 2 semanas.Global: RR: 0,86; IC95%: 0,65-1,14Ictus isquémico RR: 0,70; IC95%: 0,51-0,99; p=0,045 |
| SCAST27 | 2011 | 2.029 (1.733 isquémicos) | < 30 | ND | 8,7 | Candesartán vs. placebo 7 días | ERm > 2 a los 6 meses. OR: 1,13; IC95%: 0,97-1,32; ajustado 1,17; IC95%: 1-1,38Muerte vascular, infarto de miocardio no fatal e ictus no fatal a los 6 meses (HR: 1,09; IC95%: 0,84-1,41) |
| CATIS24 | 2013 | 4.071 con ictus isquémico | < 48 | 15 (media) | 0 | Medicación antihipertensiva o no durante la hospitalización | ERm > 2 a los 14 días o al alta hospitalaria.Global: OR: 1; IC95%: 0,88-1,14Inicio de tratamiento > 24 h: OR: 0,73; IC95%: 0,55-0,97 |
| VENTURE31 | 2015 | 393 | < 48 | 12 (media) | ND | Valsartán o no tratamiento 7 días | ERm > 2 al día 90OR: 1,1; IC95%: 0,69-1,79Mayor deterioro neurológico temprano en el grupo de valsartán. OR: 2,43; IC95%: 1,25-4,73 |
| ENOS25 | 2015 | 4.011 (3.348 isquémicos) | < 48 | 26 (mediana) | 10,6 | NTG transdérmica vs. no-NTG durante 7 días | ERm al día 90 ordinal.OR: 1,01; IC95%: 0,91-1,13 |
ERm: Escala de Rankin modificada; HR: hazard ratio; IB: índice de Barthel; IC: intervalo de confianza; ND: no disponible; OR: odds ratio; RR: riesgo relativo.
Un metaanálisis22 publicado en 2015 que incluyó 13 estudios en los que se valoró el efecto del inicio del tratamiento antihipertensivo durante los primeros 3días tras el inicio de los síntomas en 12.703 pacientes con ictus agudo demostró que el tratamiento antihipertensivo en este periodo de tiempo no se asociaba con un peor pronóstico funcional a los 3meses (OR: 1,04, IC95%: 0,96-1,13).
El estudio que incluyó pacientes de manera más precoz fue el Very Early Nimodipine Use in Stroke (VENUS)23, que comparó el uso de nimodipino durante 10días frente a placebo, iniciando el tratamiento durante las primeras 6h tras el inicio de los síntomas en 454 pacientes con ictus, sin observarse diferencias en el pronóstico funcional a los 3meses (RR 1,2; IC95%: 0,9-1,6).
Entre los estudios que incluyeron un mayor número de pacientes destacan los estudios The China Antihyperintensive Trial in Ischemic Stroke (CATIS) y el Efficacy of Nitric Oxide in Stroke (ENOS). El estudio CATIS incluyó a más de 4.000 pacientes con ictus isquémico agudo en los que se inició tratamiento antihipertensivo en las primeras 48h desde el inicio de los síntomas24. De manera global, el inicio del tratamiento antihipertensivo no modificó el pronóstico funcional a los 3meses (OR: 0,99; IC95%: 0,86-1,15). Sin embargo, el inicio del tratamiento antihipertensivo entre las 24 y las 48h se asoció con una mayor probabilidad de buen pronóstico funcional a los 3meses (OR: 0,73; IC95%: 0,55-0,97).
El estudio ENOS25 incluyó 4.011 pacientes (3.348 ictus isquémicos), también dentro de las primeras 48h desde el inicio de los síntomas. En este estudio se comparó el empleo de nitroglicerina transdérmica vs. tratamiento convencional, sin observarse ninguna diferencia en el análisis ordinal de la escala de Rankin modificada (ERm) en el día90.
El estudio Acute Candesartan Ciletexil Therapy in Stroke Survivors (ACCESS)26 valoró el tratamiento con candesartán frente a placebo en pacientes con ictus isquémico durante 7días. Los pacientes eran incluidos dentro de las primeras 36h del inicio de los síntomas, y aunque no hubo diferencias en el objetivo principal de dependencia a los 3meses, el estudio fue parado de forma prematura con 339 pacientes incluidos por mayor número de eventos vasculares (9,8 vs. 18,7%; p=0,026) y mortalidad a los 12meses (2,9 vs. 7,2%; p=0,07) en el grupo placebo. Sin embargo, estos resultados no fueron reproducidos posteriormente en el Scandinavian Candesartan Acute Stroke Trial (SCAST)27, un estudio que incluyó 2.029 pacientes, 1.733 de ellos con ictus isquémico, dentro de las primeras 30h del inicio de los síntomas y que valoraba un régimen de tratamiento con candesartán o placebo durante 7días. El estudio tuvo que ser parado prematuramente debido a un lento reclutamiento y falta de fondos. Este estudio empleó dos variables principales: la ERm a los 6meses y un objetivo combinado de muerte vascular, infarto de miocardio no fatal e ictus no fatal a los 6meses. En ningunas de las dos variables principales se observaron diferencias significativas entre ambos grupos de tratamiento. Aunque en un análisis ordinal de la ERm ajustada por edad, tipo de ictus, gravedad clínica y PAS había una tendencia a favor de placebo, la diferencia encontrada no fue estadísticamente significativa al usar dos variables principales. Entre las variables secundarias se observó un mayor porcentaje de progresión del ictus en los pacientes en el grupo de candesartán (6% vs. 4%; p=0,04).
El estudio Controlling Hypertension and Hypotension Immediately Post-Stroke (CHHIPS)28 aleatorizó a 176 pacientes, 99 con ictus isquémico, dentro de las primeras 36h desde el inicio de los síntomas a un tratamiento antihipertensivo con labetalol y/o lisinopril vs. placebo durante 2semanas. La variable principal, ERm>3 a las 2semanas, no fue diferente entre los dos grupos, pero se observó una reducción de la mortalidad a los 90días en el grupo que recibió tratamiento antihipertensivo.
En un subanálisis del estudio Prevention Regimen for Effectively Avoiding Second Strokes (PRoFESS)29 se evaluó el uso de telmisartán administrado durante las primeras 72h del ictus frente a placebo en 1.360 pacientes con ictus isquémico, sin encontrarse diferencias en el pronóstico funcional a los 3meses entre ambos grupos (OR 1,03; IC95%: 0,84-1,26).
El estudio multicéntrico Continue or Stop Post-Stroke Antihypertensives Collaborative Study (COSSACS)30 incluyó a 763 pacientes con ictus agudo que estaban recibiendo tratamiento antihipertensivo antes del ictus, de los cuales 454 eran ictus isquémicos. Este estudio evaluó el mantenimiento o la discontinuación del tratamiento antihipertensivo durante las primeras dos semanas del ictus en pacientes incluidos dentro de las 48h tras el inicio de los síntomas. Si bien tuvo que suspenderse de forma prematura por reclutamiento lento y falta de financiación, continuar el tratamiento antihipertensivo no modificó el riesgo de dependencia funcional a los 3meses (RR: 0,86; IC95%: 0,65-1,14; p=0,30). Tampoco se encontraron diferencias en cuanto al riesgo vascular, la mortalidad a los 6meses o el número de efectos adversos.
El estudio Valsartan Efficacy oN modesT blood pressUre Reduction in acute ischemic stroke (VENTURE)31 aleatorizó a 393 pacientes con ictus isquémico a un tratamiento con valsartán o placebo durante 7días. La variable principal era el grado de dependencia en la ERm el día90, para la cual no se observaron diferencias significativas. Sí se observó mayor deterioro neurológico temprano en el grupo de valsartán (OR: 2,43; IC95%: 1,25-4,73).
Recomendaciones:
- 1.
En los pacientes con ictus isquémico se recomienda iniciar el tratamiento de la presión arterial pasadas las primeras 24h desde el inicio de los síntomas (recomendación claseI, nivel de evidenciaA).
- 2.
El inicio del tratamiento antihipertensivo entre las 24-72h tras el inicio de los síntomas es seguro y puede ser razonable (recomendación claseI, nivel de evidenciaB).
- 3.
En los pacientes que estaban tomando tratamiento antihipertensivo antes del ictus puede considerarse reiniciar el tratamiento antihipertensivo entre las 24-48h tras el ictus (recomendación claseI, nivel de evidenciaB).
Diferentes estudios han demostrado que el control de la presión arterial consigue disminuir el riesgo de recurrencia tras un ictus, pero es importante conocer a partir de qué cifras de presión arterial debemos iniciar tratamiento antihipertensivo y qué cifras debemos alcanzar como objetivo de control.
El The perindopril protection against recurrent stroke study (PROGRESS)32 incluyó 6.015 pacientes, con o sin hipertensión arterial, que habían sufrido un ictus en los últimos 5años y fueron aleatorizados a recibir perindopril con o sin indapamida o placebo. El tiempo de seguimiento medio fue de 3,9años y el objetivo principal del estudio fue evaluar la recurrencia de ictus. De manera global se demostró que el tratamiento antihipertensivo disminuía el riesgo de recurrencia de ictus un 28%. Analizando por subgrupos de pacientes en función de las cifras de PAS basal se encontró que por encima de los 140mmHg el tratamiento antihipertensivo disminuía la recurrencia de ictus. Cuando las cifras de PAS basales estaban entre 120 y 139mmHg se encontró una tendencia hacia el beneficio del tratamiento, pero no fue estadísticamente significativa, y por debajo de 120mmHg el tratamiento antihipertensivo no ejercía ningún efecto en la prevención de ictus.
Más adelante surgieron otros estudios, que fueron incluidos en un metaanálisis publicado en el año 200933, en el que se demostró que el tratamiento antihipertensivo conseguía disminuir la recurrencia de ictus con cifras basales de PAS por encima de 130mmHg (OR: 0,75; IC95%: 0,62-0,89) y cifras basales de PAD por encima de 70mmHg (OR: 0,64; IC95%: 0,50-0,80). Con cifras basales de PAS por debajo de 130mmHg no se consiguieron diferencias en cuanto al riesgo de recurrencia de ictus (OR: 0,56; IC95%: 0,26-1,17).
Sin embargo, otros estudios han demostrado que cuanto más bajas sean las cifras de presión arterial alcanzadas, el riesgo de recurrencia vascular es menor. En un subanálisis del estudio PROGRESS34 el riesgo de recurrencia anual de ictus fue del 2,23% cuando las cifras de PAS alcanzadas fueron <120mmHg, del 2,81% para PAS entre 120-139mmHg, del 3,36% para PAS entre 140-159mmHg y del 5,65% para PAS >160mmHg.
En el año 2017 se publicó un metaanálisis que analizó el riesgo de recurrencia de ictus en función de las cifras de PAS alcanzadas durante el seguimiento35. El subgrupo de pacientes que alcanzó una PAS <130mmHg presentó una menor tasa de recurrencia de ictus (8,3%), comparado con el grupo que alcanzó PAS entre 130 y 140mmHg (9,2%) y el grupo de PAS >140mmHg (11,7%), alcanzando una significación estadística (p=0,048).
Otros estudios han analizado el efecto del control intensivo de la presión arterial en el riesgo de recurrencia de ictus. El Secondary Prevention of Small Subcortical Strokes (SPS3)36 comparó el control intensivo de presión arterial (PAS <130mmHg) frente al control estándar (PAS entre 130-149mmHg) en pacientes con ictus lacunar. Aunque no se observaron diferencias en cuando al riesgo de global de ictus (HR: 0,81; IC95%: 0,64-1,03), se observó una reducción del 63% del riesgo de hemorragia cerebral en el grupo de control intensivo (OR: 0,37; IC95%: 0,15-0,95). Recientemente se ha publicado el estudio Recurrent Stroke Prevention Clinical Outcome (RESPECT)37, que incluyó 1.280 pacientes con ictus en los últimos 3años que se asignaron de forma aleatoria a conseguir un control intensivo de presión arterial (PA <120/80mmHg) o tratamiento estándar (PA <140/90mmHg). En este estudio, el control intensivo no se asoció a una disminución del riesgo de ictus (OR: 0,73; IC95%: 0,49-1,11) ni de cardiopatía isquémica (OR: 1,23; IC95%: 0,33-4,59) o mortalidad (OR: 0,80; IC95%: 0,49-1,29), pero de nuevo se encontró una importante disminución del riesgo de hemorragia cerebral (OR: 0,09; IC95%: 0,01-0,70). Los datos de este estudio se incluyeron en un metaanálisis posterior37, en el que se encontró que el control intensivo de la presión arterial disminuía el riesgo relativo de recurrencia de ictus un 22% (OR: 0,78; IC95%: 0,64-0,96), siendo el objetivo de control que mostró mayor beneficio el alcanzar cifras de presión arterial <130/80mmHg.
Recomendaciones:
- 1.
En prevención secundaria de ictus se recomienda alcanzar cifras <130/80mmHg como objetivo de control de presión arterial (recomendación claseI, nivel de evidenciaB).
- 2.
Se recomienda iniciar el tratamiento antihipertensivo en pacientes que han sufrido un ictus isquémico cuando presentan cifras mantenidas de presión arterial >140/90mmHg (recomendación claseI, nivel de evidenciaA).
- 3.
En pacientes con ictus lacunar se recomienda iniciar tratamiento antihipertensivo cuando presentan cifras de presión arterial >130/80mmHg (recomendación claseI, nivel de evidenciaB).
- 4.
En pacientes que han sufrido un ictus y presentan cifras de presión arterial <140/90mmHg puede ser beneficioso iniciar tratamiento antihipertensivo (recomendación claseIIb, nivel de evidenciaB).
Se han realizado diferentes estudios en prevención secundaria de ictus que han empleado distintos fármacos, como diuréticos, IECA, ARA-II, betabloqueantes y antagonistas del calcio (tabla 2). El Post-stroke Antihypertensive Treatment Study (PATS) fue el primer estudio que mostró que el uso del diurético indapamida reducía el riesgo relativo de ictus un 29% comparado con placebo en pacientes con ictus o AIT38.
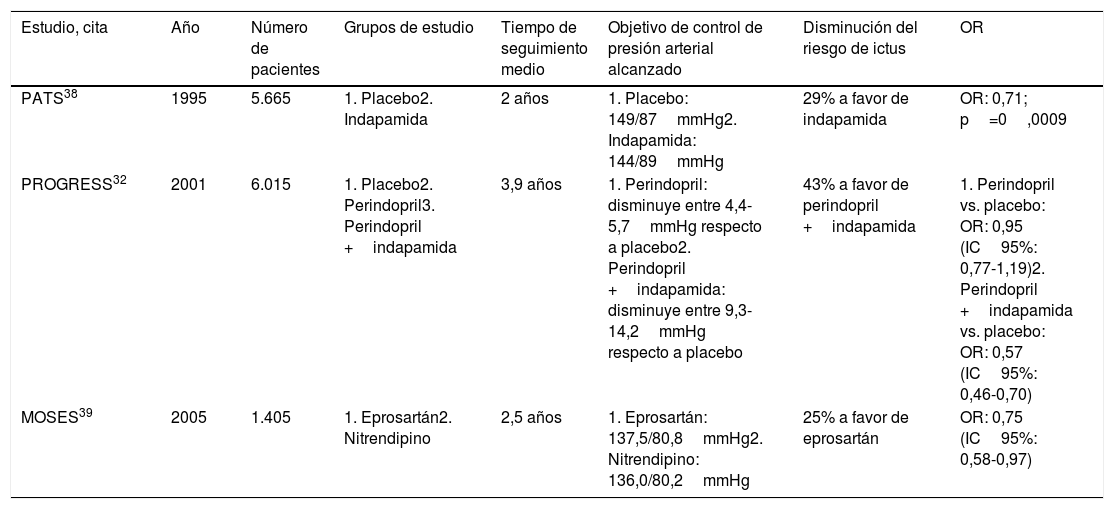
Características de los principales ensayos clínicos con fármacos antihipertensivos en prevención secundaria de ictus
| Estudio, cita | Año | Número de pacientes | Grupos de estudio | Tiempo de seguimiento medio | Objetivo de control de presión arterial alcanzado | Disminución del riesgo de ictus | OR |
|---|---|---|---|---|---|---|---|
| PATS38 | 1995 | 5.665 | 1. Placebo2. Indapamida | 2 años | 1. Placebo: 149/87mmHg2. Indapamida: 144/89mmHg | 29% a favor de indapamida | OR: 0,71; p=0,0009 |
| PROGRESS32 | 2001 | 6.015 | 1. Placebo2. Perindopril3. Perindopril +indapamida | 3,9 años | 1. Perindopril: disminuye entre 4,4-5,7mmHg respecto a placebo2. Perindopril +indapamida: disminuye entre 9,3-14,2mmHg respecto a placebo | 43% a favor de perindopril +indapamida | 1. Perindopril vs. placebo: OR: 0,95 (IC95%: 0,77-1,19)2. Perindopril +indapamida vs. placebo: OR: 0,57 (IC95%: 0,46-0,70) |
| MOSES39 | 2005 | 1.405 | 1. Eprosartán2. Nitrendipino | 2,5 años | 1. Eprosartán: 137,5/80,8mmHg2. Nitrendipino: 136,0/80,2mmHg | 25% a favor de eprosartán | OR: 0,75 (IC95%: 0,58-0,97) |
OR: odds ratio
Estudios posteriores también evidenciaron que los diuréticos ejercían un efecto beneficioso en el riesgo de recurrencia de ictus. El estudio PROGRESS32 incluyó 6.015 pacientes con ictus o AIT en los últimos 5años, que fueron aleatorizados en 3grupos: placebo, perindopril y perindopril +indapamida. Comparado con placebo, el grupo que recibió solo perindopril no consiguió disminuir el riesgo de recurrencia de ictus (OR: 0,95; IC95%: 0,77-1,19); sin embargo, la asociación de perindopril e indapamida consiguió reducir un 43% el riesgo relativo de recurrencia respecto al placebo (OR: 0,57; IC95%: 0,46-0,70).
El estudio The Morbidity and Mortality after Stroke, Eprosartan Compared with Nitrendipine for Secondary Prevention (MOSES)39 comparó un ARA-II (eprosartán) con un antagonista del calcio (nitrendipino) en pacientes que habían sufrido un ictus en los últimos 2años. A pesar de que las cifras de presión arterial alcanzadas en ambos grupos fueron similares (137,5/80,8mmHg en el grupo de eprosartán vs. 136,0/80,2 en el grupo de nitrendipino), los pacientes que recibieron eprosartán presentaron un 25% menos de riesgo relativo de recurrencia de ictus (OR: 0,75; IC95%: 0,58-0,97).
Recomendaciones:
- •
Como tratamiento de inicio es recomendable utilizar ARA-II o diuréticos solos o en asociación con IECA en prevención secundaria de ictus (recomendación claseI, nivel de evidenciaB). No obstante, no hay datos suficientes que comparen los diferentes fármacos antihipertensivos entre sí respecto a la prevención secundaria de ictus.