La epilepsia resistente a fármacos antiepilépticos (ERF) constituye un problema socio-sanitario de primer nivel, que debe ser individualizado precozmente por sus dramáticas repercusiones individuales y colectivas.
DesarrolloRecientemente, la Liga Internacional Contra la Epilepsia ha definido la ERF como aquella en la que no se controlen las crisis tras haber tomado de forma adecuada dos fármacos antiepilépticos apropiados y bien tolerados, entendiendo como falta de control la aparición de crisis en un año o en un tiempo inferior a tres veces el intervalo entre crisis que mostraba antes de iniciar el tratamiento. Esta sociedad internacional recomienda en todo paciente con ERF una evaluación rápida y detallada en una unidad de epilepsia. Se entiende como Unidad Clínica de Epilepsia (UCE) el conjunto de profesionales que actuando en colaboración tienen como objetivo primario el diagnóstico y tratamiento del paciente con epilepsia. Las UCE en España pueden ser estratificadas en distintos niveles, dependiendo de la actividad que se desarrolle en cada una de ellas. La consulta específica de epilepsia se considera como el germen de toda UCE, siendo necesaria la figura del experto en epilepsia. En las UCE médicas se realiza la monitorización vídeo-EEG prolongada. En las UCE médico-quirúrgicas además se realiza cirugía de epilepsia de dificultad diversa.
ConclusionesTodas las UCE deben cooperar con protocolos consensuados, debiendo existir un flujo bidireccional entre ellas. La estratificación de las UCE permite una alta eficacia y eficiencia, debiendo existir el suficiente número que garantice el fácil acceso de todos los pacientes con epilepsia.
Drug-resistant epilepsy (DRE) is a top-priority social health problem which requires early individual treatment due to its dramatic repercussions for the patient and society.
DevelopmentThe International League Against Epilepsy (ILAE) has recently defined DRE as that in which the seizures are not controlled after having correctly taken two appropriate and well tolerated anti-epileptic drugs, with lack of control being understood as the appearance of seizures within one year or in a period less than three times the inter-seizure interval before starting treatment. This International Society recommends a rapid and detailed assessment of all patients in an Epilepsy Unit. A Clinical Epilepsy Unit (CEU) is understood as a group of professionals who, acting in collaboration, have the diagnosis and treatment of the patient with epilepsy as their primary objective. CEUs in Spain may be stratified into different levels depending on the activity carried out in each of them. The specific epilepsy clinic is considered the fundamental type of CEU and includes the necessary figure of an expert in epilepsy. Prolonged video-monitoring is performed in medical CEUs. In medical-surgical CEUs epilepsy surgery with varying degrees of difficulty is also performed.
ConclusionsAll CEUs must cooperate with consensus protocols, and there must be a two-way flow between them. Stratification of CEUs increases efficacy and efficiency, due to there being a sufficient number of them to ensure easy access by all patients with epilepsy.
El tratamiento convencional de la epilepsia se basa en la administración crónica y continuada de fármacos antiepilépticos (FAE), que tienen como finalidad el control total de las crisis epilépticas, sin causar efectos secundarios, para alcanzar la mejor calidad de vida. Aún a pesar del tratamiento más idóneo con FAE, alrededor del 25% de los pacientes afectos de epilepsia continúan sufriendo crisis, y padeciendo de la denominada epilepsia de difícil control, refractaria o resistente a FAE (ERF)1.
Necesidad del concepto de epilepsia resistente a fármacos antiepilépticosAl ser la epilepsia un diagnóstico basado casi siempre en datos de anamnesis, el fallo diagnóstico de inicio es frecuente, tanto por error en el tipo de epilepsia, como por confusión con otros eventos paroxísticos que simulan crisis epilépticas. De forma aproximada, el 25% de los pacientes diagnosticados de ERF, tiene un diagnóstico equivocado, siendo la monitorización vídeo-EEG con visualización y filiación de los eventos críticos una técnica diagnóstica esencial en estos pacientes. Asimismo, una parte de los supuestamente afectos de ERF, no ha recibido el tratamiento apropiado o bien no lo ha tomado de forma adecuada, por lo que en muchas ocasiones una simple corrección terapéutica, puede conllevar el control de la epilepsia2.
Por otro lado, la cirugía se ha consolidado en los últimos años como una técnica eficaz y segura que puede y debe ser ofertada a numerosos pacientes con ERF. La cirugía de la epilepsia no debe ser un recurso épico en numerosos procesos y en concreto, en la epilepsia del lóbulo temporal, en la epilepsia neocortical con lesiones bien circunscritas y en los procesos hemisféricos unilaterales desencadenantes de ERF, en los que se alcanza la remisión total de las crisis en un porcentaje elevado3, persistente en el tiempo de manera habitual4. Numerosas sociedades internacionales recomiendan ofertar la cirugía a los pacientes con indicación electiva en cuanto se compruebe que no responden a FAE en un tiempo razonable5,6. Otras formas terapéuticas para la ERF, como la estimulación del nervio vago, la estimulación cerebral y la dieta cetógena, pueden ser efectivas en pacientes seleccionados.
Los pacientes con ERF presentan habitualmente una calidad de vida disminuida, distintas morbilidades asociadas y una tasa de mortalidad incrementada. Se necesitarían numerosos años para tratar a un paciente con epilepsia con todo el arsenal de FAE disponibles en la actualidad, tanto en monoterapia como en combinación y así demostrar la intratabilidad absoluta, perdiéndose un tiempo crucial, en el que se pueden producir consecuencias irreparables. Por este motivo, es necesario considerar la ERF como una entidad a individualizar precozmente, para optimizar el diagnóstico preciso, ofertar el mejor tratamiento farmacológico posible o considerar tratamientos alternativos y establecer recomendaciones de estilo de vida que son relevantes para la adaptación social7.
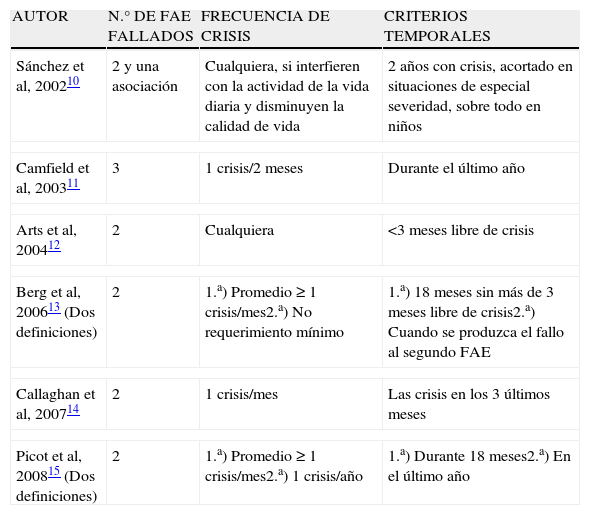
Necesidad del concepto único de epilepsia resistente a fármacos antiepilépticosHasta hace poco, el concepto de ERF ha sido variable, dependiendo del criterio de los distintos autores, de aquí el gran número de definiciones existentes8. Ésto ha estado motivado fundamentalmente por el amplio rango de refractariedad, que abarca desde pacientes con crisis leves y esporádicas, parcialmente resistentes a FAE, a otros con crisis graves y frecuentes, absolutamente intratables con FAE. También ha influido el motivo del estudio, siendo diferente para los estudios observacionales, para los ensayos clínicos con FAE en investigación o para la cirugía de la epilepsia, entre otros9. En las distintas definiciones utilizadas en los últimos años se han considerado diversos factores y en el único en el que han coincidido la mayoría de autores es que el número de FAE ineficaces en el control de las crisis sean dos o tres. En el resto de factores sí ha existido una gran variabilidad10–15 (tabla 1).
Características de algunas definiciones de epilepsia resistente a fármacos antiepilépticos, utilizadas en los últimos años (FAE: fármaco antiepiléptico)
| AUTOR | N.° DE FAE FALLADOS | FRECUENCIA DE CRISIS | CRITERIOS TEMPORALES |
| Sánchez et al, 200210 | 2 y una asociación | Cualquiera, si interfieren con la actividad de la vida diaria y disminuyen la calidad de vida | 2años con crisis, acortado en situaciones de especial severidad, sobre todo en niños |
| Camfield et al, 200311 | 3 | 1crisis/2meses | Durante el último año |
| Arts et al, 200412 | 2 | Cualquiera | <3meses libre de crisis |
| Berg et al, 200613 (Dos definiciones) | 2 | 1.a) Promedio≥1crisis/mes2.a) No requerimiento mínimo | 1.a) 18 meses sin más de 3 meses libre de crisis2.a) Cuando se produzca el fallo al segundo FAE |
| Callaghan et al, 200714 | 2 | 1crisis/mes | Las crisis en los 3 últimos meses |
| Picot et al, 200815 (Dos definiciones) | 2 | 1.a) Promedio≥1crisis/mes2.a) 1crisis/año | 1.a) Durante 18meses2.a) En el último año |
Esta variabilidad ha motivado que los resultados clínicos y de investigación sean dispares en cuanto a epidemiología, diagnóstico y tratamiento de la ERF. Así ocurre por ejemplo, en un estudio epidemiológico en adultos, en el que al utilizar el concepto de dos FAE fallados y padecer una crisis mensual de media durante los últimos 18meses, la prevalencia de ERF fue del 15,6% de los pacientes con epilepsia activa, y al considerarla como fallo de dos FAE y haber padecido una crisis en el último año, ascendió al 22,5%15. Por este motivo, es necesario contar con una definición única, que permita conocer de forma válida y fiable la epidemiología de la ERF para implementar los recursos sanitarios necesarios, investigar cuales son las aplicaciones terapéuticas más adecuadas a cada tipo de paciente y proporcionar a los clínicos un criterio claro y operativo para el manejo adecuado de los pacientes con ERF7.
Definición actual de ERF según la Liga Internacional contra la EpilepsiaAnte la necesidad de unificar criterios en el concepto de ERF, un grupo de trabajo de la Liga Internacional Contra la Epilepsia (ILAE), compuesto por expertos en diversos campos de la epilepsia, ha propuesto una definición bien estructurada, cuyo objetivo primario es mejorar la atención a los pacientes con epilepsia. En sus conclusiones, los autores comentan una serie de desconocimientos que deben ser investigados en el futuro utilizando la nueva definición. Por este motivo, destacan que la definición propuesta necesita ser validada en estudios prospectivos rigurosos y redefinida si se obtienen nuevas evidencias. Por lo tanto, es una definición de consenso respaldada por la ILAE y es considerada como el punto de partida para un mejor conocimiento de los pacientes con ERF16.
La estructura global de la definición de la ILAE tiene dos niveles «jerárquicos». En el nivel 1 se definen los conceptos básicos de respuesta y fallo al tratamiento de un FAE. En el nivel 2 se establece el concepto de ERF, basada en los criterios obtenidos en el nivel 1. Analicémoslos:
Nivel 1: Incluye el conjunto de datos que es necesario conocer al utilizar un FAE, analizando conceptualmente los siguientes aspectos:
- •
FAE «apropiado» para la patología en la que se emplea: Debe de haber demostrado su eficacia en el tipo concreto de epilepsia que vamos a tratar.
- •
Uso «adecuado» del FAE: Tanto en dosis, intervalo entre tomas, adherencia necesaria, como en otros aspectos. No obstante, la dosis puede tener un amplio margen de variabilidad interindividual, especialmente la edad, sexo, modalidad de empleo (monoterapia, terapia asociada) o morbilidades asociadas. Para adultos, se recomienda usar la dosis diaria definida por la Organización Mundial de la Salud, que es la dosis diaria de mantenimiento de un fármaco para su indicación principal17.
- •
Efectos adversos del FAE: Se valorará razonablemente, basándose en la anamnesis y exploración clínica18. No obstante, algunos de ellos pueden ser sutiles, como los cognitivos, y estar presentes sin que el paciente los manifieste, en cuyo caso se deberá valorar si está indicado otro FAE u otra intervención terapéutica, especialmente si para el control de las crisis se necesitan dosis altas de FAE causantes de los mismos.
En el caso de que un FAE no haya sido «apropiado» o tomado de forma «adecuada» o haya sido retirado por intolerancia, o bien no ha sido posible contactar al paciente para el seguimiento, el resultado de ese FAE es indeterminado y no debe ser considerado como ineficaz16.
- •
Paciente libre de crisis: Situación en la que se constata ausencia total de crisis, incluyendo las auras y las crisis provocadas (inducidas por privación de sueño, fiebre, estimulación luminosa, etc.).
- •
Tiempo de duración del control de crisis para que un FAE sea considerado eficaz: Se emplea la denominada «regla del tres»: para alcanzar la certeza del 95% de que ha existido un efecto positivo en el control de la crisis con un FAE, se postula que la duración del tiempo libre de crisis ha de ser tres veces superior al mayor intervalo entre crisis en el año previo a la instauración del tratamiento.
Ejemplo: Si se constatan 6meses libre de crisis como período máximo de control en el año inmediato anterior al de instauración del tratamiento, se requieren 18meses sin crisis para considerar el FAE como efectivo.
Esta regla obviamente no puede aplicarse cuando se instaura un tratamiento tras la primera crisis, o cuando las crisis previas al tratamiento tienen una recurrencia superior al año, pues en este caso habría que alcanzar un período de control de crisis muy prolongado, lo que le hace perder valor práctico. Por otro lado, se establece que para considerar un FAE eficaz, la duración mínima del tiempo libre de crisis debe ser de 1año, tiempo mínimo necesario como para tener repercusiones significativas en la calidad de vida.
Se considera pues como evolución libre de crisis, la ausencia total de crisis durante un tiempo mínimo superior a tres veces el tiempo entre crisis más largo en el año previo a la instauración del FAE, o bien un tiempo de 1año tras el inicio del tratamiento, eligiendo el período más largo. Si un paciente está libre de crisis durante un tiempo superior a tres veces el intervalo de crisis pre-tratamiento, pero menos de 12meses, debe ser considerado como indeterminado. Sin embargo, si el paciente tiene otra crisis antes de finalizar el año, ese FAE se considera como fallido, aún a pesar de que la frecuencia de crisis se ha reducido respecto al pre-tratamiento16.
Nivel 2: Es el núcleo central de la definición de ERF, que queda definida como aquélla en la que el empleo de dos FAE ha resultado ineficaz en el control de las crisis. Ésto es consecuencia del resultado de estudios en los que se analizó el control de crisis con los sucesivos regímenes de FAE, demostrando que cuando fallan dos FAE, difícilmente se consigue con el empleo de otros FAE en monoterapia o en asociación, tanto en niños12, como en adultos19. Los factores de frecuencia de crisis, duración del tratamiento y tiempo de observación de las definiciones de autor se obvian, por estar incluidos en el nivel 1, al analizar el fallo de tratamiento (tabla 2).
Definición actual de epilepsia refractaria a fármacos antiepilépticos según la Liga Internacional contra la Epilepsia (ver texto para complementar) (FAE: fármaco antiepiléptico)
| Se define la epilepsia resistente a FAE como aquella en la que no se ha conseguido una evolución libre de crisis tras haber tomado dos FAE, en monoterapia o asociados, siempre que sean «apropiados» al tipo de epilepsia, tomados de forma «adecuada», no retirados por intolerancia, y: |
| 1. Todos los datos acerca de cómo han sido tomados esos dos FAE, sean conocidos. |
| 2. Se considera «evolución libre de crisis» la ausencia de cualquier tipo de crisis, incluido auras, durante un período mínimo superior a tres veces el tiempo entre crisis más largo en el año previo a la instauración del tratamiento de un FAE, o bien durante 1año desde que se instauró el tratamiento con ese FAE, eligiendo el período más largo. |
La epilepsia es un proceso dinámico y por ello el diagnóstico de ERF en un momento dado solo es válido para ese instante, no implicando una situación permanente, ya que puede solventarse con diferentes intervenciones terapéuticas, farmacológicas o de otro tipo. Durante la evolución de un proceso epiléptico se puede pasar de epilepsia resistente a sensible a FAE y viceversa. En algunos momentos de la evolución no puede decirse si se es resistente o sensible a FAE, como por ejemplo, en un paciente de nuevo diagnóstico que no ha alcanzado el tiempo requerido para definir la resistencia; en estos casos se dice que la respuesta a FAE es indefinida16 (tabla 3).
Ejemplo de la evolución en el tiempo de la denominación de una epilepsia en un paciente con respecto a su respuesta a fármacos antiepilépticos (FAE: fármaco antiepiléptico. ERF: epilepsia resistente a fármacos antiepilépticos)
| HISTORIA SUCINTA DE UN PACIENTE CON EPILEPSIA TRATADO CON FAE | NIVEL 1 CATEGORIZACIÓN DEL RESULTADO | NIVEL 2 CLASIFICACIÓN DE RESPUESTA A FAE | COMENTARIOS |
| Un paciente tiene>1crisis/semana durante 1año, a pesar de haber tomado 2 FAE apropiados de forma adecuada. Ahora toma 1 FAE diferente sin control de crisis | 2 FAE previos y 1 actual con fallo a los mismos | ERF | Fallo de 2 FAE mínimo |
| Se cambia por otro FAE (X),y no tiene crisis en 8meses | 3 FAE previos con fallo de tratamiento1 FAE (X) con evolución indeterminada | ERF | La evolución con el FAE (X) es indeterminada y la epilepsia permanece como resistente, porque no ha estado libre de crisis durante 12meses |
| Con un seguimiento de 16meses,sigue permaneciendo sin crisis | 3 FAE previos con fallo de tratamiento1 FAE (X) con evolución libre de crisis | Epilepsia sensible a FAE | El paciente no ha tenido crisis durante un tiempo tres veces superior al intervalo entre crisis antes de instaurar el FAE (X) y durante más de 12meses |
| El paciente a los 18meses tiene 2 crisis en un mes | 3 FAE previos con fallo de tratamiento1 FAE actual (X) con fallo de tratamiento | Indefinida | A pesar de que ha fallado al FAE (X), se comienza como desde un punto en el que es sensible a FAE, y por lo tanto es necesario demostrar que no es sensible a dos FAE. En el momento actual no reúne los criterios de ERF |
| Se añade un FAE apropiado y es tomado de forma adecuada, pero el paciente continúa teniendo crisis mensuales | 3 FAE previos y 2 FAE actuales con fallo de tratamiento | ERF | Después de la recaída el paciente ha fallado a dos ensayos de FAE apropiados y tomados de forma adecuada |
La definición de ERF según la ILAE tiene numerosas virtudes. Es útil y operativa para los clínicos implicados en el manejo de pacientes con epilepsia, sobre todo para profesionales no expertos en el manejo de la ERF. Considera a los pacientes con epilepsia de forma individualizada, dado que la frecuencia de crisis de un paciente y su respuesta a FAE es la que indica si padece o no de ERF. Con ella es posible la individualización rápida de ERF, y así, si un paciente tiene una crisis cada 2meses, y éstas persisten con esa frecuencia a pesar de haber tomado dos FAE adecuados, apropiados y bien tolerados, podría ser considerado como resistente a FAE en pocos meses. Pero el aspecto más destacable de la definición es que la ILAE se ha pronunciado en el tema, favoreciendo el estudio y tratamiento adecuado de este subgrupo de pacientes. Como bien se indica en el consenso de la ILAE, todo paciente con criterios de ERF debería ser evaluado de forma precoz en cuanto al diagnóstico y tratamiento recibido en el pasado y planificar el futuro, preferentemente en un centro o unidad de epilepsia16.
La aplicación de esta definición puede ser usada tanto para justificar una evaluación diagnóstica en una unidad de epilepsia, considerar la opción de cirugía, diseñar ensayos aleatorizados con FAE, como para otros fines de investigación. Ahora bien, como la decisión de una evaluación prequirúrgica, cirugía, o cualquier otro ensayo terapéutico entraña ciertos riesgos, siempre se debe realizar una valoración individual del riesgo-beneficio, en función de las características del paciente. Con respecto a la cirugía, el realizar algún ensayo farmacológico supletorio puede estar más que justificado en algunos casos. En diversos estudios ha sido demostrado que la sustitución o adicción de un nuevo FAE en pacientes con ERF que han tomado varios FAE previamente pueden conseguir que entren en remisión14,20, aunque en otros la remisión alcanzada con FAE posteriores al diagnóstico de ERF ha sido temporal, tanto en niños21, como en adultos22,23.
Otros autores han estudiado el número de FAE que puede mostrar algún beneficio en cuanto a respuesta adicional y lo han cifrado en seis para demostrar la intratabilidad absoluta con FAE24. Por este motivo, ha sido argumentado que la resistencia a FAE debería ser estratificada en función del número de FAE fallidos, sugiriéndose que los criterios para optar a cirugía deberían tener en cuenta el número de FAE tomados previamente25. No obstante, todo paciente con ERF debería ser estudiado de forma detenida en una unidad de epilepsia para conocer si realmente padece resistencia a FAE y evaluar las expectativas terapéuticas adecuadas a desarrollar en el futuro. El objetivo debe ser huir del escepticismo terapéutico en el paciente con ERF y tratar de controlar sus crisis lo más precozmente posible para proporcionarle la mejor calidad de vida relacionada con la salud y garantizar su integración social y laboral.
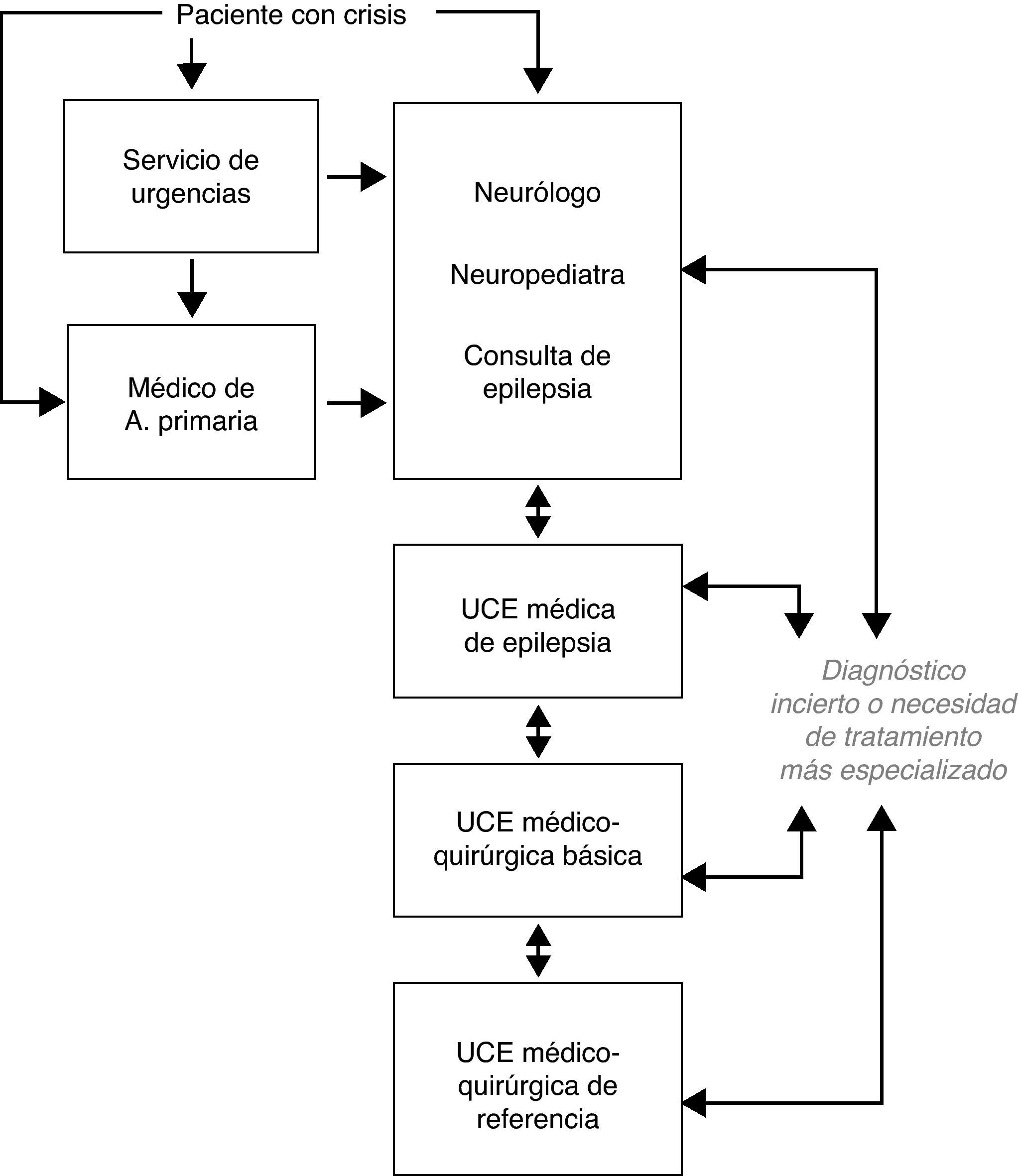
Niveles asistenciales en epilepsia. Unidades clínicas de epilepsiaEn los países con un buen sistema sanitario, como España, habitualmente los pacientes con epilepsia son atendidos en primera instancia en los servicios de urgencia o por los médicos de atención primaria, y éstos, como norma, remiten al paciente al neurólogo o neuropediatra general, que alcanza el diagnóstico preciso, instaura el tratamiento más adecuado y sigue a largo plazo al paciente en colaboración con el médico de atención primaria. Una parte de estos pacientes pueden ser adecuadamente diagnosticados y controlados de sus crisis y permanecer en este nivel asistencial sanitario. Sin embargo, en una proporción variable de pacientes, pueden existir dudas diagnósticas, continuar padeciendo crisis, o precisar de alguna actuación concreta, por lo que deben ser evaluados de forma más especializada y detallada.
Fue definida la Unidad Clínica de Epilepsia (UCE) como el conjunto de médicos y otros profesionales con especial entrenamiento y experiencia en epilepsia, que actuando en colaboración, tienen como objetivo primario el diagnóstico y tratamiento del paciente con ERF26. Se incluyen los diferentes medios y equipamiento diagnóstico y terapéutico, o bien tener un acceso facilitado a los mismos. Recientemente, se ha redefinido el concepto de UCE como el mismo conjunto de profesionales y equipamiento destinados a proporcionar el manejo integral del paciente con epilepsia, y se han establecido los servicios esenciales, personal e infraestructura que deben tener las UCE en sus diferentes niveles asistenciales27. De esta forma, aunque la UCE tiene como objetivo primario el manejo del paciente con ERF, puede proporcionar apoyo diagnóstico y terapéutico al paciente con epilepsia controlada en su inicio o en alguna fase de su evolución.
Las UCE en nuestro entorno social y económico pueden ser estratificadas en distintos niveles, dependiendo de la actividad concreta que se desarrolla en cada una de ellas. Actualmente, se puede establecer que están en actividad creciente las consultas específicas de epilepsia dentro de un servicio o sección de neurología o neuropediatría, la denominada UCE médica, la UCE médico-quirúrgica básica y la UCE médico- quirúrgica de referencia. Estos niveles asistenciales deben estar estrechamente relacionados e interconectados entre sí (fig. 1). Con respecto a anteriores revisiones sobre el tema realizadas en nuestro país, la figura de la consulta específica de epilepsia constituía por sí sola un nivel de actuación, pero en la actualidad el segundo escalón asistencial lo debe constituir la UCE médica, en las que se realiza monitorización vídeo-EEG con registro de crisis, debido a la amplia extensión y desarrollo de esta técnica; también se diferencian de forma clara las UCE médico-quirúrgicas en básicas y de referencia, dada la gran profusión de centros en donde se practica en la actualidad cirugía básica de la epilepsia28,29.
Primer nivel asistencial. Consulta específica de epilepsiaEl primer nivel de atención lo debe realizar el neurólogo general o el neuropediatra, en estrecha relación con el médico de atención primaria. Es el nivel de inicio en la evaluación del paciente con epilepsia mediante la clínica, la neurofisiología y la imagen cerebral básicas. Desde este nivel se pueden llevar a cabo consultas con el experto en epilepsia o se remitirá al paciente a la consulta específica de epilepsia, en aquellos centros en los que sea factible para una mayor profundización diagnóstica y una mejor selección del tratamiento, estando ésta imbricada entre el primer y segundo nivel asistencial. En aquellos centros que no cuenten con una consulta específica de epilepsia, debería estar facilitada la remisión de pacientes que lo necesiten a niveles asistenciales más especializados (UCE médica o médico-quirúrgica). Alrededor de las dos terceras partes de los pacientes con epilepsia pueden ser atendidos en este nivel de forma adecuada, sobre la base de una continuidad asistencial y protocolo de actuación.
La consulta específica de epilepsia debe estar a cargo de un neurólogo o neuropediatra con al menos 2años de experiencia en epilepsia, capaz de interpretar los medios complementarios de diagnóstico y de utilizar los FAE y sus combinaciones más apropiadas en cada tipo de epilepsia. Debería tener una frecuencia al menos semanal y evaluar un mínimo de 40 pacientes nuevos con epilepsia al año. Las funciones de esta consulta quedan reflejadas en la tabla 4.
Funciones de la consulta específica de epilepsia
| • Evaluación diagnóstica y terapéutica precisa de pacientes remitidos desde servicios de urgencias, atención primaria u otros servicios de atención especializada y dentro del propio servicio de neurología o neuropediatría. |
| • Remitir a los pacientes que lo necesiten a un nivel más especializado (UCE médica o médico-quirúrgica) para realizar una monitorización vídeo-EEG prolongada en pacientes con sospecha de error diagnóstico o pacientes con posibilidad de ser susceptibles de evaluación quirúrgica. |
| • Seguimiento y optimización terapéutica de aquellos pacientes en los que se ha confirmado el diagnóstico de epilepsia y se han descartado otras medidas terapéuticas en pacientes con ERF en un nivel más especializado (tratamiento quirúrgico, estimulación vagal). |
Constituye un continuo desde la consulta específica de epilepsia, siendo su diferencia fundamental, la disponibilidad de monitorización vídeo-EEG prolongada con registro de crisis, lo que permite el diagnóstico de certeza de epilepsia y su tipo, en concurrencia con otros medios diagnósticos de imagen cerebral, estructural o funcional. Existe un amplio cúmulo de evidencia para asegurar que la monitorización vídeo-EEG prolongada es de importancia vital en documentar la correlación electroclínica en los pacientes con crisis epilépticas para diferenciarlas de otros eventos paroxísticos no epilépticos, para filiar el tipo de epilepsia que padece un paciente y en el estudio de un paciente subsidiario de cirugía de epilepsia. Así mismo, existen unos estándares tanto de equipamiento necesario, de protocolos de adquisición y transferencia de datos, de seguridad para el paciente, como de su uso efectivo y eficiente, que deben estar implementados en todo centro que realice monitorización vídeo-EEG prolongada con registro de crisis epilépticas30.
Desde el primer nivel, deben remitirse a la UCE médica aquellos pacientes con epilepsia con diagnóstico incierto, aquéllos en los que las crisis epilépticas no se controlen en un plazo aproximado de un año, los que presenten recidiva de crisis sintomáticas agudas de cualquier causa en un plazo precoz, recidiva de crisis tardías recurrentes o aparición de efectos adversos de los FAE utilizados.
Sería recomendable además que la UCE médica contase con medios propios o posibilidades de referir a otros centros, para:
- •
Estudios de farmacocinética de FAE.
- •
Imagen cerebral estructural y funcional con protocolos específicos para epilepsia.
- •
Realización de estudios genéticos.
- •
Valoración neuropsicológica y cognitiva.
- •
Valoración y tratamiento de poblaciones especiales (embarazo, anciano, comorbilidades médicas y psiquiátricas).
- •
Valoración y tratamiento de crisis psicógenas no epilépticas u otros eventos paroxísticos no epilépticos.
- •
Aplicación de la dieta cetógena en los pacientes subsidiarios.
- •
La UCE médica debería tener establecidos unos protocolos claros de derivación a una UCE médico-quirúrgica para pacientes subsidiarios de valoración de cirugía.
Las UCE médicas deben estar coordinadas por un neurólogo epileptólogo. El «epileptólogo» es un neurólogo o neuropediatra interesado en el estudio de las epilepsias y con experiencia suficiente (al menos 3años) en el diagnóstico, tratamiento y cuidados de las personas con epilepsia. En ellas, se debería estudiar un mínimo de 80 pacientes con epilepsia nuevos y realizar un mínimo de 40 monitorizaciones vídeo-EEG prolongadas al año. Las funciones de las UCE médicas quedan reflejadas en la tabla 5.
Funciones de la UCE médica
| • Evaluación diagnóstica y terapéutica de pacientes remitidos desde servicios de urgencias, atención primaria u otros médicos de atención especializada o consultas de epilepsia. |
| • Monitorización vídeo-EEG prolongada de pacientes con sospecha de eventos paroxísticos no epilépticos. |
| • Monitorización vídeo-EEG prolongada de pacientes con epilepsia en los que se precise una filiación diagnóstica de precisión de las crisis epilépticas. |
| • Monitorización vídeo-EEG prolongada de pacientes con ERF. |
| • Evaluación y seguimiento terapéutico de pacientes con epilepsia pertenecientes a poblaciones especiales o con comorbilidades. |
| • Participación en ensayos clínicos de nuevos FAE. |
| • Remisión a UCE médico-quirúrgica a aquellos pacientes susceptibles de cirugía de epilepsia. |
| • Seguimiento y optimización terapéutica de aquellos pacientes en que se ha confirmado el diagnóstico de epilepsia y se han descartado otras medidas terapéuticas en un nivel más especializado (tratamiento quirúrgico, estimulación vagal). |
En este nivel se debe proporcionar todo tipo de tratamiento médico, psicológico y de apoyo social al paciente con ERF y en caso de estar indicada, una cirugía básica de epilepsia, como es la lobectomía temporal antero-medial, la lesionectomía temporal y extra-temporal en zonas alejadas de áreas funcionales elocuentes, algunas técnicas básicas de desconexión y la estimulación del nervio vago. En estas UCE se completarán los estudios practicados en otros niveles en caso de ser necesario y deben estar interconectadas de forma estrecha con las UCE médico-quirúrgicas de referencia, con objeto de remitir aquellos pacientes con necesidad de estudio prequirúrgico con medios invasivos o realizar cirugía más sofisticada, debiendo contar con unos protocolos claros de derivación de pacientes. Sería conveniente que la UCE médico-quirúrgica básica contase, además de los mismos medios que la UCE médica, con los medios necesarios para llevar a cabo las distintas técnicas quirúrgicas básicas, con sus respectivos estudios prequirúrgicos.
Se recomienda que estas UCE cuenten al menos con un neurólogo o neuropediatra epileptólogo, que actúe como coordinador, un neurorradiólogo con experiencia en epilepsia y un neurocirujano con experiencia en cirugía de epilepsia. Estas UCE deberían estudiar un mínimo de 100 pacientes con epilepsia nuevos, realizar un mínimo de 60 monitorizaciones vídeo-EEG prolongadas y un mínimo de 12 cirugías de epilepsia al año. Las funciones de la UCE médico-quirúrgica básica quedan reflejadas en la tabla 6.
Funciones de la UCE médico-quirúrgica básica
| • Las mismas que la UCE médica y además: |
| • Monitorización vídeo-EEG prolongada con electrodos no invasivos, salvo electrodos esfenoidales, en candidatos a cirugía de epilepsia. |
| • Evaluación, instauración y seguimiento de pacientes subsidiarios de estimulación vagal. |
| • Cirugía de epilepsia del lóbulo temporal, lesionectomías en el lóbulo temporal y extra-temporal en zonas cerebrales no elocuentes, y algunas técnicas básicas de desconexión, que no requieran de gran complejidad. |
| • Remisión de pacientes subsidiarios de estudios con electrodos invasivos o cirugía más sofisticada a UCE médico-quirúrgicas de referencia. |
| • Seguimiento y optimización terapéutica de aquellos pacientes en los que se ha confirmado el diagnóstico de epilepsia y se han descartado otras formas terapéuticas de cirugía en una UCE médico-quirúrgica de referencia. |
En éstas se debe ofertar al paciente con epilepsia cualquier tipo de actuación médica, psicológica, psicosocial y deben practicarse, además de las técnicas quirúrgicas básicas, las que precisen de estudio prequirúrgico invasivo (electrodos subdurales, profundos y epidurales, estimulación eléctrica cortical), resecciones temporales y extra-temporales con lesión adyacente o incluida en zonas funcionales elocuentes, las resecciones corticales sin lesión detectable en la imagen cerebral, todas las técnicas de desconexión y la cirugía de epilepsia infantil. Dado que los pacientes pediátricos quirúrgicos tienen procesos subyacentes que difieren de los del adulto y se requiere un manejo diferente, estos pacientes sería conveniente que fueran concentrados en UCE pediátricas específicas.
Recientemente ha sido revisada la acreditación de UCE médico-quirúrgica de referencia por el Consejo Interterritorial del Sistema Nacional de Salud Español. En este documento de acreditación se revisan los requerimientos de equipamiento específico necesario, los indicadores de resultados, considerándose que el número de cirugías mínimas que deben realizarse debe ser de 15-20 anuales y se establece que el personal específico la UCE médico-quirúrgica de referencia debe contar entre otros, con dos neurólogos, dos neurocirujanos, dos neurofisiólogos, atención continuada diaria de neurología y neurocirugía, y que todos los facultativos deben tener una experiencia superior a 3años en evaluación y tratamiento médico-quirúrgico de pacientes con ERF, tanto en edad pediátrica como en adultos31.
En este nivel asistencial es donde debe se debe dar una atención multidisciplinaria completa a los pacientes con ERF. La UCE debe tener protocolos de seguridad y de derivación y coordinación con los otros niveles asistenciales, facilitando el acceso de los pacientes con ERF que lo precisen. Debe contar además de los mismos medios que la UCE médico-quirúrgica básica, con los medios necesarios para llevar a cabo cualquier tipo de cirugía de epilepsia con sus respectivos estudios prequirúrgicos, incluidos los estudios con técnicas invasivas.
Opinamos que una UCE médico-quirúrgica de referencia debe contar al menos con un equipo compuesto por 2 neurólogos o neuropediatras epileptólogos, uno o dos neurocirujanos con experiencia en cirugía de epilepsia y un neurorradiólogo con experiencia en epilepsia. Debería actuar como coordinador de la UCE un neurólogo o neuropediatra con al menos 5años de experiencia en epilepsia. Estas UCE deberían estudiar un mínimo de 100 pacientes con epilepsia nuevos, realizar un mínimo de 60 monitorizaciones vídeo-EEG prolongadas y practicar 15-20 cirugías de epilepsia al año, incluyendo todo tipo de actuación. Las funciones de la UCE médico-quirúrgica de referencia quedan reflejadas en la tabla 7.
Funciones de la UCE médico-quirúrgica de referencia
| • Las mismas que la UCE médico-quirúrgica básica y además: |
| • Monitorización vídeo-EEG prolongada con electrodos invasivos (intracraneales), en candidatos a cirugía de epilepsia. |
| • Estimulación eléctrica cortical para el estudio y posible cirugía en zonas cerebrales elocuentes |
| • Todo tipo de técnica de cirugía de resección de epilepsia del lóbulo temporal y extra-temporal. |
| • Todo tipo de técnica de desconexión cerebral (hemisferectomía o variantes, técnicas de desconexión inter-hemisféricas y secciones subpiales). |
| • Evaluación prequirúrgica y cirugía en la edad pediátrica. |
Todos los pacientes con ERF precisan de un estudio pormenorizado para asegurar el diagnóstico y tratamiento idóneos. Ésto debe realizarse en las UCE en donde la monitorización vídeo-EEG constituye la técnica «estándar-oro» que permite el manejo apropiado de estos pacientes. Además, un número apreciable de pacientes con ERF puede beneficiarse de la cirugía electiva de epilepsia. La puesta en marcha de UCE mejorará los fallos detectados en el seguimiento de los pacientes con epilepsia, como son entre otros el uso de investigaciones diagnósticas utilizadas de forma incorrecta, el diagnóstico erróneo de epilepsia y del tipo de epilepsia, el uso de FAE y de asociaciones no apropiadas y retrasos innecesarios en la aplicación de tratamientos no farmacológicos de la epilepsia, fundamentalmente de la cirugía.
La estratificación de las UCE, en función del grado de complejidad y de los estudios que se practiquen en ellas, va a permitir hacerlas eficientes y alcanzar el desarrollo necesario que permita ofertar sus recursos al paciente con ERF con la mayor eficacia y efectividad posible. Las diferentes UCE deben de estar en estrecho contacto y cooperar con protocolos consensuados entre ellas para evitar estudios y tratamientos innecesarios o reiterativos y además debe de existir un flujo de pacientes en ambas direcciones, cuando se precisen procedimientos más complejos o cuando éstos se concluyan. Aunque el número exacto de UCE en nuestro medio está por precisar, debe contarse con las suficientes para garantizar el acceso rápido y facilitado de todos los pacientes con epilepsia, refractaria a FAE o no, evitando demoras innecesarias y potencialmente peligrosas. Todos los profesionales que atienden pacientes con epilepsia deben contar con las UCE y utilizar sus recursos de forma rápida, adecuada y protocolizada para garantizar el control apropiado del paciente con epilepsia.