Sr. Editor:
Los inhibidores del factor de necrosis tumoral alfa (TNFα), y entre ellos el adalimumab, son fármacos utilizados como agentes inmunosupresores en varias enfermedades inflamatorias crónicas, incluida la artritis reumatoide (AR). Han demostrado que disminuyen significativamente la progresión de la lesión articular y aseguran un alivio prolongado de los síntomas de la AR1. Presentan una efectividad terapéutica superior y mayor supervivencia de los pacientes con respecto a los fármacos tradicionales. Además de la AR, su uso se ha extendido a otras enfermedades inflamatorias crónicas, como enfermedad de Crohn, espondilitis anquilosante, psoriasis y artritis psoriásica2.
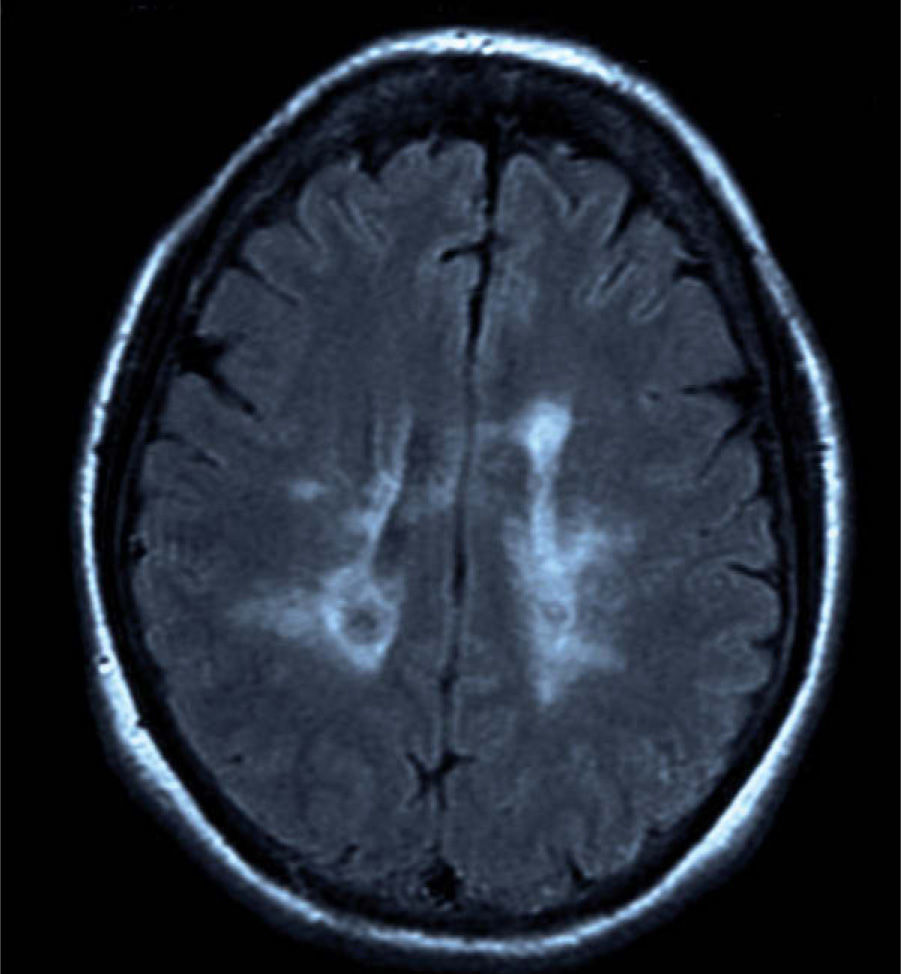
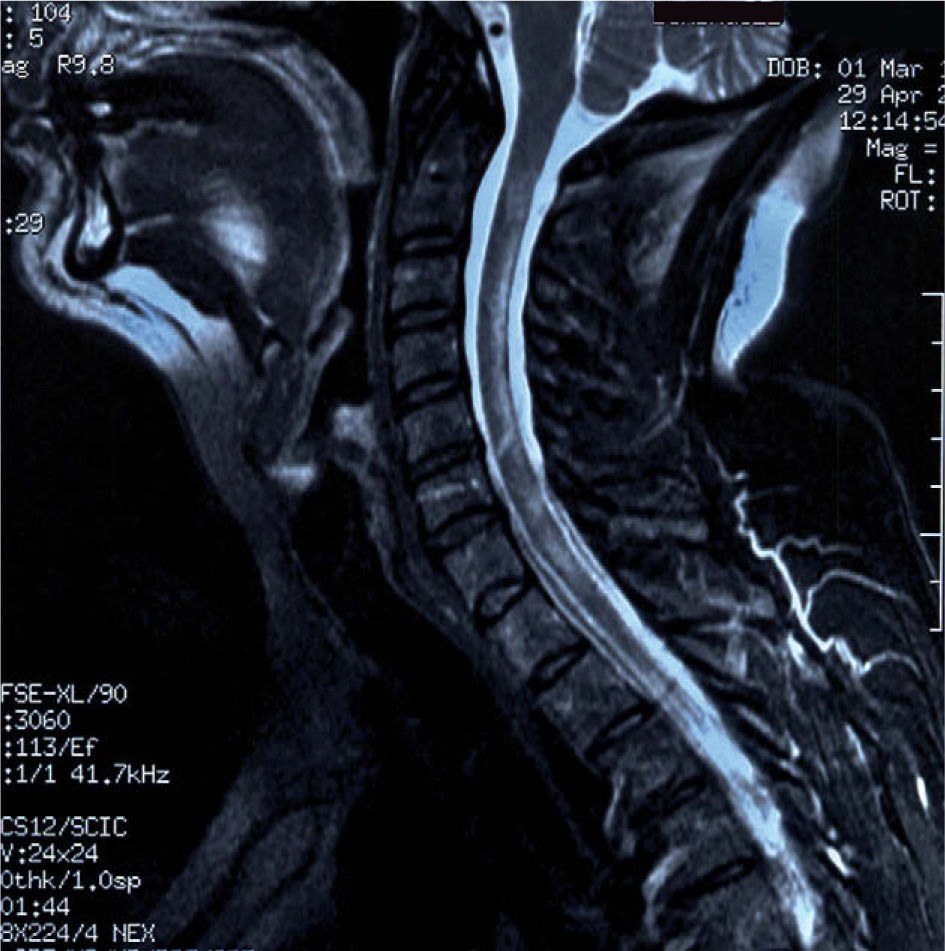
Se presenta el caso de una mujer de 55 años de edad, diagnosticada de AR en 1989, que presentó un cuadro de 2 meses de evolución de alteración de la marcha. La paciente seguía tratamiento con metotrexato oral y, en noviembre de 2008, se añadió adalimumab a una dosis de 40mg cada 2 semanas, por empeoramiento clínico. En la exploración, se objetivaba ataxia de la marcha con inestabilidad en los giros, imposibilidad para la realización de tándem y Romberg con caída multidireccional; el resto de la exploración era normal. Se realizó una resonancia magnética (RM) craneal que mostró lesiones desmielinizantes en la sustancia blanca periventricular, alguna de las cuales realzaban tras la administración de contraste (fig. 1). En la RM medular también se observaron lesiones de aspecto desmielinizantes a nivel cervical y dorsal con realce alguna de ellas tras el contraste (fig. 2). Se llevó a cabo estudio de LCR que fue normal, bandas oligoclonales negativas y determinación de PCR de virus JC negativos. Los ANA y los anticuerpos anti-ADN fueron negativos. Por último, el estudio de potenciales evocados visuales fue normal.
La paciente inició tratamiento con bolos de metilprednisolona intravenosa con lo que mejoró la sintomatología.
Adalimumab es un anticuerpo monoclonal humano anti-TNFα producido mediante tecnología ADN recombinante3. Se trata de la última generación de anticuerpos monoclonales. Es en general bien tolerado y las reacciones adversas son poco frecuentes. Así pues, pueden aumentar el número de infecciones, sobre todo del tracto respiratorio superior y urinario, que suelen ser leves. Otras reacciones adversas incluyen autoinmunidad (aparición de autoanticuerpos, antinucleares, anti-ADN o anticardiolipinas), enfermedad desmielinizante (de novo o, más común, reactivación de una preexistente), discrasias sanguíneas, empeoramiento de insuficiencia cardíaca e incremento en la aparición de linfomas2.
En 2001, Mohan et al4 describieron una serie de 20 pacientes que seguían tratamiento con anti-TNFα tipo infliximab o etanercept (aún no estaba aprobado el uso de adalimumab), que presentaron signos y síntomas neurológicos, la mayoría de ellos asociados a desmielinización del sistema nervioso central. Estos síntomas aparecieron entre una semana y 15 meses después del inicio de la terapia, con un promedio de 5 meses.
La forma clínica de presentación por esta desmielinización es variada: alteraciones sensitivas, neuritis óptica, debilidad, ataxia, mielitis transversa y alteración cognitiva5. La RM cerebral muestra lesiones hiperintensas en sustancia blanca en secuencias T2 y flair, algunas de las cuales pueden realzar con gadolinio si son recientes. También se puede encontrar hiperintensidad o realce con el contraste en el nervio óptico en caso de neuritis óptica y/o lesiones medulares captantes o no.
Los mecanismos por los que los inhibidores del TNFα inducen desmielinización no están claramente establecidos. La exposición prolongada al anti-TNFα podría incrementar la activación y la supervivencia de células T potencialmente autorreactivas periféricas, que serían susceptibles de penetrar el sistema nervioso central y causar desmielinización5.
Recientemente, se han descrito varios casos de desmielinización del sistema nervioso periférico inducidos por el tratamiento con anti-TNFα.
Así pues, estos fármacos podrían producir una reacción inmunitaria contra antígenos comunes de la mielina, tanto central como periférica5,7,8.
Los anti-TNFα han transformado el tratamiento de la AR. Sin embargo, complicaciones debidas a desmielinización del sistema nervioso central pueden asociarse a su uso. En la mayoría de los casos, la enfermedad neurológica mejora o desaparece cuando se retira el tratamiento con anti-TNFα5.
Los pacientes con AR en tratamiento con anti-TNFα se beneficiarían, por lo tanto, de un seguimiento que incluya RM cerebral, lo cual revelaría anormalidades tempranas incluso si el paciente se encuentra asintomático5,6.
Se debe suspender el uso de agentes anti-TNFα ante la aparición de eventos neurológicos y evitar su uso en pacientes con enfermedad desmielinizante diagnosticada, e incluso tener precaución en los que presentan historia familiar de esclerosis múltiple9.