La falta de cumplimiento terapéutico en la esclerosis múltiple puede asociarse a menor eficacia. En este estudio evaluamos el cumplimiento terapéutico, las razones para su incumplimiento, satisfacción con el tratamiento y calidad de vida (CdV) de pacientes en terapia de primera línea (terapias modificadoras de la enfermedad [TME]).
MétodosEstudio transversal, multicéntrico, de pacientes con EM que cursa a brotes. El cumplimiento en el último mes se evaluó mediante test de Morisky-Green, el cumplimiento estacional y las razones para el incumplimiento mediante cuestionario ad-hoc, y la satisfacción y CdV a través de los cuestionarios TSQM y PRIMUS.
ResultadosSe evaluaron 220 pacientes (un 91% remitentes-recidivantes); la media de edad fue 39,1 años, el 70% eran mujeres y el tiempo en tratamiento 5,4 años. El 23% estaba tratado con interferón (IFN) β-1b subcutáneo, el 21% con IFN β-1a intramuscular, el 37% con IFN β-1a subcutáneo y el 19% con acetato de glatirámero. El cumplimento global fue del 75%, sin diferencias significativas en función del TME, y no refirieron cambios estacionales el 81%. Los pacientes cumplidores presentaban significativamente menores valores de discapacidad y de tiempo de diagnóstico, y mayor satisfacción con el tratamiento y su efectividad. Las molestias y los síntomas seudogripales fueron las razones más frecuentes para el incumplimiento. La satisfacción y la CdV se relacionaron con una menor discapacidad y número de cambios terapéuticos.
ConclusionesEn pacientes con TME el grado de cumplimiento, satisfacción y CdV son altos, en especial para aquellos de diagnóstico reciente, menos discapacitados y con menos cambios terapéuticos. Las molestias y síntomas seudogripales asociados a las terapias inyectadas influyen en el cumplimiento.
Non-adherence to disease-modifying therapies (DMTs) in multiple sclerosis may be associated with reduced efficacy. We assessed compliance, the reasons for non-compliance, treatment satisfaction, and quality of life (QoL) of patients treated with first-line therapies.
MethodsA cross-sectional, multicenter study was conducted that included relapsing multiple sclerosis patients. Compliance in the past month was assessed using Morisky-Green test. Seasonal compliance and reasons for non-compliance were assessed by an ad-hoc questionnaire. Treatment satisfaction and QoL were evaluated by means of TSQM and PRIMUS questionnaires.
ResultsA total of 220 patients were evaluated (91% relapsing-remitting); the mean age was 39.1 years, 70% were female, and the average time under treatment was 5.4 years. Subcutaneous interferon (IFN) β-1b was used in 23% of the patients, intramuscular IFN β-1a in 21%, subcutaneous IFN β-1a in 37%, and with glatiramer acetate in 19%. The overall compliance was 75%, with no significant differences related to the therapy, and 81% did not report any seasonal variation. Compliant patients had significantly lower disability scores and time of diagnosis, and greater satisfaction with treatment and its effectiveness. Discomfort and flu-like symptoms were the most frequent reasons for non-compliance. The satisfaction and QoL were associated with less disability and number of therapeutic switches.
ConclusionsThe rate of compliance, satisfaction and QoL in multiple sclerosis patients under DMTs is high, especially for those newly diagnosed, less disabled, and with fewer therapeutic switches. Discomfort and flu-like symptoms associated with injected therapies significantly affect adherence.
La esclerosis múltiple (EM) es la causa más frecuente de discapacidad neurológica no traumática en adultos jóvenes1. La mayoría de los pacientes (80%) presentan un curso que evoluciona a brotes, autolimitados, EM remitente-recidivante (EMRR), que a medida que se repiten van ocasionando un déficit residual funcional. Con el tiempo, aproximadamente el 50% de estos pacientes pasará a presentar un curso secundariamente progresivo de aumento de la discapacidad no relacionado con los brotes (esclerosis múltiple secundaria progresiva [EMSP]) aunque también puede acompañarse de brotes esporádicos2.
El tratamiento actual de primera línea para la EMRR y la EMSP consiste en terapias modificadoras de la enfermedad (TME), pues reducen la tasa de brotes y enlentecen la progresión de la discapacidad, e incluyen el interferón (IFN) β-1a, IFN β-1b, y acetato de glatirámero, administrados bien por vía subcutánea (sc) bien intramuscular (im)3. La adherencia a un tratamiento, definida por la Organización Mundial de la Salud como el cumplimiento (tomar la medicación de acuerdo con la pauta prescrita en cuanto a dosis y frecuencia) y su persistencia (desde el inicio hasta la discontinuación de la terapia indicada), parece ser un factor contribuyente a la falta de eficacia en enfermedades crónicas4. Aunque varios estudios han mostrado la importancia de la adherencia a estos tratamientos para controlar tanto la frecuencia de los brotes como la progresión de la EM5–8, el porcentaje de adherencia descrito oscila entre el 41 y el 88%9. Las causas más importantes de no adherencia al tratamiento incluyen la percepción de falta de eficacia por parte del paciente, y los efectos adversos (EA)10.
La disminución en la calidad de vida (CdV), fruto de las alteraciones físicas, psicológicas y sociales derivadas de la EM, también se relaciona con la motivación para seguir el tratamiento con TME11,12 y es un factor pronóstico para el curso de la enfermedad13,14. En estudios en otras patologías crónicas se ha observado que tanto la CdV como el cumplimiento están directamente relacionados con la satisfacción con el tratamiento15–17.
El objetivo principal del presente estudio fue evaluar el grado de cumplimiento terapéutico de los pacientes con EM que cursa con brotes en tratamiento con TME de primera línea. Los objetivos secundarios incluyeron investigar las razones de no cumplimiento, describir el cumplimiento estacional, determinar el grado de satisfacción con el tratamiento y conocer la CdV en estos pacientes. Asimismo, se pretendió determinar la relación entre el cumplimiento y la satisfacción con el tratamiento, y conocer si existe una relación entre el cumplimiento, la satisfacción o la CdV y diferentes variables demográficas y clínicas.
Pacientes y métodosSe incluyeron de forma consecutiva pacientes adultos (≥18 años) con diagnóstico de EMRR o EMSP que cursara con brotes según los criterios de McDonald18, en tratamiento con TME durante al menos 6 meses, y que acudieron a las consultas de neurología para una visita rutinaria. Se excluyeron los pacientes que presentaban otros tipos de EM, cambios o retiradas de TME en las 4 semanas anteriores, y/o tratamiento con natalizumab u otros inmunosupresores, aquellos incluidos en otro ensayo clínico (en el momento de la visita o en los últimos 6 meses), o que no eran aptos para el estudio según opinión del investigador.
Diseño del estudioEstudio epidemiológico, observacional, transversal y multicéntrico. En la visita de inclusión, y tras obtener el consentimiento informado, se determinaron la variable principal y las secundarias mediante revisión de la historia clínica, entrevista con el paciente y contestación de cuestionarios.
Variable principalEl cumplimiento terapéutico en el mes previo se evaluó mediante el test de Morisky-Green adaptado y validado en población española19, que valoró las actitudes del paciente frente al tratamiento durante el mes anterior. El paciente se clasificó como cumplidor si respondía de forma correcta a las 4 preguntas: ¿Ha olvidado administrarse la medicación para la EM en alguna ocasión?; ¿Se ha administrado la medicación en la hora y día indicados?; Cuando se ha encontrado bien ¿ha dejado de administrarse la medicación?; Si alguna vez le ha sentado mal la medicación ¿ha dejado de administrarse dicha medicación?
Variables secundariasSe obtuvieron los datos demográficos de los pacientes, así como variables clínicas históricas y actuales. El cumplimiento estacional y las razones para el incumplimiento se investigaron mediante cuestionario ad-hoc. La satisfacción de los pacientes con varios aspectos del tratamiento (efectividad, seguridad, comodidad y satisfacción global) en las 2-3 semanas anteriores se determinó mediante la versión española del Treatment Satisfaction Questionnaire for Medication (TSQM)20, en el que la puntuación de cada dominio oscila de 0 a 100 (grado de satisfacción más bajo/alto). La CdV de los pacientes en el momento de la visita se determinó mediante el cuestionario Patient-Reported Indices for Multiple Sclerosis (PRIMUS)21,22. Este consta de 2 escalas (actividades de la vida diaria y CdV) cuya puntuación oscila entre 0-30 y 0-22 puntos, respectivamente, con puntuaciones mayores indicando mayor limitación de la actividad y mayor CdV, respectivamente. Adicionalmente, los pacientes situaron su estado de ánimo en el momento de la visita en una escala visual analógica de 0 a 100 («peor/mejor estado de ánimo imaginable»).
Análisis estadísticoSe analizaron aquellos pacientes que cumplieron los criterios de selección y que disponían de datos válidos para la variable principal (test de Morisky-Green). No se emplearon técnicas de sustitución de datos ausentes. Todos los análisis estadísticos se realizaron mediante el paquete SAS® para Windows versión 9.2. Las variables cualitativas o cuantitativas discretas se resumieron mediante frecuencias absolutas y relativas; las cuantitativas continuas se describieron mediante medidas de tendencia central y dispersión. Se realizaron pruebas de contraste de hipótesis (Chi cuadrado, T de Student o test exacto de Fisher, según procediera) para determinar la relación entre: (a) el cumplimiento, (b) las razones para no cumplimiento, (c) la satisfacción con el tratamiento y (d) la calidad de vida, con una selección de variables demográficas y clínicas. También se utilizó el test T de Student para determinar la relación entre el cumplimiento y la satisfacción de los pacientes con el tratamiento. Para todas las pruebas se adoptó un nivel de significación estadística de 0,05 bilateral.
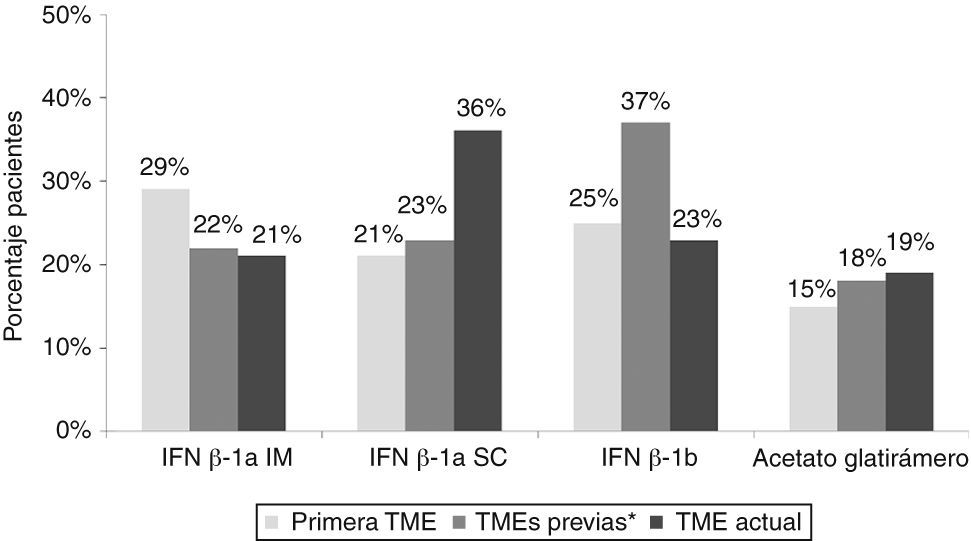
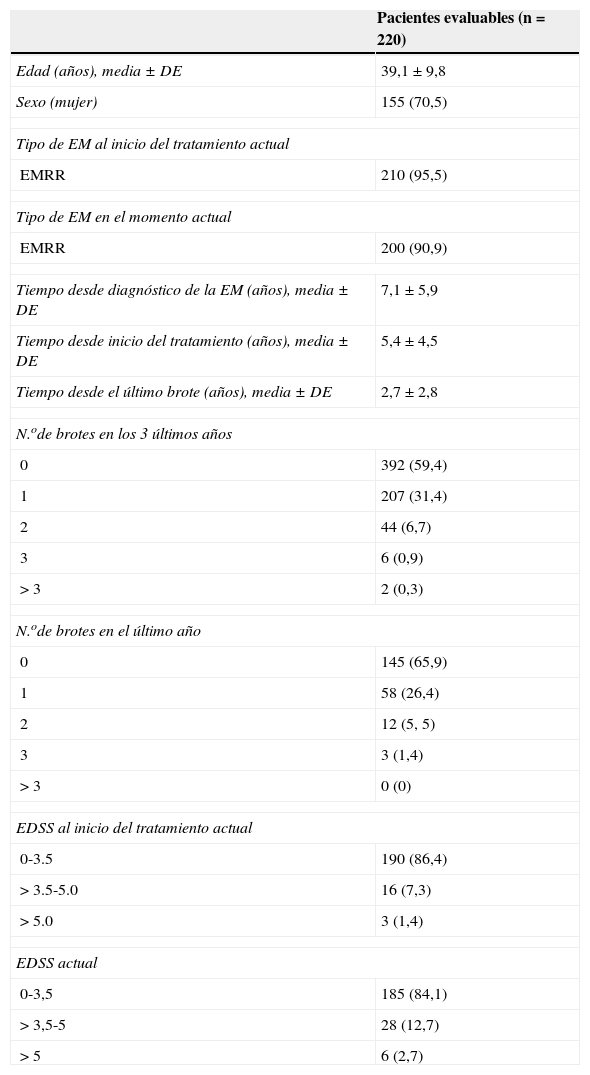
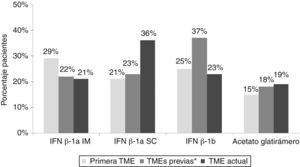
ResultadosCaracterísticas basales y tratamientoSe incluyeron 259 pacientes de 32 centros distribuidos por toda la geografía española, de los que 220 fueron finalmente evaluables. Sus características demográficas y clínicas se resumen en la tabla 1. La figura 1 muestra las características del tratamiento. El 60% inició su tratamiento con interferón (IFN) β-1a y el 40% cambió de fármaco durante la media (±desviación estándar [DE]) de 5,4±4,5 años de tratamiento, siendo lo más habitual la sustitución de un IFN por otro. La causa de sustitución más frecuente fue la ineficacia a juicio del neurólogo. En el momento del estudio, el 57% de los pacientes estaba recibiendo IFN β-1a, y la media de tiempo en tratamiento con la TME actual se situó entre 1,2±0,5 y 5,0±4,1 años, dependiendo del fármaco.
Características demográficas y clínicas de los pacientes
| Pacientes evaluables (n=220) | |
|---|---|
| Edad (años), media±DE | 39,1±9,8 |
| Sexo (mujer) | 155 (70,5) |
| Tipo de EM al inicio del tratamiento actual | |
| EMRR | 210 (95,5) |
| Tipo de EM en el momento actual | |
| EMRR | 200 (90,9) |
| Tiempo desde diagnóstico de la EM (años), media±DE | 7,1±5,9 |
| Tiempo desde inicio del tratamiento (años), media±DE | 5,4±4,5 |
| Tiempo desde el último brote (años), media±DE | 2,7±2,8 |
| N.ode brotes en los 3 últimos años | |
| 0 | 392 (59,4) |
| 1 | 207 (31,4) |
| 2 | 44 (6,7) |
| 3 | 6 (0,9) |
| >3 | 2 (0,3) |
| N.ode brotes en el último año | |
| 0 | 145 (65,9) |
| 1 | 58 (26,4) |
| 2 | 12 (5, 5) |
| 3 | 3 (1,4) |
| >3 | 0 (0) |
| EDSS al inicio del tratamiento actual | |
| 0-3.5 | 190 (86,4) |
| >3.5-5.0 | 16 (7,3) |
| >5.0 | 3 (1,4) |
| EDSS actual | |
| 0-3,5 | 185 (84,1) |
| >3,5-5 | 28 (12,7) |
| >5 | 6 (2,7) |
Todas las variables resumidas como n (%), excepto si se indica lo contrario.
DE: desviación estándar; EDSS: Expanded Disability Status Scale; EM: esclerosis múltiple; EMRR: esclerosis múltiple remitente-recidivante.
Características del tratamiento farmacológico con TME de primera línea en los pacientes evaluables. IFN: interferón; im: intramuscular; sc: subcutáneo; TME: terapias modificadoras de la enfermedad. aCada paciente podía haber utilizado previamente más de un tratamiento farmacológico.
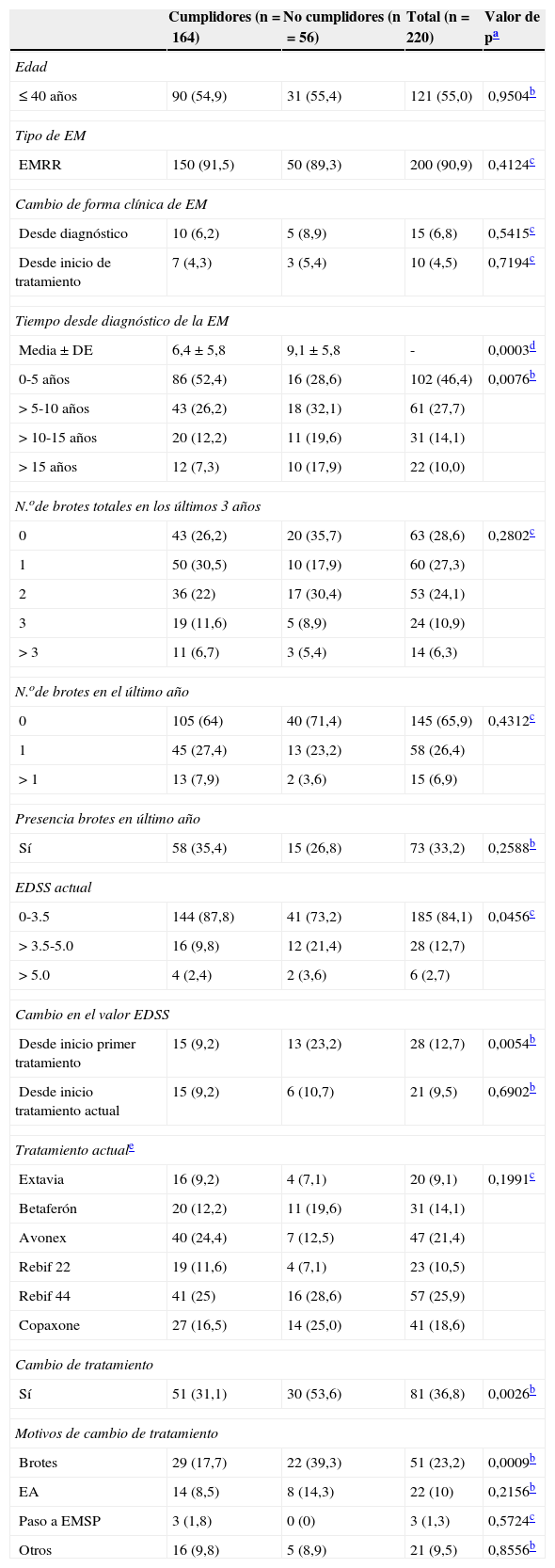
El 75% de los pacientes fue cumplidor. El grupo con buen cumplimiento presentó una mayor proporción de pacientes con diagnostico reciente (<5 años) y con baja discapacidad (Expanded Disability Status Scale [EDSS]23, 0-3.5). Este grupo también presentó una menor proporción de pacientes con progresión de la discapacidad desde el inicio de la TME, con menor número de cambios de tratamiento, y entre estos últimos, con cambios debidos a la aparición de brotes (tabla 2).
Características clínicas y terapéuticas para el total de pacientes evaluables y para los subgrupos de pacientes cumplidores y no cumplidores
| Cumplidores (n=164) | No cumplidores (n=56) | Total (n=220) | Valor de pa | |
|---|---|---|---|---|
| Edad | ||||
| ≤40 años | 90 (54,9) | 31 (55,4) | 121 (55,0) | 0,9504b |
| Tipo de EM | ||||
| EMRR | 150 (91,5) | 50 (89,3) | 200 (90,9) | 0,4124c |
| Cambio de forma clínica de EM | ||||
| Desde diagnóstico | 10 (6,2) | 5 (8,9) | 15 (6,8) | 0,5415c |
| Desde inicio de tratamiento | 7 (4,3) | 3 (5,4) | 10 (4,5) | 0,7194c |
| Tiempo desde diagnóstico de la EM | ||||
| Media±DE | 6,4±5,8 | 9,1±5,8 | - | 0,0003d |
| 0-5 años | 86 (52,4) | 16 (28,6) | 102 (46,4) | 0,0076b |
| >5-10 años | 43 (26,2) | 18 (32,1) | 61 (27,7) | |
| >10-15 años | 20 (12,2) | 11 (19,6) | 31 (14,1) | |
| >15 años | 12 (7,3) | 10 (17,9) | 22 (10,0) | |
| N.ode brotes totales en los últimos 3 años | ||||
| 0 | 43 (26,2) | 20 (35,7) | 63 (28,6) | 0,2802c |
| 1 | 50 (30,5) | 10 (17,9) | 60 (27,3) | |
| 2 | 36 (22) | 17 (30,4) | 53 (24,1) | |
| 3 | 19 (11,6) | 5 (8,9) | 24 (10,9) | |
| >3 | 11 (6,7) | 3 (5,4) | 14 (6,3) | |
| N.ode brotes en el último año | ||||
| 0 | 105 (64) | 40 (71,4) | 145 (65,9) | 0,4312c |
| 1 | 45 (27,4) | 13 (23,2) | 58 (26,4) | |
| >1 | 13 (7,9) | 2 (3,6) | 15 (6,9) | |
| Presencia brotes en último año | ||||
| Sí | 58 (35,4) | 15 (26,8) | 73 (33,2) | 0,2588b |
| EDSS actual | ||||
| 0-3.5 | 144 (87,8) | 41 (73,2) | 185 (84,1) | 0,0456c |
| >3.5-5.0 | 16 (9,8) | 12 (21,4) | 28 (12,7) | |
| >5.0 | 4 (2,4) | 2 (3,6) | 6 (2,7) | |
| Cambio en el valor EDSS | ||||
| Desde inicio primer tratamiento | 15 (9,2) | 13 (23,2) | 28 (12,7) | 0,0054b |
| Desde inicio tratamiento actual | 15 (9,2) | 6 (10,7) | 21 (9,5) | 0,6902b |
| Tratamiento actuale | ||||
| Extavia | 16 (9,2) | 4 (7,1) | 20 (9,1) | 0,1991c |
| Betaferón | 20 (12,2) | 11 (19,6) | 31 (14,1) | |
| Avonex | 40 (24,4) | 7 (12,5) | 47 (21,4) | |
| Rebif 22 | 19 (11,6) | 4 (7,1) | 23 (10,5) | |
| Rebif 44 | 41 (25) | 16 (28,6) | 57 (25,9) | |
| Copaxone | 27 (16,5) | 14 (25,0) | 41 (18,6) | |
| Cambio de tratamiento | ||||
| Sí | 51 (31,1) | 30 (53,6) | 81 (36,8) | 0,0026b |
| Motivos de cambio de tratamiento | ||||
| Brotes | 29 (17,7) | 22 (39,3) | 51 (23,2) | 0,0009b |
| EA | 14 (8,5) | 8 (14,3) | 22 (10) | 0,2156b |
| Paso a EMSP | 3 (1,8) | 0 (0) | 3 (1,3) | 0,5724c |
| Otros | 16 (9,8) | 5 (8,9) | 21 (9,5) | 0,8556b |
DE: desviación estándar; EA: efectos adversos; EDSS: Expanded Disability Status Scale; EM: esclerosis múltiple; EMRR: esclerosis múltiple remitente-recidivante; EMSP: esclerosis múltiple secundaria progresiva.
Todas las variables resumidas como n (%), excepto si se indica lo contrario.
El 68% de los pacientes no refirió variaciones a lo largo del tiempo en sus pautas de administración, y el 81% declaró que la época del año no afectaba a su cumplimiento. No obstante, los pacientes con más brotes en el último año tendieron a cumplir con su tratamiento de forma diferente según la época del año; la calificada como más dificultosa fue el verano, aunque las vacaciones solo supusieron un impedimento ocasional. El número de sustituciones del tratamiento también se relacionó con más variaciones en la pauta de administración de los pacientes a lo largo del tiempo, con impedimentos para el cumplimiento en vacaciones y con el uso de sistemas para recordar la medicación.
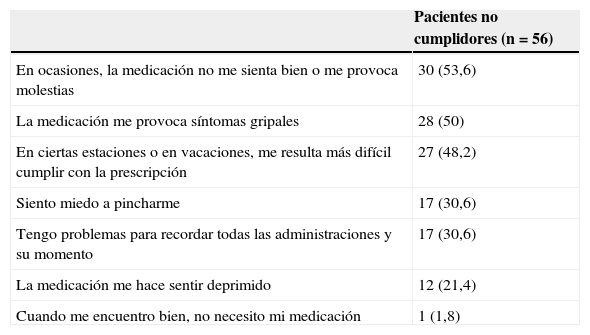
Las razones más frecuentes para el incumplimiento fueron las molestias ocasionadas por la medicación y los síntomas seudogripales, así como la dificultad para el cumplimiento en ciertos periodos del año (tabla 3). Ninguna de las causas argumentadas se relacionó de forma significativa con características clínicas de los pacientes. El 70% de los pacientes refirió que recibía algún grado de apoyo familiar para recordar las pautas de administración, mientras que el 75% manifestó carecer de sistemas que le recuerden la medicación.
Razones argumentadas para el incumplimiento terapéutico
| Pacientes no cumplidores (n=56) | |
|---|---|
| En ocasiones, la medicación no me sienta bien o me provoca molestias | 30 (53,6) |
| La medicación me provoca síntomas gripales | 28 (50) |
| En ciertas estaciones o en vacaciones, me resulta más difícil cumplir con la prescripción | 27 (48,2) |
| Siento miedo a pincharme | 17 (30,6) |
| Tengo problemas para recordar todas las administraciones y su momento | 17 (30,6) |
| La medicación me hace sentir deprimido | 12 (21,4) |
| Cuando me encuentro bien, no necesito mi medicación | 1 (1,8) |
Todas las respuestas resumidas como n (%). Cada paciente podía indicar más de un motivo de incumplimiento.
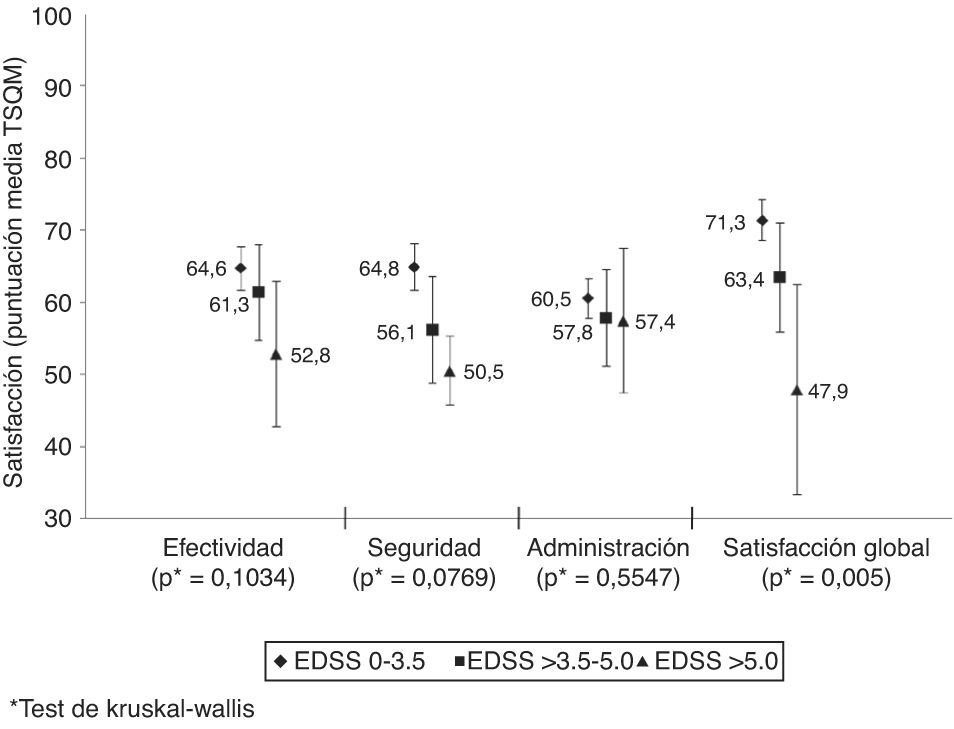
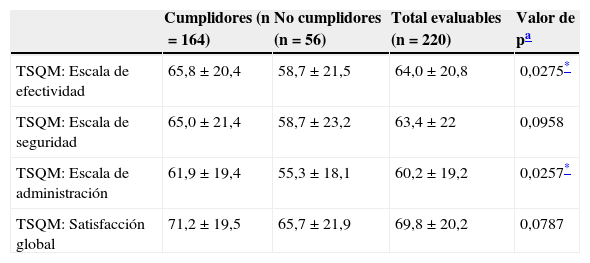
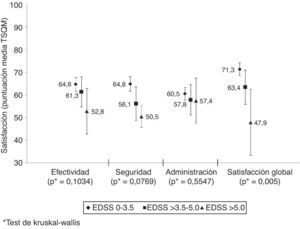
En el total de pacientes, la satisfacción global con el tratamiento se evaluó con una media de 70±20 puntos. Los pacientes cumplidores mostraron una puntuación media superior a los no cumplidores en todos los dominios del TSQM, aunque la diferencia fue significativa solo para la efectividad y comodidad del tratamiento (tabla 4). La satisfacción global se relacionó de forma inversa con el grado de discapacidad (fig. 2), mientras que la satisfacción relativa a la efectividad del tratamiento se relacionó, también de forma inversa, con el número de cambios en el tratamiento (media de 66,6±19,9 puntos en pacientes con un cambio; 61,3±20,8 con 2 cambios; 58,8±21,9 con 3 cambios; y 48,1 (DE no calculada) con 4 cambios; p=0,0324).
Satisfacción con las TME de primera línea para el total de pacientes evaluables y para los subgrupos de pacientes cumplidores y no cumplidores
| Cumplidores (n=164) | No cumplidores (n=56) | Total evaluables (n=220) | Valor de pa | |
|---|---|---|---|---|
| TSQM: Escala de efectividad | 65,8±20,4 | 58,7±21,5 | 64,0±20,8 | 0,0275* |
| TSQM: Escala de seguridad | 65,0±21,4 | 58,7±23,2 | 63,4±22 | 0,0958 |
| TSQM: Escala de administración | 61,9±19,4 | 55,3±18,1 | 60,2±19,2 | 0,0257* |
| TSQM: Satisfacción global | 71,2±19,5 | 65,7±21,9 | 69,8±20,2 | 0,0787 |
DE: desviación estándar; TME: terapias modificadoras de la enfermedad; TSQM: Treatment Satisfaction Questionnaire for Medication.
Todas las escalas informadas como puntuación media±DE.
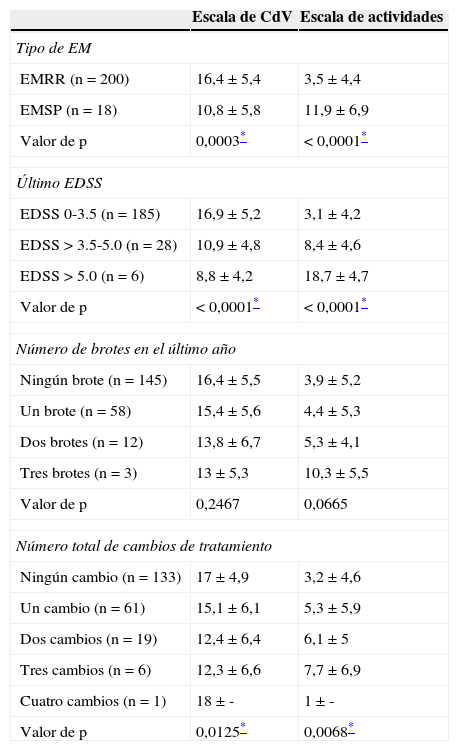
Para el total de pacientes evaluados, la puntuación media del PRIMUS en las escalas de actividades de la vida diaria y de CdV fue de 4,1±5,2 y 16±5,6 respectivamente. Los pacientes con EMRR (respecto a EMSP), con menor discapacidad, y aquellos con un número menor de cambios de TME, mostraron menor limitación en las actividades diarias y mayor calidad de vida (tabla 5). El estado de ánimo fue evaluado mediante la escala visual analógica con un valor medio de 68,7 (19,1).
Resultados del cuestionario PRIMUS según características clínicas y/o terapéuticas
| Escala de CdV | Escala de actividades | |
|---|---|---|
| Tipo de EM | ||
| EMRR (n=200) | 16,4±5,4 | 3,5±4,4 |
| EMSP (n=18) | 10,8±5,8 | 11,9±6,9 |
| Valor de p | 0,0003* | <0,0001* |
| Último EDSS | ||
| EDSS0-3.5 (n=185) | 16,9±5,2 | 3,1±4,2 |
| EDSS >3.5-5.0 (n=28) | 10,9±4,8 | 8,4±4,6 |
| EDSS>5.0 (n=6) | 8,8±4,2 | 18,7±4,7 |
| Valor de p | <0,0001* | <0,0001* |
| Número de brotes en el último año | ||
| Ningún brote (n=145) | 16,4±5,5 | 3,9±5,2 |
| Un brote (n=58) | 15,4±5,6 | 4,4±5,3 |
| Dos brotes (n=12) | 13,8±6,7 | 5,3±4,1 |
| Tres brotes (n=3) | 13±5,3 | 10,3±5,5 |
| Valor de p | 0,2467 | 0,0665 |
| Número total de cambios de tratamiento | ||
| Ningún cambio (n=133) | 17±4,9 | 3,2±4,6 |
| Un cambio (n=61) | 15,1±6,1 | 5,3±5,9 |
| Dos cambios (n=19) | 12,4±6,4 | 6,1±5 |
| Tres cambios (n=6) | 12,3±6,6 | 7,7±6,9 |
| Cuatro cambios (n=1) | 18±- | 1±- |
| Valor de p | 0,0125* | 0,0068* |
«n» indica el número de pacientes que respondieron al cuestionario PRIMUS en cada una de las categorías clínicas; todos los ítems informados como puntuación media±DE.
CdV: calidad de vida; DE: desviación estándar; EDSS: Expanded Disability Status Scale; EM: esclerosis múltiple; EMRR: esclerosis múltiple remitente-recidivante; EMSP: esclerosis múltiple secundaria progresiva; PRIMUS: Patient-Reported Indices for Multiple Sclerosis.
En nuestro entorno, el porcentaje de cumplimiento con las TME de primera línea en los pacientes con EM oscila entre el 62 y el 87%24–28. Las diferencias en el diseño, las TME evaluadas, los métodos elegidos para valorar el cumplimiento y la definición de cumplimiento empleada en estos estudios dificultan las comparaciones. No obstante, en un estudio retrospectivo español que utilizó una metodología similar al nuestro (test de Morisky-Green), el cumplimiento fue del 68%27. A la luz de estas cifras, el cumplimiento del 75% observado en el presente estudio se podría considerar alto, aunque también revela un amplio margen de mejora.
El cumplimiento terapéutico se asoció con EM de diagnóstico reciente, menor grado y progresión de discapacidad, y el mantenimiento del tratamiento inicial. Por el contrario, el incumplimiento mostró una relación directa y especialmente significativa con el cambio de la TME por ineficacia (aparición de brotes). Aunque estudios realizados hasta la fecha han descrito la relación entre el cumplimiento y las variables clínicas mencionadas27–31, también se han obtenido resultados contrarios, como por ejemplo un mayor cumplimiento en la EM de evolución más larga32, o al cambiar de TME28,33. También se ha relacionado el cumplimiento con el tipo de EM26,30 y con la edad de los pacientes27, lo cual no se observó en el presente estudio. La direccionalidad de estas relaciones no está clara, y su heterogeneidad entre estudios sugiere que el cumplimiento depende también de otros factores. Por ejemplo, se sabe que la autoadministración del tratamiento, el apoyo por parte de los profesionales sanitarios, o los sistemas para recordar la medicación aumentan el cumplimiento30,34,35.
El principal motivo argumentado por los pacientes para el incumplimiento fueron las molestias ocasionadas por la medicación y los síntomas seudogripales. Esto concuerda con los resultados de una revisión sistemática sobre la tolerabilidad de las TME, en la que los EA fueron la razón más frecuente de discontinuación del tratamiento con IFN β-1a sc e IFN β-1b, y la segunda más frecuente con IFN β-1a im y acetato de glatirámero. Los síntomas seudogripales fueron el EA más frecuente durante el tratamiento con IFN β-1a im e IFN β-1b, y el segundo más frecuente con IFN β-1a sc36. Los pacientes de nuestro estudio llevaban como media más de 5 años en tratamiento con TME y más de un año en tratamiento con la terapia actual, lo cual contrasta con la observación de O’Rourke y Hutchinson de que el incumplimiento debido a los EA ocurre principalmente en los primeros meses de tratamiento37. No obstante, en el mismo estudio se vio que en fases más prolongadas del tratamiento el incumplimiento pasa a relacionarse con la ineficacia del mismo, y nuestros datos mostraron una relación directa y consistente entre el incumplimiento y los cambios en relación con brotes en el año anterior. En cualquier caso, en el presente estudio no observamos diferencias significativas en cuanto al cumplimento en función del tipo de TME.
La estacionalidad también fue un impedimento importante entre los pacientes incumplidores y, aunque no de forma significativa, más relacionada con los meses de verano. Las vacaciones no fueron un impedimento especialmente frecuente, por lo que las causas podrían ser otras. Se sabe que los meses más cálidos del año se relacionan con un aumento de brotes en los pacientes con EM38, y en nuestro estudio, se observó una relación entre la presencia de brotes y pautas de administración menos estables. En contraste con otras series de pacientes27,31,39, los olvidos fueron relativamente poco frecuentes entre los pacientes incumplidores. En relación con esto, Arroyo et al. encontraron que los olvidos dejaban de ser la razón mayoritaria para el incumplimiento durante las primeras fases del tratamiento, siendo pronto sustituidos por factores relacionados con la administración24. En nuestro estudio, algunos de estos factores (incluyendo miedo a las inyecciones y percepción de no necesitarlas) fueron referidos por el 32,4% de los pacientes incumplidores. Por otra parte, pocos de los pacientes incluidos en el presente estudio usaban sistemas de recuerdo de dosis, por lo que el bajo porcentaje de olvidos podría deberse en su mayor parte al apoyo familiar.
La satisfacción con las TME, especialmente en términos de comodidad y efectividad, fue mayor en los pacientes cumplidores, tal como se ha observado en estudios previos39,40. No obstante, como en el caso de las variables clínicas asociadas al cumplimiento, la dirección de esta relación no es clara, y el diseño observacional del estudio no permitió determinarla. La EM comporta un tratamiento crónico con inyecciones de frecuencia de diaria a semanal dependiendo del tratamiento, cuyos beneficios pueden ser modestos en relación con las expectativas del paciente y no apreciables a corto plazo. Por tanto, es más probable que los pacientes que perciben su tratamiento como cómodo y albergan expectativas realistas sobre su efectividad presenten un cumplimiento mayor41. A la inversa, los pacientes con buen cumplimiento tienen un menor número de brotes28, lo que implicaría mejor estado de salud y mayor satisfacción con el tratamiento. Como muestra, en nuestro estudio, los pacientes con menor discapacidad presentaron también mayor satisfacción global con el tratamiento. La disminución de la satisfacción relacionada con la efectividad, observada al aumentar el número de cambios en el tratamiento, podría deberse a que los cambios fueron principalmente por ineficacia del fármaco. Por otro lado, la mayoría consistieron en sustituir un IFN por otro, aunque se ha observado que la satisfacción con el tratamiento no mejora con cambios entre fármacos similares, probablemente porque estos cambios no aportan una efectividad adicional. Sí aumentarían la satisfacción con el tratamiento aquellos cambios que implican nuevas estrategias o vías terapéuticas42.
Los pacientes de este estudio mostraron poca limitación en las actividades de la vida diaria y una CdV considerable, especialmente aquellos con EMRR, menos discapacitados y con menos cambios en el tratamiento. En un estudio anterior en población con EM evaluada mediante el PRIMUS, también se observó esta relación entre menor discapacidad y mejor CdV y/o menor limitación en las actividades, mientras que la EMRR se correlacionó únicamente con una mejor CdV43. De nuevo, la relación entre el número de cambios en el tratamiento y la CdV podría deberse a la relación entre estos cambios y la ineficacia del tratamiento.
Este estudio presenta las limitaciones propias de los estudios observacionales. Por otra parte, el test de Morisky-Green utilizado para evaluar el cumplimiento, aunque restrictivo, tiene el inconveniente de ser una medida indirecta que en ocasiones puede sobrestimar el cumplimiento27. Finalmente, la falta de asociación entre el cumplimiento y ciertas variables clínicas podría deberse a que el número de pacientes incluidos en algunas de las categorías clínicas fue escaso, afectando a la potencia estadística.
En resumen, el cumplimiento con las TME de primera línea fue alto en nuestra población de pacientes, y aparentemente se ve poco afectado por la estacionalidad. No obstante, la proporción de pacientes no cumplidores, especialmente debido a los EA asociados a la terapia inyectada, indica un posible punto de mejora. Sin embargo, que el incumplimiento se relacionara con el tiempo de evolución de la EM, la progresión y grado de la discapacidad, y con el número de cambios en el tratamiento, nos indica que también tiene que ver con la eficacia limitada de la TME actual. Así, aunque el grado de satisfacción con el tratamiento y la CdV fueron altos, ambas estuvieron relacionadas con la discapacidad y el número de cambios en el tratamiento.
FinanciaciónEl estudio COMPLIANCE ha recibido financiación privada con fines de investigación de Novartis Farmacéutica S.A.
Conflicto de interesesAlbert Saiz ha recibido honorarios como asesor y ponente promovidos por Bayer-Schering, Merck-Serono, Biogen-Idec, Sanofi-Aventis, Teva Pharmaceutical Industries Ltd y Novartis. Sheila Mora y Julia Blanco son trabajadores de Novartis Farmacéutica, S.A.
Agradecemos la colaboración en la elaboración del presente manuscrito de Beatriz del Val y Emili González-Pérez del Departamento Científico de TFS Develop, España.
María Eugenia Marzo (H. San Pedro), Francisco Lacruz (H. de Navarra), Joaquín Peña (H. San Agustín), Dionisio Fernández (H. Cabueñes), Agustín Oterino (H. Marqués de Valdecilla), Miguel Ángel Lláneza (H. Arquitecto Marcide), Robustiano Pego (S. Nosa Sra. dos Ollos Grandes), María Ángeles del Real (H.G. de Ciudad Real), Ricardo Ginestal (F. Jiménez Díaz), Luis Ignacio Casanova (H.C. San Carlos), Lluïsa Rubio (H.U. Príncipe de Asturias), Antonio Escartín (H. Sant Pau), Joan Massons (H. Sagrat Cor), Yolanda Blanco (H. Clínic), Francisco Barrero (H.U. San Cecilio), Jesús Foronda (H. de Jaén), Esther Dionisia Cancho (C.E. Don Benito), Ricardo Fernández (H. de Valme), Francisco Javier Carod (H. Virgen de la Luz), María Rosa García (H. Virgen de la Salud), José Manuel Flores (H. Virgen de Altagracia), Ramón Villaverde (H. Morales Meseguer), José Manuel López (H. Virgen de los Lirios), José Meca (C. Virgen de la Vega), Virginia María Araña (H.U. Doctor Negrín), Cristina Croissier (H.U. de Canarias), Virginia Meca (H. La Princesa), Jesús Cacho (H.U. de Salamanca), Wadih Bowakim (H. Río Hortega), Ambrosio Miralles (H. Infanta Sofía), José Francisco Plaza (H. del Sureste), Beatriz Romero (H. Son Llatzer).