El curso natural de la enfermedad pulmonar obstructiva crónica incluye habitualmente exacerbaciones. Los pacientes con enfermedad pulmonar obstructiva crónica sufren de 1-4 exacerbaciones al año de media. Estas se asocian a un empeoramiento de la calidad de vida y a un aumento de la mortalidad. Disminuir y controlar el número de exacerbaciones es uno de los objetivos principales del tratamiento de la enfermedad pulmonar obstructiva crónica. Entre los tratamientos actuales, tiotropio es el principio activo que dispone de la evidencia más sólida en la reducción de exacerbaciones moderadas/graves, acompañado de un buen perfil de seguridad y tolerabilidad. La suma de olodaterol a tiotropio ofrece una doble broncodilatación bien tolerada y eficaz en la mejora de la función pulmonar, calidad de vida y disminución de la disnea en comparación con sus monocomponentes, y reduce un 7% la tasa anual de exacerbaciones moderadas/graves vs. tiotropio, no alcanzando el nivel de significación estadística preespecificado de p<0,01.
The natural course of chronic obstructive pulmonary disease usually includes exacerbations. chronic obstructive pulmonary disease patients suffer from 1-4 exacerbations per year on average. These are associated with worsening quality of life and increased mortality. Reducing and controlling the number of exacerbations is one of the main goals of chronic obstructive pulmonary disease treatment. Among current treatments, tiotropium is the active substance with the strongest evidence in the reduction of moderate/severe exacerbations, together with a good safety and tolerability profile. The addition of olodaterol to tiotropium offers well-tolerated and effective double bronchodilation for improving lung function, quality of life, and decreased dyspnoea compared to its single components. This also reduces the annual rate of moderate/severe exacerbations vs. tiotropium by 7%, although not reaching the pre-specified statistical significance level of P<.01.
Las exacerbaciones de la enfermedad pulmonar obstructiva crónica (EPOC) suponen un importante problema de salud pública1. En España, se estima que generan el 10-12% de las consultas de Atención Primaria, entre el 1-2% de todas las visitas a urgencias y cerca del 10% de los ingresos médicos. Las exacerbaciones generan un gran impacto socioeconómico. En particular las hospitalizaciones constituyen la parte más importante de los costes sanitarios directos asociados a la EPOC2. Además, son las principales determinantes de la morbilidad y mortalidad de la EPOC3. La exacerbación o agudización se define como un episodio agudo de inestabilidad clínica que acontece en el curso natural de la enfermedad y se caracteriza por un empeoramiento mantenido de los síntomas respiratorios que va más allá de sus variaciones diarias4. Los principales síntomas referidos son empeoramiento de la disnea, tos, incremento del volumen y/o cambios en el color del esputo4. Las exacerbaciones se asocian generalmente a un deterioro de la función pulmonar5 y a un aumento de la morbimortalidad6,7.
Más allá de la frecuencia, la intensidad del evento también tiene importancia, siendo peores las consecuencias a medida que la gravedad de la exacerbación es mayor8. Las exacerbaciones leves conllevan un aumento del uso de los broncodilatadores inhalados en dosis o frecuencia y suelen manejarse en el domicilio del paciente9. En estos casos, se recomienda iniciar el tratamiento con un beta-2 agonista de corta duración y, si la respuesta con altas dosis no es satisfactoria, añadir un anticolinérgico10. Las exacerbaciones moderadas requieren el tratamiento con antibióticos y/o corticoesteroides y las exacerbaciones graves precisan una hospitalización9. Precisamente las exacerbaciones graves pueden ser, por sí mismas, un factor de riesgo independiente de mortalidad8,11–13.
Los pacientes en estadios avanzados de la enfermedad, con mayor limitación al flujo aéreo o con antecedentes de exacerbaciones tienen mayor riesgo de sufrir futuras exacerbaciones. El diagnóstico temprano de la EPOC es por tanto de vital importancia para la prevención de las exacerbaciones, un objetivo fundamental en el tratamiento y el manejo de la EPOC en estos pacientes6,10,14. En este sentido, se ha puesto en marcha el estudio epidemiológico EPISCAN II con el objetivo de actualizar la prevalencia y los determinantes de la EPOC en España y confirmar si se ha producido, como sería deseable, un descenso del infradiagnóstico observado en el estudio EPISCAN previo15,16.
A pesar de que a mayor gravedad de la obstrucción, mayor es el número de exacerbaciones moderadas/graves, estas pueden aparecer desde los primeros estadios de la enfermedad, lo que demuestra que el fenotipo exacerbador es independiente de la gravedad de la obstrucción17,18. Aquellos pacientes que presentan dos o más exacerbaciones al año, o una exacerbación que cursa con ingreso hospitalario se definen como paciente con fenotipo exacerbador o agudizador10. La disminución y el control de las exacerbaciones son objetivos prioritarios en este fenotipo.
Importancia de su prevención y de la reducción del riesgo de estasEn promedio, los pacientes con EPOC experimentan de 1-4 exacerbaciones por año19. Para los pacientes con riesgo aumentado de exacerbaciones (limitación del flujo aéreo o antecedentes de exacerbaciones), prevenirlas es un objetivo prioritario en el tratamiento y manejo de la EPOC6. Reducir el riesgo de exacerbaciones moderadas y graves es uno de los objetivos más importantes del tratamiento de la EPOC10,14.
¿Qué dicen las guías?Tanto el documento de consenso internacional GOLD14, como la guía española GesEPOC10 coinciden a la hora de incluir las exacerbaciones como una variable fundamental en el riesgo futuro de la enfermedad, siendo necesario su abordaje para disminuir el impacto clínico en los pacientes. De hecho, en su actualización de 2017, GesEPOC estratifica a los pacientes en bajo y alto riesgo, siendo las exacerbaciones o agudizaciones uno de los factores considerados para la evaluación del riesgo, junto con el FEV1 y el grado de disnea10. Los pacientes con dos o más exacerbaciones moderadas (que requieran tratamiento con corticosteroides sistémicos y/o antibióticos) o con un ingreso hospitalario por exacerbación presentan un mayor riesgo de sufrir una exacerbación en el futuro10.
Para la GesEPOC, los objetivos generales del tratamiento de la EPOC se resumen en tres: a) reducir los síntomas crónicos de la enfermedad, b) disminuir la frecuencia y la gravedad de las exacerbaciones, y c) mejorar el pronóstico. Se deben alcanzar tanto los beneficios a corto plazo (control de la enfermedad) como los objetivos a medio y largo plazo (reducción del riesgo)10.
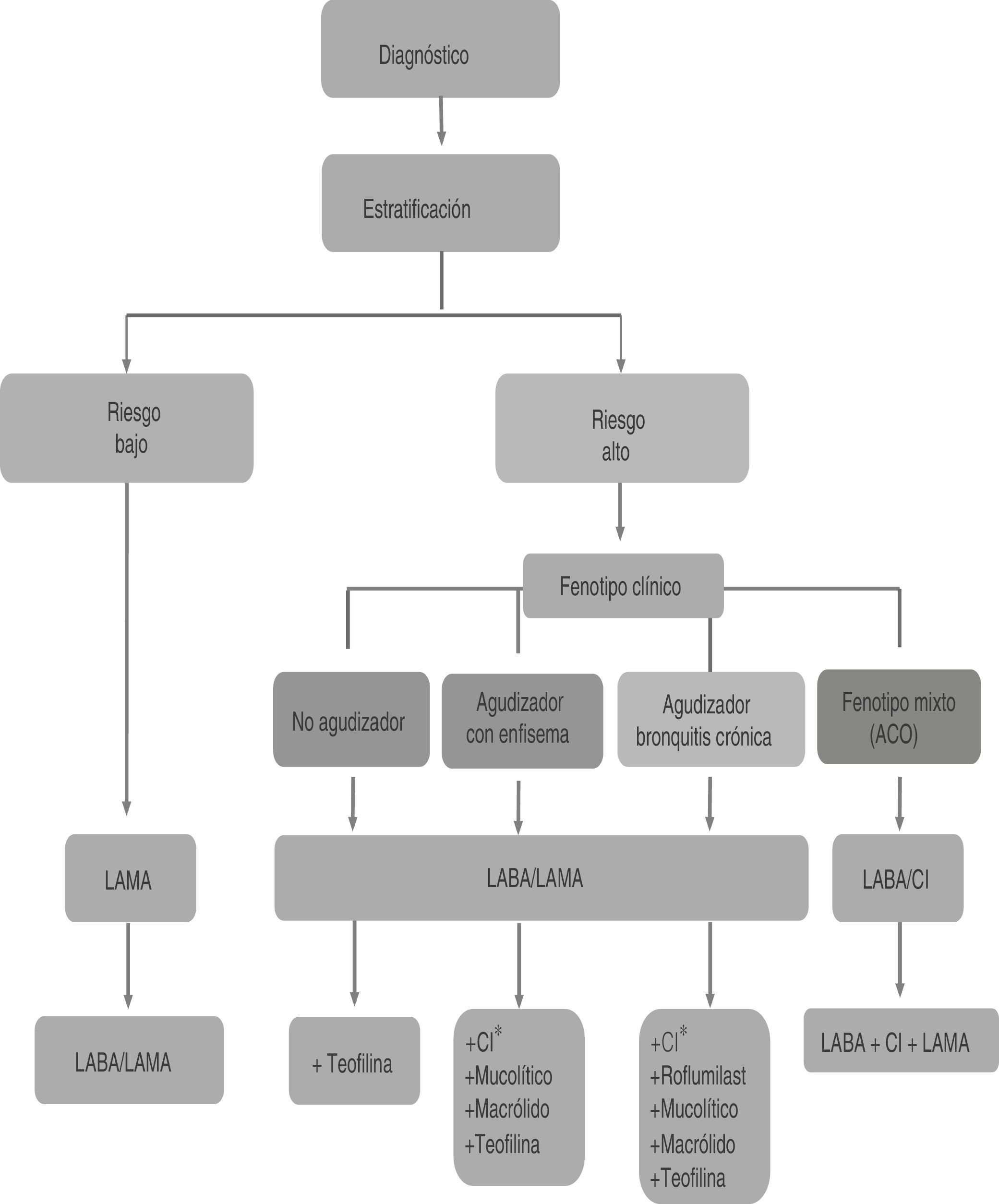
Los broncodilatadores de larga duración (BDLD) deben utilizarse como primer escalón en el tratamiento de todos los pacientes con síntomas permanentes que precisen tratamiento de forma regular10, porque permiten un mayor control de los síntomas que el conseguido con los broncodilatadores de corta duración y mejoran tanto la calidad de vida como la función pulmonar20,21. La figura 1 resume el esquema inicial de tratamiento de la EPOC estable según GesEPOC 201710.
Algoritmo de tratamiento según la guía GesEPOC 2017. CopyRight de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR).
CI: corticosteroides inhalados; LABA: agonista β2 adrenérgico de larga duración; LAMA: antimuscarínico de larga duración. *Las opciones de tratamiento no están en orden de preferencia.
El tratamiento del paciente de bajo riesgo –obstrucción: FEV1 posbroncodilatación ≥ 50% y disnea (mMRC): 0-2 y exacerbaciones en el último año: 0 o 1 sin ingreso hospitalario– consiste en el uso de broncodilatadores de larga duración10. Se recomienda utilizar un agente antimuscarínico de acción prolongada (LAMA) en caso de utilizar monoterapia (fig. 1), debido a la superioridad mostrada frente a los agonistas beta-adrenérgicos de acción prolongada (LABA). Los resultados del ensayo clínico aleatorizado UPLIFT22 demostraron una reducción significativa en el número de exacerbaciones, hospitalizaciones e insuficiencia respiratoria en los pacientes tratados con tiotropio (TIO) frente a placebo durante 4 años.
Ambas guías coinciden en que, en los casos poco frecuentes, de obstrucción leve y ausencia de sintomatología, puede estar indicada la administración de broncodilatadores de corta duración a demanda. Aunque hay que considerar que en los estadios más tempranos de la enfermedad es cuando parece existir un mayor declive de la función pulmonar y, es en estos casos, en los que se debería valorar instaurar un tratamiento, precisamente para evitar la progresión de la enfermedad10,14,23,24.
En relación con la prevención de exacerbaciones, un ensayo clínico aleatorizado demostró que TIO era más eficaz que salmeterol (SAL) en la prevención de exacerbaciones en pacientes con EPOC e historial de al menos una exacerbación durante el año previo25. También ha demostrado superioridad frente a indacaterol (IND) en la prevención de exacerbaciones6. Por estos motivos, ante la elección de un broncodilatador en monoterapia, se recomienda un LAMA como primera opción sobre un LABA. GesEPOC matiza que la evidencia analizada que soporta dicha recomendación se basa únicamente en estudios realizados con el LAMA TIO10.
En relación a los pacientes de alto riesgo –obstrucción: FEV1 posbroncodilatación < 50% o disnea (mMRC): >2 o =2 (con tratamiento) o exacerbaciones en el último año: ≥2 o 1 con ingreso hospitalario–, el tratamiento con doble broncodilatación (LAMA/LABA) es de elección frente al tratamiento con corticoesteroides inhalados (CI) LABA/CI (fig. 1)10. En pacientes de alto riesgo que no presentan un buen control de las exacerbaciones con doble terapia (doble broncodilatación o BDLD/CI), GesEPOC recomienda utilizar la triple terapia LAMA/LABA/CI10, puntualizando que hasta el momento de la actualización existía escasa evidencia disponible con esta triple terapia, pero que indicaría un mayor efecto sobre la función pulmonar y sobre la disminución de las exacerbaciones y las hospitalizaciones en pacientes graves26–28. En esta línea, los últimos estudios publicados revelan una mejora de la función pulmonar y una reducción de la tasa de exacerbaciones de la terapia triple frente a LABA/CI29,30 y a LAMA/LABA30,31.
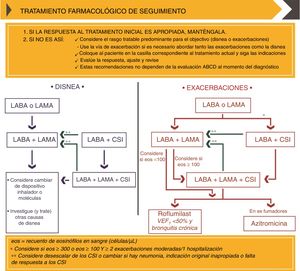
El documento de consenso GOLD, en su actualización del 2019 propone dos algoritmos terapéuticos: uno para el tratamiento inicial y otro para el ajuste del tratamiento de mantenimiento (figs. 2 y 3), e incorpora el uso de la eosinofilia en sangre periférica como marcador para la elección terapéutica de CI14.
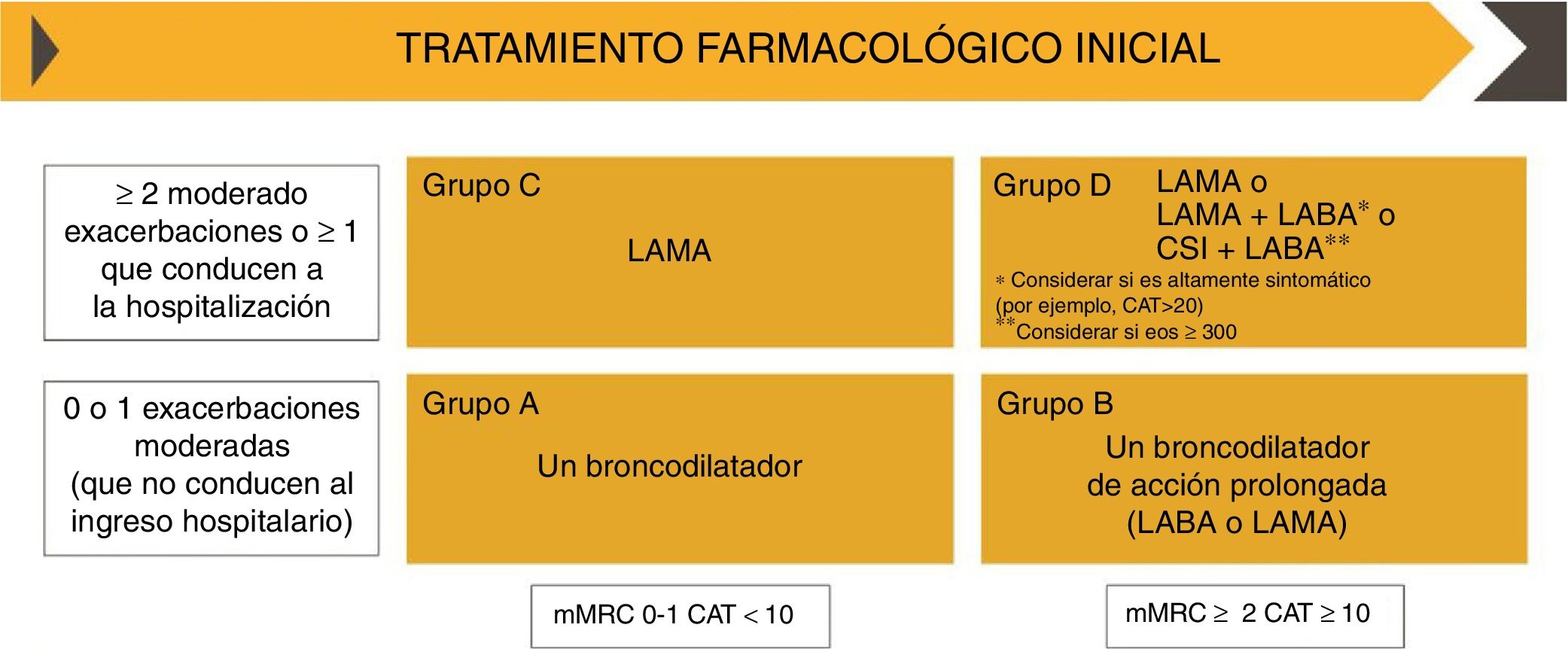
Tratamiento farmacológico inicial según el documento GOLD 2019. CopyRight de la Global Strategy for diagnosis, Management and Prevention of COPD 2019©.
CAT: del inglés; CSI: corticosteroides inhalados; COPD Assessment Test; LABA: agonista β2 adrenérgico de larga duración; LAMA: antimuscarínico de larga duración; mMRC: escala modificada de disnea del Medical Research Council.
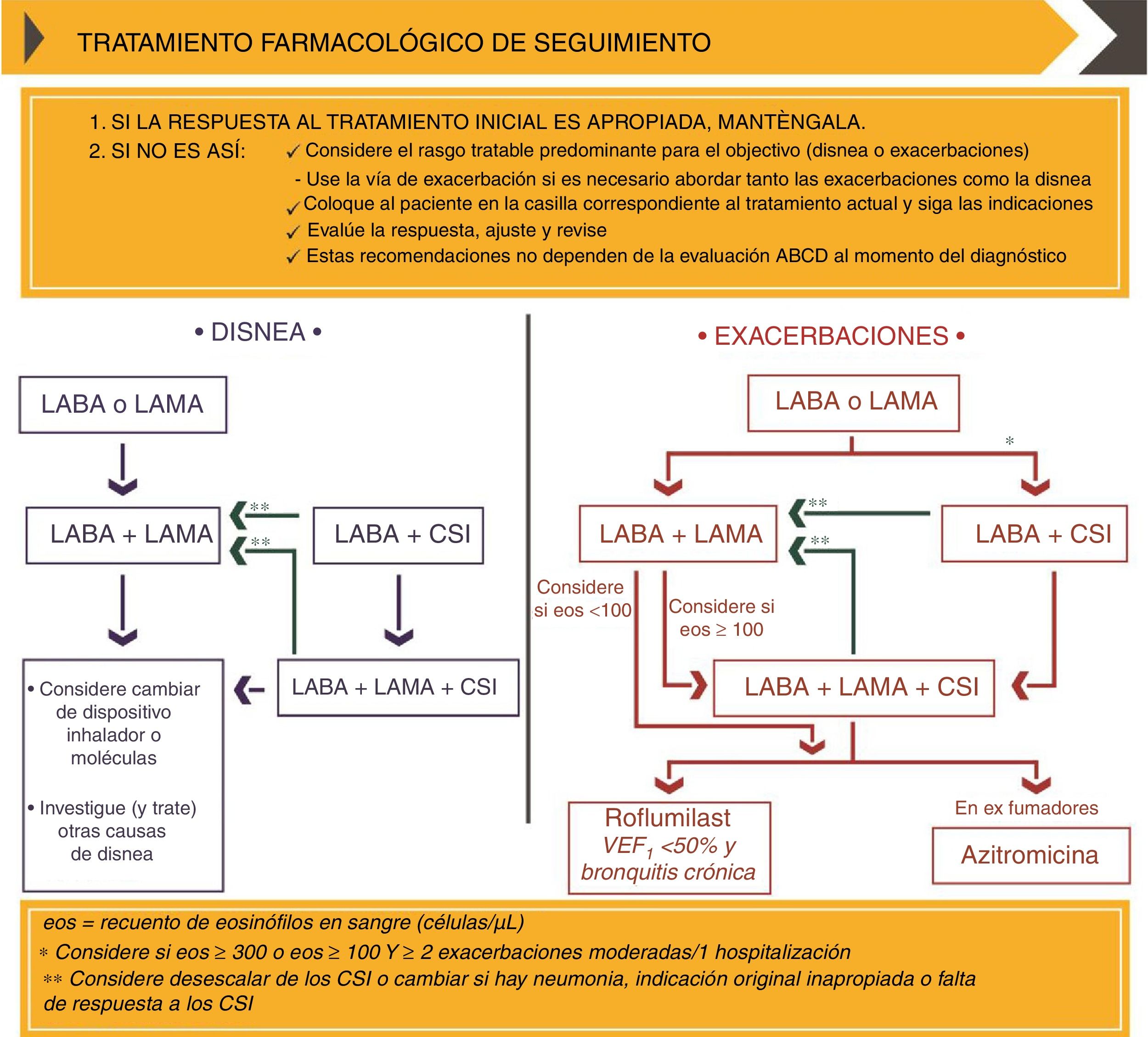
Tratamiento farmacológico de mantenimiento según el documento GOLD 2019. CopyRight de la Global Strategy for diagnosis, Management and Prevention of COPD 2019©.
CSI: corticosteroides inhalados; eos: eosinófilos; LABA: agonista β2 adrenérgico de larga duración; LAMA: antimuscarínico de larga duración; VEF1: volumen espiratorio forzado en un segundo.
Para la elección del tratamiento farmacológico inicial, GOLD continúa recomendando clasificar a los pacientes en cuatro categorías (A, B, C y D), según el grado de sintomatología y las exacerbaciones el año previo (fig. 2). No incluye la función pulmonar, siendo esta una diferencia esencial con la guía GesEPOC10,14.
Tanto en pacientes GOLD C, poco sintomáticos y con alto riesgo de exacerbaciones, como en pacientes GOLD D, muy sintomáticos y con alto riesgo de exacerbaciones, se recomienda un LAMA como tratamiento de elección, por su eficacia en la reducción de las exacerbaciones y las hospitalizaciones y en la mejora de la función pulmonar y la disnea frente a placebo5,14. En pacientes GOLD D con mayor sintomatología (COPD Assessment Test [CAT]>20), se recomienda iniciar el tratamiento con doble broncodilatación LAMA/LABA, y en pacientes GOLD D con eosinofilia en sangre periférica ≥300 céls/μl o con antecedentes de asma, se recomienda la combinación LABA/CI (fig. 2)14. GOLD indica que es necesario evaluar la relación riesgo/beneficio al indicar un CI, ya que el tratamiento con CI está asociado a un aumento del riesgo de neumonía, además de a una mayor prevalencia de candidiasis oral, disfonía y hematomas cutáneos14. Por otro lado, el principal efecto adverso de los LAMA es la sequedad bucal14I.
Para la elección del tratamiento farmacológico de mantenimiento, se propone un algoritmo independiente de la categoría GOLD establecida en diagnóstico, basado en estrategias de escalado y desescalado en función de la eficacia, beneficio clínico y/o presencia de reacciones adversas. En aquellos pacientes con mal control de la enfermedad, primero debe evaluarse la técnica inhalatoria y la adherencia, y luego valorar el ajuste del tratamiento14.
GOLD propone dos estrategias para el ajuste del tratamiento: una para aquellos pacientes que precisen mejorar la disnea y otra para aquellos que requieran mejorar el control sobre las exacerbaciones (con o sin disnea) (fig. 3). En pacientes con mal control de las exacerbaciones con monoterapia LAMA o LABA, se recomienda el escalado a doble terapia LAMA/LABA o LABA/CI14. La combinación LABA/CI se recomienda en pacientes con antecedentes de asma, pacientes con eosinofilia en sangre periférica ≥300 céls/μL, o pacientes con fenotipo exacerbador y eosinofilia en sangre periférica ≥100 céls/μL (fig. 3). Para pacientes con mal control de las exacerbaciones con LAMA/LABA y eosinofilia <100 céls/μL, GOLD recomienda la adición de roflumilast o azitromicina. El escalado a triple terapia LAMA/LABA/CI solo se recomienda en aquellos casos con eosinofilia en sangre periférica ≥100 céls/μL (fig. 3)14. Por último, el algoritmo también incluye estrategias de desescalado: GOLD propone considerar la eliminación de CI o su sustitución por LAMA en aquellos pacientes que no respondan a CI, que presenten neumonía, o cuya indicación original fuera inadecuada (fig. 3)14.
Tanto la GesEPOC como el documento de consenso GOLD subrayan la importancia de un abordaje integral y personalizado en el manejo de la EPOC10,14. Además del tratamiento farmacológico, ambas recomiendan la vacunación, el tratamiento de las comorbilidades y la inclusión de estrategias de educación terapéutica y de autocuidado para reducir el tabaquismo, mantener la actividad física y mejorar la adherencia terapéutica10,14. En pacientes sintomáticos recomiendan educación en estrategias de manejo de la disnea, ahorro de energía y manejo del estrés y en pacientes con exacerbaciones, estrategias para la prevención e identificación temprana de las mismas. En pacientes de alto riesgo (o GOLD B-D), ambos documentos recomiendan intervenciones no farmacológicas como programas de rehabilitación respiratoria y la oxigenoterapia crónica domiciliaria. Aunque no son motivo de este artículo, cabe destacar que estas intervenciones han demostrado mejorar la disnea, la capacidad de ejercicio y la calidad de vida del paciente, y se han asociado a la reducción del número de exacerbaciones y hospitalizaciones y a una menor mortalidad10,14.
Cómo prevenir las exacerbaciones moderadas/gravesEl objetivo del tratamiento de las exacerbaciones consiste en minimizar el impacto de la exacerbación actual y prevenir la aparición de exacerbaciones futuras.
Tiotropio en monoterapiaEl TIO es la molécula que ha demostrado mayor eficacia en la prevención de las exacerbaciones moderadas/graves de la EPOC. No solo es el LAMA con la evidencia más sólida, sino que, hasta la fecha, ningún otro agente o combinación ha demostrado superioridad en la reducción de las exacerbaciones. Por ello, TIO ha sido utilizado como tratamiento de referencia (gold standard) para evaluar la eficacia de otros principios activos en la EPOC. Podríamos afirmar que TIO es la referencia de las terapias respiratorias en la prevención de las exacerbaciones de la EPOC. El documento de consenso de ERS/ATS sobre la prevención de las exacerbaciones de la EPOC32 incluye un metaanálisis que indica que los pacientes con obstrucción moderada o grave tratados con LAMA presentan una menor probabilidad de sufrir una o más exacerbaciones moderadas/graves y una menor probabilidad de sufrir una exacerbación grave que requiera hospitalización, en comparación con los pacientes que recibieron LABA. Además, los pacientes tratados con LAMA mostraron una mejoría en el FEV1, superior a los que recibieron LABA32. Distintos ensayos clínicos con TIO en comparación con otros agentes farmacológicos y con combinaciones han demostrado que su eficacia no ha sido superada en relación al riesgo de exacerbaciones moderadas/graves de la EPOC. A continuación, se describen los resultados relativos a los diferentes ensayos clínicos que han evaluado la eficacia de TIO frente a otras moléculas.
Tiotropio frente a salmeterol(LAMA frente a LABA). El ensayo POET demostró que TIO reduce el riesgo de exacerbaciones moderadas y/o graves frente a SAL con inhalador dosificador en pacientes con EPOC moderada a grave, de forma independiente al uso concomitante de CI. TIO reduce de forma significativa la tasa de exacerbaciones anuales totales en un 11% frente a SAL (RR: 0,89; IC95%: 0,83-0,96; p = 0,002) y reduce la tasa de exacerbaciones moderadas en un 7% (RR: 0,93; IC95%: 0,86-1,00; p = 0,048) y de las graves en un 27% (RR: 0,73; IC95%: 0,66-0,82; p <0,001)25. Además, TIO aumenta el tiempo hasta la primera exacerbación, con una reducción del 17% del riesgo (187 frente a 145 días; HR: 0,83; IC95%: 0,77-0,90; p <0,0001)25. TIO reduce el riesgo de exacerbaciones moderadas un 14% (HR: 0,86; IC95%: 0,79-0,93; p <0,0001) y de exacerbaciones graves un 28% (HR: 0,72; IC95%: 0,61-0,85; p <0,0001) en comparación con SAL25. En base a estos datos, el documento de consenso GOLD 2019 recomienda iniciar el tratamiento con LAMA en monoterapia en pacientes GOLD C14.
Tiotropio frente a indacaterol (LAMA frente a LABA). En el estudio INVIGORATE, los pacientes tratados con indacaterol presentaron un mayor riesgo de sufrir exacerbaciones moderadas y graves que los tratados con TIO. Los pacientes que recibieron IND presentaron una tasa de exacerbaciones un 29% más elevada que el grupo con TIO6. En el análisis de superioridad, la tasa anual de exacerbaciones fue superior con IND en comparación con TIO (0,90 frente a 0,73; RR: 1,24; IC95% 1,12-1,37; p <0,0001)6. En relación con el tiempo hasta la primera exacerbación, TIO fue superior a IND, suponiendo IND un riesgo un 20% mayor en el tiempo hasta la primera exacerbación6. La tasa de exacerbaciones moderadas/graves que requirieron tratamiento con corticosteroides, antibiótico o ambos, o las exacerbaciones que requirieron hospitalización o visitas a urgencias también fueron superiores con IND frente a TIO6.
Los resultados de este ensayo (TIO frente a IND)6 junto a los resultados del ensayo POET (TIO frente a SAL)25 fundamentan la recomendación de GOLD 2019 de iniciar el tratamiento con LAMA en monoterapia en pacientes GOLD C14. De forma similar, GesEPOC también recomienda iniciar con un LAMA en monoterapia en los pacientes de bajo riesgo10. Si las exacerbaciones persisten con este tratamiento, la recomendación es escalar a doble broncodilatación LAMA/LABA10.
Tiotropio frente a glicopirronio (GLI)(LAMA frente a LAMA). En el ensayo SPARK, los pacientes tratados con GLI presentaron un 43% más de riesgo de sufrir exacerbaciones graves que aquellos tratados con TIO (RR: 1,43; IC95%: 1,05-1,97; p = 0,025)33.
Tiotropio frente a salmeterol/fluticasona (SAL/FLU)(LAMA frente a LABA/CI). En el ensayo INSPIRE, la combinación SAL/FLU no mostró superioridad frente a TIO en la reducción de las exacerbaciones moderadas/graves. No se observaron cambios en la tasa anual de exacerbaciones que requirieron recursos sanitarios en SAL/FLU y TIO (1,28/anual y 1,32/anual respectivamente; RR: 0,967; p = 0,656), y la incidencia de exacerbaciones que requirieron hospitalización fue similar en ambos grupos (16% frente a 13%; p = 0,085)3. Así, TIO en monoterapia presenta una eficacia equivalente a la doble terapia (SAL/FLU) en la prevención de exacerbaciones.
Terapia doble LAMA/LABALa GesEPOC recomienda la doble broncodilatación LAMA/LABA en aquellos pacientes con EPOC de bajo riesgo cuyos síntomas no están controlados con LAMA. Además, LAMA/LABA es el tratamiento de elección en pacientes de alto riesgo.
Distintos ensayos clínicos han demostrado que la combinación fija de un LAMA y un LABA es significativamente superior a sus monocomponentes y a la combinación de un LABA y un CI en la reducción de la frecuencia de exacerbaciones en pacientes con EPOC, aunque existen diferencias según los principios activos estudiados.
GesEPOC recomienda el tratamiento con LAMA/LABA frente a LABA/CI en pacientes sintomáticos y con riesgo de sufrir exacerbaciones10. El documento de consenso GOLD también recomienda LAMA/LABA frente a LABA/CI en pacientes exacerbadores sin antecedentes de asma o con una eosinofilia en sangre <100 céls/μL14.
Actualmente no se conocen completamente los mecanismos de la doble broncodilatación LAMA/LABA que explican el efecto favorable observado en ensayos clínicos frente a LABA/CI o a sus monocomponentes. Sin embargo, existen mecanismos potenciales por los que las combinaciones LAMA/LABA podrían ejercer efectos aditivos o sinérgicos que condujeran a una disminución de las exacerbaciones:
- Mecánica pulmonar: la administración de LAMA/LABA disminuye la hiperinsuflación pulmonar, puede reducir el estrés alveolar y mejora la disnea del paciente y la tolerancia al ejercicio34.
- Mucosidad: los LAMA como TIO reducen la producción de esputo en los pacientes con EPOC y mejoran la función mucociliar gracias a su acción anticolinérgica34. Por otro lado, el tratamiento con LABA ha demostrado aumentar el movimiento ciliar in vitro y en las vías respiratorias periféricas en pacientes con EPOC34.
- Síntomas: la combinación LAMA/LABA ocasiona una mejora en los síntomas de los pacientes que se añadiría a su efecto sobre la reducción de las exacerbaciones34.
- Efecto antiinflamatorio: aunque la evidencia del efecto antiinflamatorio de la combinación LAMA/LABA es limitada, en un estudio con esputo inducido de pacientes con EPOC se observó que la administración de TIO atenúa la inflamación neutrofílica mediada por TGF-β1 y que la combinación de TIO/OLO incrementa este efecto34.
LAMA/LABA frente a tiotropioLa eficacia de la doble broncodilatación en la reducción de exacerbaciones de LAMA/LABA frente a TIO varía según los principios activos que componen la combinación33,35–37.
Tiotropio frente a glicopirronio/indacaterol (GLI/IND). El ensayo SPARK evaluó la eficacia de GLI/IND frente a TIO y mostró que GLI/IND no es superior a TIO en la reducción de las exacerbaciones moderadas/graves o graves. GLI/IND previene de forma comparable a TIO tanto las exacerbaciones moderadas/graves (reducción no significativa; 0,90; p = 0,096)33 como las exacerbaciones graves (reducción no significativa; 1,16; p = 0,36)33. En este estudio, las tasas de exacerbaciones graves fueron bajas y similares entre GLI/IND y ambos comparadores en monoterapia33.
TIO frente a umeclidinio/vilanterol (UME/VIL). Hasta la fecha, tres estudios han analizado la eficacia y seguridad de UME/VIL frente a TIO35,36. Los estudios 1 y 2 compararon la combinación UME/VIL frente a TIO y sus monocomponentes35. UME/VIL no redujo el tiempo hasta la primera exacerbación frente a TIO en ninguno de los ensayos (ensayo 1, HR:1,2; IC95% 0,5-2,6; p = 0,709; ensayo 2, HR:1,9; IC95% 1,0-3,6; p = 0,062)35. Otro estudio comparó la combinación UME/VIL frente a TIO, y encontró una reducción de un 50% en el riesgo de exacerbaciones de UME/VIL frente a TIO (HR: 0,5; p = 0,044)36. Cabe destacar que en este último estudio se utilizó un procedimiento estadístico escalonado descendente y que esta comparación estaba en un nivel de comparación inferior a otra que no alcanzó significación estadística36, por lo que no se puede inferir significación estadística. Así, UME/VIL no ha demostrado ser superior a TIO de manera consistente en la reducción del riesgo de exacerbaciones moderadas/graves o graves.
TIO frente a tiotropio/olodaterol (TIO/OLO). El estudio DYNAGITO comparó la eficacia de TIO/OLO frente a TIO37. No se encontraron diferencias significativas en el tiempo hasta la primera exacerbación moderada o grave entre TIO/OLO frente a TIO (HR: 0,95; IC99% 0,87-1,03; p = 0,12). Sin embargo, TIO/OLO redujo un 7% la tasa anual de exacerbaciones moderadas/graves frente a TIO (RR: 0,93; IC99% 0,85-1,02; p = 0,0498), aunque sin alcanzar el nivel de significación preespecificado en el estudio (p = 0,01)37. Es importante destacar que en el análisis post hoc de estos resultados, ajustado por las mismas covariables que estudios similares (estudio SPARK y estudio FLAME33,38), TIO/OLO muestra una reducción de un 11% en las exacerbaciones moderadas/graves frente a TIO (RR: 0,89; IC95% 0,84-0,96; p = 0,0010)37. El tratamiento con TIO/OLO mostró una reducción de la tasa de exacerbaciones moderadas y graves tratadas con corticosteroides (RR: 0,80; IC95% 0,68-0,94; p = 0,0068) y tratadas con corticosteroides + antibióticos (RR: 0,91: IC95% 0,83-1,00; p = 0,045). Por el contrario, no se observaron diferencias entre TIO/OLO y TIO en la tasa de exacerbaciones moderadas y graves tratadas solamente con antibióticos37.
LAMA/LABA frente a LABA/CIEn el estudio FLAME se observó que la doble broncodilatación a dosis fijas LAMA/LABA (GLI/IND) es superior a LABA/CI (SAL/FLU) en la prevención de exacerbaciones con una reducción del 11% en la tasa anual de exacerbaciones totales de la EPOC (RR: 0,89; IC95%: 0,83-0,96; p = 0,003)38 y del 16% en el tiempo hasta la primera exacerbación (HR: 0,84; IC95%: 0,78-0,91; p <0,001)38. Los mismos efectos se observaron al analizar las exacerbaciones moderadas/graves. Estos resultados confirman los obtenidos en un metaanálisis previo con datos combinados procedentes de 4 ensayos clínicos (OR: 0,77; IC95%: 0,62-0,96)39.
Terapia triple: LAMA/LABA/CIEn pacientes que siguen presentando exacerbaciones a pesar de estar en tratamiento con doble terapia (LAMA/LABA o LABA/CI), tanto el documento de consenso GOLD como la guía GesEPOC recomiendan el escalado de doble terapia a terapia triple inhalada (LAMA/LABA/CI)10,14. GOLD matiza que la adición de CI deberá hacerse solo en aquellos pacientes con eosinofilia en sangre ≥100 céls/μL14. Hay pocos estudios que evalúen el riesgo/beneficio de la terapia triple frente a la doble, aunque los últimos estudios indican una mejora de la función pulmonar y una reducción de la tasa de exacerbaciones de la terapia triple frente a LABA/CI29,30 y a LAMA/LABA30,31.
LAMA/LABA/CI frente a LABA/CIEn el estudio IMPACT, la tasa de exacerbaciones graves o moderadas con el tratamiento triple LAMA/LABA/CI (UME/VIL/FLU) fue inferior que en el grupo LABA/CI (VIL/FLU) (RR: 0,85; IC95% 0,80-0,90; p <0,001, 15% de diferencia)30. El estudio FULFIL también demostró una reducción estadísticamente significativa de las exacerbaciones moderadas/graves con la terapia triple (UME/VIL/FLU) en comparación con LABA/CI (formoterol/budesonida) (reducción del 35%; RR: 0,65; IC95%, 0,49-0,86; p = 0,002) en pacientes con EPOC avanzada40.
LAMA/LABA/CI frente a LAMA/LABALa eficacia de la terapia triple frente a LAMA/LABA es controvertida. En el estudio WISDOM, el tratamiento LAMA/LABA/CI (TIO/SAL/propionato de fluticasona) no mostró diferencias frente a LAMA/LABA (TIO/SAL) en las exacerbaciones moderadas/graves (HR: 1,06; IC95% 0,94-1,19) o en las exacerbaciones graves (HR: 1,20; IC95%: 0,98-1,48)41. Sin embargo, un análisis de subgrupos de este estudio mostró que los pacientes con un recuento eosinofílico ≥4% o ≥300 céls/μl sí presentaron una reducción de las exacerbaciones moderadas o graves con la triple terapia42.
Por el contrario, resultados de dos estudios recientes favorecen la terapia triple frente a LAMA/LABA30,31. En el estudio TRIBUTE, la terapia triple (budesonida/fumarato de formoterol/GLI) redujo la tasa de exacerbaciones moderadas o graves respecto a LAMA/LABA (GLI/IND) (RR: 0,848; IC95%: 0,723-0,995; p = 0,043)31. En el estudio IMPACT, la tasa anual de exacerbaciones graves o moderadas fue inferior en el grupo terapia triple (UME/VIL/FLU) que en el grupo LAMA/LABA (UME/VIL) (RR: 0,75; IC95% 0,70-0,81; p <0,001)30. Asimismo, la terapia triple redujo la tasa anual de exacerbaciones graves que conllevaron un ingreso hospitalario (RR: 0,66; IC95% 0,56-0,78; p <0,001)30. Cabe destacar que, a pesar de que la tasa anual de exacerbaciones moderadas o graves fue menor con terapia triple que con la doble en todos los pacientes, en el estudio IMPACT también se observó una mayor reducción de las exacerbaciones en los pacientes con un recuento eosinofílico de al menos 150 céls/μl, confirmando las observaciones anteriores30,42.
La divergencia de resultados encontrados en los estudios WISDOM, TRIBUTE e IMPACT puede deberse a diferencias en el diseño de los estudios y en los perfiles de paciente incluidos. Por ejemplo, en el ensayo IMPACT se asignaron pacientes en tratamiento con CI al grupo LAMA/LABA sin periodo de adaptación, lo que puede conllevar un incremento de sus exacerbaciones causado por la retirada brusca de CI30,43. Por el contrario, el estudio WISDOM diseñó una retirada escalonada de CI con un periodo de preinclusión de 6 semanas41,43. Por otro lado, en IMPACT se incluyeron pacientes con antecedentes de asma, que responden mejor a CI30,43. Por último, los pacientes incluidos en el estudio TRIBUTE presentaban una EPOC grave y sintomática a pesar de estar en tratamiento con una doble broncodilatación, por lo que los resultados de este estudio podrían no ser extrapolables a pacientes con una EPOC menos grave31,44.
Seguridad del tratamiento utilizado para prevenir las exacerbacionesTodos los tratamientos incluidos en esta revisión disponen de una amplia evidencia de seguridad en el tratamiento de las exacerbaciones, con datos que provienen tanto de sus programas de ensayos clínicos, como de la práctica clínica habitual. Sin embargo, las diferencias entre ellos sí que puede condicionar la elección del tratamiento broncodilatador. En general, la reducción de las exacerbaciones con TIO se acompaña de un buen perfil de seguridad y tolerabilidad. El riesgo de neumonía con SAL/FLU fue significativamente mayor, comparado con TIO, a lo largo de los 2 años de tratamiento (HR: 1,94; IC95%: 1,19-3,17; p = 0,008)3. El perfil de seguridad de SAL y TIO fue similar en relación a los acontecimientos adversos (AA), a la discontinuación del fármaco y las muertes25.
También existen evidencias de que la incidencia de AA fue similar entre TIO e IND6. En ambos grupos, los AA más comunes fueron el empeoramiento de la EPOC y las infecciones del tracto respiratorio superior e inferior. La incidencia de AA graves (AAG) también fue similar entre grupos y los más comunes fueron enfermedades respiratorias6. En otro ensayo33, la incidencia de AA, AAG y muertes fue similar entre los distintos grupos de tratamiento (GLI/IND, GLI y TIO). En el estudio DYNAGITO, la incidencia de AA fue similar entre los grupos TIO y TIO/OLO37.
La incidencia de AA y muertes fue similar entre LAMA/LABA y LABA/CI; sin embargo, la incidencia de neumonía fue significativamente superior (3,2% frente a 4,8%; p = 0,02) en el grupo con tratamiento con corticosteroides, LABA/CI38. En otro ensayo39, se observó que la combinación LAMA/LABA se asoció a una menor frecuencia de neumonía comparada con LABA/CI (OR: 0,28; IC95%: 0,12-0,68). Finalmente, la incidencia total de AA, AA de especial interés y AAG fue similar entre los grupos de tratamiento UME/VIL y TIO (44% frente a 42%)36.
La incidencia de AA y AAG fue similar entre la terapia triple y LAMA/LABA o LABA/CI30,31, aunque en el estudio IMPACT se observó una mayor incidencia de neumonía en los grupos con CI30. El grupo LAMA/LABA/CI presentó menor tiempo hasta el primer acontecimiento que el grupo LAMA/LABA (HR: 1,53; IC95% 1,22-1,92; p <0,001); y por el contrario, el grupo de terapia triple no mostró diferencias frente a LABA/CI (HR, 1,02; IC95% 0,87-1,19; p = 0,85)30. Sin embargo, en el estudio TRIBUTE, la proporción de pacientes con neumonía fue similar entre los grupos LAMA/LABA/CI y LAMA/LABA31.
ConclusionesLas exacerbaciones de la EPOC son eventos que ocurren en el trascurso de la enfermedad y que impactan en la evolución de la misma y en la calidad de vida del paciente. Por ello, su prevención es un objetivo fundamental en el manejo de la enfermedad.
Existen distintas estrategias tanto farmacológicas como no farmacológicas que cumplen ese objetivo. Los programas de rehabilitación respiratoria se han asociado a una mejora de la disnea, la capacidad de ejercicio y la calidad de vida del paciente, y la práctica de ejercicio físico regular y la oxigenoterapia crónica domiciliaria a una reducción del riesgo de exacerbaciones. Dentro de los tratamientos farmacológicos, los LAMA han demostrado ser eficaces en la prevención de las exacerbaciones. En concreto, TIO ha demostrado una eficacia no superada en la reducción del riesgo de exacerbaciones moderadas/graves en comparación con otros tratamientos de mantenimiento de la EPOC (monoterapia o doble terapia). Además, TIO se acompaña de un buen perfil de seguridad y tolerabilidad. Todo ello ha hecho que las guías de práctica clínica lo posicionen como un fármaco de primera elección para el paciente con EPOC.
Recientemente se han desarrollado varias combinaciones de LAMA/LABA a dosis fijas que son bien toleradas para el tratamiento de mantenimiento de la EPOC y la reducción de las exacerbaciones33. Estas combinaciones han demostrado su superioridad frente a LABA/CI en la reducción de la tasa anual de exacerbaciones totales de la EPOC. Este hecho, sumado a su perfil de seguridad, las ha colocado en un papel central en el tratamiento de los pacientes con perfil exacerbador. Entre las distintas combinaciones disponibles de LAMA/LABA, la formada por TIO/OLO ha demostrado ser bien tolerada, y presentar una reducción de las exacerbaciones moderada/graves frente a TIO37.
FinanciaciónEl presente trabajo ha recibido financiación de Boehringer Ingelheim España durante la preparación del manuscrito. Boehringer Ingelheim tuvo la oportunidad de comprobar los datos utilizados en este manuscrito sólo para verificar su exactitud.
Conflicto de interesesPatricia Sobradillo ha recibido honorarios por ponencias de AstraZeneca, Boehringer Ingelheim, Chiesi, Ferrer, GlaxoSmithKline, Menarini, Novartis y Teva y honorarios por asesoría de AstraZeneca, Boehringer Ingelheim, Esteve, GlaxoSmithKline, Menarini y Novartis.
Juan Luis García-Rivero ha recibido honorarios por ponencias de AstraZeneca, Boehringer Ingelheim, Chiesi, Ferrer, GlaxoSmithKline, Menarini, Novartis y Teva; y honorarios por asesoría de AstraZeneca, Boehringer Ingelheim, Esteve, GlaxoSmithKline, Menarini y Novartis.
Juan Carlos López Caro ha recibido honorarios por ponencias de AstraZeneca, Boehringer Ingelheim, Chiesi, Esteve, GlaxoSmithKline, Menarini, Novartis, Rovi y Teva.