El déficit de glucosa-6-fosfato-deshidrogenasa (G6PD) es la enzimopatía más prevalente en población general, pero la mayoría de los pacientes son asintomáticos (las crisis son desencadenadas por ciertos fármacos o alimentos). La repercusión clínica es mayor en pacientes procedentes de áreas endémicas de malaria (la medicación antipalúdica puede desencadenar una crisis).
El aumento de flujos migratorios hace que las personas afectadas por el déficit en nuestra consulta estén en aumento, lo que hace interesante una revisión bibliográfica de esta entidad.
Algunos autores han comunicado que los pacientes con déficit de G6PD presentan un aumento de enfermedades cardiovasculares, lo que lleva a plantear un control estricto de factores de riesgo cardiovasculares. Por otro lado, estos pacientes presentan una disminución en la prevalencia de cáncer colorrectal. Además, las donaciones de médula ósea y de derivados hematopoyéticos podrían hacerse con seguridad.
Glucose-6-phosphate-dehydrogenase (G6PD) deficiency is the most prevalent abnormal enzyme condition in the general population, but most patients are asymptomatic (crises are triggered by certain drugs or foods). The clinical consequences are greater in patients coming from endemic areas of malaria (antimalarial medication can trigger a crisis).
The increase in migratory flows has led to an increase in the number of people affected by the deficiency in our practice, which makes it interesting to carry out a literature review of this condition.
Some authors have communicated that patients with G6PD deficiency have an increase in prevalence of cardiovascular diseases, which requires the strict control of cardiovascular risk factors. However, these patients show a decrease in colorectal cancer prevalence. In addition, donations of bone marrow and haematopoietic derivatives could be performed safely.
El déficit de glucosafosfato deshidrogenasa (G6PD) es una enfermedad hereditaria recesiva ligada al cromosoma X1-3, por ello, más frecuente en varones; las mujeres son mayoritariamente portadoras, si bien no desarrollan la enfermedad (con una copia de cromosoma X no alterado, la cantidad de enzima sintetizada es suficiente). La prevalencia es mayor en personas de raza negra y en las pertenecientes a la cuenca mediterránea; sin embargo, la expresión de la enfermedad es más grave en la raza blanca2.
Es el déficit enzimático más frecuente1-3 y consiste en la ausencia de la G6PD, que se encarga de estabilizar la membrana de los glóbulos rojos. La falta de dicha enzima provoca la lisis de los eritrocitos de forma brusca, lo que produce en el individuo afectado una crisis hemolítica. Los factores que pueden desencadenar una crisis son variados; destacan las infecciones (pirexia), algunos alimentos (habas2,4 y derivados) y ciertos medicamentos2 (ácido acetil salicílico, paracetamol, primaquina, nitrofurantoína, isoniazida, L-dopa, entre otros).
La OMS describe 5 clases en función de la actividad de la enzima3, que se nombran desde la I hasta la V. Su clasificación y características aparecen recogidos en la tabla 1.
Actualmente no existe tratamiento específico para este déficit1-3: la actitud médica se limita a prevenir la aparición de crisis hemolíticas (evitando los desencadenantes) y a aplicar medidas de apoyo en caso de aparición. En casos graves, podrían verse beneficiados de una esplenectomía.
Debido a la baja prevalencia en nuestro medio y a la ausencia de síntomas en la vida diaria, puede resultar complicado el abordaje de dichos pacientes en las consultas de Atención Primaria. El incremento en los flujos migratorios desde el Mediterráneo aumenta la probabilidad de que alguno de nuestros pacientes presente esta deficiencia4.
Como consecuencia de ello, y tras la lectura del artículo de Brandt et al.4, en el que realizan una revisión del déficit de G6PD a partir de un caso clínico, se decide hacer una nueva búsqueda bibliográfica como actualización, respecto a este déficit, desde la fecha de publicación de ese artículo hasta la actualidad.
Los objetivos de esta revisión incluyen el resumen del estado actual del conocimiento sobre la deficiencia de G6PD para determinar cómo mejorar su abordaje en la consulta de Atención Primaria de adultos a partir del conocimiento de las complicaciones asociadas y a través del establecimiento de perfiles de riesgo.
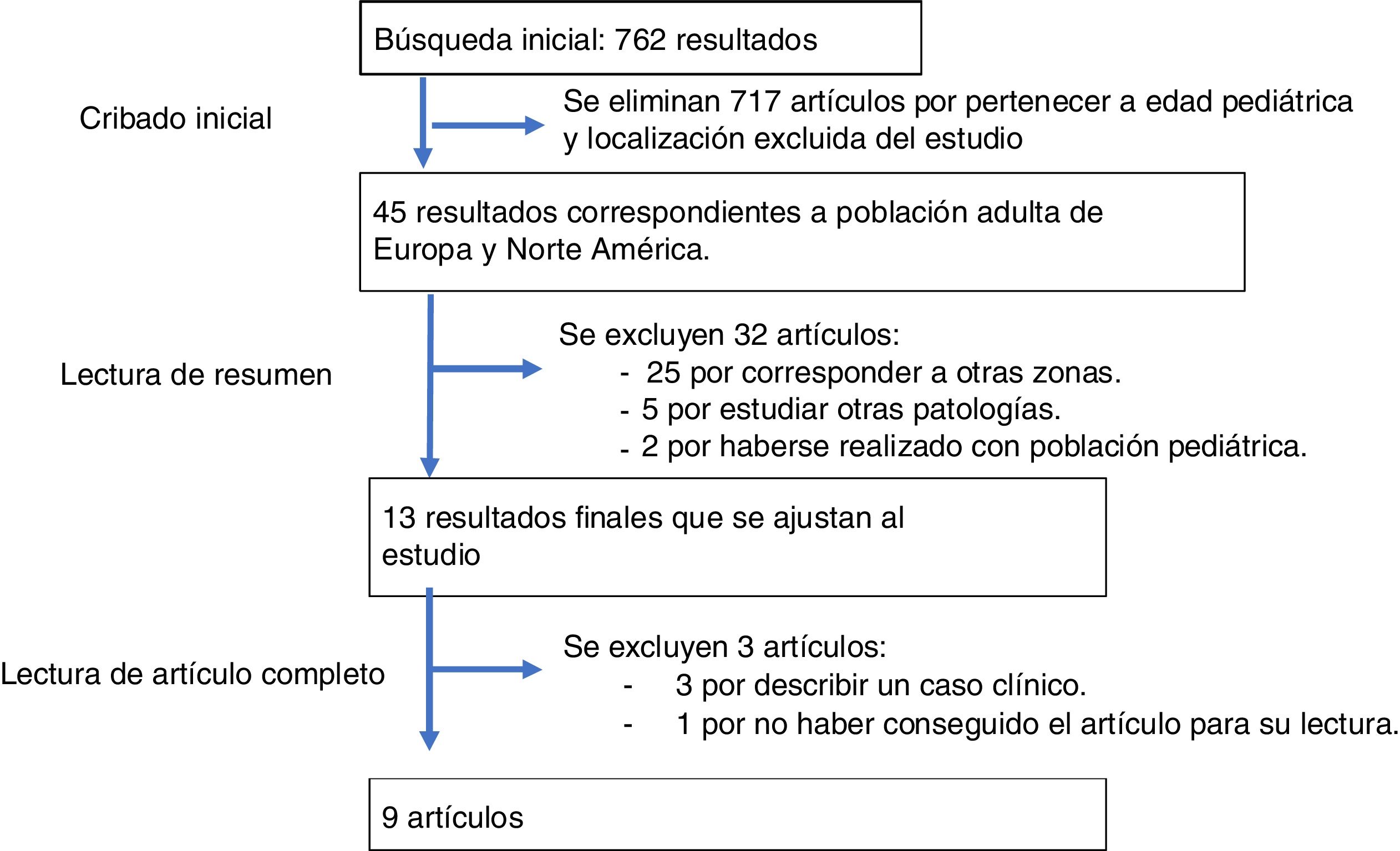
Material y métodosSe realizó una búsqueda sistemática en la base de datos PubMed empleando los términos «G6PD deficiency AND (Europe OR America)» y se obtuvieron 762 resultados. Se seleccionaron únicamente los resultados referentes a población adulta (≥18 años), con pacientes europeos o norteamericanos y publicados desde agosto de 2008 hasta la actualidad para asegurar que la bibliografía estaba actualizada. La edad de los pacientes vino determinada porque no manejamos en nuestra práctica habitual a pacientes pediátricos y las citadas localizaciones, porque presentan características similares a las de nuestro país.
Se obtuvieron 45 resultados, de los cuales se eliminaron 32 por diferentes motivos previa lectura del resumen. Posteriormente y tras la lectura del artículo completo, se descartaron otros 45-8, para analizar finalmente 9 artículos. Se puede apreciar el flujo de selección de artículos y los motivos de exclusión en el esquema PRISMA (fig. 1).
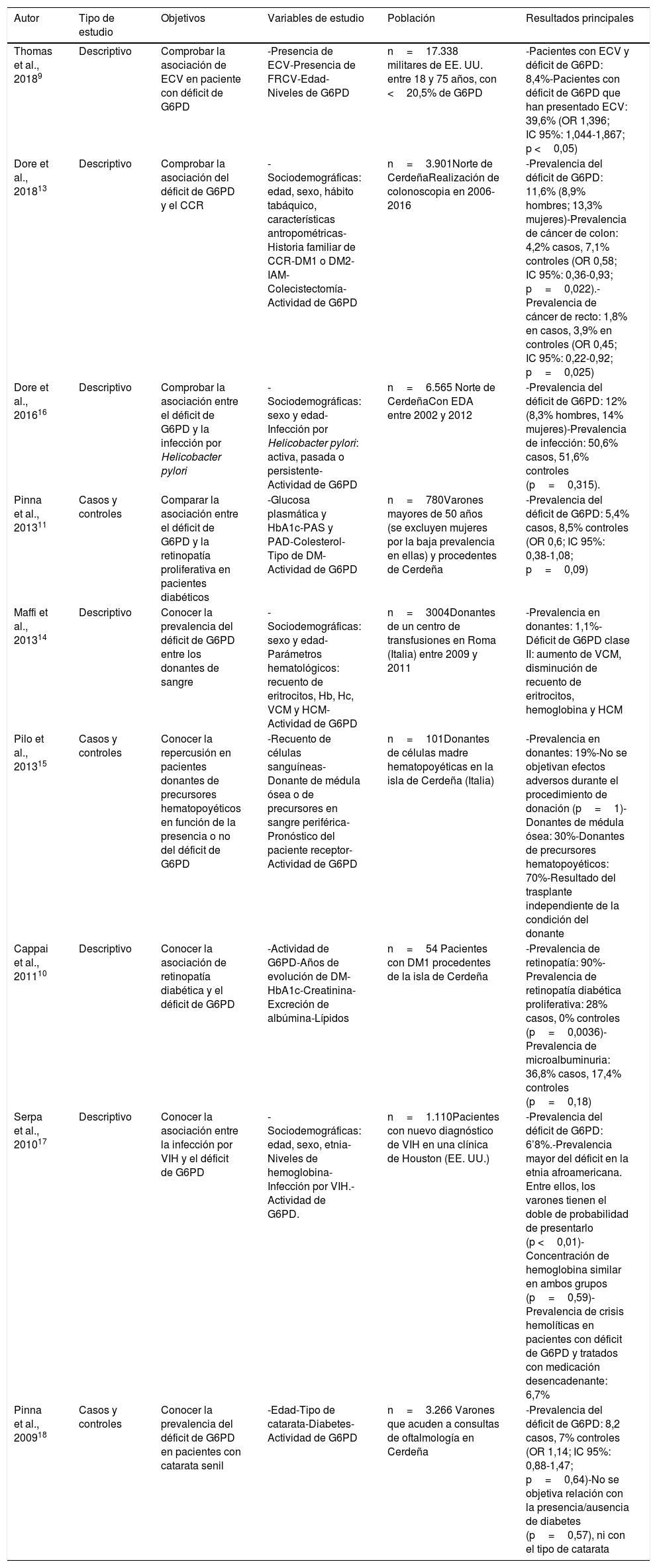
ResultadosLas características y conclusiones de los estudios analizados aparecen recogidos en la tabla 2.
Principales resultados
| Autor | Tipo de estudio | Objetivos | Variables de estudio | Población | Resultados principales |
|---|---|---|---|---|---|
| Thomas et al., 20189 | Descriptivo | Comprobar la asociación de ECV en paciente con déficit de G6PD | -Presencia de ECV-Presencia de FRCV-Edad-Niveles de G6PD | n=17.338 militares de EE. UU. entre 18 y 75 años, con <20,5% de G6PD | -Pacientes con ECV y déficit de G6PD: 8,4%-Pacientes con déficit de G6PD que han presentado ECV: 39,6% (OR 1,396; IC 95%: 1,044-1,867; p <0,05) |
| Dore et al., 201813 | Descriptivo | Comprobar la asociación del déficit de G6PD y el CCR | -Sociodemográficas: edad, sexo, hábito tabáquico, características antropométricas-Historia familiar de CCR-DM1 o DM2-IAM-Colecistectomía-Actividad de G6PD | n=3.901Norte de CerdeñaRealización de colonoscopia en 2006-2016 | -Prevalencia del déficit de G6PD: 11,6% (8,9% hombres; 13,3% mujeres)-Prevalencia de cáncer de colon: 4,2% casos, 7,1% controles (OR 0,58; IC 95%: 0,36-0,93; p=0,022).-Prevalencia de cáncer de recto: 1,8% en casos, 3,9% en controles (OR 0,45; IC 95%: 0,22-0,92; p=0,025) |
| Dore et al., 201616 | Descriptivo | Comprobar la asociación entre el déficit de G6PD y la infección por Helicobacter pylori | -Sociodemográficas: sexo y edad-Infección por Helicobacter pylori: activa, pasada o persistente-Actividad de G6PD | n=6.565 Norte de CerdeñaCon EDA entre 2002 y 2012 | -Prevalencia del déficit de G6PD: 12% (8,3% hombres, 14% mujeres)-Prevalencia de infección: 50,6% casos, 51,6% controles (p=0,315). |
| Pinna et al., 201311 | Casos y controles | Comparar la asociación entre el déficit de G6PD y la retinopatía proliferativa en pacientes diabéticos | -Glucosa plasmática y HbA1c-PAS y PAD-Colesterol-Tipo de DM-Actividad de G6PD | n=780Varones mayores de 50 años (se excluyen mujeres por la baja prevalencia en ellas) y procedentes de Cerdeña | -Prevalencia del déficit de G6PD: 5,4% casos, 8,5% controles (OR 0,6; IC 95%: 0,38-1,08; p=0,09) |
| Maffi et al., 201314 | Descriptivo | Conocer la prevalencia del déficit de G6PD entre los donantes de sangre | -Sociodemográficas: sexo y edad-Parámetros hematológicos: recuento de eritrocitos, Hb, Hc, VCM y HCM-Actividad de G6PD | n=3004Donantes de un centro de transfusiones en Roma (Italia) entre 2009 y 2011 | -Prevalencia en donantes: 1,1%-Déficit de G6PD clase II: aumento de VCM, disminución de recuento de eritrocitos, hemoglobina y HCM |
| Pilo et al., 201315 | Casos y controles | Conocer la repercusión en pacientes donantes de precursores hematopoyéticos en función de la presencia o no del déficit de G6PD | -Recuento de células sanguíneas-Donante de médula ósea o de precursores en sangre periférica-Pronóstico del paciente receptor-Actividad de G6PD | n=101Donantes de células madre hematopoyéticas en la isla de Cerdeña (Italia) | -Prevalencia en donantes: 19%-No se objetivan efectos adversos durante el procedimiento de donación (p=1)-Donantes de médula ósea: 30%-Donantes de precursores hematopoyéticos: 70%-Resultado del trasplante independiente de la condición del donante |
| Cappai et al., 201110 | Descriptivo | Conocer la asociación de retinopatía diabética y el déficit de G6PD | -Actividad de G6PD-Años de evolución de DM-HbA1c-Creatinina-Excreción de albúmina-Lípidos | n=54 Pacientes con DM1 procedentes de la isla de Cerdeña | -Prevalencia de retinopatía: 90%-Prevalencia de retinopatía diabética proliferativa: 28% casos, 0% controles (p=0,0036)-Prevalencia de microalbuminuria: 36,8% casos, 17,4% controles (p=0,18) |
| Serpa et al., 201017 | Descriptivo | Conocer la asociación entre la infección por VIH y el déficit de G6PD | -Sociodemográficas: edad, sexo, etnia-Niveles de hemoglobina-Infección por VIH.-Actividad de G6PD. | n=1.110Pacientes con nuevo diagnóstico de VIH en una clínica de Houston (EE. UU.) | -Prevalencia del déficit de G6PD: 6’8%.-Prevalencia mayor del déficit en la etnia afroamericana. Entre ellos, los varones tienen el doble de probabilidad de presentarlo (p <0,01)-Concentración de hemoglobina similar en ambos grupos (p=0,59)-Prevalencia de crisis hemolíticas en pacientes con déficit de G6PD y tratados con medicación desencadenante: 6,7% |
| Pinna et al., 200918 | Casos y controles | Conocer la prevalencia del déficit de G6PD en pacientes con catarata senil | -Edad-Tipo de catarata-Diabetes-Actividad de G6PD | n=3.266 Varones que acuden a consultas de oftalmología en Cerdeña | -Prevalencia del déficit de G6PD: 8,2 casos, 7% controles (OR 1,14; IC 95%: 0,88-1,47; p=0,64)-No se objetiva relación con la presencia/ausencia de diabetes (p=0,57), ni con el tipo de catarata |
CCR: cáncer colorrectal; DM: diabetes mellitus; ECV: enfermedad cardiovascular; EDA: endoscopia digestiva alta; FRCV: factores de riesgo cardiovascular; G6PD: glucosa-6-fosfato deshidrogenasa; Hb: hemoglobina; Hc: hematocrito; HCM: hemoglobina corpuscular media; IAM: infarto agudo de miocardio; IC: intervalo de confianza; OR: odds ratio; PAD: presión arterial diastólica; PAS: presión arterial sistólica; VCM: volumen corpuscular medio; VIH: virus de la inmunodeficiencia humana.
El concepto de enfermedad cardiovascular (ECV) engloba el infarto agudo de miocardio (IAM), la insuficiencia cardiaca congestiva, la miocardiopatía, la presencia de bypass coronario, la arteriopatía periférica, el accidente cerebrovascular y las anomalías eléctricas.
Se encuentran diferencias estadísticamente significativas para la presencia de riesgo cardiovascular aumentado (p<0,0001), anomalías eléctricas (p=0,007) y miocardiopatía (p<0,001) en mayor proporción en pacientes con déficit de G6PD. El resto de las ECV se producen con mayor frecuencia en pacientes sin el déficit, según Thomas et al.9; sin embargo, las diferencias no son estadísticamente significativas.
Por otro lado, se estudió la influencia del déficit en los factores de riesgo cardiovascular (FRCV), en los que se engloba la hipertensión arterial, dislipidemia y la diabetes mellitus. Se encontraron diferencias estadísticamente significativas solo para la presencia de hipertensión arterial (p<0,0001).
Con relación a los pacientes diabéticos, se han encontrado estudios en los que se relaciona el déficit de G6PD con la presencia de retinopatía diabética proliferativa. Sin embargo, no en todos se encuentra una significación estadística. Cappani et al.10 relacionan ambas entidades con una p=0,0036. Por el contrario, en la serie estudiada por Pinna et al.11, la frecuencia es mayor en pacientes con déficit de G6PD, sin ser estadísticamente significativa. Este último estudio objetiva el aumento de riesgo de retinopatía diabética a la hipertensión arterial y a la glucemia plasmática alterada.
El déficit de G6PD disminuye el riesgo de cáncer colorrectalSegún el informe de 2018 de la Sociedad Española de Oncología Médica (SEOM), el cáncer colorrectal es el segundo en incidencia y el tercero en prevalencia12. Dore et al.13 realizaron un estudio con pacientes intervenidos de colonoscopia por cualquier motivo, y compararon la presencia de lesiones malignas con la presencia o ausencia del déficit de G6PD.
Se objetivó una prevalencia de cáncer de colon del 4,2% en pacientes con déficit, siendo del 7,1% en los pacientes sin él (OR 0,58; IC 95%: 0,36-0,93; p=0,022). Lo mismo sucedía con el cáncer de recto, cuya prevalencia en pacientes con déficit es del 1,8% frente al 3,9% en los pacientes con la enzima presente (OR 0,45; IC 95%: 0,22-0,92; p=0,025).
Teniendo en cuenta el cáncer colorrectal en conjunto, los resultados se mantuvieron similares: se afirma que en pacientes con déficit de G6PD se produce una reducción de la prevalencia del cáncer colorrectal en un 43,2% (OR 0,568; IC 95%: 0,371-0,872; p=0,01).
Influencia del déficit de G6PD y la transfusión de hemoderivadosOtro de los aspectos estudiados durante estos años ha sido la relación entre las transfusiones sanguíneas y el déficit de G6PD, alteración que no es estudiada en un donante de manera habitual.
Maffi et al.14 estudiaron la prevalencia del déficit de G6PD en pacientes donantes y obtuvieron un resultado del 1,1%. La frecuencia, entre los portadores del déficit, fue de un 48% de clase II y un 43% de clase III. El objetivo de dicho estudio consiste en conocer qué pacientes son portadores del déficit y así evitar transfundir esos hematíes a pacientes de riesgo, tales como neonatos o con anemia falciforme.
En el mismo campo, Pilo et al.15 realizaron un estudio con pacientes donantes de médula ósea o de precursores hematopoyéticos y sus receptores. El 19% eran portadores del déficit de G6PD, sin embargo, ninguno de ellos presentó efectos adversos en el procedimiento de donación (p=1), utilizando parámetros como hemoglobina, recuento de eritrocitos, bilirrubina y LDH.
Respecto al paciente trasplantado, se realizaron comparaciones dividendo a los pacientes según el pronóstico. En ambos grupos la supervivencia fue similar tanto para los que habían sido trasplantados de donantes con el déficit como sin él.
Otros resultadosPor otro lado, se han publicado estudios en los que no ha sido posible comprobar asociación con el déficit de G6PD.
Dore et al.16 estudiaron la posible relación de la infección por Helicobacter pylori con el déficit de G6PD. Los pacientes presentaron resultados similares: la frecuencia de la infección fue del 50,6% en los portadores del déficit frente al 51,6% en los que no la presentaban. Sin embargo, la ausencia de significación estadística no permite concluir que la infección sea menos frecuente en los deficitarios de la enzima. La edad es factor pronóstico de la infección por H. pylori: es más frecuente en mayores de 50 años (OR 2,090; IC 95%: 1,894-2,307; p <0,0001).
Serpa et al.17 estudiaron la prevalencia en pacientes diagnosticados de VIH. Se objetivó una prevalencia del 6,8% de pacientes con déficit de G6PD, con mayor frecuencia en la población afroamericana; del 9,7% frente al 2% en hispanos y del 0,7% en raza blanca. En conjunto, la media de concentración de hemoglobina era la misma, sin significación estadística en el resultado (p=0,59).
Pinna et al.18 estudiaron su relación con la catarata senil en la que había una diferencia del 1,2% en su frecuencia; la mayor prevalencia de catarata se daba en los pacientes con el déficit. Sin embargo, los resultados no fueron estadísticamente significativos (p=0,64).
DiscusiónEl déficit de G6PD es el déficit enzimático más frecuente en población general. Aunque habitualmente cursa de forma asintomática, la frecuencia de la enfermedad y la gravedad potencial de las crisis dan relevancia a conocer qué pacientes tienen un mayor riesgo de presentar este déficit.
La frecuencia del déficit es mayor en personas procedentes de África, Oriente Medio, sudeste asiático y países de la cuenca mediterránea. Además, en áreas endémicas de malaria, los pacientes con dicha deficiencia tienen mayor probabilidad de presentar síntomas debido a la medicación antipalúdica, que es desencadenante de crisis hemolíticas. Por otro lado, se piensa que el déficit de G6PD tiene un efecto protector frente a la infección por Plasmodium falciparum1. La revisión concuerda con los diversos estudios encontrados; destaca el estudio realizado con militares de la armada de EE. UU., el cual se inició debido a los efectos adversos que presentaron muchos de ellos tras la administración de primaquina para la prevención de malaria9.
Por otro lado, aquellos pacientes inmigrantes procedentes de zonas endémicas de paludismo tendrían recomendación del cribado del déficit de G6PD (debido al aumento de la prevalencia en pacientes procedentes de dichos países) en caso de necesitar la profilaxis contra la malaria (por la pérdida de inmunidad con el paso de los años).
La prevalencia del déficit en nuestro medio está en aumento debido al incremento de los flujos migratorios precedentes de regiones endémicas de malaria. Sin embargo, la bibliografía relativa al déficit de G6PD en países occidentales es aún escasa. Esta revisión refleja este nivel bajo de investigación, que son los problemas principales encontrados.
Se podría definir como grupo de riesgo en nuestro medio a los pacientes varones, procedentes de los países con mayor prevalencia del déficit de G6PD, como indican Serpa et al.17 en su estudio. Por tanto, podría ser interesante su cribado en los pacientes que cumplan estos criterios, así como en la población general en países mediterráneos. Así lo hacen Cladera Serra et al. en un estudio realizado en la población de la isla de Menorca19.
Además, podría ser interesante el cribado del déficit en mujeres procedentes de áreas con alta prevalencia, debido a su patrón de herencia. Una mujer portadora tendría un 50% de probabilidades de tener un hijo varón afectado o una hija portadora.
La asociación del déficit de G6PD con las enfermedades cardiovasculares hace reflexionar sobre la importancia de un control estricto de los factores de riesgo cardiovascular en dichos pacientes con la realización de test de screening precoz9. Sin embargo, un estudio previo propone la protección cardiovascular en pacientes con el déficit20, aunque sus limitaciones reflejan la necesidad de continuar investigando sobre esta relación.
El estudio realizado por Thomas et al.9 señala el aumento en estos pacientes de anomalías eléctricas y miocardiopatías, por lo que podría ser interesante la realización de ECG a dichos pacientes con frecuencia mayor a la población general.
En la misma línea, el déficit de G6PD se ha relacionado en algunos trabajos con la presencia de retinopatía diabética proliferativa10, que es una de las complicaciones microvasculares de la diabetes mellitus y, por tanto, de utilidad ampliar su estudio debido a las controversias de la afectación cardiovascular en estos pacientes.
El efecto protector sobre la aparición de cáncer colorrectal es mayor en los adultos menores de 50 años, en los que la disminución en la OR no es despreciable (43%). Sin embargo, a partir de esa edad, la influencia de otros factores hace que la protección que otorga el déficit no sea tan marcada13. Con relación a otras enfermedades gastrointestinales, la edad también ha demostrado influencia positiva en la infección por H. pylori; no la ha demostrado así la presencia del déficit de G6PD16.
Un paciente con déficit de G6PD puede realizar donaciones de médula ósea o hemoderivados con seguridad14,15, a pesar de las posibles alteraciones en el hemograma, tal como han descrito diversos estudios, con tasas de éxito y complicaciones similares en ambos grupos.
Debido a las áreas de mayor prevalencia de esta entidad, se podría pensar en una posible asociación del déficit de G6PD con la infección por VIH; sin embargo, algunos estudios describen prevalencias similares que en pacientes no infectados17. La relación señalada entre VIH y el déficit no está claramente fundamentada, según la bibliografía revisada.
Clásicamente, en ciertas regiones con prevalencia aumentada de déficit de G6PD, aparece un elevado número de personas con alergia a las habas. Refieren malestar general e ictericia; lo mismo les sucede con la toma de cierta medicación. En la actualidad, esto lleva a pensar que esas «reacciones alérgicas» eran en realidad crisis hemolíticas en pacientes con el déficit4.
Sin embargo, la revisión bibliográfica realizada presenta limitaciones porque la mayoría de los estudios publicados recientemente son descriptivos. Se incluyen además, 3estudios de casos y controles.
ConclusionesEl grupo de riesgo para presentar el déficit de G6PD son los varones (herencia recesiva ligada al sexo), procedentes de África, Oriente Medio, el sudeste asiático y países de la cuenca mediterránea.
El manejo de la enfermedad sería diferente en función de la localización en la que nos encontremos. En países occidentales, donde la prevalencia es menor y donde suele ser más grave, el diagnóstico se suele hacer tras una crisis hemolítica y, después, se deben evitar los desencadenantes. Por otro lado, en países donde la prevalencia está aumentada y la gravedad de las crisis son menores, se debería hacer un cribado, sobre todo a aquellos pacientes que vayan a recibir tratamientos antipalúdicos, por ser los mayores desencadentes de crisis en esta población.
Tras la revisión, podríamos aportar nuevas líneas de investigación para seguir ampliando conocimientos que permitan dar recomendaciones para estos pacientes:
Realizar un control más estricto de los factores de riesgo cardiovascular a los pacientes con déficit de G6PD.
Corroborar la seguridad de las donaciones de médula ósea o hemoderivados con seguridad.
Mantener el cribado de cáncer colorrectal igual que en población general, a pesar de tener una incidencia menor.
Evitando los factores desencadenantes de crisis hemolíticas, los pacientes con déficit de G6PD pueden tener una vida completamente normal.
Conflicto de interesesLos autores declaramos no tener conflictos de intereses.